Mechanism of Biliverdin in Improving Cerebral Ischemia-reperfusion Injury in Rats
-
摘要:
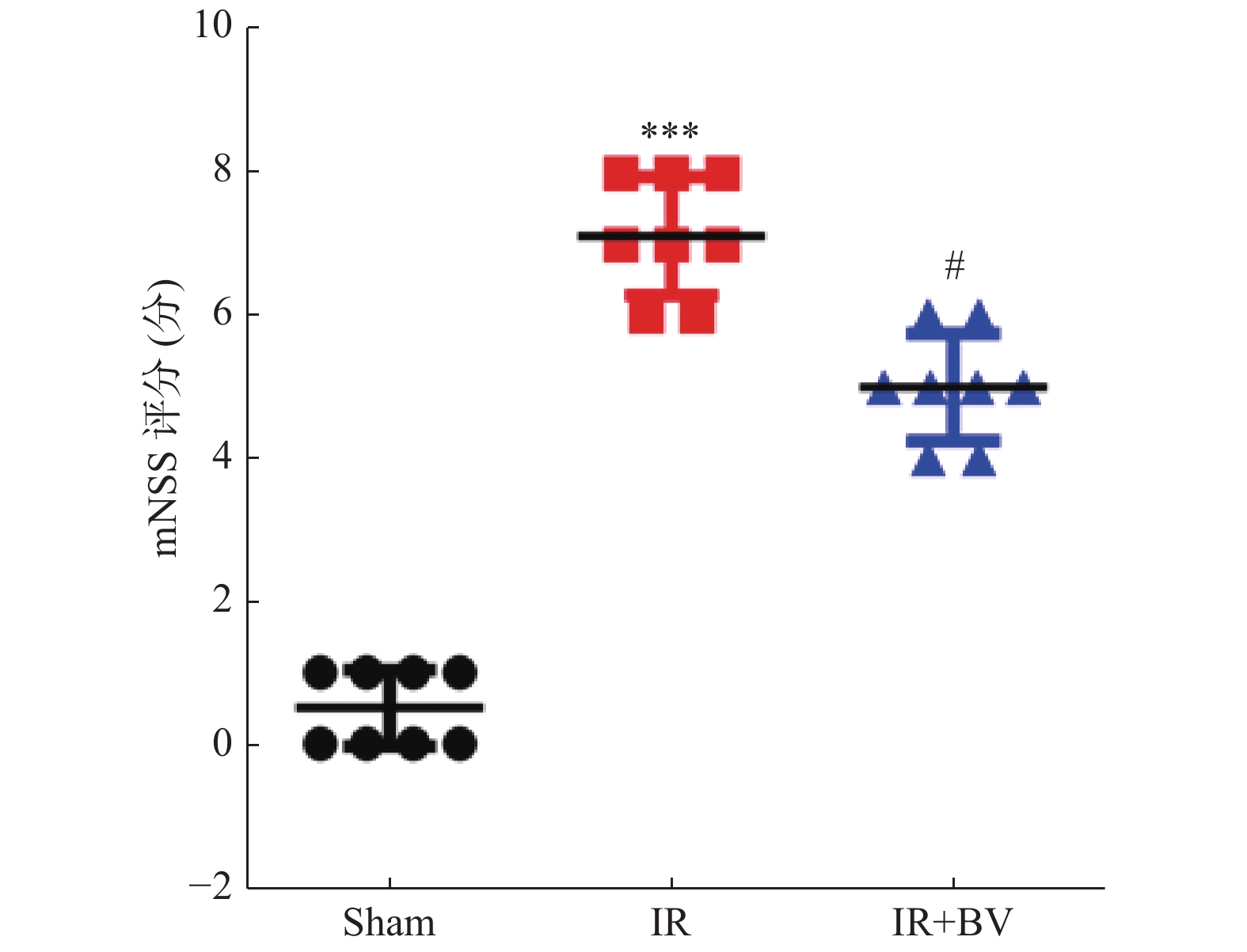
目的 探讨胆绿素对大鼠脑缺血再灌注损伤的保护作用以及机制。 方法 采用线栓法建立大鼠大脑中动脉栓塞模型(middle cerebral artery occlusion model,MCAO),给予胆绿素治疗后,采用改良版神经功能缺损评分评价大鼠神经功能缺损情况,干湿重法测定脑组织含水量,TTC染色测定脑梗死面积,Iba-1/DAPI染色标记缺血侧脑组织小胶质细胞活化情况,免疫荧光染色检测脑组织炎症因子TNF-α表达,Western blot测定脑组织Iba-1/CD68的蛋白表达。 结果 和IR组比较,胆绿素治疗可改善MCAO大鼠的神经功能缺损(P < 0.05),同时,还能减轻脑组织含水量(P < 0.05),降低大脑梗死面积(P < 0.05),以及降低缺血侧脑组织中小胶质细胞的表达和Iba-1/CD68蛋白的表达(P < 0.05)。此外,胆绿素治疗还能减少缺血侧脑组织中炎症因子TNF-α的表达(P < 0.05)。 结论 胆绿素在MCAO大鼠中可能通过抑制小胶质细胞活化而减轻大鼠脑缺血再灌注损伤。 Abstract:Objective To investigate the protective effect and underlying mechanism of biliverdin on cerebral ischemia-reperfusion injury in rats. Methods The middle cerebral artery occlusion model(MCAO)was established by inserting nylon thread, after biliverdin treatment, the neurological deficit were evaluated by modified neurological severity score, the brain water content were detected by dry and wet weight method, the cerebral infarction were detected by TTC staining, the activation of microglia in ischemic brain tissue were marked by Iba-1/DAPI staining, the expression of TNF-α were detected by immunofluorescence staining, the protein expression of Iba-1/CD68 were detected by Western blot. Results Compared with the IR group, after biliverdin treatment, the neurological deficits were improved(P < 0.05), Meanwhile, the brain water content was reduced(P < 0.05), and the cerebral infarction were attenuated(P < 0.05). What's more, the microglia expression and Iba-1/CD68 protein expression were decreased(P < 0.05)and the inflammatory factor TNF-α expression was also reduced(P < 0.05). Conclusion Biliverdin may attenuate cerebral ischemia-reperfusion injury by inhibiting microglia activation in rats. -
Key words:
- Biliverdin /
- Microglia /
- Cerebral ischemia reperfusion injury
-
表 1 动物分组和处理
Table 1. Animal grouping and treatment
组别 处理 检测指标 数量 Sham组 只暴露颈内动脉,不做其他处理 mNSS/干湿重 n = 8 TTC染色 n = 4 WB n = 4 免疫荧光双染 n = 8 IR组 缺血2 h再灌注24 h mNSS/干湿重 n = 8 TTC染色 n = 4 WB n = 4 免疫荧光双染 n = 8 IR + BV组 缺血2 h再灌注24 h + 胆绿素治疗 mNSS/干湿重 n = 8 TTC染色 n = 4 WB n = 4 免疫荧光双染 n = 8 -
[1] Zhou M, Wang H, Zeng X, et al. Mortality, morbidity, and risk factors in China and its provinces, 1990-2017: A systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet,2019,394(10204):1145-1158. doi: 10.1016/S0140-6736(19)30427-1 [2] Janus-laszuk B, Mirowska-guzel D, Sarzynska I, et al. Effect of medical complications on the after-stroke rehabilitation outcome[J]. Neuro Rehabilitation,2017,40(2):223-232. doi: 10.3233/NRE-161407 [3] Tschoe C, Bushnell C D, Duncan P W, et al. Neuroinflammation after intracerebral hemorrhage and potential therapeutic targets[J]. J Stroke,2020,22(1):29-46. doi: 10.5853/jos.2019.02236 [4] Duris K, Splichal Z, Jurajda M. The role of inflammatory response in stroke associated programmed cell death[J]. Curr Neuropharmacol,2018,16(9):1365-1374. doi: 10.2174/1570159X16666180222155833 [5] Zhao S C, Ma L S, Chu Z H, et al. Regulation of microglial activation in stroke[J]. Acta Pharmacol Sin,2017,38(4):445-458. doi: 10.1038/aps.2016.162 [6] Jayaraj R L, Azimullah S, Beiram R, et al. Neuroinflammation: friend and foe for ischemic stroke[J]. Journal of Neuroinflammation,2019,16(1):142. doi: 10.1186/s12974-019-1516-2 [7] Zhang Y, Ding Y, Lu T, et al. Biliverdin reductase-A attenuated GMH-induced inflammatory response in the spleen by inhibiting toll-like receptor-4 through eNOS/NO pathway[J]. Journal of Neuroinflammation,2018,15(1):118. doi: 10.1186/s12974-018-1155-z [8] Zhang Y, Shan Z, Zhao Y, et al. Sevoflurane prevents miR-181a-induced cerebral ischemia/reperfusion injury[J]. Chem Biol Interact,2019,308(1):332-338. [9] Longa E Z, Weinstein P R, Carlson S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats[J]. Stroke,1989,20(1):84-91. doi: 10.1161/01.STR.20.1.84 [10] Yang W T, Wang Y, Shi Y H, et al. Herbal compatibility of ginseng and rhubarb exerts synergistic neuroprotection in cerebral ischemia/reperfusion injury of rats[J]. Front Physiol,2019,10(1):174. [11] Li J J, Zou Z Y, Liu J, et al. Biliverdin administration ameliorates cerebral ischemia reperfusion injury in rats and is associated with proinflammatory factor downregulation[J]. Exp Ther Med,2017,14(1):671-679. doi: 10.3892/etm.2017.4549 [12] Zou Z Y, Liu J, Chang C, et al. Biliverdin administration regulates the microRNA-mRNA expressional network associated with neuroprotection in cerebral ischemia reperfusion injury in rats[J]. Int J Mol Med,2019,43(3):1356-1372. [13] Eady T N, Khoutorova L, Obenaus A, et al. Docosahexaenoic acid complexed to albumin provides neuroprotection after experimental stroke in aged rats[J]. Neurobiol Dis,2014,62(1):1-7. [14] Crespo-araico L A, Veralechuga R, Cruz-culebras A, et al. Reperfusion therapy in patients with acute ischaemic stroke caused by cervical artery dissection[J]. Neurologia,2019,34(3):153-158. doi: 10.1016/j.nrl.2016.11.005 [15] Hankey G J. Stroke[J]. Lancet,2017,389(10069):641-654. doi: 10.1016/S0140-6736(16)30962-X [16] Ayer A, Zarjou A, Agarwal A, et al. Heme oxygenases in cardiovascular health and disease[J]. Physiological reviews,2016,96(4):1449-1508. doi: 10.1152/physrev.00003.2016 [17] Sun J, Zhang P, Yang X, et al. Biliverdin protects the isolated lungs from ischemia/reperfusion injury via anti-apoptosis[J]. Zhonghua Wei Zhong Bing Ji Jiu Yi Xue,2017,29(1):25-29. [18] Aono H, Choudhury M E, Higaki H, et al. Microglia may compensate for dopaminergic neuron loss in experimental parkinsonism through selective elimination of glutamatergic synapses from the subthalamic nucleus[J]. Glia,2017,65(11):1833-1847. doi: 10.1002/glia.23199 [19] 谢风帆, 张玉琴, 赖文芳, 等. 栝楼桂枝汤通过抑制小胶质细胞活化改善大鼠脑缺血/再灌注损伤[J].中国药理学通报,2020,36(05):703-709. doi: 10.3969/j.issn.1001-1978.2020.05.022 -






 下载:
下载: