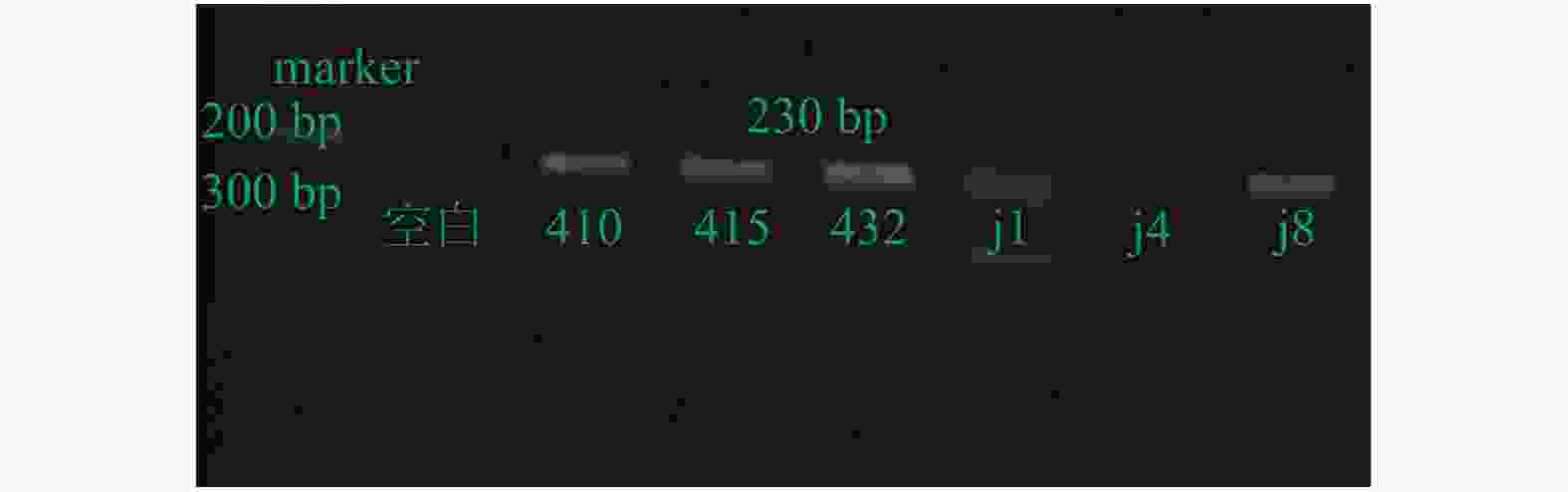
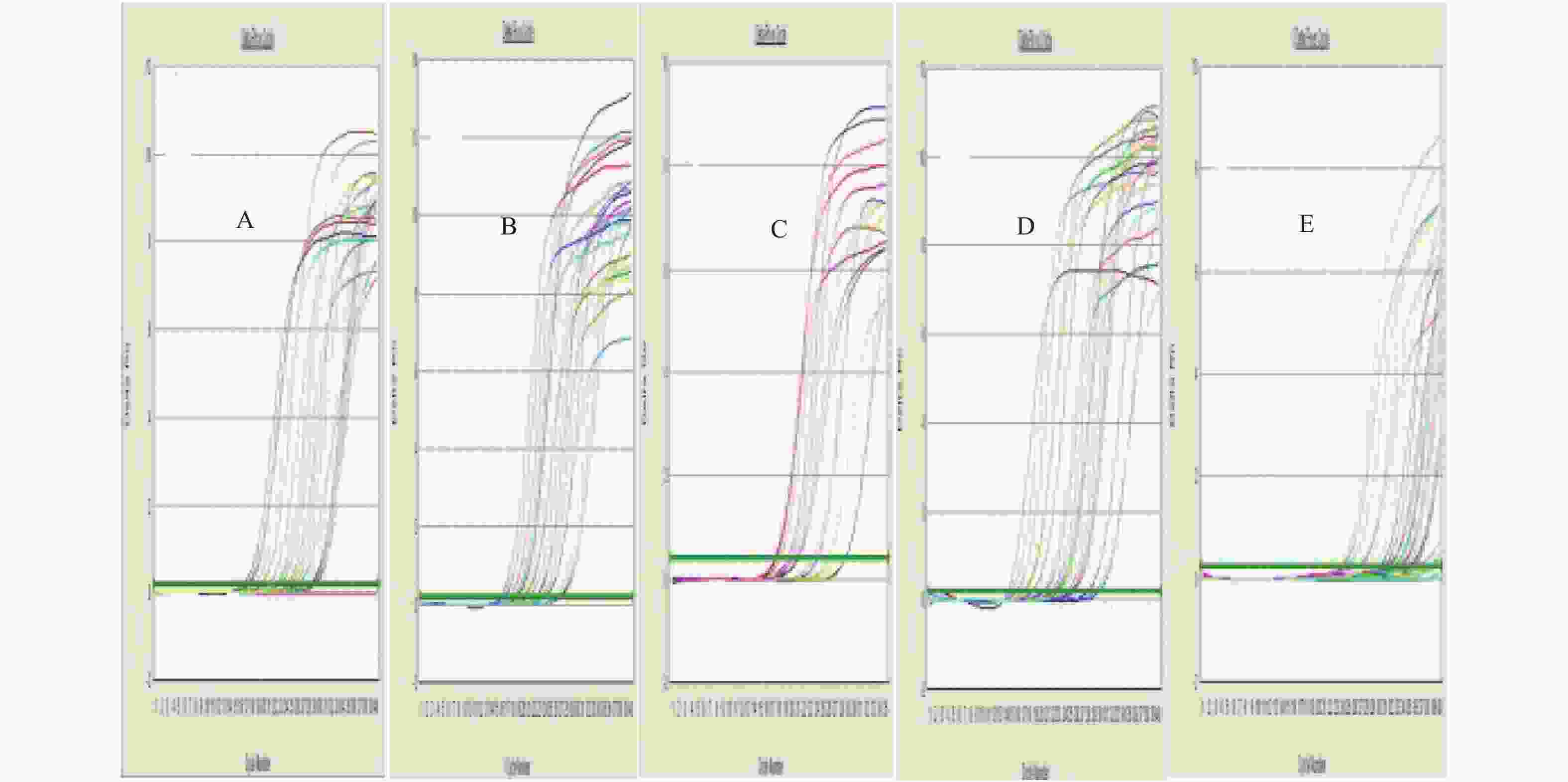
Changes of Intestinal Flora in Non-alcoholic Fatty Liver Disease
-
摘要:
目的 测定非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)患者肠道中目标细菌的数量,探讨肠道菌群在NAFLD发生发展中的作用。 方法 随机选取150例NAFLD患者,60例健康对照者,采用实时荧光定量PCR法检测粪便中目标细菌DNA的表达量。 结果 NAFLD患者粪便中的乳酸杆菌、直肠真杆菌数量显著增加(P = 0.00、P = 0.007),双歧杆菌、多形拟杆菌数量显著降低(P = 0.00、P = 0.022)。 结论 NAFLD患者肠道中存在乳酸杆菌、直肠真杆菌、双歧杆菌、多形拟杆菌的结构失衡,肠道菌群失衡可能参与NAFLD的发生发展,改善肠道菌群失衡对NAFLD具有一定治疗价值。 Abstract:Objective To observe the changes of intestinal flora in patients with non-alcoholic fatty liver disease (NAFLD) and the role in occurrence and development of the disease. Methods One hundred and fifty patients who were diagnosed as NAFLD and 60 healthy controls were randomly selected. Used the relative quantification of Real Time PCR to detecte the expression level of DNA of target bacteria. Results Compared to the control group, the quantity of Lactobacillus and Eubacterium rectale in NAFLD patients were significant increased, Bifidobacterium and Bacteroides thetaiotaomicron were decreased. Conclusion The quantity of Lactobacillus, Eubacterium rectale, Bifidobacterium, Bacteroides thetaiotaomicron in patients with NAFLD may exist structural imbalance of intestinal flora, gut microbiome probably participate in the occurrence and development of NAFLD, improve the intestinal flora imbalance has a certain treatment value in NAFLD. -
Key words:
- Intestinal flora /
- Non-alcoholic fatty liver disease /
- Phylum firmicutes /
- Bacteroidetes
-
表 1 NAFLD组与对照组目标细菌比较[M(P25,P75)]
Table 1. The target bacteria comparation of NAFLD and the control group[M(P25,P75)]
目标细菌 NAFLD组 正常对照组 Z P 多形拟杆菌 1.99(0.671,6.311) 1.854,6.267 −2.23 0.022* 直肠真杆菌 0.31(0.028,1.444) 0.003,0.340 −3.67 0.007* 双歧杆菌 0.59(0.237,2.148) 1.053,10.602 −5.06 < 0.001* 乳酸杆菌 0.24(0.001,0.247) 0.001,0.203 −2.68 < 0.001* *P < 0.05。 -
[1] Chalasani N,Younossi Z,Lavine J E,et al. The diagnosis and management of nonalcoholic fatty liver disease:practice guidance from the American Association for the Study of Liver Diseases[J]. Hepatology,2018,67(1):328-357. doi: 10.1002/hep.29367 [2] Marshall J C. The gut as a potential trigger of exercise-induced inflammatory responses[J]. Can J Physiol Pharmacol,1998,76(5):479-484. doi: 10.1139/y98-049 [3] Tilg H,Moschen A R. Evolution of inflammation in nonalcoholic fatty liver disease:the multiple parallel hits hypothesis[J]. Hepatology,2010,52(5):1836-1846. doi: 10.1002/hep.24001 [4] Polyzos S A,Kountouras J,Mantzoros C S,et al. Obesity and nonalcoholic fatty liver disease:From pathophysiology to therapeutics[J]. Metabolism,2019,92(3):82-97. [5] Yufang Ding,Karin Yanagi,Clint Cheng,et al. Interactions between gut microbiota and non-alcoholic liver disease:The role of microbiota-derived metabolites[J]. Pharmacol Res,2019,141(5):521-529. [6] Jasirwan C O M,Lesmana C R A,Hasan I,et al. The role of gut microbiota in non-alcoholic fatty liver disease:pathways of mechanisms[J]. Biosci Microbiota Food Health,2019,38(3):81-88. doi: 10.12938/bmfh.18-032 [7] Akhmedov V A,Gaus O V. Role of intestinal microbiota in the formation of non-alcoholic fatty liver disease[J]. Terapevticheskii Arkhiv,2019,91(2):143-148. [8] 易艳容,曾亚,何佳,等. 非酒精性脂肪性肝病患者肠道菌群变化及双歧杆菌三联活菌胶囊对肠道菌群、肝功能、血脂及胰岛素抵抗的影响[J].中国肝脏病杂志(电子版),2016,8(3):87-92. doi: 10.3969/j.issn.1674-7380.2016.03.019 [9] 中华医学会肝病学分会脂肪肝和酒精性肝病学组. 非酒精性脂肪性肝病诊疗指南(2010年修订版)[J].中华肝脏病杂志,2010,18(3):163-166. doi: 10.3760/cma.j.issn.1007-3418.2010.03.002 [10] Jayakumar S,Loomba R. Review article:emerging role of the gut microbiome in the progression of nonalcoholic fatty liver disease and potential therapeutic implications[J]. Aliment Pharmacol Ther,2019,50(2):144-158. doi: 10.1111/apt.15314 [11] Alexander W,Lukas J G,Frank T. Microbiome & NASH-partners in crime driving progression of fatty liver disease[J]. Z Gastroenterol,2019,57(7):871-882. doi: 10.1055/a-0755-2595 [12] Aleksandra A K,Danping Zheng,Oren S H,et al. The role of the microbiome in NAFLD and NASH[J]. EMBO Mol Med,2019,11(2):e9302. [13] Woodhouse C A,Patel V C,Singanayagam A,et al. Review article:the gut microbiome as a therapeutic target in the pathogenesis and treatment of chronic liver disease[J]. Aliment Pharmacol Ther,2018,47(2):192-202. doi: 10.1111/apt.14397 [14] Lau L H S,Wong S H. Microbiota,obesity and NAFLD[J]. Adv Exp Med Biol,2018,1061(6):111-125. [15] Mouzaki M,Comelli E M,Arendt B M,et al. Intestinal microbiota in patients with nonalcoholic fatty liver disease[J]. Hepatology,2013,58(1):120-127. doi: 10.1002/hep.26319 [16] Wong V W,Tse C H,Lam T T,et al. Molecular characterization of the fecal microbiota in patients with nonalcoholic steatohepatitis-A longitudinal study[J]. PLoS One,2013,8(4):e62885. doi: 10.1371/journal.pone.0062885 [17] Wang B,Jiang X,Cao M,et al. Altered fecal microbiota correlates with liver biochemistry in nonobese patients with non-alcoholic fatty liver disease[J]. Sci Rep,2016,8(6):32002. [18] Da Silva H E,Teterina A,Comelli E M,et al. Nonalcoholic fatty liver disease is associated with dysbiosis independent of body mass index and insulin resistance[J]. Sci Rep,2018,8(1):1466. doi: 10.1038/s41598-018-19753-9 [19] Sobhonslidsuk A,Chanprasertyothin S,Pongrujikorn T,et al. The association of gut microbiota with nonalcoholic steatohepatitis in Thais[J]. Bio Med Res Int,2018,8(16):9340316. [20] Boursier J,Mueller O,Barret M,et al. The severity of nonalcoholic fatty liver disease is associated with gut dysbiosis and shift in the metabolic function of the gut microbiota[J]. Hepatology,2016,63(3):764-775. doi: 10.1002/hep.28356 [21] Ge H,Li X,Weiszmann J,et al. Activation of G protein-coupled receptor 43 in adipocytes leads to inhibition of lipolysis and suppression of plasma free fatty acids[J]. Endocrinology,2008,149(9):4519-4526. doi: 10.1210/en.2008-0059 [22] Fetissov S O. Role of the gut microbiota in host appetite control:bacterial growth to animal feeding behaviour[J]. Nat Rev Endocrinol,2017,13(1):11-25. doi: 10.1038/nrendo.2016.150 [23] Torres-Fuentes C,Schellekens H,Dinan T G,et al. The microbiota-gut-brain axis in obesity[J]. Lancet Gastroenterol Hepatol,2017,2(10):747-756. doi: 10.1016/S2468-1253(17)30147-4 -






 下载:
下载: