Genetic Characteristic Analysis of Coxsackievirus A16 in Wenshan Prefecture of Yunnan Province in 2019
-
摘要:
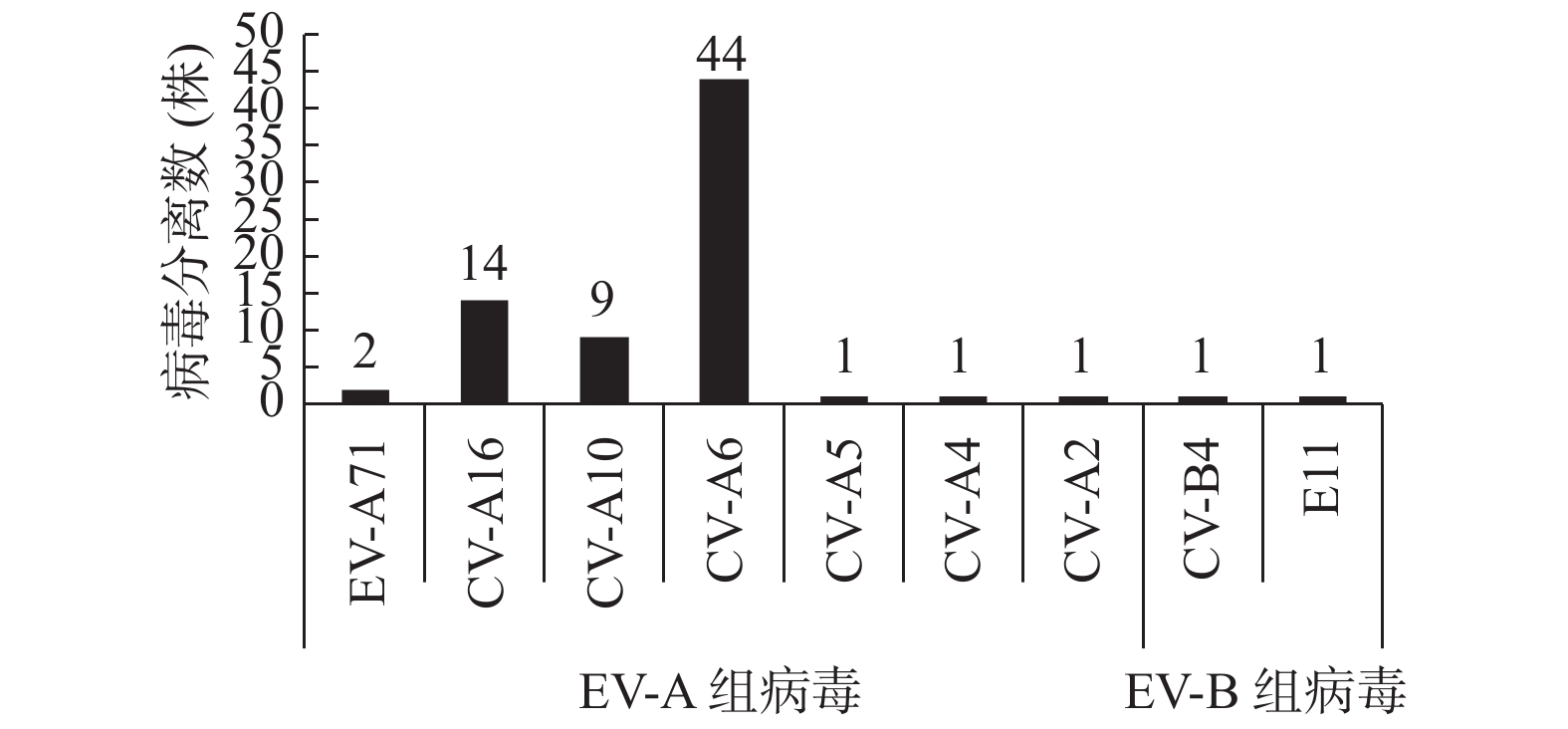
目的 对云南省文山州2019年手足口病(hand,foot and mouth disease,hfmd)病原分离情况和14株柯萨奇病毒a16型(coxsackievirus a16,cv-a16)的基因特征进行分析。 方法 对文山州2019年hfmd实验室送到云南省疾病预防控制中心hfmd实验室的595份手足口病患者粪便标本进行病毒分离,并对分离到的74株肠道病毒(enterovirus,ev)vp1区基因进行扩增和测序定型,对cv-a16病毒进行基因特征和分子流行病学分析。 结果 共从595份标本中分离到74株ev,ev分离率为12.44%(74/595),其中a组病毒(enterovirus species a,ev-a)72株,占97.30%(72/74),ev-b组病毒2株,占2.70%(2/74),未分离到ev-c和ev-d组病毒。ev-a组病毒中,cv-a6病毒最多,共44株,占ev-a组分离数的61.11%(44/72),cv-a16次之,共14株,占ev-a组病毒的19.44%(14/72),ev-a10 9株,占12.50%(9/72)。基因进化分析表明,14株cv-a16均为b1基因亚型(subgenotype b1)。它们分为2个不同的进化分支(b1a和b1b),其中8株为b1a,6株为b1b。 结论 2019年文山州hfmd病原以cv-a6组为主,cv-a16次之。cv-a16病毒b1a和b1b两个分支同时在文山州流行。 Abstract:Objective To isolate the enterovirus(EV)from 595 stool samples collected from hand, foot and mouth disease(HFMD)patients from Wenshan prefecture of Yunnan province in 2019 and to analyze the epidemiology of EVs and the genetic characteristics of coxsackievirus A16(CV-A16). Methods Virus isolated from 595 stool samples was carried out and the VP1 gene of 74 positive samples was amplified and identified by sequencing and the genetic characteristics and molecular epidemiology of CV-A16 were analyzed. Results Seventy-four strains of EVs were isolated from 595 samples with an isolation rate of 12.44(74/595), of which, 72 strains were enterovirus species A(EV-A), accounting for 97.30%(72/74), 2 strains were EV-B, accounting for 2.70%(2/74), EV-C and EV-D viruses were not isolated. Among EV-A viruses, CV-A6 was most frequently isolated, accounting for 61.11%(44/72), CV-A16 was the second, accounting for 19.44%(14/72), 9 strains were CV-A10, accounting for 12.50%(9/72). The genetic characteristics analysis showed that all 14 strains of CV-A16 belonged to subgenotype B1, they were further divided into 2 subgenotypes(B1a and B1b), among which, 8 strains were B1a subgenotype, 6 strains were B1b subgenotype. Conclusions The main etiology of HFMD in Wenshan prefecture in 2019 was CV-A6, CV-A16 was the second. Two subgenotypes(B1a and B1b)of CV-A16 co-circulated in Wenshan prefecture in 2019. -
表 1 本文所用CV-A16参考株及文山州分离株情况
Table 1. The reference strains and Wenshan strains used in this study
病毒名 基因库编号 分离年份 分离地点 基因型 J140-WS-YN-CHN-2019 LC533792 2019年 中国/云南省文山州 B1a J144-WS-YN-CHN-2019 LC533793 2019年 中国/云南省文山州 B1a J145-WS-YN-CHN-2019 LC533794 2019年 中国/云南省文山州 B1a J16-WS-YN-CHN-2019 LC533784 2019年 中国/云南省文山州 B1a J23-WS-YN-CHN-2019 LC533786 2019年 中国/云南省文山州 B1a J151-WS-YN-CHN-2019 LC533795 2019年 中国/云南省文山州 B1a J115-WS-YN-CHN-2019 LC533790 2019年 中国/云南省文山州 B1a J104-WS-YN-CHN-2019 LC533789 2019年 中国/云南省文山州 B1a GS001F-GS-CHN-2007 GQ429230 2007年 中国/甘肃省 B1a QH0202T-QH-CHN-2008 GQ429266 2008年 中国/青海省 B1a 521-06F-SD-CHN-2007 GQ429223 2007年 中国/山东省 B1a GS0151V-GS-CHN-2008 GQ429246 2008年 中国/甘肃省 B1a TS1-2000-THAI-00 AM292477 2000年 泰国 B1a S10051-SAR-98 AM292454 1998年 马来西亚 B1a 266-Toyama-2002 AB465395 2002年 日本 B1a UM15923-MAL-00 AM292481 2000年 马来西亚 B1a SB2000-SAR-00 AM292466 2000年 马来西亚 B1a GS008T-GS-CHN-2007 GQ429237 2007年 中国/甘肃省 B1b 521-01TS-SD-CHN-2007 GQ429221 2007年 中国/山东省 B1b NM0710-NM-CHN-2007 GQ429240 2007年 中国/内蒙古自治区 B1b GS0366T-GS-CHN-2008 GQ429257 2008年 中国/甘肃省 B1b GS0405V-GS-CHN-2008 GQ429260 2008年 中国/甘肃省 B1b QH0549T-QH-CHN-2008 GQ429274 2008年 中国/青海省 B1b J53-WS-YN-CHN-2019 LC533788 2019年 中国/云南省文山州 B1b J153-WS-YN-CHN-2019 LC533796 2019年 中国/云南省文山州 B1b J21-WS-YN-CHN-2019 LC533785 2019年 中国/云南省文山州 B1b J8-WS-YN-CHN-2019 LC533783 2019年 中国/云南省文山州 B1b J25-WS-YN-CHN-2019 LC533787 2019年 中国/云南省文山州 B1b J120-WS-YN-CHN-2019 LC533791 2019年 中国/云南省文山州 B1b PM-31131-05-MAL-05 JN248418 2005年 马来西亚 B1c PM-1795457-07 JN248417 2007年 马来西亚 B1c PM-1694925-06 JN248419 2006年 马来西亚 B1c PM-35210-06 JN248420 2006年 马来西亚 B1c PM-1824818-07 JN248422 2007年 马来西亚 B1c PM-1651402-06 JN248421 2006年 马来西亚 B1c SB16087-SAR-05 AM292476 2005年 马来西亚 B1c CF361090-FRA10 HE573007 2010年 法国 B1c CF335030-FRA10 HE573000 2010年 法国 B1c CF279014-FRA10 HE572994 2010年 法国 B1c CF348018-FRA10 HE573004 2010年 法国 B1c CF341014-FRA10 HE573002 2010年 法国 B1c CF355014-FRA10 HE573005 2010年 法国 B1c CF355015-FRA10 HE573006 2010年 法国 B1c CF341020-FRA10 HE573003 2010年 法国 B1c 379-Toyama-1984 AB465367 1984年 日本 B2 392-Toyama-1995 AB465370 1995年 日本 B2 24-Toyama-1981 AB465366 1981年 日本 B2 576-Toyama-1988 AB465368 1988年 日本 B2 107-Toyama-1990 AB465369 1990年 日本 B2 S70382-SAR-98 AM292461 1998年 马来西亚 B2 S10432-SAR-98 AM292455 1998年 马来西亚 B2 SB1660-SAR-00 AM292465 2000年 马来西亚 B2 SB2239-SAR-00 AM292468 2000年 马来西亚 B2 G-10 U05876 1951年 南非 A BrCr(EV-A71) U22521 1970年 美国 外部组 表 2 CV-A16基因型A、基因型B和外部组之间的nt和aa差异率(%)
Table 2. The nucleotide(nt)and amino acid(aa)diversities between CV-A16 genotype A,B and Out group(%)
基因型 基因型A 基因型B 外部组 基因型A − 7.94 28.57 基因型B 24.10 − 28.45 外部组 37.95 34.15 − 注:表左下角为核苷酸差异率,右上角为氨基酸差异率。 表 3 2019年CV-A16文山分离株B1a分支1和分支2之间及它们与基因型A和外部组的核苷酸(nt)和氨基酸(aa)差异率(%)
Table 3. The nucleotide(nt)and amino acid(aa)diversities between CV-A16 Wenshan B1a and B1b clusters,genotype A and Out group(%)
基因型/分支 B1a分支1 B1a分支2 基因型A 外部组 B1a分支1 − 1.43 8.83 28.49 B1a分支2 12.21 − 7.85 28.95 基因型A 25.14 24.33 − 28.95 外部组 35.03 34.23 38.04 − 注:表左下角为核苷酸差异率,右上角为氨基酸差异率。 -
[1] LG Chan, UD Parashar, MS Lye, et al. Deaths of children during an outbreak of hand, foot, and mouth disease in sarawak, malaysia: clinical and pathological characteristics of the disease[J]. Clin Infect Dis, 2000, 31(3): 678-683. doi: 10.1086/314032 [2] P McMinn, I Stratov, L Nagarajan, et al. Neurological manifestations of enterovirus 71 infection in children during an outbreak of hand, foot, and mouth disease in Western Australia[J]. Clin Infect Dis, 2001, 32(2): 236-242. doi: 10.1086/318454 [3] Chan KP, Goh KT, Chong CY, et al. Epidemic hand, foot and mouth disease caused by human enterovirus 71, Singapore. Emerg Infect Dis[J].2003, 9(1): 78-85. doi: 10.3201/eid1301.020112 [4] Shimizu H, Utama A, Onnimala N, et al. Molecular epidemiology of enterovirus 71 infection in the Western Pacific Region[J]. Pediatr Int, 2004, 46(2): 231-235. doi: 10.1046/j.1442-200x.2004.01868.x [5] Zhang Y, Zhu Z, Yang W, et al. An emerging recombinant human enterovirus 71 responsible for the 2008 outbreak of hand foot and mouth disease in Fuyang city of China[J]. Virol J, 2010, 7(6): 94. [6] Yang F, Ren L, Xiong Z, et al. Enterovirus 71 outbreak in the People’s Republic of China in 2008[J]. J Clin Microbiol, 2009, 47(7): 2351-2352. doi: 10.1128/JCM.00563-09 [7] 国家卫生健康委员会.手足口病诊疗指南(2018年版)[J].中国病毒病杂志, 2018, 8(5): 347-352. [8] Xiao-ni Zou, Xiao-zhuang Zhang, Bo Wang, et al. Etiologic and Epidemiologic Analysis of Hand, Foot, and Mouth Disease in Guangzhou City: A Review of 4, 753 Cases[J]. Braz J Infect Dis, 2012, 16(5): 457-465. doi: 10.1016/j.bjid.2012.08.001 [9] Wei Xu, Chun-feng Liu, Li Yan, et al. Distribution of Enteroviruses in Hospitalized Children With Hand, Foot and Mouth Disease and Relationship Between Pathogens and Nervous System Complications[J]. Virol J, 2012, 9(1): 1-8. doi: 10.1186/1743-422X-9-1 [10] Mong How Ooi, See Chang Wong, Penny Lewthwaite, et al. Clinical Features, Diagnosis, and Management of Enterovirus 71[J]. Lancet Neurol, 2010, 9(11): 1097-1105. doi: 10.1016/S1474-4422(10)70209-X [11] Wu JT, Jit M, Zheng YM, et al. Routine Pediatric Enterovirus 71 Vaccination in China: a Cost-Effectiveness Analysis[J]. Plos Medicine, 2016, 13(3): e1001975. doi: 10.1371/journal.pmed.1001975 [12] Zhu FC, Xu WB, Xia JL, et al. Efficacy, safety, and immunogenicity of an enterovirus 71 vaccine in China. N Engl J Med, 2014, 370(9): 818-828. doi: 10.1056/NEJMoa1304923 [13] Li RC, Liu LD, Mo ZJ, et al. An inactivated enterovirus 71 vaccine in healthy children. N Engl J Med, 2014; 370(9): 829-37. doi: 10.1056/NEJMoa1303224 [14] 中国疾病预防控制信息系统[EB/OL]. (2020-02-28). https://10.249.6.18:8880/portal/subSystemList.do. [15] 国家脊髓灰质炎和国家麻疹实验室. 手足口病实验室手册[K]. 第4版. 北京: 中国疾病预防控制中心, 2010: 1-49. [16] Oberste MS, Maher K, Williams AJ, et al. Species-specific RT-PCR amplification of human enteroviruses: a tool for rapid species identification of uncharacterized enteroviruses[J]. J Gen Virol, 2006, 87(1): 119-128. doi: 10.1099/vir.0.81179-0 [17] Obester MS, Maher K, Kilpatrick DR, et al. Typing of human enteroviruses by partial sequencing of VPl[J]. J Clin Microbiol, 1999, 37(5): 1288-1293. doi: 10.1128/JCM.37.5.1288-1293.1999 [18] Obester MS, Maher K, Flemister MR, et al. Comparison of Classic and Molecular Approaches for the Identification of Untypeable Enteroviruses[J]. J Clin Microbiol, 2000, 38(3): 1170-1174. doi: 10.1128/JCM.38.3.1170-1174.2000 [19] Zhang Y, Wang D, Yan D, et al. Molecular evidence of persistent epidemic and evolution of subgenotype B1 coxsackievirus A16-associated hand, foot, and mouth disease in China[J]. J Clin Microbiol. 2010, 48(2): 619-622. doi: 10.1128/JCM.02338-09 [20] Chen X, Tan X, Li J, et al. Molecular epidemiology of coxsackievirus A16: intratype and prevalent intertype recombination identified[J]. PLoS One, 2013, 8(12): e82861. doi: 10.1371/journal.pone.0082861 [21] 田晓灵, 张勇, 宋壮志, 等. 柯萨奇病毒A16型的B1a和B1b两个进化分支在内蒙古自治区共同流行[J]. 病毒学报, 2013, 29(4): 426-431. [22] 许玉玲, 卫海燕, 穆玉娇, 等. 河南省2010年柯萨奇病毒A组16型VP1区基因特征分析[J]. 中国病毒病杂志, 2011, 1(3): 200-203. [23] 文婕, 王鹏飞, 李秀芳, 等. 2015年昆明市柯萨奇病毒A16型VP1区基因特征分析[J]. 中华疾病控制杂志, 2018, 22(6): 607-612. [24] 李静, 金玉, 檀晓娟, 等. 南京市2010年柯萨奇病毒A组16型VP1区基因特征分析[J]. 中中华流行病学杂志, 2012, 33(10): 1099-1100. [25] D Perera, MA Yusof, Y Podin, et al. Molecular phylogeny of modern coxsackievirus A16[J]. Arch Virol, 2007, 152(6): 1201-1208. doi: 10.1007/s00705-006-0934-5 -






 下载:
下载: