The Correlation between Myocardial Enzymes and the Severity of Ketoacidosis in Children with Type 1 Diabetes
-
摘要:
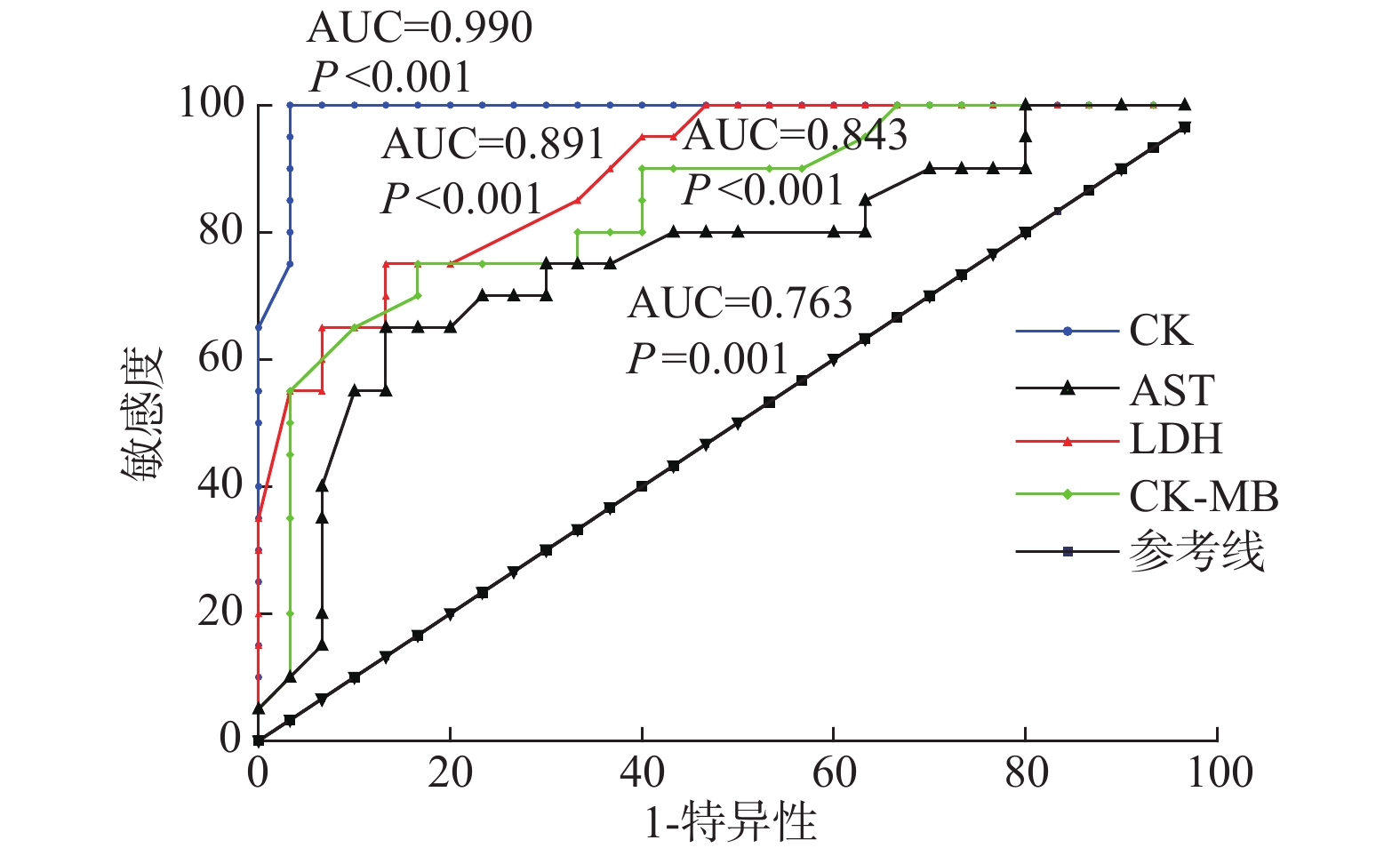
目的 探究心肌酶谱与儿童1型糖尿病酮症酸中毒(DKA)病情严重程度的相关性。 方法 选取安徽省儿童医院2016年1月至2019年12月期间收治的30例儿童1型糖尿病DKA患儿作为研究对象,另选取同期1型糖尿病非DKA患儿20例作为对照组,分析心肌酶谱与疾病严重程度的相关性。 结果 DKA组患儿血清LDH、CK、CK-MB、AST水平明显高于对照组(P < 0.05)。血清CK、LDH、CK-MB、AST对1型糖尿病患者DKA均具有一定的预测价值,ROC曲线下面积AUC分别为0.990(95%CI:0.969~1.011, P < 0.001)、0.891(95%CI:0.805~0.977, P < 0.001)、0.843(95%CI:0.731~0.956, P < 0.001)、0.763(95%CI:0.622~0.905, P < 0.001)。DKA组患儿LDH、CK水平随着病情加重逐级上升(F = 39.251,11.458;P < 0.001,< 0.001)。与缓解期比较,DKA患儿急性期血清LDH、CK、CK-MB、AST水平均升高,差异有统计学意义(P < 0.05)。Spearman相关分析结果显示,CK、LDH与DKA严重程度呈正相关(r = 0.933、0.793,P < 0.0001、< 0.0001)。 结论 随病情进展,DKA患儿心肌酶逐渐升高,动态监测患儿心肌酶指标变化,对于病情评估及治疗具有重大意义。 Abstract:Objective To investigate the correlation between myocardial enzymes and the severity of type 1 diabetic ketoacidosis in children. Methods From January 2016 to December 2019, thirty children with type 1 diabetes and DKA treated in Anhui Provincial Children's Hospital were selected as the research objects, and twenty children with type 1 diabetes and non-DKA during the same period were selected as the control group to analyze the correlation between myocardial enzymes and disease severity. Results The serum levels of LDH, CK, CK-MB and AST in children with DKA were significantly higher than those in the control group(all P < 0.05). Serum CK, LDH, CK-MB, AST had certain predictive value for DKA in patients with type 1 diabetes, the area under the ROC curve AUC was 0.990(95%CI: 0.969~1.011), 0.891(95%CI: 0.805~0.977), 0.843(95%CI: 0.731~0.956), 0.763(95%CI: 0.622~0.905). The levels of LDH and CK in children with DKA increased gradually with the progression of the disease(F = 39.251, 11.458; P < 0.001, < 0.001). Compared with the remission period, the serum levels of LDH, CK, CK-MB and AST in children with DKA increased during the acute phase, and the differences were statistically significant(all P < 0.05). Multivariate Logistic regression analysis showed that CK and LDH were the independent risk factors for DKA(OR = 1.582, 1.651, P < 0.05). Spearman correlation analysis showed that CK and LDH were positively correlated with the progression of DKA(r = 0.933, 0.793, P < 0.0001, < 0.0001). Conclusion As the disease progresses, myocardial enzymes in patients with DKA gradually increase, and dynamic monitoring of changes in myocardial enzymes in patients is of great significance for the disease evaluation and treatment. -
Key words:
- Myocardial enzymes /
- Diabetic ketoacidosis /
- Type 1 diabetes /
- Condition /
- Correlation
-
表 1 两组对象一般资料、心肌酶水平的比较(
$\bar x \pm s$ )Table 1. Comparation of basic information and myocardial enzymes between the two groups(
$\bar x \pm s$ )参数 DKA组(n = 30) 对照组(n = 20) χ2/t P 年龄(岁) 10.0 ± 2.3 12.1 ± 0.4 0.089 0.839 性别[(n),%] 男 16(53.33) 9(45.00) 0.3333 0.564 女 14(46.67) 11(55.00) BMI(kg/m2) 16.12 ± 2.87 17.67 ± 2.46 1.915 0.384 LDH(U/L) 230.01 ± 70.01 167.73 ± 2.38 7.518 0.023* CK(U/L) 542.04 ± 96.03 88.23 ± 18.03 7.373 0.025* CK-MB(U/L) 48.23 ± 4.91 24.34 ± 2.43 9.600 0.008* AST(U/L) 69.09 ± 6.09 33.09 ± 5.89 9.078 0.011* 两组比较,*P < 0.05。 表 2 急性期不同病情程度的DKA组患儿血清中心肌酶水平的比较(
$\bar x \pm s$ )Table 2. Comparation of serum levels of myocardial enzymes in acute DKA phase children with different disease severity(
$\bar x \pm s$ )DKA分级 n LDH(U/L) CK(U/L) CK-MB(U/L) AST(U/L) 轻度 13 217.75 ± 24.37 400.35 ± 12.17 30.03 ± 4.91 44.65 ± 6.19 中度 10 235.49 ± 17.54 569.49 ± 8.27 69.98 ± 5.63 89.56 ± 6.32 重度 7 375.32 ± 18.59 690.26 ± 6.84 47.98 ± 5.63 68.34 ± 5.34 F − 39.251 11.458 1.79 1.890 P − < 0.001* < 0.001* 0.173 0.169 表 3 DKA组患儿急性期和缓解期心肌酶谱对比(
$\bar x \pm s$ )Table 3. Comparation of serum myocardial enzymes in DKA children between acute and relieving stages(
$\bar x \pm s$ )时间 LDH(U/L) CK(U/L) CK-MB(U/L) AST(U/L) 急性期 230.01 ± 70.01 542.04 ± 96.03 48.23 ± 4.91 69.09 ± 6.09 缓解期 210.01 ± 67.34 305.38 ± 75.55 26.13 ± 4.54 36.78 ± 4.45 t 27.478 41.374 16.322 10.345 P 0.015* < 0.001* < 0.001* 0.021* -
[1] 中华医学会儿科分会内分泌遗传代谢学组. 儿童时期1型糖尿病诊疗常规[J].中华儿科杂志,2001,39(3):180-182. doi: 10.3760/j.issn:0578-1310.2001.03.026 [2] Cashen K,Petersen T. Diabetic Ketoacidosis[J]. Pediatrics in Review,2019,40(8):412-420. doi: 10.1542/pir.2018-0231 [3] 李进,王淑娟,吴爱英. 糖尿病酮症酸中毒致多器官功能衰竭的分析[J].中国医师杂志,2003,5(1):51-53. [4] 陈丽婷,黄春荣,周祥敏. 糖尿病急性并发症中肌酸激酶升高患者的临床特征及其临床意义探讨[J].中国地方病防治杂志,2017,32(9):插3-插4. [5] Bellazzini M A,Meyer T. Pseudo-myocardial infarction in diabetic ketoacidosis with hyperkalemia[J]. Journal of Emergency Medicine,2010,39(4):e139-e141. doi: 10.1016/j.jemermed.2007.04.024 [6] 中华医学会儿科学分会内分泌遗传代谢学组,《中华儿科杂志》编辑委员会. 中国儿童1型糖尿病标准化诊断与治疗专家共识(2020版)[J].中华儿科杂志,2020,58(6):447-454. [7] 中华医学会儿科学分会内分泌遗传代谢学组,《中华儿科杂志》编辑委员会. 儿童糖尿病酮症酸中毒诊疗指南(2009年版)[J].中华儿科杂志,2009,47(6):421-425. doi: 10.3760/cma.j.issn.0578-1310.2009.06.005 [8] Agus M S,Wolfsdorf J I. Diabetic ketoacidosis in children[J]. Pediatric Clinics of North America,2005,52(4):1147-1163. doi: 10.1016/j.pcl.2005.03.006 [9] Yang W Y,Lu J M,Weng J P,et al. Prevalence of diabetes among men and women in China[J]. The New England Journal of Medicine,2010,362(12):1090-1101. [10] Wolfsdorf J,Glaser N,Sperling M A. Diabetic ketoacidosis in infants,children,and adolescents:A consensus statement from the American Diabetes Association[J]. Diabetes Care,2006,29(5):1150-1159. doi: 10.2337/dc06-9909 [11] Moller N,Foss A C,Gravholt C H,et al. Myocardial injury with biomarker elevation in diabetic ketoacidosis[J]. J Diabetes Complications,2005,19(6):361-363. doi: 10.1016/j.jdiacomp.2005.04.003 [12] 高艳霞,张如意,刘翔. 糖尿病酮症酸中毒心肌酶谱与心电图变化的临床分析[J].宁夏医学杂志,2017,39(5):448-450. [13] Shen Y Q,Tang L,Zhou H M,et al. Structure of human muscle creatine kinase[J]. Acta Crystallographica Section D-Biological Crystallography,2001,57(Pt 8):1196-1200. [14] 曾俊,包可久,陈刘,等. 糖尿病酮症酸中毒患者血pH值、血糖水平与心肌酶、淀粉酶的相关性分析[J].疑难病杂志,2018,17(5):468-471. doi: 10.3969/j.issn.1671-6450.2018.05.009 [15] 蔡莹,罗真春,王鹏飞,等. 糖尿病酮症酸中毒或高渗性高血糖状态致横纹肌溶解临床分析[J].现代医药卫生,2015(5):651-653,656. doi: 10.3969/j.issn.1009-5519.2015.05.005 [16] 钟芳,钟碧波. 血淀粉酶、心肌酶谱与糖尿病酮症酸中毒患者病情相关性分析[J].现代仪器与医疗,2018,24(2):76-77,83. -






 下载:
下载: