Influencing Factors of Moderate to Severe Liver Injury in Patients with Chronic Hepatitis B and NAFLD
-
摘要:
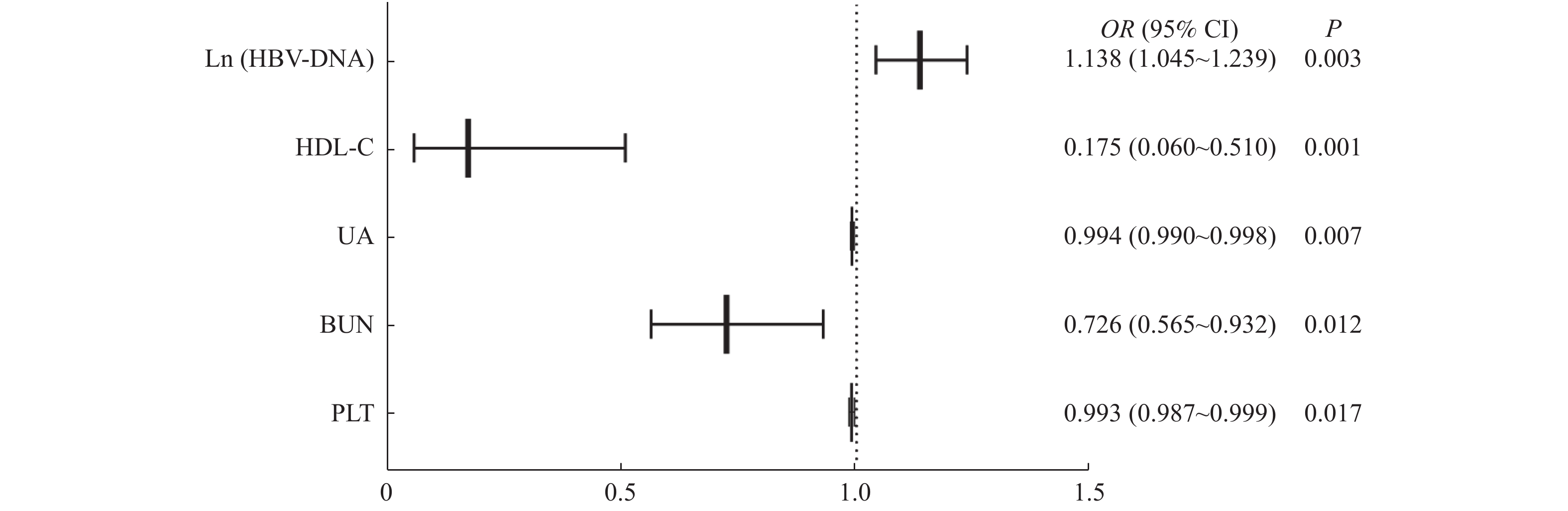
目的 探讨CHB合并NAFLD患者发生明显肝损伤的影响因素。 方法 回顾性分析2020年1月1日至2020年12月30日期间就诊于昆明市第三人民医院的225例CHB合并NAFLD患者的临床资料,根据肝损伤程度分为A组(120例,无肝损伤或轻度肝损伤)和B组(105例,中度或重度肝损伤)。对2组患者的基本资料、代谢相关指标、血细胞分析、肾功能、乙肝相关病原学等实验室资料进行单因素分析,然后将单因素分析中筛查得到的指标全部纳入二元Logistic回归分析,探索CHB合并NAFLD患者发生中度或重度肝损伤的影响因素。 结果 (1)A组 vs B组:男性占比(76.67% vs 87.62%)、HBeAg阳性占比(49.17% vs 53.91%)、CHOL[(4.89±0.95)mmol/L vs(4.23±1.17)mmol/L]、HDL-C[1.10(0.94~1.28)mmol/L vs 0.90(0.53~1.18)mmol/L]、LDL-C[3.03(2.52~3.60)mmol/L vs 2.70(2.05~3.19)mmol/L]、PLT[(202.47±60.79)×109/L vs(173.37±60.89)×109/L]、BUN[4.51(3.83~5.41)mmol/L vs 3.92(3.37~5.02)mmol/L]、UA[369.00(314.00~421.00)μmol/L vs 338.50(292.00~397.25)μmol/L]、Ln(HBV-DNA)[12.79(7.82~17.31)IU/mL vs 15.44(12.64~17.76)IU/mL]在2组间比较差异有统计学意义,均P < 0.05。(2)二元Logisitic回归分析显示,PLT[OR(95%CI) = 0.993(0.987~0.999)]、BUN[OR(95%CI) = 0.726(0.565~0.932)]、UA[OR(95%CI) = 0.994(0.990~0.998)]、HDL-C[OR(95%CI) = 0.175(0.060~0.510)]每下降1个单位,发生中重度肝损伤的可能性分别增加0.7%、27.4%、0.6%、82.5%;Ln(HBV-DNA)[OR(95%CI) = 1.138(1.045~1.239)]每升高1个单位,发生中重度肝损伤的可能性增加13.8%,均P < 0.05。 结论 HBV-DNA、HDL-C、BUN、UA、PLT是CHB合并NAFLD患者发生中度或重度肝损伤的影响因素,临床需高度重视。 Abstract:Objective To investigate the influencing factors of liver injury in patients with chronic hepatitis B (CHB) and non-alcoholic fatty liver disease (NAFLD). Methods The clinical data of 225 patients with CHB complicated with NAFLD admitted to the Third People’ s Hospital of Kunming from January 1st, 2020 to December 30th, 2020 were retrospectively analyzed. According to the liver function, they were divided into group A (120 cases, no liver injury or mild liver injury) and group B (105 cases, moderate or severe liver injury). The basic information, metabolism biomarkers, routine blood, renal functions and etiology markers of hepatitis B were used to perform an unifactor analysis. To explore the influencing factors of moderate or severe liver injury, binary logistic regression analysis were further performed. Results 1. There were significant differences in gender[group A vs. group B (the same as following): proportion of males = 76.67% vs. 87.62%], HBeAg (+/-) [(HBeAg positive) = 49.17% vs. 53.91%], CHOL[(4.89±0.95) mmol/L vs.(4.23±1.17) mmol/L], HDL-C[1.10 (0.94~1.28) mmol/L vs. 0.90 (0.53~1.18) mmol/L], LDL-C[3.03 (2.52~3.60)mmol/L vs. 2.70 (2.05~3.19) mmol/L], PLT[(202.47±60.79)*109/L vs.(173.37±60.89)*109/L], BUN[4.51 (3.83~5.41) mmol/L vs. 3.92 (3.37~5.02) mmol/L], UA[369.00 (314.00~421.00) μmol/L vs. 338.50 (292.00~397.25) μmol/L], Ln (HBV-DNA) [12.79 (7.82~17.31) IU/mL vs. 15.44 (12.64~17.76) IU/mL] between two groups (P < 0.05). 2. Binary Logisitic regression analysis showed that PLT[OR (95%CI) = 0.993 (0.987~0.999)], BUN[OR (95%CI) = 0.726 (0.565~0.932)], UA[OR (95%CI) = 0.994 (0.990~0.998)], HDL-C[OR (95%CI) = 0.175 (0.060~0.510)] were protective factors, with 1 unit decrease of which, the probability of moderate and severe liver injury increased by 0.7%, 27.4%, 0.6% and 82.5%, respectively; ; and HBV-DNA [OR (95%CI)=1.138 (1.045~1.239)] was a risk factor, the probability of moderate to severe liver damage increased by 13.8% with 1 unit increase of Ln (HBV-DNA). Conclusion HBV-DNA, HDL-C, BUN, UA and PLT are influencing factors for moderate or severe liver injury in CHB patients with NAFLD and a higher attention should to be paid. -
表 1 单因素分析CHB合并NAFLD患者发生中重度肝损伤的影响因素[
$\bar x \pm s$ /n(%)/M(P25,P75)]Table 1. Univariate analysis of suspected influencing factors of moderate to severe liver injury in patients with CHB and NAFLD[
$\bar x \pm s$ /n(%)/M(P25,P75)]临床指标 A组 B组 χ2/F/Z P 性别 女性 28(23.33) 13(12.38) 4.508 0.034* 男性 92(76.67) 92(87.62) 年龄(岁) < 30 16(13.33) 17(16.19) 0.365 0.546 ≥ 30 104(86.67) 88(83.81) HBeAg状态 阴性 61(50.83) 36(37.11) 6.252 0.012* 阳性 59(49.17) 69(53.91) BMI(kg/m2) 25.96 ± 2.91 25.25 ± 3.66 2.413 0.109 CHOL(mmol/L) 4.89 ± 0.95 4.23 ± 1.17 2.843 < 0.001* PLT(×109/L) 202.47 ± 60.79 173.37 ± 60.89 0.024 < 0.001* BUN(mmol/L) 4.51(3.83~5.41) 3.92(3.37~5.02) −3.368 0.001* CREA(mmol/L) 74.00(62.00~83.00) 72.00(60.75~80.00) −1.212 0.226 UA(μmol/L) 369.00(314.00~421.00) 338.50(292.00~397.25) −2.241 0.025* WBC(×109/L) 5.91(5.11~7.17) 5.76(4.70~6.95) −1.064 0.287 RBC(×1012/L) 5.31(4.76~5.69) 5.13(4.64~5.49) −1.877 0.060 HGB(g/L) 162.00(148.00~173.00) 159.00(144.75~169.00) −1.657 0.097 TG(mmol/L) 1.73(1.19~2.78) 1.68(1.12~2.33) −0.533 0.594 HDL-C(mmol/L) 1.10(0.94~1.28) 0.90(0.53~1.18) −4.881 < 0.001* LDL-C(mmol/L) 3.03(2.52~3.60) 2.7(2.05~3.19) −3.351 0.001* FPG(mmol/L) 5.33(5.00~5.85) 5.26(4.83~5.77) −1.495 0.135 HBsAg(IU/mL) 2703.00(667.20~23846.00) 3154.00(909.88~14839.75) −0.245 0.806 Ln(HBV-DNA)(IU/mL) 12.79(7.82~17.31) 15.44(12.64~17.76) −3.550 < 0.001* *P < 0.05。 表 2 变量赋值
Table 2. The variable assignment table
因变量(分组) 0 = A组(轻度及以下
肝损伤)1 = B组(中重度
肝损伤)自变量 性别 0 = 男性 1 = 女性 HBeAg 0 = 阳性 1 = 阴性 表 3 二元Logistic回归分析筛查CHB合并NAFLD患者发生中重度肝损伤的影响因素
Table 3. Binary logistic regression analysis to screen influencing factors of moderate to severe liver damage in patients with CHB and NAFLD
自变量 B S.E, Wals DF P OR OR的95%CI 下限 上限 性别
(参考类别:男性)−0.910 0.515 3.121 1 0.077 0.402 0.147 1.105 HBeAg状态
(参考类别:阳性)−0.007 0.391 0.000 1 0.987 0.994 0.462 2.138 PLT −0.007 0.003 5.665 1 0.017* 0.993 0.987 0.999 CHOL −0.514 0.355 2.102 1 0.147 0.598 0.299 1.198 BUN −0.321 0.128 6.288 1 0.012* 0.726 0.565 0.932 UA −0.006 0.002 7.227 1 0.007* 0.994 0.990 0.998 HDL-C −1.741 0.545 10.211 1 0.001* 0.175 0.060 0.510 LDL-C 0.421 0.398 1.117 1 0.291 1.523 0.698 3.325 Ln(HBV-DNA) 0.129 0.043 8.848 1 0.003* 1.138 1.045 1.239 常量 5.998 1.470 16.659 1 < 0.001* 402.780 *P < 0.05。 -
[1] Hanif H,Khan M M,Ali M J,et al. A new endemic of concomitant nonalcoholic fatty liver disease and chronic hepatitis B[J]. Microorganisms,2020,8(10):1526. doi: 10.3390/microorganisms8101526 [2] Hou C,Hua Z,Xu P,et al. Estimating the prevalence of hepatitis B by wastewater-based epidemiology in 19 cities in China[J]. Sci Total Environ,2020,740(10):139696. [3] Karacaer Z,Okur G,Cermik H,et al. Is there an influence of hepatic steatosis on fibrosis and necroinflammation in young patients with chronic viral hepatitis B?[J]. Postgrad Med,2016,128(7):697-700. doi: 10.1080/00325481.2016.1221733 [4] Kim D S,Jeon M Y,Lee H W,et al. Influence of hepatic steatosis on the outcomes of patients with chronic hepatitis B treated with entecavir and tenofovir[J]. Clin Mol Hepatol,2019,25(3):283-293. doi: 10.3350/cmh.2018.0054 [5] 中华医学会肝病学分会脂肪肝和酒精性肝病学组,中国医师协会脂肪性肝病专家委员会. 酒精性肝病防治指南(2018年更新版)[J]. 临床肝胆病杂志,2018,34(5):939-946. doi: 10.3969/j.issn.1001-5256.2018.05.006 [6] Schwimmer J B,Ugalde-Nicalo P,Welsh J A,et al. Effect of a low free sugar diet vs usual diet on nonalcoholic fatty liver disease in adolescent boys:a randomized clinical trial[J]. JAMA,2019,321(3):256-265. doi: 10.1001/jama.2018.20579 [7] 中华医学会感染病学分会,中华医学会肝病学会. 慢性乙型肝炎防治指南(2019年版)[J]. 临床肝胆病杂志,2019,35(12):2648-2669. [8] 杨小琴. HBV感染者外周血单核细胞Toll样受体4表达及意义[D]. 昆明: 昆明医科大学硕士学位论文, 2012. [9] Wang F S,Fan J G,Zhang Z,et al. The global burden of liver disease:the major impact of China[J]. Hepatology,2014,60(6):2099-2108. doi: 10.1002/hep.27406 [10] Sheka A C,Adeyi O,Thompson J,et al. Nonalcoholic steatohepatitis:a review[J]. JAMA,2020,323(12):1175-1183. doi: 10.1001/jama.2020.2298 [11] Liu W,Baker R D,Bhatia T,et al. Pathogenesis of nonalcoholic steatohepatitis[J]. Cellular and molecular life sciences:CMLS,2016,73(10):1969-1987. doi: 10.1007/s00018-016-2161-x [12] Mak L Y,Hui R W,Fung J,et al. Diverse effects of hepatic steatosis on fibrosis progression and functional cure in virologically quiescent chronic hepatitis B[J]. J Hepatol,2020,73(4):800-806. doi: 10.1016/j.jhep.2020.05.040 [13] Choi J S,Han K J,Lee S,et al. Serum HBV surface antigen positivity is associated with low prevalence of metabolic syndrome in Korean adult men[J]. J Epidemiol,2015,25(1):74-79. doi: 10.2188/jea.JE20140053 [14] 莫小庆,黄春,宋青青,等. 2型糖尿病伴非酒精性脂肪肝患者胱抑素C与胰岛素抵抗的相关性研究[J]. 中国医药导报,2017,14(24):78-80. [15] Brunham L R,Hayden M R. Human genetics of HDL:Insight into particle metabolism and function[J]. Prog Lipid Res,2015,58(4):14-25. [16] Lin Y Y,Hu C T,Sun D S,et al. Thioacetamide-induced liver damage and thrombocytopenia is associated with induction of antiplatelet autoantibody in mice[J]. Sci Rep,2019,9(1):17497. doi: 10.1038/s41598-019-53977-7 [17] 谢放,孟庆华,侯维,等. HBeAg阳性慢性乙型肝炎合并非酒精性脂肪肝患者的临床与病理学特征[J]. 中华实验和临床感染病杂志(电子版),2018,12(3):256-261. doi: 10.3877/cma.j.issn.1674-1358.2018.03.011 [18] Amin A A,Alabsawy E I,Jalan R,et al. Epidemiology,pathophysiology,and management of hepatorenal syndrome[J]. Semin Nephrol,2019,39(1):17-30. doi: 10.1016/j.semnephrol.2018.10.002 -






 下载:
下载: