Significance of Dynamic Monitoring of T Lymphocyte Subsets and NK Cells in Patients with Esophageal Cancer before and after the Surgery and Chemotherapy
-
摘要:
目的 探讨在食管癌患者手术及化疗前后对外周血T淋巴细胞亚群及NK细胞水平进行多时间点检测的价值及临床意义。 方法 采用流式细胞技术检测39例食管癌患者在手术及化疗前后外周血T淋巴细胞亚群和NK细胞的百分率,并与健康对照组比较并进行统计学分析。 结果 食管癌患者T淋巴细胞不同的亚群及NK细胞水平与正常人群相比差异有统计学意义(P < 0.05);手术后T淋巴细胞各亚群及NK细胞水平均较术前明显下降(P < 0.05),且在术后第3天为最低值,随后逐渐升高,但CD4+/CD8+未见明显变化;患者化疗后CD3+、CD4+比例及CD4+/CD8+有所升高,而CD8+比例下降,差异有统计学意义(P < 0.05),在化疗后3周各T淋巴细胞亚群比例与化疗前相似,化疗前后NK细胞水平虽表现出与CD3+、CD4+类似的变化趋势,但是并不显著。 结论 食管癌患者的免疫功能处于受抑制的状态,手术后免疫功能更是出现一过性降低,化疗能够一定程度上改善这种状态,但长期来看,化疗对T淋巴细胞亚群及NK细胞水平的影响可能很小,这可能支持化疗与T细胞依赖性免疫治疗在同步或序贯方案中有效结合的观点。 Abstract:Objective To explore the clinical value of peripheral blood T lymphocyte subsets and NK cell levels measured at multi-time points in patients with esophageal cancer. Methods A total of 39 cases of esophageal cancer patients were enrolled. Flow cytometry was used to detect the T lymphocyte subsets and NK cells in peripheral blood before and after the surgery and chemotherapy. Another 39 cases of healthy adults in the clinic during the same period were included as the control group, and the level of T lymphocyte subsets and NK cells were detected in the same way. Results The proportions of lymphocytes subsets and the levels of NK cells in patients with esophageal cancer were significantly lower compared with the control group before the surgery and chemotherapy (P < 0.05), and decreased significantly after the surgery (P < 0.05), the lowest value was found on the 3rd day after the surgery, then increased gradually, the ratio of CD4+/CD8+ didn’ t show the obvious difference in this period. After the chemotherapy, the proportion of CD3+、CD4+ and the ratio of CD4+/CD8+ increased significantly, while the proportion of CD8+ decreased significantly (P < 0.05). 3 weeks after the chemotherapy, the proportions of T lymphocyte subsets were similar to that before the chemotherapy. There was no significant difference in NK cells though it showed a similar trend as T lymphocyte subsets before and after the chemotherapy (P > 0.05). Conclusion The immune function of patients with esophageal cancer is in a suppressed state. After the surgery, their immune function reduced temporarily. Chemotherapy can improve this situation but it actually useful in the long term, which may support the idea of effective combinations of chemotherapy and T cell-dependent immunotherapy in a simultaneous or sequential regimen. -
Key words:
- Esophageal cancer /
- T lymphocyte subsets /
- NK cell /
- Surgery /
- Chemotherapy
-
表 1 患者基本信息(n)
Table 1. Clinical and pathological characteristics of patients enrolled in the study (n)
项目 食管癌组 正常对照组 性别(男/女) 37/2 35/4 年龄(${{\bar x} } \pm s$),岁 58.38 ± 7.48 55.50 ± 11.00 病例类型 鳞癌 39 腺癌 0 分化程度 低 9 中-低 19 中 10 中-高 1 高 0 TNM分期 Ⅰ 0 Ⅱ 29 Ⅲ 10 Ⅳ 0 表 2 食管癌组术前与对照组T细胞亚群及NK细胞水平的比较(
$\bar{x} \pm s$ )Table 2. The proportions of lymphocytes subsets and the levels of NK cells in healthy controls and in patients with esophageal cancer before surgery (
$\bar{x} \pm s$ )组别 CD3+ CD4+ CD8+ NK细胞 CD4+/CD8+ 正常对照组 72.02 ± 5.76 44.52 ± 5.15 25.96 ± 7.01 17.55 ± 6.70 1.71 ± 0.52 食管癌组 67.40 ± 8.11 38.10 ± 9.60 28.25 ± 3.74 14.46 ± 7.55 1.35 ± 0.28 t 2.497 6.413 2.232 2.843 4.834 P 0.025 0.008 0.032 0.014 < 0.001 表 3 食管癌组术前、术后T细胞亚群及NK细胞水平的变化(
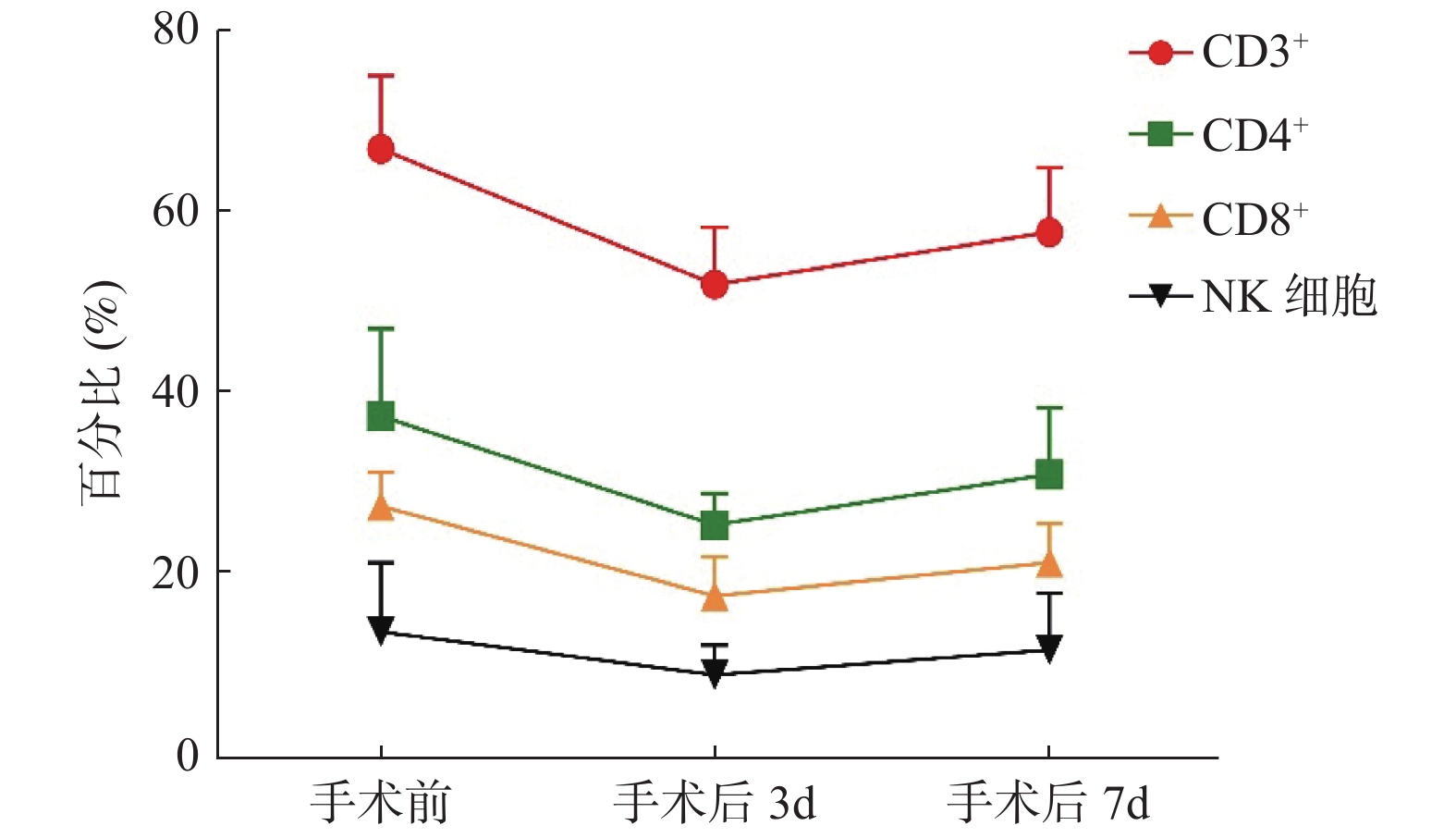
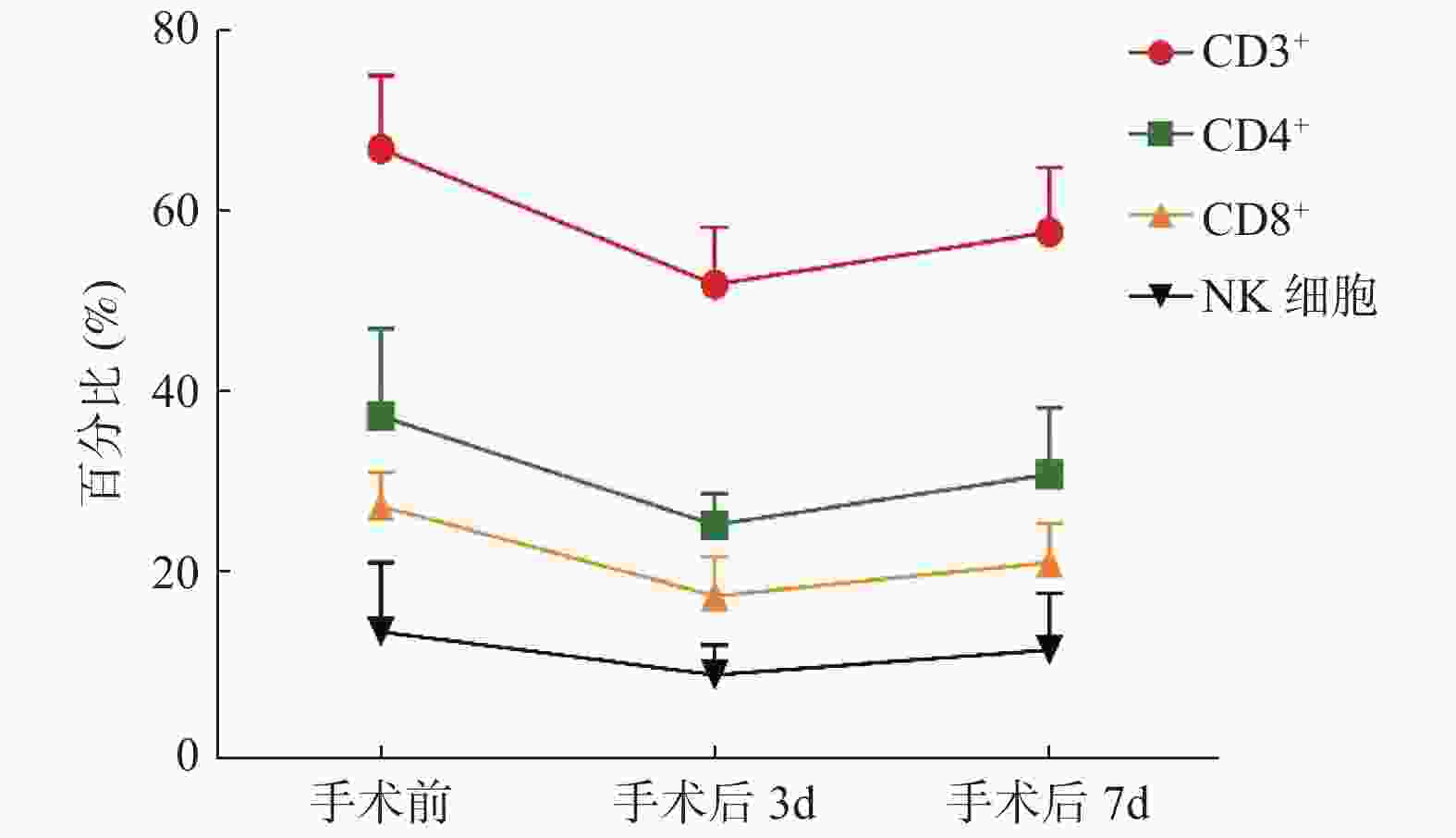
$\bar{x} \pm s$ )Table 3. The proportions of lymphocytes subsets and the levels of NK cells before and after surgery (
$\bar{x} \pm s$ )时间点 CD3+ CD4+ CD8+ NK细胞 CD4+/CD8+ 手术前 67.40 ± 8.11 38.10 ± 9.60 28.25 ± 3.74 14.46 ± 7.55 1.35 ± 0.28 手术后3 d 52.56 ± 6.29* 26.17 ± 3.45* 18.36 ± 4.26* 9.69 ± 3.27* 1.42 ± 0.58 手术后7 d 58.33 ± 7.08* 31.67 ± 7.39* 22.05 ± 4.27* 12.42 ± 6.25* 1.43 ± 0.75 F 24.985 44.659 25.476 65.440 1.290 P < 0.001 < 0.001 < 0.001 < 0.001 0.533 与手术前比较,*P < 0.05。 表 4 食管癌组化疗前后T细胞亚群水平的变化(
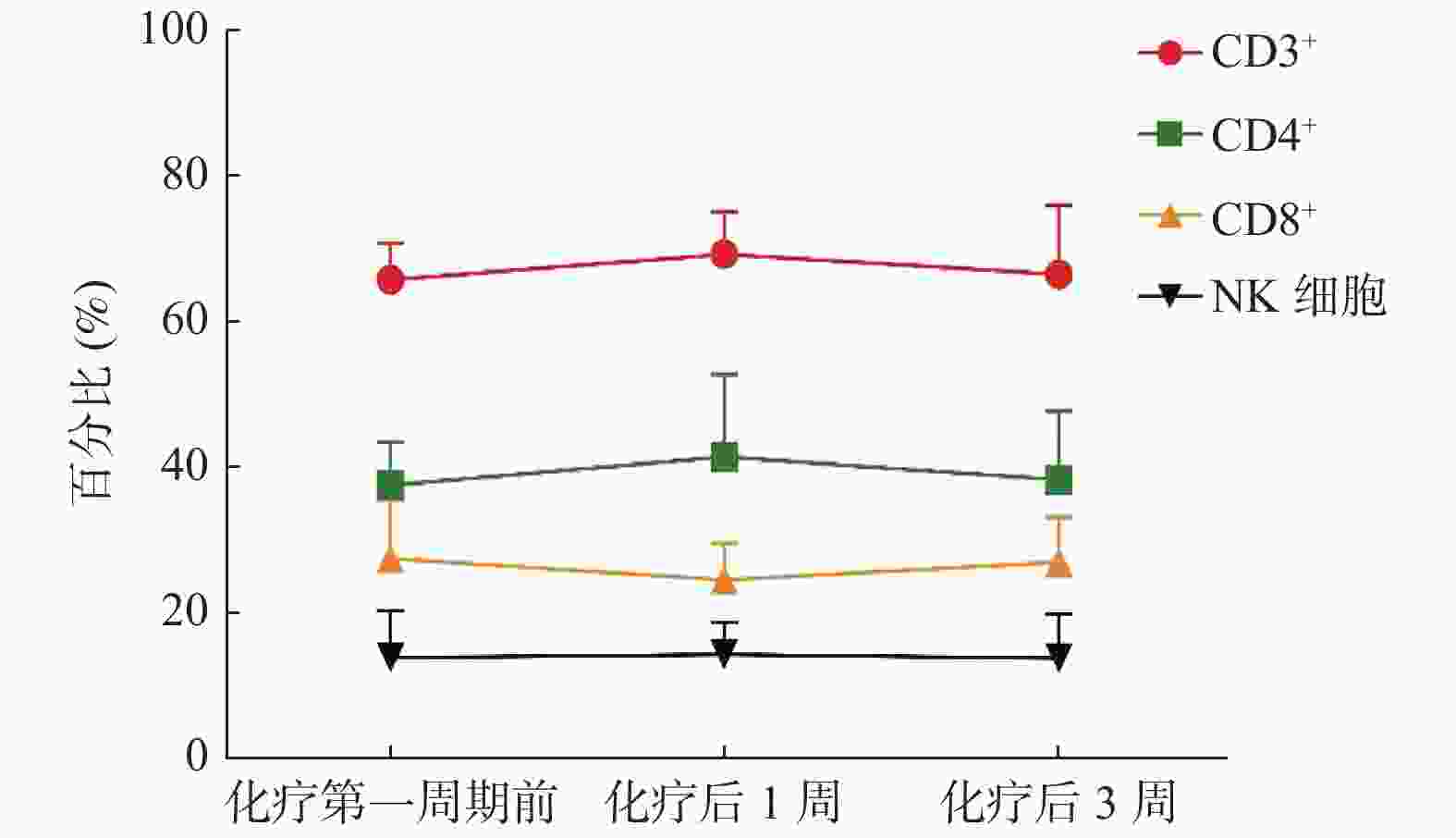
$\bar{x} \pm s$ )Table 4. The proportions of T lymphocyte subsets and NK cells in patients with esophageal cancer before and after chemotherapy (
$\bar{x} \pm s$ )时间点 CD3+ CD4+ CD8+ NK细胞 CD4+/CD8+ 化疗第一周期前 66.33 ± 4.98 38.00 ± 6.03 27.94 ± 8.16 14.41 ± 6.34 1.36 ± 0.81 化疗后1周 69.81 ± 5.79# 41.96 ± 11.21# 25.02 ± 5.05# 14.75 ± 4.49 1.68 ± 0.79# 化疗后3周 67.04 ± 9.46 38.80 ± 9.41 27.48 ± 6.13 14.30 ± 6.02 1.41 ± 0.93 F 21.012 25.231 18.439 0.646 2.655 P < 0.001 < 0.001 0.003 0.593 0.049 与化疗前比较,#P < 0.05。 -
[1] Wang Q,Yang L,Xu F,et al. Changes of Lymphocyte Subgroups in Non-Small Cell Lung Cancer Patients Before and During Chemotherapy[J]. Clinical laboratory,2015,61(10):1343-1351. [2] Gajewski T F,Woo S R,Zha Y,et al. Cancer immunotherapy strategies based on overcoming barriers within the tumor microenvironment[J]. Curr Opin Immunol,2013,25(2):268-276. doi: 10.1016/j.coi.2013.02.009 [3] Herbst R S,Soria J C,Kowanetz M,et al. Predictive correlates of response to the anti-PD-L1 antibody MPDL3280A in cancer patients[J]. Nature,2014,515(7528):563-567. doi: 10.1038/nature14011 [4] Hegde P S,Karanikas V,Evers S. The where,the when,and the how of immune monitoring for cancer immunotherapies in the era of checkpoint inhibition[J]. Clin Cancer Res,2016,22(8):1865-1874. doi: 10.1158/1078-0432.CCR-15-1507 [5] 国家卫生健康委员会. 食管癌诊疗规范(2018年版)[J]. 中华消化病与影像杂志(电子版),2019,9(4):158-192. doi: 10.3877/cma.j.issn.2095-2015.2019.04.005 [6] Rice T W,Ishwaran H,Ferguson M K,et al. Cancer of the esophagus and esophagogastric junction:An eighth edition staging primer[J]. Journal of Thoracic Oncology,2017,12(1):36-42. doi: 10.1016/j.jtho.2016.10.016 [7] 王登峰,雷利强. 食管癌患者外周血T淋巴细胞亚群水平变化及临床意义[J]. 临床医学研究与实践,2018,3(14):91-92. [8] Ubukata H,Konishi S,Nagata H,et al. Significance of preoperative evaluations of tumor necrosis factor-alpha,the granulocyte/lymphocyte ratio and their correlation with regard to outcome in gastric cancer patients[J]. Digestive Surgery,2010,27(4):324-330. doi: 10.1159/000308461 [9] 蔡子仁,王建,周新明,等. 开胸与胸腔镜手术影响肺癌患者术后调节T细胞功能和T淋巴细胞亚群的临床研究[J]. 河北医药,2019,41(19):2944-2947. doi: 10.3969/j.issn.1002-7386.2019.19.016 [10] Gomatos I P,Alevizos L,Kalathaki O,et al. Changes in T-lymphocytes’viability after laparoscopic versus open cholecystectomy[J]. Int Surg,2015,100(4):696-701. doi: 10.9738/INTSURG-D-14-00137.1 [11] 罗俐梅,罗娅,蔡宜含,等. 外周血淋巴细胞绝对计数在结直肠癌和食管癌肿瘤进展与治疗前后免疫状态评估的临床应用研究[J]. 中华临床实验室管理电子杂志,2019,7(3):137-144. [12] Westerterp M,Boermeester M A,Omloo J M,et al. Differential responses of cellular immunity in patients undergoing neoadjuvant therapy followed by surgery for carcinoma of the oesophagus[J]. Cancer Immunology,Immunotherapy,2008,57(12):1837-1847. [13] 崔鹏龙,何世杰. 全麻复合硬膜外麻醉对肺癌根治术患者外周血T细胞亚群及NK细胞活性的影响[J]. 实用癌症杂志,2020,35(2):212-214. doi: 10.3969/j.issn.1001-5930.2020.02.011 [14] 陈榕,陈国平,汪家航,等. 乳腺癌患者围手术期免疫指标的变化及其临床意义[J]. 中华肿瘤杂志,2019(11):849-853. doi: 10.3760/cma.j.issn.0253-3766.2019.11.009 [15] Krijgsman D,de Vries N L,Skovbo A,et al. Characterization of circulating T-,NK-,and NKT cell subsets in patients with colorectal cancer:The peripheral blood immune cell profile[J]. Cancer Immunology,Immunotherapy,2019,68(6):1011-1024. [16] Ogura M,Ishida T,Tsukasaki K,et al. Effects of first-line chemotherapy on natural killer cells in adult T-cell leukemia-lymphoma and peripheral T-cell lymphoma[J]. Cancer Chemother Pharmacol,2016,78(1):199-207. doi: 10.1007/s00280-016-3070-2 -





 下载:
下载: