Impact of Acute Non-normovolemic Hemodilution on Perioperative NK Cell, NKT cell and Th1/Th2 in Elderly Patients Undergoing Rectal Carcinoma Radical Resection
-
摘要:
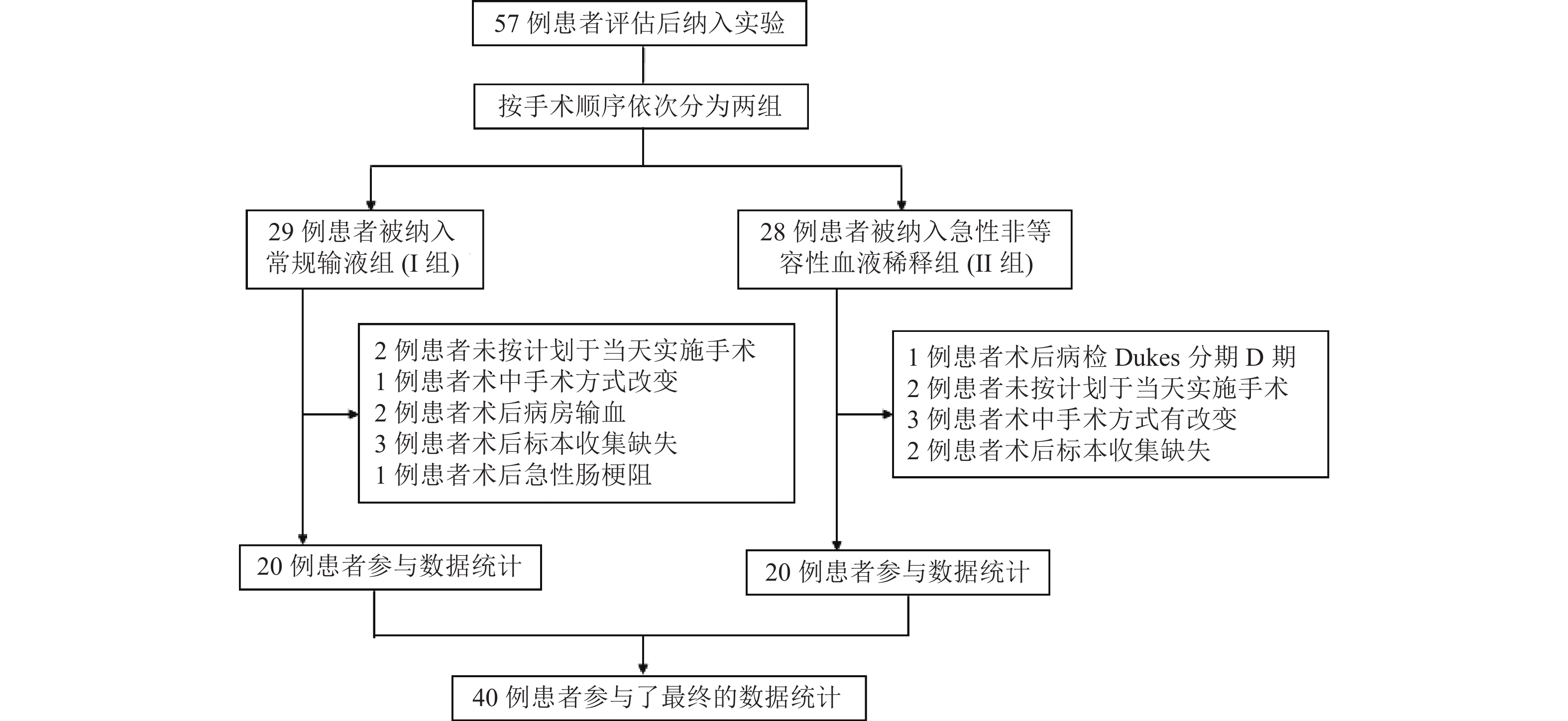
目的 观察急性非等容量血液稀释(acute nonnormovolemic hemodilution,ANIH)对于老年直肠癌根治术患者围术期NK细胞数量和毒性功能、NKT细胞数量及Th1/Th2细胞因子比值的影响。 方法 40例最终入选老年患者分为常规输液组(I组,n = 20)和ANIH组(II组,n = 20)。所有患者分别于麻醉前1 d(T1)、术后第1天(T2)、第3天(T3)、第7天(T4)抽取外周静脉血,以EPICS XL流式细胞仪检测外周血单核细胞中NK细胞数量和细胞毒性功能、NKT细胞数量、血清Th1型及Th2型细胞因子浓度,计算Th1/ Th2型细胞因子比值。 结果 与T1时比较,2组NK细胞数量T2和T3时都有升高,T3时II组升高与I组相比差异有统计学意义(P < 0.05); T4时2组都明显减少(P < 0.05),I组减少的程度明显大于II组(P < 0.05)。与T1时比较,NK细胞毒性T2时2组均有所减少,I组减少更为明显(P < 0.01),T3时2组均显著增加(P < 0.05),II组增加更为明显(P < 0.05),T4时2组均降低,基本恢复到T1时水平。与T2时比较,T3时2组NKT细胞数量都明显增高(P < 0.05),II组升高明显(P < 0.05)。T4时2组均降低,相比无统计学差异(P > 0.05)。2组Th1/Th2型细胞因子比值在各时间点,组间差异均无统计学意义(P > 0.05)。 结论 ANIH与常规输液相比可以保护和改善老年直肠癌根治术患者围术期细胞免疫功能,是一种安全有效的血液保护方法。 Abstract:Objective To investigate the impact of acute non-normovolemic hemodilution (ANIH) on the numbers of NK cell, the NK cell cytotoxicity, numbers of NKT cell and the ratio of Th1 /Th2 cytokines in elderly patients undergoing rectal carcinoma radical resection. Methods Forty patients undergoing rectal carcinoma radical resection in the final date analysis were divided into two groups: Conventional Infusion (Group I, n = 20) and ANIH (Group II, n = 20). The venous blood samples were taken at 1 day before surgery (T1), at the first day after surgery (T2), the third day after surgery (T3) and the seventh day after surgery (T4) and measured the numbers of NK cell, NKT cell, Th1 and Th2 cytokines as well as the function of NK cell cytotoxicity by flow cytometry. Then we calculated the rate of Th1/Th2 to observe its variation trend. Results Compared with groups at T1, the NK cell numbers of the two groups at T2 and T3 both increased and the growth of cell numbers from group II had significant statistical deference with that of group I at T3 (P < 0.05). Oppositely the data of both groups reduced at T4 (P < 0.05) and the reduction from group I was obviously greater than group II (P < 0.05). Compared with T1, the function of NK cell cytotoxicity of both groups decreased at T2, and the change of group I was more obviously (P < 0.01). At T3 both groups increased markedly and compared with T1 and T2 it had statistical difference (P < 0.05). The data from group II rised higher than group I (P < 0.05). The data from both groups decreased at T4, which almost restore to T1 level. Compared with T2, the NKT cell number of both groups elevated at T3 (P < 0.05), and the augment of group II was more than group I (P < 0.05). At T4 the number of both groups went lower than at T3, and there was no significant statistical difference between of two groups. The change of Th1/Th2 made no sense from statistical perspective between two groups at any time point (P > 0.05). Conclusion Compared with conventional infusion, ANIH can protect and improve the perioperation cellular immunity in elderly patients undergoing rectal carcinoma radical resection as an effective measure of blood protection. -
Key words:
- Hemodilution /
- Rectal neoplasms /
- NK cell /
- NKT cell /
- Th1/Th2
-
表 1 2组患者一般情况的比较 (
$\bar x \pm s $ )Table 1. Comparison of general information between two groups (
$\bar x \pm s $ )组别 n 项目 年龄(岁) 性别男/女 身高(cm) 体重(kg) ASA分级I/II/III Dukes分期B/C I组 20 65.15 ± 7.15 7/13 161.35 ± 6.48 57.75 ± 8.80 4/14/2 12/8 II组 20 63.25 ± 6.30 11/9 163.3 ± 6.79 59.90 ± 8.88 6/11/3 11/9 表 2 2组患者手术时间、术中出入量的比较 (
$\bar x \pm s $ )Table 2. Comparison of operating time,transfusion volume,bleeding volume and urine volume between two groups (
$\bar x \pm s $ )组别 n 项目 手术时间(min) 累计输液量(ml) 出血量(ml) 尿量(ml) I组 20 180 ± 44.52 2427 ± 478.61 376 ± 92.13 535 ± 237.92 II组 20 184 ± 55.84 3070 ± 696.87* 386 ± 89.64 562 ± 188.39 与I组比较,*P < 0.05。 表 3 2组患者不同时间点NK细胞数量组内及组间的比较[(
$\bar x \pm s $ ),%]Table 3. Comparison of the NK cell numbers at different time points in two groups and between the two groups [(
$\bar x \pm s$ ),%]组别 n T1 T2 T3 T4 I组 20 22.11 ± 7.69 23.91 ± 7.87 26.78 ± 8.87 17.97 ± 7.89△# II组 20 21.25 ± 7.55 24.36 ± 10.23 33.36 ± 9.95abd 23.64 ± 9.67#▲ 与T1时比较,*P < 0.01;与T2时比较,△P < 0.05;与T3时比较,#P < 0.05;与I组比较,▲P < 0.05。 表 4 2组患者不同时间点NK细胞毒性功能组内及组间的比较 [(
$\bar x \pm s $ ),%]Table 4. Comparison of the NK cell cytotoxicity at different time points in two groups and between the two groups [(
$\bar x \pm s $ ),%]组别 n T1 T2 T3 T4 I组 20 15.71 ± 3.47 13.18 ± 1.41* 17.95 ± 2.75*△ 15.11 ± 2.13△# II组 20 16.02 ± 4.38 14.89 ± 2.60▲ 19.82 ± 2.74*△▲ 15.82 ± 1.94# 与T1时比较,*P < 0.01;与T2时比较,△P < 0.05;与T3时比较,#P < 0.05;与I组比较,▲P < 0.05。 表 5 2组患者不同时间点NKT细胞数量组内及组间的比较 [(
$\bar x \pm s $ ),%]Table 5. Comparison of the NKT cell numbers at different time points in two groups and between the two groups [(
$\bar x \pm s $ ),%]组别 n T1 T2 T3 T4 I组 20 1.99 ± 0.77 1.70 ± 0.73 2.69 ± 1.13△ 2.02 ± 0.76 II组 20 2.04 ± 1.04 1.92 ± 0.98 3.53 ± 1.24*△▲ 2.42 ± 1.24# 与T1时比较,*P < 0.01;与T2时比较,△P < 0.05;与T3时比较,#P < 0.05;与I组比较,▲P < 0.05。 表 6 2组患者不同时间点Th1/Th2比值组内及组间的比较(
$\bar x \pm s $ )Table 6. Comparison of the ratio of Th1/Th2 cytokines at different time points in two groups and between the two groups (
$\bar x \pm s $ )组别 n T1 T2 T3 T4 I组 20 2.48 ± 0.66 2.11 ± 0.45 2.25 ± 0.42 2.40 ± 0.54 II组 20 2.45 ± 0.54 1.97 ± 0.36* 2.31 ± 0.49△ 2.43 ± 0.51△ 与T1时比较,*P < 0.01;与T2时比较,△P < 0.05。 -
[1] McSorley S T,Tham A,Dolan R D,et al. Perioperative Blood Transfusion is Associated with Postoperative Systemic Inflammatory Response and Poorer Outcomes Following Surgery for Colorectal Cancer[J]. Ann Surg Oncol,2020,27(3):833-843. doi: 10.1245/s10434-019-07984-7 [2] 丁明,蒋豪,王婷,等. 急性非等容量血液稀释用于围术期老年患者的可行性[J]. 中华麻醉学杂志,2003,23(5):343-346. doi: 10.3760/j.issn:0254-1416.2003.05.006 [3] Cooper M A,Fehniger T A,Caligiuri M A. The biology of human natural killer-cell subsets[J]. TRENDS in Immunology,2001,22(11):633-640. doi: 10.1016/S1471-4906(01)02060-9 [4] Due S,Wattchow D,Sweeney J,et al. Colorectal cancer surgery 2000–2008:evaluation of a prospective database[J]. ANZ J Surg,2012,82(6):412-419. doi: 10.1111/j.1445-2197.2012.06078.x [5] Acheson A G,Brookes M J,et al. Effects of allogeneic red blood cell transfusions on clinical outcomes inpatients undergoing colorectal cancer surgery[J]. Annals of surgery,2012,256(2):235-244. doi: 10.1097/SLA.0b013e31825b35d5 [6] Cata J P,Wang H,Gottumukkala V,et al. Inflammatory response,immunosuppression,and cancer recurrence after perioperative blood transfusions[J]. British Journal of Anaesthesia,2013,110(5):690-701. doi: 10.1093/bja/aet068 [7] Lu Q,Lu J W,Zheng W,et al. Perioperative outcome of elderly versus younger patients undergoing major hepatic or pancreatic surgery[J]. Clinical Interventions in Aging,2018,13:133-141. doi: 10.2147/CIA.S153058 [8] 戴春宇,赵光瑜,吕志勇. 急性非等容量血液稀释对直肠癌病人围术期Th1/Th2型细胞因子的影响[J]. 中华麻醉学杂志,2010,30(10):1273-1274. doi: 10.3760/cma.j.issn.0254-1416.2010.10.036 [9] Mallevaey T,Fontaine J,Breuilh L,et al. Invariant and Noninvariant Natural Killer T Cells Exert Opposite Regulatory Functions on the Immune Response during Murine Schistosomiasis[J]. Infect Immun,2007,75(5):2171-2180. doi: 10.1128/IAI.01178-06 [10] Horiuchi Y,Hanazawa A,Nakajima Y,et al. T-Helper Th1/Th2 Imbalance in the Peripheral Blood of Dogs with Malignant Tumor[J]. Microbiol Immunol,2007,51(11):1135-1138. doi: 10.1111/j.1348-0421.2007.tb03999.x -






 下载:
下载: