Comparison of Serum PCT, IL-6, SAA Levels and Clinical Characteristics between Rotavirus and Norovirus Enteritis in Children
-
摘要:
目的 研究小儿轮状病毒(RV)和诺如病毒(NV)性肠炎的血清PCT、IL-6、SAA水平的变化及临床特征,并分析二者鉴别要素。 方法 选取2019年11月至2021年01月昆明市儿童医院感染性疾病科收住院的水样腹泻、诊断病毒性肠炎的患儿作为研究对象。在入院24 h内采集粪便和收集静脉血,进行粪便轮状病毒、诺如病毒检测及血细胞、血清降钙素原(PCT)、白介素-6(IL-6)、血清淀粉样蛋白A(SAA)水平的测定,记录患儿的性别、年龄、24 h内最多的呕吐及腹泻次数、并发症、最高体温(maximum BT)、Vesikari评分等临床特征,采用多因素Logistic回归分析并通过ROC评估模型的准确性。 结果 143例患儿进入研究,其中RV76例,NV67例。RV组maximum BT,24 h内腹泻最多次数,Vesikari评分,中性粒细胞计数(NEUT)、SAA、体温 > 38 ℃病人数高于NV组,且差异有统计学意义( P < 0.05);2组在性别、年龄、24 h呕吐最多次数、并发症、Vesikari评分≥11分人数、白细胞计数(WBC)、PCT、CRP、IL-6水平比较,差异无统计学意义( P > 0.05)。多因素Logistic回归分析显示,maximum BT、NEUT、及SAA是鉴别二者的独立因素,运用ROC评估模型的准确性,其AUC 0.838 (95% CI: 0.770~0.907, P < 0.001),最大约登指数(J = 0.573),其敏感性为83.6%,特异性为73.7%。 结论 RV性肠炎相对NV来说,病情更危重,引起发热且体温 > 38 ℃的人数、24 h内腹泻次数更多。一个包含maximum BT、NEUT及SAA的模型可以协助儿科医生在未知病原体感染前进行鉴别。 Abstract:Objective To investigate the changes in serum PCT, IL-6, SAA levels and clinical characteristics of pediatric rotavirus (RV) and norovirus (NV) enteritis, and to analyze the factors for distinguishing the two. Methods In a prospective observational study, we selected children with watery diarrhea and diagnosed viral enteritis who were admitted to the Department of Infectious Diseases of Kunming Children’s Hospital from November 2019 to January 2021 as the research objects. Stool and venous blood samples were collected within 24 hours after admission for detection of fecal rotavirus and norovirus and determination of blood cells, serum procalcitonin (PCT), interleukin-6 (IL-6) and serum amyloid A (SAA). The gender, age, the most vomiting and diarrhea times within 24 h, complications, maximum BT, Vesikari score and other clinical characteristics of the children were analyzed by multivariate logistic regression and the accuracy of the model was assessed by ROC. Results 143 children were eligible, among which 76 were RV and 67 were NV. The maximum BT, the highest number of diarrhea within 24 hours, Vesikari score, neutrophil count (NEUT), SAA, and the number of patients with body temperature > 38 ℃ were significantly higher in the RV group than those in the NV group ( P < 0.05); There were no statistically significant differences in gender, age, the maximum number of vomiting at 24 h, complications, the number of people with Vesikari score ≥11, white blood cell count (WBC), PCT, CRP, and IL-6 levels ( P > 0.05). Multivariate logistic regression analysis showed that maximum BT, NEUT, and SAA were independent factors that distinguished the two. ROC was used to assess the accuracy of the model, and its AUC was 0.838 (95%CI: 0.770-0.907, P < 0.001), maximum approximate den index (J = 0.573), sensitivity was 83.6%, specificity was 73.7%. Conclusion RV enteritis causes more patients with higher fever ( > 38 ℃), and there are more frequent diarrhea within 24 hours, which is more serious than NV enteritis. A model containing maximum BT, NEUT and SAA can assist pediatricians in differential diagnosis of infection by unknown pathogens. -
表 1 修正后的Vesikari 量表
Table 1. Modified Vesikari scale
特征 0分 1分 2分 3分 腹泻持续时间(h) 0 1~96 97~120 ≥121 腹泻期间每天排便次数最大值(次) 0 1~3 4~5 ≥6 呕吐持续时间(h) 0 1~24 25~48 ≥49 腹泻期间每天呕吐次数最大值(次) 0 1 2~4 ≥5 体温最高值(℃) < 37.0 37.1~38.4 38.5~38.9 ≥39.0 预期的就诊方式 无 无 初级医疗机构 医院急诊 治疗 无 静脉补液 住院 无 表 2 RV与NV组在临床特征比较[
$ \bar x \pm s $ /n(%)]Table 2. Comparison of clinical characteristics between rotavirus and norovirus groups [
$ \bar x \pm s $ /n(%)]临床特征 RV组 NV组 t值/ χ2 P 性别(男/女) 51/25 45/22 0.000 0.994 年龄(月) 14.93 ± 0.95 13.51 ± 0.79 1.134 0.259 腹泻(最多次数/d) 9.58 ± 0.57 7.46 ± 0.45 2.189 0.030* 呕吐(最大次数/d) 3.39 ± 0.51 2.33 ± 0.30 1.739 0.084 maximum BT(℃) 38.66 ± 0.64 37.83 ± 1.08 5.544 0.000* 发热( > 38 ℃/≤38 ℃) 65/11 22/45 41.494 0.000* Vesikari评分 15.11 ± 3.11 13.76 ± 3.11 2.576 0.011* Vesikari评分(≥11分/ < 11分) 71/5 57/10 2.642 0.104 支气管肺炎 16(21.05) 10(14.93) 0.899 0.343 良性惊厥 4(5.26) 4(5.97) 0.034 0.854 病毒性脑炎 8(10.53) 2(2.99) 2.062 0.151 横纹肌溶解综合征 0(0.0) 2(0.94) - 0.218 *P <0.05。 表 3 RV组和NV组实验室检查结果比较 (
$ \bar x \pm s $ )Table 3. Comparison of Results of laboratory tests between rotavirus and norovirus groups (
$ \bar x \pm s $ )组别 WBC(×109/L) NEUT(×109/L) CRP(mg/L) PCT(ng/mL) IL-6(ng/mL) SAA(mg/L) RV组 9.09 ± 0.51 7.06 ± 0.85 8.72 ± 1.78 0.52 ± 0.07 6.65 ± 1.60 62.72 ± 9.72 NV组 9.13 ± 0.50 3.94 ± 0.39 8.45 ± 1.92 0.36 ± 0.03 3.33 ± 0.55 26.49 ± 6.52 t −0.057 3.180 0.103 2.120 1.951 3.095 p 0.955 0.002* 0.918 0.056 0.054 0.002* *P < 0.05。 表 4 鉴别RV和NV组实验室检测的诊断性能
Table 4. Diagnostic performance of laboratory tests for differentiating between rotavirus and norovirus infections
检测变量结果 AUC SEa Sigb. 95% CI for AUC PCT 0.585 0.048 0.081 0.491~0.678 IL-6 0.551 0.048 0.295 0.457~0.645 WBC 0.504 0.050 0.929 0.407~0.602 NEUT 0.778 0.042 0.000* 0.696~0.859 CRP 0.533 0.049 0.502 0.437~0.628 SAA 0.703 0.044 0.000* 0.617~0.789 a 按非参数假定;b 原假设:真区域 = 0.5。*P <0.05。 表 5 RV与NV感染鉴别因素的Logistic回归分析
Table 5. Logistic regression analysis of clinical predictors in differentiating rotavirus from norovirus infections
变量 B Sig OR 95%CI for OR Lower Upper 年龄 −0.009 0.759 0.991 0.937 1.048 NEUT −0.193 0.009* 1.824 0.713 0.953 SAA −0.009 0.025* 0.991 0.983 0.999 腹泻最多次数/d −0.102 0.057 0.903 0.814 1.003 呕吐最多次数/d −0.084 0.167 0.920 0.816 1.036 maximum BT −0.912 0.000* 3.402 0.248 0.652 常量 37.127 0.000* *P <0.05。 表 6 ROC曲线分析结果
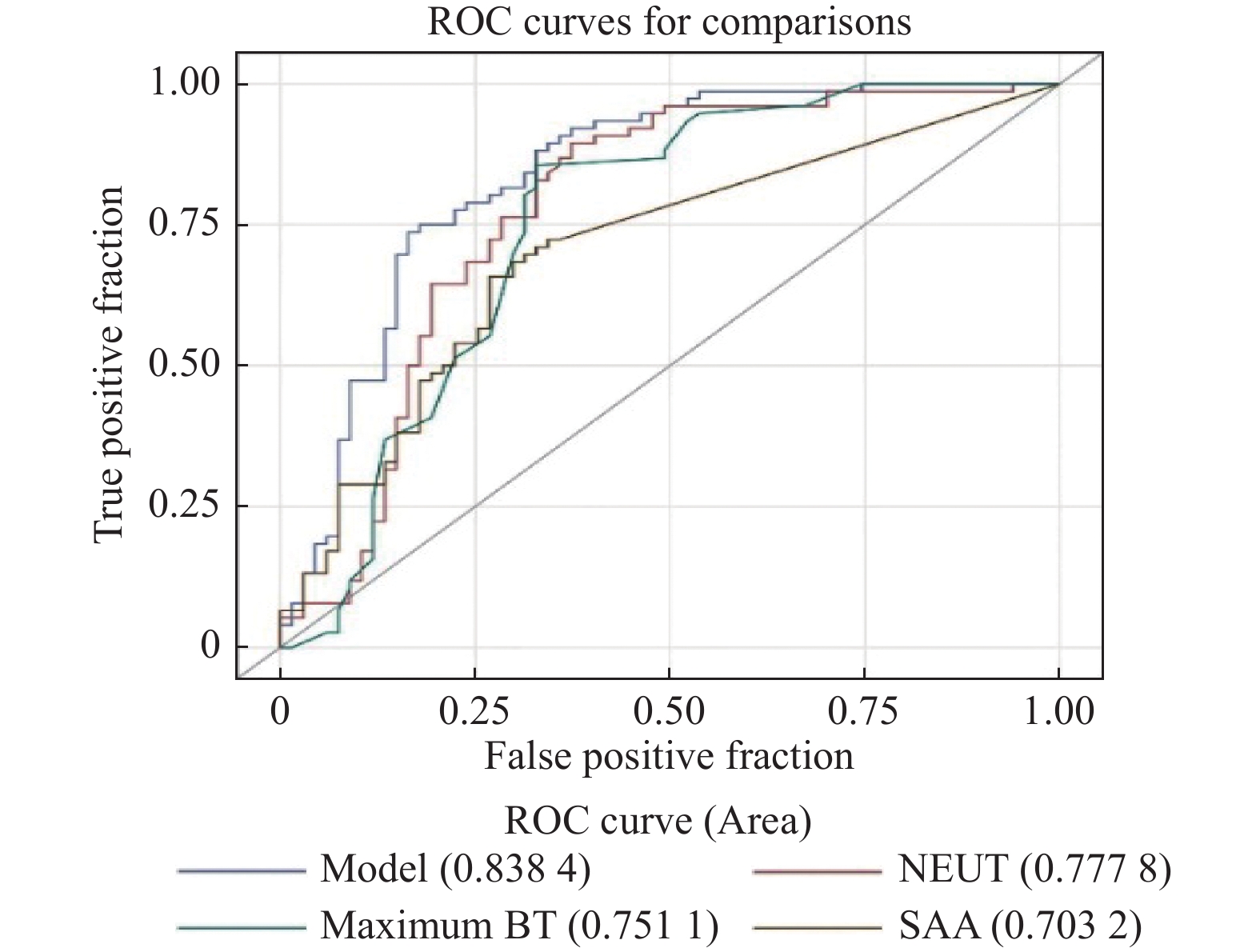
Table 6. ROC analysis results
测试变量 曲线下面积(95% CI) P 截断值 灵敏度/特异度 Model 0.8384(0.7697~0.907) < 0.001 * 0.573 0.736/0.835 NEUT 0.7778(0.6958~0.8598) < 0.001 * 5.46 0.894/0.626 maximum BT 0.7511(0.6658~0.8363) < 0.001 * 38.10 0.855/0.671 SAA 0.7032(0.6209~0.7855) 0.0075* 42.07 0.657/0.731 *P < 0.05。 -
[1] Rönnelid Y,Bonkoungou I J O,Ouedraogo N,et al. Norovirus and rotavirus in children hospitalised with diarrhoea after rotavirus vaccine introduction in Burkina Faso[J]. Epidemiology and Infect,2020,148(1):245. [2] Da Cruz Gouveia M A, Lins MTC, da Silva GAP. Acute diarrhea with blood: Diagnosis and drug treatment [J]. Jornal De Pediatria, 2020, 96(Suppl 1): 20-28. [3] 方铁夫,耿岚岚,龚四堂. 欧洲儿童急性胃肠炎处理循证指南(2014年版)[J]. 中华儿科杂志,2015,53(7):499-509. doi: 10.3760/cma.j.issn.0578-1310.2015.07.008 [4] Shin H J,Kang S H,Moon H S,et al. Serum procalcitonin levels can be used to differentiate between inflammatory and non-inflammatory diarrhea in acute infectious diarrhea[J]. Medicine,2018,97(32):11795. doi: 10.1097/MD.0000000000011795 [5] Aktaş O,Aydin H,Timurkan M O. A molecular study on the prevalence and coinfections of rotavirus,norovirus,astrovirus and adenovirus in children with gastroenteritis[J]. Minerva Pediatrica,2019,71(5):431-437. [6] Rossouw E,Brauer M,Meyer P,et al. Virus etiology,diversity and clinical characteristics in south african children hospitalised with gastroenteritis[J]. Viruses,2021,13(2):215. doi: 10.3390/v13020215 [7] Zbinden A. Virale Gastroenteritis:Es muss nicht immer Norovirus sein[J]. Praxis,2019,108(5):335-339. doi: 10.1024/1661-8157/a003182 [8] Hu M H,Lin K L,Wu C T,et al. Clinical characteristics and risk factors for seizures associated with norovirus gastroenteritis in childhood[J]. Journal of Child Neurology,2017,32(9):810-814. [9] Riera-Montes M,O'Ryan M,Verstraeten T. Norovirus and rotavirus disease severity in children:Systematic review and meta-analysis[J]. Pediatr Infect Dis J,2018,37(6):501-505. [10] Chen S M,Lin C P,Tsai J D,et al. The significance of serum and fecal levels of interleukin-6 and interleukin-8 in hospitalized children with acute rotavirus and norovirus gastroenteritis[J]. Pediatrics and Neonatology,2014,55(2):120-126. doi: 10.1016/j.pedneo.2013.05.008 [11] Eschborn S,Weitkamp J H. Procalcitonin versus C-reactive protein:Review of kinetics and performance for diagnosis of neonatal sepsis[J]. Journal of Perinatology:Official Journal of the California Perinatal Association,2019,39(7):893-903. doi: 10.1038/s41372-019-0363-4 [12] 中华医学会儿科学分会医院感染管理与控制专业委员会. 血清降钙素原检测在儿童感染性疾病中的临床应用专家共识[J]. 中华儿科杂志,2019,57(1):9-15. doi: 10.3760/cma.j.issn.0578-1310.2019.01.005 [13] 杨雪利,白静,宋紫霞,等. 血清降钙素原联合可溶性髓样细胞触发受体-1对儿童细菌性腹泻和病毒性腹泻的鉴别诊断价值[J]. 中国当代儿科杂志,2020,22(8):887-89. doi: 10.7499/j.issn.1008-8830.2002191 [14] 武宇辉,杨燕澜,张蕾,等. 血清降钙素原在儿童急性病毒性腹泻病中的临床价值探讨[J]. 中国小儿急救医学,2016,23(12):830-833. [15] Del Giudice M,Gangestad S W. Rethinking IL-6 and CRP:Why they are more than inflammatory biomarkers,and why it matters[J]. Brain,Behavior,and Immunity,2018,70(2):61-75. [16] 中国中西医结合学会检验医学专业委员会. 血清淀粉样蛋白A在感染性疾病中临床应用的专家共识[J]. 中华检验医学杂志,2019,42(3):186-192. [17] Sui Y D,Xin W N,Feng L L. Comparison of the clinical application values of PCT,hs-CRP and SAA detection in the early diagnosis of sepsis[J]. Pakistan Journal of Medical Sciences,2020,36(7):1683-1687. [18] Yang M,Liu Y,Dai J,et al. Apolipoprotein A-II induces acute-phase response associated AA amyloidosis in mice through conformational changes of plasma lipoprotein structure[J]. Sci Rep.,2018,8(1):5620. [19] Zhang Y,Zhang J,Sheng H,Li H,et al. Acute phase reactant serum amyloid A in inflammation and other diseases[J]. Advances in Clinical Chemistry,2019,90(1):25-80. [20] Sack G H Jr. Serum amyloid A (SAA) proteins[J]. Sub-Cellular Biochemistry,2020,94:421-436. -






 下载:
下载: