An Analysis of PLA2G1B Expression and Prognosis in Patients with Lung Adenocarcinoma
-
摘要:
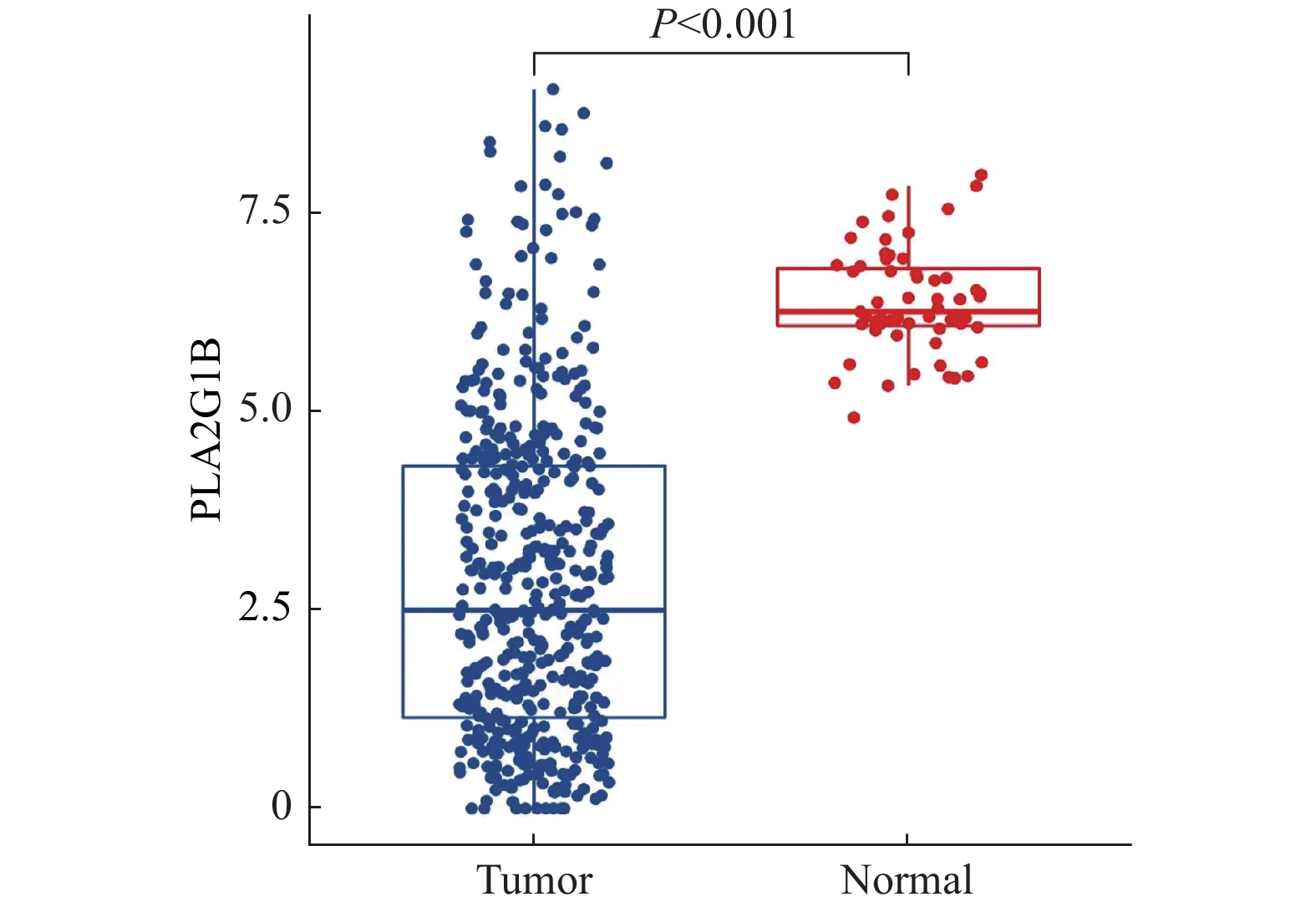
目的 基于数据挖掘分析PLA2G1B基因在肺腺癌患者中的表达特征、预后特征、免疫特征以及潜在的治疗方案影响。 方法 通过对TCGA以及GEO数据库中的肺腺癌患者RNAseq表达谱数据以及临床信息进行分析,对比PLA2G1B高表达和低表达在肺腺癌患者的预后差异,并通过CIBERSORT计算患者的免疫细胞浸润程度,对比PLA2G1B高低表达组之间的浸润程度差异。并通过pRRophetic算法分析2组之间的药物敏感性差异。 结果 PLA2G1B基因在肺腺癌组织中相比癌旁表达量显著降低,且表达量越低其患者的预后总生存越差,在TCGA以及2个GEO的独立验证数据集中均表现出一致的统计学差异,经多因素校正之后证明PLA2G1B低表达为差预后的独立因素(P < 0.05),且在预后较差的样本中其免疫浸润水平更低,主要表现为Bcellmemory,Tcell CD4+ memoryresting,Monocyte,Myeloiddendriticcell,Mastcellactivated细胞类型。但差预后的样本对多种化疗药物的敏感性要显著更好。 结论 PLA2G1B低表达为肺腺癌独立的差预后风险因素,且低表达患者中整体免疫浸润水平显著更低。 Abstract:Objective To analyze PLA2G1B gene expression, prognosis, immunologic features and potential therapeutic effects in patients with lung adenocarcinoma, based on the data-mining of public databases. Methods Data from TCGA and GEO database of LUAD were collected, including gene expression matrix and clinical data. The overall survival (OS) rate was compared between these two groups of PLA2G1B high expressed and low expressed. CIBERSORT algorithm was introduced to calculate totally 22 immune cells infiltration level and their difference was also compared between PLA2G1B high and low groups. Finally, pRRophetic was used to find some drugs that were probably sensitive to the worse OS groups. Results PLA2G1B was down regulated in LUAD samples and the lower expression of PLA2G1B led to a worse OS in LUAD, this result was validated in two independent GEO cohorts. After adjusting three main clinical elements, PLA2G1B was proved to be an independent prognosis biomarker (P < 0.05). For the worse OS group, we also found its immune infiltration level was lower than the better OS group, especially for B cell memory, T cell CD4+ memory resting, Monocyte, Myeloid dendritic cell and Mast activated cells. For the worse OS group, we found they might be more sensitive to several chemo drugs including Cisplatin, Docetaxel, Etoposide, Gemcitabine, Paclitaxeland Vinorelbine. Conclusion PLAG21B is an independent prognosis biomarker in LUAD and the ones low expressed showed worse OS and lower immune infiltration level. -
Key words:
- Lung adenocarcinoma /
- PLA2G1B /
- Prognosis /
- Data mining /
- Immune infiltration
-
表 1 GSE11969、TCGA的年龄、分期、性别分布情况
Table 1. GSE11969、TCGA age,stage,gender distribution
项目 合计(n = 580) GSE11969(n = 90) TCGA(n = 490) 年龄 平均值 64.55 (10.08) 61.02 (9.80) 65.21 (10.01) 中位值 65.00(59.00、72.00) 62.00(55.00、67.00) 66.00(59.00、72.00) 不详 10 (1.72%) 0 (0.00%) 10 (2.04%) 分期n(%) Ⅰ 315 (54.31) 52 (57.78) 263 (53.67) Ⅱ 128 (22.07) 13 (14.44) 115 (23.47) Ⅲ 104 (17.93) 25 (27.78) 79 (16.12) Ⅳ 25 (4.31) 0 (0.00) 25 (5.10) 不详 8 (1.38) 0 (0.00) 8 (1.63) 性别n(%) 女 305 (52.59) 43 (47.78) 262 (53.47) 男 275 (47.41) 47 (52.22) 228 (46.53) 表 2 GSE72094、TCGA的年龄、分期、性别分布情况
Table 2. GSE72094、TCGA age,stage,gender distribution overall
项目 合计(n = 888) GSE72094(n = 398) TCGA(n = 490) 年龄 平均值 67.09 (9.97) 69.36 (9.45) 65.21 (10.01) 中位值 68.00(60.25、74.00) 70.00(64.00、76.00) 66.00(59.00、72.00) 不详 10 (1.13%) 0 (0.00%) 10 (2.04%) 分期n(%) Ⅰ 517 (58.22) 254 (63.82) 263 (53.67) Ⅱ 182 (20.50) 67 (16.83) 115 (23.47) Ⅲ 136 (15.32) 57 (14.32) 79 (16.12) Ⅳ 40 (4.50) 15 (3.77) 25 (5.10) 不详 13 (1.46) 5 (1.26) 8 (1.63) 性别n(%) 女 484 (54.40) 222 (55.78) 262 (53.47) 男 404 (45.50) 176 (44.22) 228 (46.53) -
[1] Siegel,R L,K. D. Miller,A. Jemal. Cancer statistics 2020[J]. CA Cancer J Clin,2020,70(1):7-30. doi: 10.3322/caac.21590 [2] Sung H,Ferlay J,Siegel R L,et al. Global cancer stastistics 2020:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2021,71(3):209-249. doi: 10.3322/caac.21660 [3] Little A G,Gay E G,Gaspar L E,et al. National survey of non-small cell lung cancer in the United States:Epidemiology,pathology and patterns of care[J]. Lung Cancer,2007,57(3):253-260. doi: 10.1016/j.lungcan.2007.03.012 [4] Kleczko E K,Kwak J W,Schenk E L,et al. Targeting the complement pathway as a therapeutic strategy in lung cancer[J]. Front Immunol,2019,10(10):954. [5] Herbst R S,Soria J C,Kowanetz M,et al. Predictive correlates of response to the anti-PD-L1 antibody MPDL3280A in cancer patients[J]. Nature,2014,515(7528):563-567. doi: 10.1038/nature14011 [6] Shukuya T,Carbone D P. Predictive markers for the efficacy of anti-PD-1/PD-L1 antibodies in lung cancer[J]. J Thorac Oncol,2016,11(7):976-988. doi: 10.1016/j.jtho.2016.02.015 [7] Rizvi N A,Hellmann M D,Snyder A,et al. Cancer immunology. Mutational landscape determines sensitivity to PD-1 blockade in non-small cell lung cancer[J]. Science,2015,348(6230):124-128. doi: 10.1126/science.aaa1348 [8] Kanda A,Tamaki M,Nakamura E,et al. Characterization of recombinant human and rat pancreatic phospholipases A2 secreted from saccharomyces cerevisiae:Difference in proteolytic processing[J]. Biochim Biophys Acta,1992,1171(1):1-10. doi: 10.1016/0167-4781(92)90133-K [9] Hu B,Yang X B,Sang X T. Construction of a lipid metabolism-related and immune-associated prognostic signature for hepatocellular carcinoma[J]. Cancer Medicine,2020,9(20):7646-7662. doi: 10.1002/cam4.3353 [10] Matsuyama Y,Suzuki M,Arima C,et al. Proteasomal non-catalytic subunit PSMD2 as a potential therapeutic target in association with various clinicopathologic features in lung adenocarcinomas[J]. Mol Carcinog.,2011,50(4):301-309. doi: 10.1002/mc.20632 [11] Schabath M B,Welsh E A,Fulp W J,et al. Differential association of STK11 and TP53 with KRAS mutation-associated gene expression,proliferation and immune surveillance in lung adenocarcinoma[J]. Oncogene,2016,35(24):3209-3216. doi: 10.1038/onc.2015.375 [12] Chen B,Khodadoust M S,Liu CL,et al. Profiling tumor infiltrating immune cells with CIBERSORT[J]. Methods Mol Biol,2018,17(11):243-259. [13] Geeleher P,Cox N,Huang R S. pRRophetic:An R package for prediction of clinical chemotherapeutic response from tumor gene expression levels[J]. PloS One,2014,9(9):e107468. doi: 10.1371/journal.pone.0107468 [14] Selvanesan B C,Chandra D,Quispe-Tintaya W,et al. Listeria delivers tetanus toxoid protein to pancreatic tumors and induces cancer cell death in mice[J]. Sci Transl Med,2022,14(637):1600. doi: 10.1126/scitranslmed.abc1600 -






 下载:
下载: