LINC00341 Inhibits the Proliferation of Lung Adenocarcinoma Cells Through the MAPK Pathway
-
摘要:
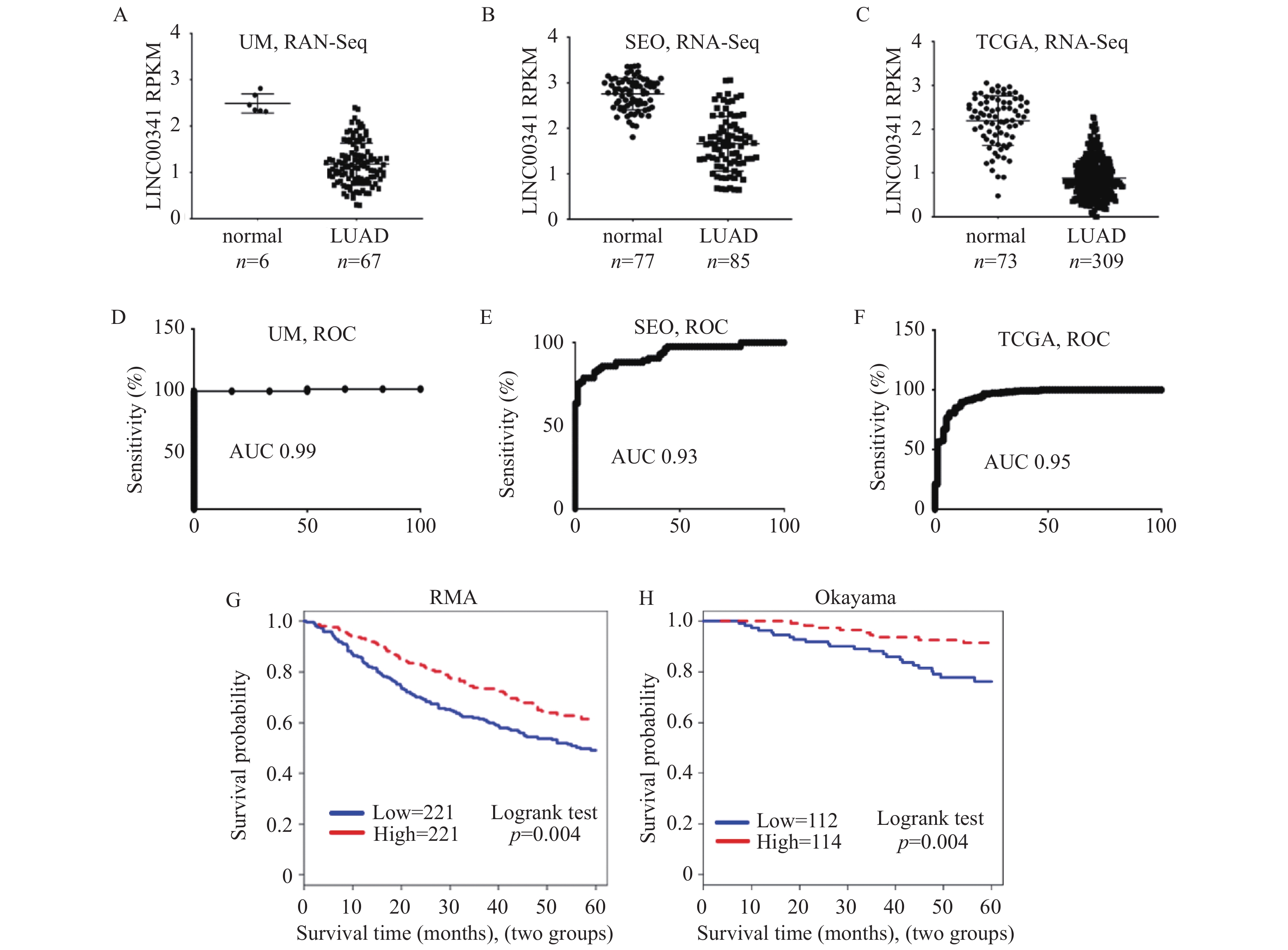
目的 探讨LINC00341对肺腺癌细胞增殖的影响及其潜在机制。 方法 在公共数据集SEO和TCGA中分析肺腺癌中LINC00341 mRNA的表达,ROC曲线分析其诊断价值,对RMA和OKAYAMA数据进行生存分析,并通过美国密歇根大学医院肺癌样本进行RNA-seq验证和ROC曲线分析;结合基因本体(gene otology,GO)分析LINC00341基因生物学功能;通过siRNA沉默LINC00341的表达,根据不同处理分为对照组(NT)和沉默组(siLINC00341),并验证细胞转染效率;采用WST-1和平板克隆实验检测细胞增殖能力;RNA亚细胞定位检测LINC00341定位,Western blotting检测其对MAPK信号通路相关蛋白表达水平的影响。 结果 LINC00341在肺腺癌组织中低表达(3个数据集P < 0.0001),ROC曲线分析表明其可作为肺腺癌的诊断标记物,同时低表达LINC00341与患者较好的预后相关( P = 0.004)。GO富集分析结果表明LINC00341主要与RNA聚合酶II启动子转录调控、蛋白质结合等有关。沉默LINC00341可以促进肺腺癌细胞的增殖(P < 0.05)和克隆形成( P < 0.05),且MAPK信号通路蛋白STAT3和ERK均被激活( P < 0.05),RNA定位显示LINC00341主要分布在细胞核。 结论 LINC00341可能在转录水平调控MAPK通路,进而抑制肺腺癌发展,并可作为肺腺癌重要的诊断和预后标志物。 Abstract:Objective To explore the underlying mechnisms and effect of LINC00341 on the proliferation of lung adenocarcinoma cells. Methods The expression of LINC00341 mRNA in lung adenocarcinoma was analyzed in public data set SEO and TCGA, and its diagnostic value was analyzed by ROC curve. Survival analysis was performed on RMA and OKAYAMA data, and RNA-seq validation and ROC curve analysis were performed on lung cancer samples from Hospital of University of Michigan, USA. The biological function of LINC00341 gene was analyzed by gene otology (GO). The expression of LINC00341 was silenced by siRNA and cells were divided into control group (NT) and silenced group (siLINC00341) according to different treatments, and the transfection efficiency was verified. Cell proliferation was detected by WST-1 and plate cloning assay. RNA subcellular localization was detected for LINC00341 localization, and Western blot was used to detect the effect of LINC00341 on the expression level of proteins related to MAPK signaling pathway. Results Low expression of LINC00341 was found in lung adenocarcinoma tissues (P < 0.0001 for 3 data sets). ROC curve analysis indicated that LINC00341 could be used as a biomarker for lung adenocarcinoma , and low expression of LINC00341 was associated with better prognosis in patients ( P = 0.004). GO enrichment analysis showed that LINC00341 was mainly related to transcriptional regulation of RNA polymerase II promoter and protein binding. Silencing LINC00341 could promote the proliferation of lung adenocarcinoma cells (P < 0.05) and clone formation ( P < 0.05) , and the MAPK signaling pathway proteins STAT3 and ERK were activated ( P < 0.05). RNA localization showed that LINC00341 was mainly distributed in the nuclear. Conclusion LINC00341 may regulate MAPK pathway at transcriptional level, thus inhibiting the development of lung adenocarcinoma, and can be used as an important diagnostic and prognostic marker for lung adenocarcinoma. -
Key words:
- Lung adenocarcinoma /
- LINC00341 /
- MAPK
-
图 4 沉默LINC00341对通路蛋白的影响以及LINC00341的亚细胞定位
A:qRT-PCR显示LINC00341在肺腺癌细胞中的核和细胞质部分;B:Western blot检测LINC00341沉默后STAT3(信号传导及转录激酶蛋白),ERK1/2(细胞外调节蛋白激酶)和P38(丝裂原活化蛋白激酶)蛋白表达情况;C:各个目的蛋白相对表达水平。*P < 0.05,**P < 0.01,***P < 0.001。
Figure 4. Effect of silencing LINC00341 on proteins and subcellular localization of LINC00341
-
[1] Sung H,Ferlay J,Siegel R L,et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2021,71(3):209-249. doi: 10.3322/caac.21660 [2] Turner M C,Andersen Z J,Baccarelli A,et al. Outdoor air pollution and cancer: An overview of the current evidence and public health recommendations[J]. CA Cancer J Clin,2020, published online ahead of print. [3] Malhotra J,Malvezzi M,Negri E,et al. Risk factors for lung cancer worldwide[J]. Eur Respir J,2016,48(3):889-902. [4] Succony L,Rassl D M,Barker A P,et al. Adenocarcinoma spectrum lesions of the lung: Detection,pathology and treatment strategies[J]. Cancer Treat Rev,2021,99:102237. doi: 10.1016/j.ctrv.2021.102237 [5] Guo C J,Ma X K,Xing Y H,et al. Distinct processing of lncRNAs contributes to non-conserved functions in stem cells[J]. Cell,2020,181(3):621-636.e622. doi: 10.1016/j.cell.2020.03.006 [6] Qian X,Zhao J,Yeung P Y,et al. Revealing lncRNA structures and interactions by sequencing-based approaches[J]. Trends Biochem Sci,2019,44(1):33-52. [7] Nojima T,Proudfoot N J. Mechanisms of lncRNA biogenesis as revealed by nascent transcriptomics[J]. Nat Rev Mol Cell Biol,2022,23(6):389-406. doi: 10.1038/s41580-021-00447-6 [8] Slack F J,Chinnaiyan A M. The role of non-coding RNAs in oncology[J]. Cell,2019,179(5):1033-1055. doi: 10.1016/j.cell.2019.10.017 [9] Wang H,Meng Q,Qian J,et al. Review: RNA-based diagnostic markers discovery and therapeutic targets development in cancer[J]. Pharmacol Ther,2022,234:108123. doi: 10.1016/j.pharmthera.2022.108123 [10] Bhan A,Soleimani M,Mandal S S. Long noncoding RNA and cancer: A new paradigm[J]. Cancer Res,2017,77(15):3965-3981. doi: 10.1158/0008-5472.CAN-16-2634 [11] Li S,Chen S,Wang B,et al. The long noncoding RNA LINC00341 suppresses colorectal carcinoma by preventing cell migration and apoptosis[J]. Cell Biochem Funct,2020,38(3):266-274. doi: 10.1002/cbf.3473 [12] Yang Q,Li X,Zhou Y,et al. A LINC00341-mediated regulatory pathway supports chondrocyte survival and may prevent osteoarthritis progression[J]. J Cell Biochem,2019,120(6):10812-10820. doi: 10.1002/jcb.28372 [13] Pan L,Tan Y,Wang B,et al. Caspase recruitment domain containing protein 9 suppresses non-small cell lung cancer proliferation and invasion via inhibiting MAPK/p38 pathway[J]. Cancer Res Treat,2020,52(3):867-885. doi: 10.4143/crt.2019.606 [14] Zheng G,Shen Z,Chen H,et al. Metapristone suppresses non-small cell lung cancer proliferation and metastasis via modulating RAS/RAF/MEK/MAPK signaling pathway[J]. Biomed Pharmacother,2017,90:437-445. doi: 10.1016/j.biopha.2017.03.091 [15] Okayama H,Kohno T,Ishii Y,et al. Identification of genes upregulated in ALK-positive and EGFR/KRAS/ALK-negative lung adenocarcinomas[J]. Cancer Res,2012,72(1):100-111. doi: 10.1158/0008-5472.CAN-11-1403 [16] Irizarry R A,Hobbs B,Collin F,et al. Exploration,normalization,and summaries of high density oligonucleotide array probe level data[J]. Biostatistics,2003,4(2):249-264. doi: 10.1093/biostatistics/4.2.249 [17] Seo J S,Ju Y S,Lee W C,et al. The transcriptional landscape and mutational profile of lung adenocarcinoma[J]. Genome Res,2012,22(11):2109-2119. doi: 10.1101/gr.145144.112 [18] Cancer genome atlas research network. Comprehensive molecular profiling of lung adenocarcinoma [J]. Nature, 2014, 511(7511): 543-550. [19] Dhanasekaran S M,Balbin O A,Chen G,et al. Transcriptome meta-analysis of lung cancer reveals recurrent aberrations in NRG1 and Hippo pathway genes[J]. Nat Commun,2014,5:5893. doi: 10.1038/ncomms6893 [20] Liao Y,Wang J,Jaehnig E J,et al. WebGestalt 2019: Gene set analysis toolkit with revamped UIs and APIs[J]. Nucleic Acids Res,2019,47(W1):W199-W205. doi: 10.1093/nar/gkz401 [21] Yan H,Bu P. Non-coding RNA in cancer[J]. Essays Biochem,2021,65(4):625-639. [22] Zhang Y X,Yuan J,Gao Z M,et al. LncRNA TUC338 promotes invasion of lung cancer by activating MAPK pathway[J]. Eur Rev Med Pharmacol Sci,2018,22(2):443-449. [23] Hua Q,Jin M,Mi B,et al. LINC01123,a c-Myc-activated long non-coding RNA,promotes proliferation and aerobic glycolysis of non-small cell lung cancer through miR-199a-5p/c-Myc axis[J]. J Hematol Oncol,2019,12(1):91. doi: 10.1186/s13045-019-0773-y [24] Del Real A,López-Delgado L,Sañudo C,et al. Long noncoding RNAs as bone marrow stem cell regulators in osteoporosis[J]. DNA Cell Biol,2020,39(9):1691-1699. doi: 10.1089/dna.2020.5672 [25] Wang L,He Y,Liu W,et al. Non-coding RNA LINC00857 is predictive of poor patient survival and promotes tumor progression via cell cycle regulation in lung cancer[J]. Oncotarget,2016,7(10):11487-11499. doi: 10.18632/oncotarget.7203 [26] Fang J Y,Richardson B C. The MAPK signalling pathways and colorectal cancer[J]. Lancet Oncol,2005,6(5):322-327. doi: 10.1016/S1470-2045(05)70168-6 [27] Liu F,Yang X,Geng M,et al. Targeting ERK,an Achilles' Heel of the MAPK pathway,in cancer therapy[J]. Acta Pharm Sin B,2018,8(4):552-562. doi: 10.1016/j.apsb.2018.01.008 [28] Ullah R,Yin Q,Snell A H,et al. RAF-MEK-ERK pathway in cancer evolution and treatment[J]. Semin Cancer Biol,2022,85:123-154. [29] Yang S H,Sharrocks A D,Whitmarsh A J. MAP kinase signalling cascades and transcriptional regulation[J]. Gene,2013,513(1):1-13. doi: 10.1016/j.gene.2012.10.033 [30] Ye D,Li Y,Zhang H,et al. Silencing PRSS1 suppresses the growth and proliferation of gastric carcinoma cells via the ERK pathway[J]. Int J Biol Sci,2021,17(4):957-971. doi: 10.7150/ijbs.52591 [31] Pranteda A,Piastra V,Stramucci L,et al. The p38 MAPK signaling activation in colorectal cancer upon therapeutic treatments[J]. Int J Mol Sci,2020,21(8):2773. doi: 10.3390/ijms21082773 [32] Feng S,Zhang J,Su W,et al. Overexpression of LINC00152 correlates with poor patient survival and knockdown impairs cell proliferation in lung cancer[J]. Sci Rep,2017,7(1):2982. doi: 10.1038/s41598-017-03043-x [33] Jiang Q G,Xiong C F,Lv Y X. Kin17 facilitates thyroid cancer cell proliferation,migration,and invasion by activating p38 MAPK signaling pathway[J]. Mol Cell Biochem,2021,476(2):727-739. doi: 10.1007/s11010-020-03939-9 -






 下载:
下载: