Enhanceing Effect of EZH2 Inhibitors in Combination with GC Chemotherapeutic Agents in Bladder Cancer
-
摘要:
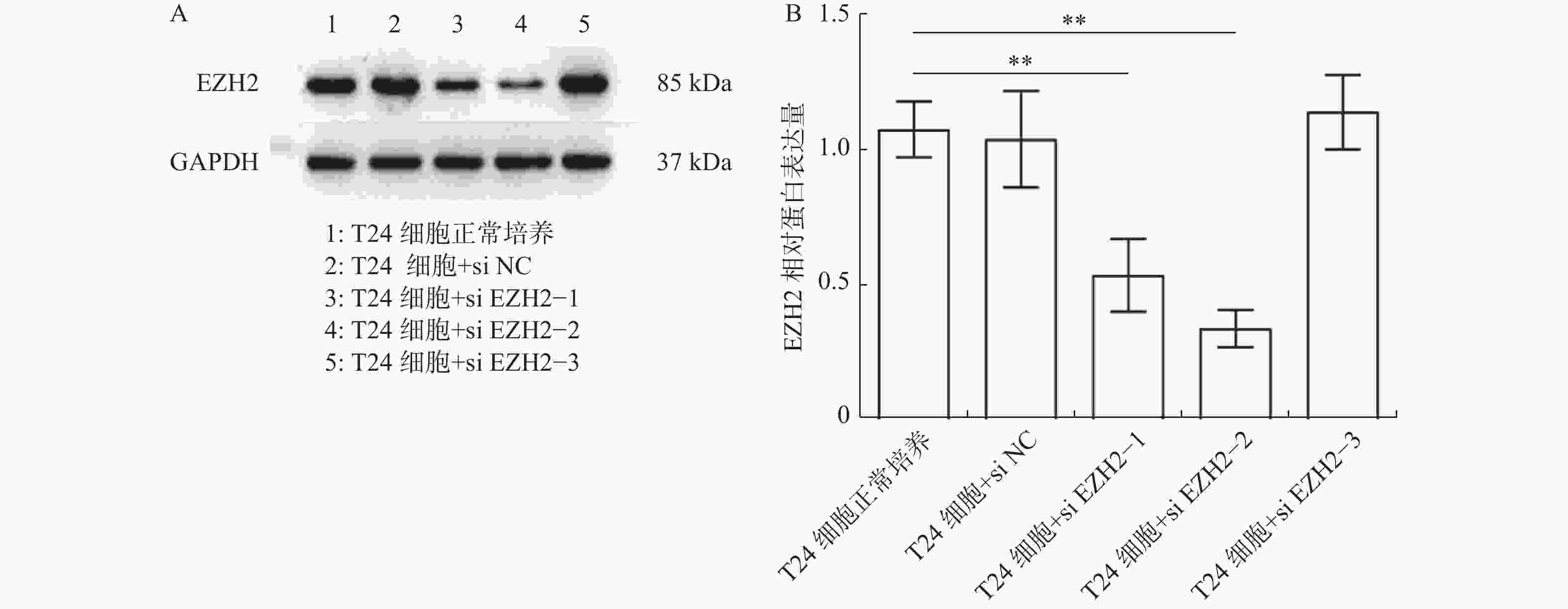
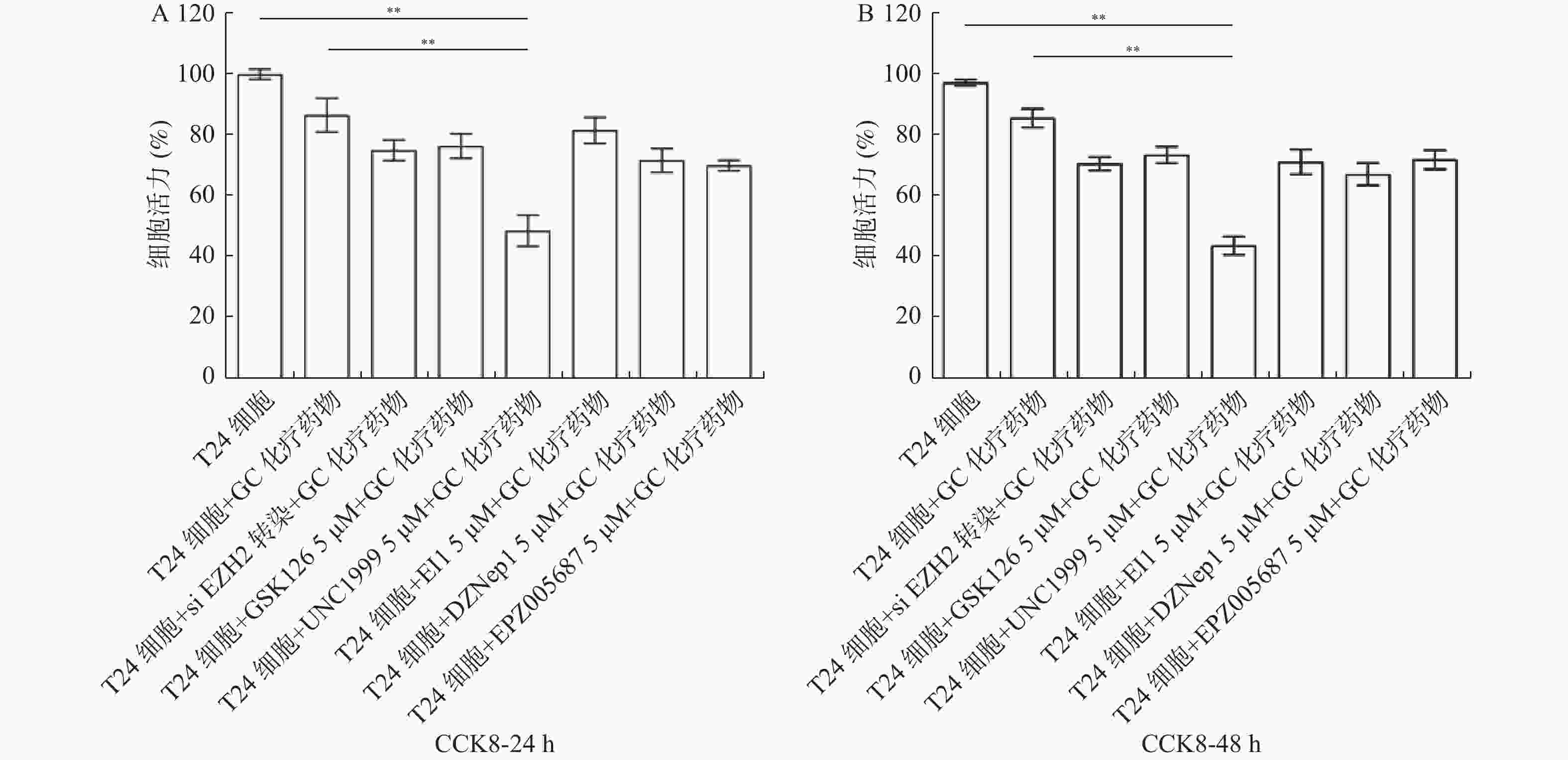
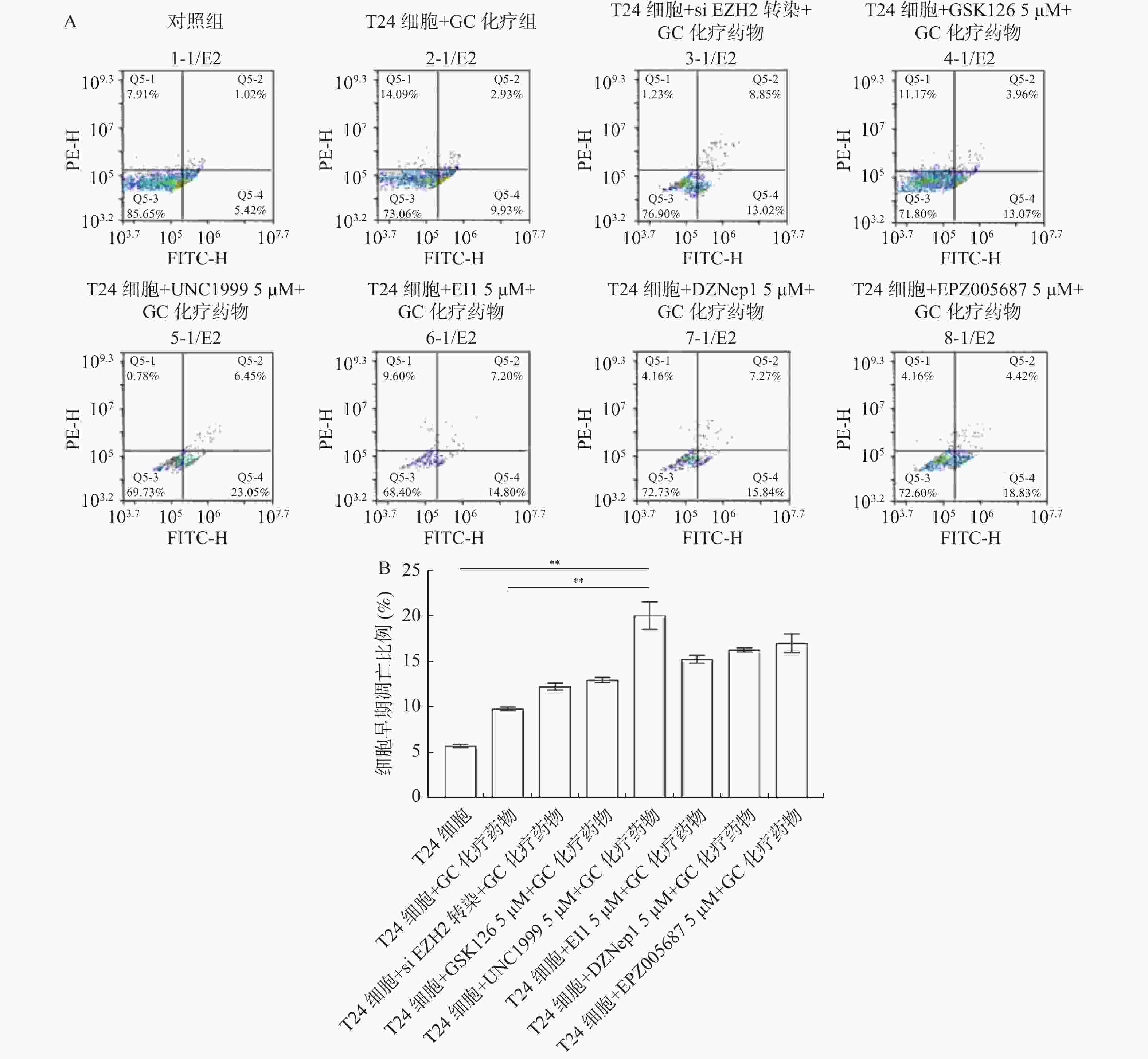
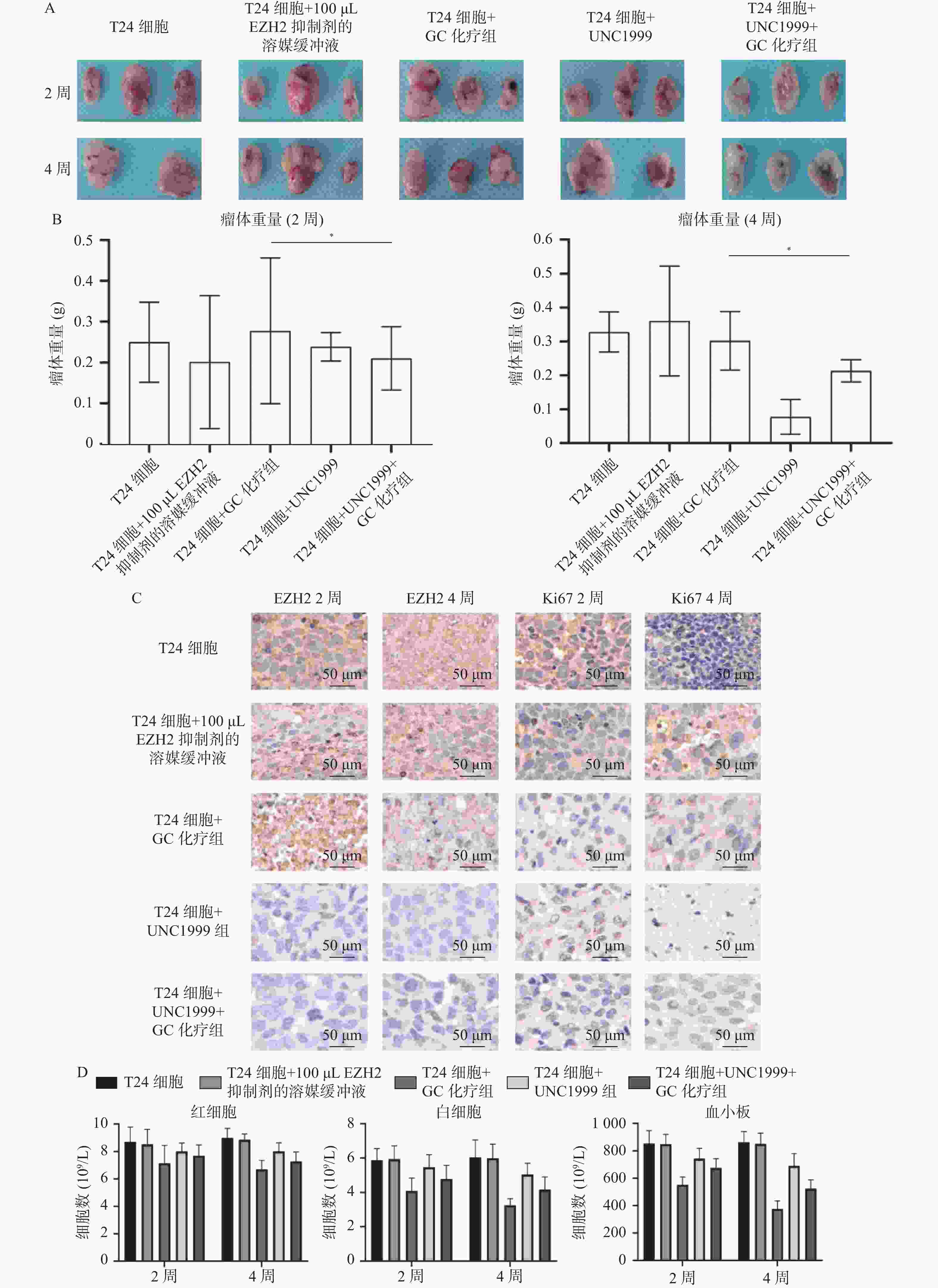
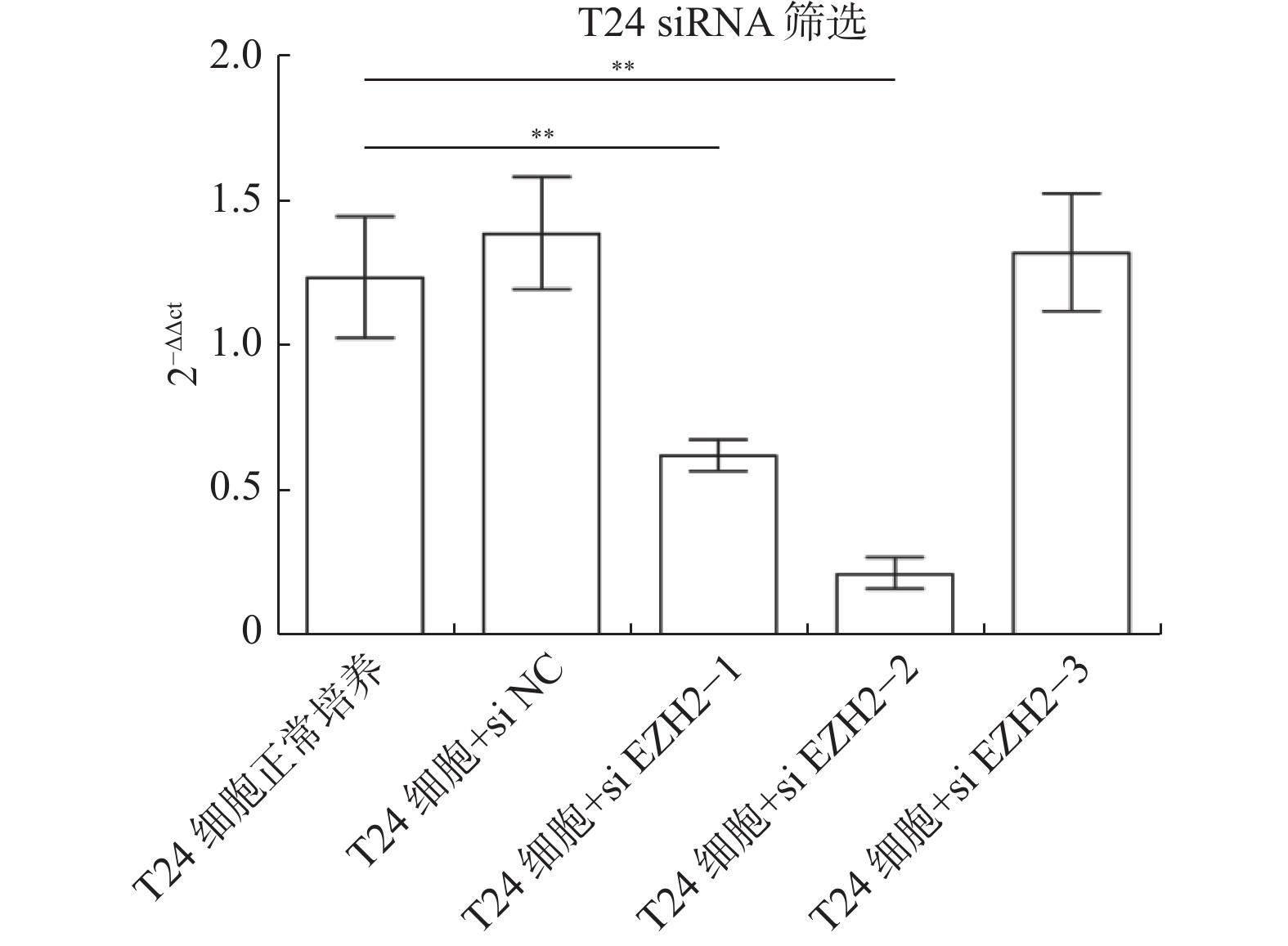
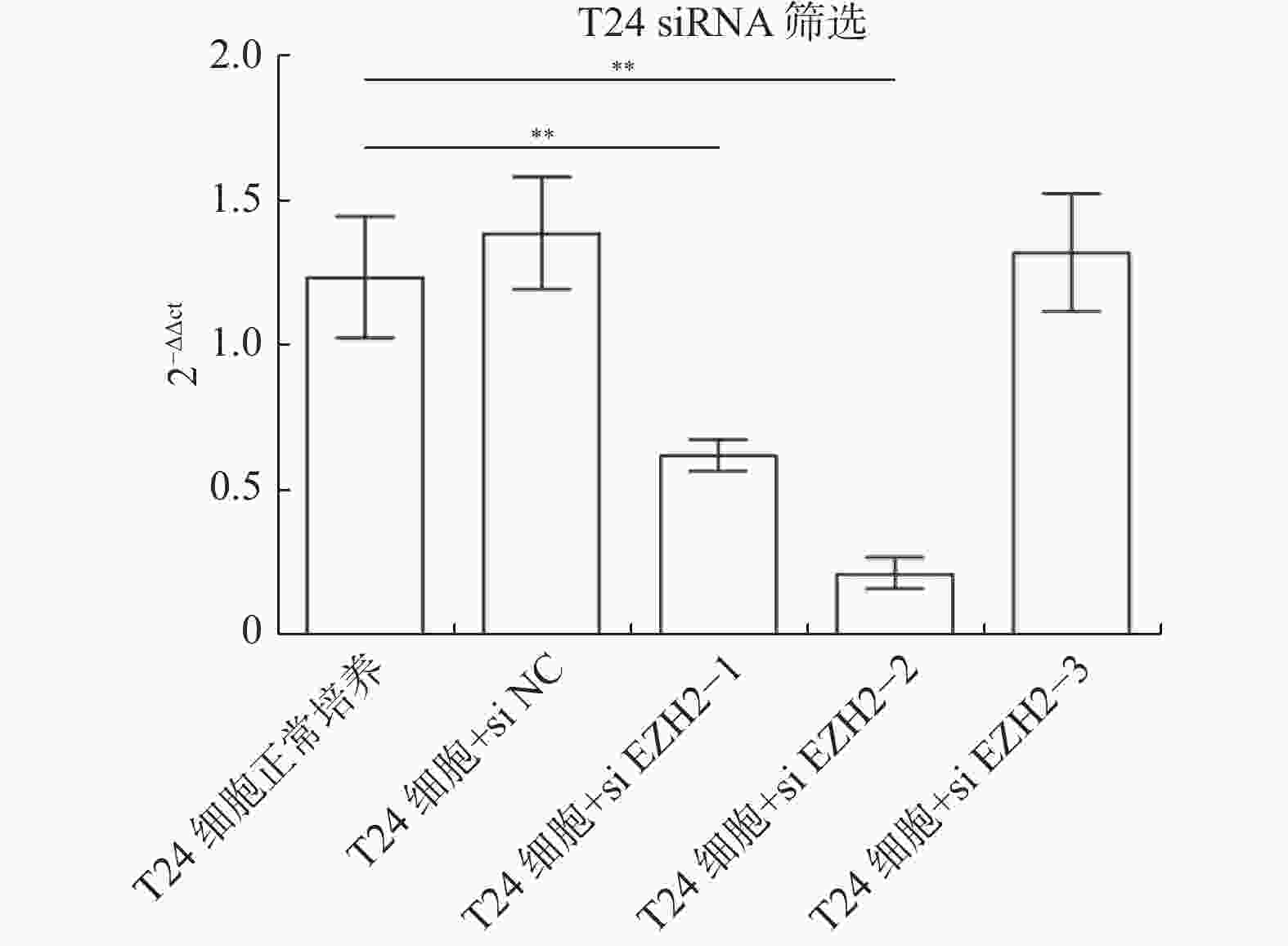
目的 探究多梳蛋白zeste基因増强子类同源物2(histone methyltransferase enhancer of Zeke 2,EZH2)抑制剂对膀胱癌治疗中吉西他滨联合顺铂(gemcitabine and cisplatin,GC)化疗方案中的增敏作用。 方法 首先构建 EZH2 siRNA敲低系,然后使用qPCR与WB检测验证siRNA在膀胱癌UCC细胞中的表达水平。根据不同的处理分为对照组(膀胱癌T24细胞正常培养)、GC化疗组(T24细胞+GC化疗药物)、si EZH2转染组(T24细胞+si EZH2转染+GC化疗药物)、GSK126抑制剂组(T24细胞+GSK126 5 μM+GC化疗药物)、UNC1999抑制剂组(T24细胞+UNC1999 5 μM+GC化疗药物)、EI1抑制剂组(T24细胞+ EI1 5 μM+GC化疗药物)、DZNep1抑制剂(T24细胞+DZNep1 5 μM+GC化疗药物)与EPZ005687抑制剂(T24细胞+EPZ005687 5 μM+GC化疗药物),采用CCK-8、平板克隆形成与Annexin/PI等实验分别检测8组细胞增殖率、凋亡率及其对细胞周期影响。随后将30只BALB/C雌裸鼠随机分为对照组(膀胱癌T24细胞正常培养)、T24细胞+ EZH2抑制剂的溶媒缓冲液组、T24细胞+GC化疗组、T24细胞+UNC1999 EZH2抑制剂组与T24细胞+ UNC1999 EZH2抑制剂+GC化疗组,每组6只。裸鼠成瘤实验检测转染后各组UCC细胞移植瘤的生长情况,免疫组化染色法观察移植瘤组织中Ki67和EZH2的表达,血常规检测白细胞、红细胞及血小板数量裸鼠骨髓抑制情况。 结果 在已转染了siRNA质粒的T24细胞中,siEZH2-1与siEZH2-2在siRNA与蛋白表达水平上与对照组的差异有统计学意义(P < 0.01)。在细胞实验中,与对照组相比,上述7组实验组通过CCK-8、平板克隆与Annexin V/PI双染、Pi单染实验发现EZH2抑制剂可以抑制T24细胞的增殖、迁移和侵袭能力,早期凋亡细胞比例上调( P < 0.01)。其中在平板克隆实验中,实验组T24细胞+EPZ005687 5 μM+GC化疗药物组细胞克隆数与对照组相比,差异有统计学意义( P < 0.05)。小鼠体内实验表明,与对照组相比,经GC化疗药物或EZH2抑制剂的裸鼠瘤体重量减少( P < 0.05),并且在血常规检测中血细胞含量也有所增高。 结论 EZH2抑制剂能够提高膀胱癌GC化疗方案的敏感性,从而降低膀胱癌细胞的增殖、迁移与裸鼠体内移植瘤的生长。同时,联合用药也能够显著减少其骨髓抑制情况。提示协同治疗在膀胱癌化疗增敏中具有一定的作用。 -
关键词:
- 膀胱癌 /
- 多梳蛋白zeste基因増强子类同源物2 /
- GC化疗
Abstract:Objective To explore the synergizing effect of histone methyltransferase enhancer of Zeke 2 (EZH2) inhibitors on Gemcitabine and Cisplatin (GC) chemotherapy regimen in bladder cancer treatment. Methods Firstly, EZH2 siRNA knockdown lines were constructed, and then the expression level of siRNA in bladder cancer UCC cells was verified using qPCR and WB. According to different treatments, these cells were divided into control group (bladder cancer T24 cells cultured normally), GC chemotherapy group (T24 cells + GC), siEZH2 transfection group (T24 cells + siEZH2 transfection + GC), GSK126 inhibitor group (T24 cells + GSK126 5 μM + GC), UNC1999 inhibitor group (T24 cells + UNC1999 5 μM + GC), EI1 inhibitor group (T24 cells + EI1 5 μM + GC), DZNep1 inhibitor group (T24 cells + DZNep1 5 μM + GC), and EPZ005687 inhibitor group (T24 cells + EPZ005687 5 μM + GC). CCK-8, plate clone formation, Annexin/PI, and other experiments were used to detect the proliferation rate, apoptosis rate, and the effect on the cell cycle of the eight groups of cells respectively. Then, 30 female BALB/C nude mice were randomly divided into control group (bladder cancer T24 cells cultured normally), T24 cells + EZH2 inhibitor solvent buffer group, T24 cells + GC chemotherapy group, T24 cells + UNC1999 EZH2 inhibitor group, and T24 cells + UNC1999 EZH2 inhibitor + GC chemotherapy group, with 6 mice in each group. Tumor formation experiment in nude mice was used to detect the growth of transplanted tumors in each group after transfection, immunohistochemistry was used to observe the expression of Ki67 and EZH2 in the transplanted tumor tissues, and blood routine examination was used to detect the number of white blood cells, red blood cells, and platelets and the degree of bone marrow suppression in nude mice. Results In T24 cells transfected with siRNA plasmids, siEZH2-1 and siEZH2-2 showed statistically significant differences in siRNA and protein expression levels compared to the control group (P < 0.01). Compared to the control group, the above experimental groups found that EZH2 inhibitors can inhibit the proliferation, migration, and invasion ability of T24 cells, and increase the proportion of early apoptotic cells through CCK-8, plate cloning, and Annexin V/PI double staining, and Pi single staining experiments ( P < 0.01). Among them, in the plate cloning experiment, the difference in the number of cell clones between the experimental group T24 cells+EPZ005687 5 μM+GC chemotherapy drug group and the control group was statistically significant ( P < 0.05). In vivo experiments in mice showed that the tumor weight of nude mice treated with GC chemotherapy drugs or EZH2 inhibitors decreased compared to the control group ( P < 0.05), and the blood cell content also increased in the blood routine examination. Conclusion EZH2 inhibitors can enhance the sensitivity of bladder cancer GC chemotherapy regimen, thereby reducing the proliferation, migration, and growth of bladder cancer cells in nude mice xenografts. Additionally, combination therapy can significantly reduce bone marrow suppression. These findings suggest that combination therapy plays a role in sensitizing bladder cancer chemotherapy. -
图 4 平板克隆形成实验检测使用EZH2抑制剂对膀胱癌T24细胞增殖的影响
A:对照组与7组实验组平板克隆形成实验;B:细胞克隆数统计图。T24细胞 + DZNep1 5 μM + GC化疗药物组与T24细胞正常培养比较,**P < 0.01;T24细胞 + EPZ005687 5 μM + GC化疗药物组与T24细胞正常培养比较,*P < 0.05。
Figure 4. Effect of using EZH2 inhibitor on the proliferation of bladder cancer T24 cells detected by plate clone formation assay
表 1 EZH2 引物序列
Table 1. Primer sequences of EZH2
基因名称 序列 (5′→3′) 长度(bp) GAPDH(H)-F TTGCCCTCAACGACCACTTT 120 GAPDH(H)-R TGGTCCAGGGGTCTTACTCC 120 EZH2(H)-F AAGAAGAAGAAGAGAAGAA 161 EZH2(H)-R ATAGTAAGTGCCAATGAG 161 F:上游引物、正向;R:下游引物、反向。 -
[1] Van Hoogstraten L M C,Vrieling A,Van Der Heijden A G,et al. Global trends in the epidemiology of bladder cancer: Challenges for public health and clinical practice[J]. Nat Rev Clin Oncol,2023,20(5):287-304. doi: 10.1038/s41571-023-00744-3 [2] Ramakrishnan S,Granger V,Rak M,et al. Inhibition of EZH2 induces NK cell-mediated differentiation and death in muscle-invasive bladder cancer[J]. Cell Death Differ,2019,26(10):2100-2114. doi: 10.1038/s41418-019-0278-9 [3] Bai Y,Zhang Z,Cheng L,et al. Inhibition of enhancer of zeste homolog 2 (EZH2) overcomes enzalutamide resistance in castration-resistant prostate cancer[J]. J Biol Chem,2019,294(25):9911-9923. doi: 10.1074/jbc.RA119.008152 [4] Yetişir A E,Paydaş S,Büyükşimşek M,et al. Effects of enhancer of zeste homolog 2 and mucin 1 expressions on treatment response in breast cancer[J]. Rev Assoc Med Bras (1992),2023,69(1):153-158. [5] Hong S H,Hwang H J,Son D H,et al. Inhibition of EZH2 exerts antitumorigenic effects in renal cell carcinoma via LATS1[J]. FEBS Open Bio,2023,13(4):724-735. doi: 10.1002/2211-5463.13579 [6] Hu F F,Chen H,Duan Y,et al. CBX2 and EZH2 cooperatively promote the growth and metastasis of lung adenocarcinoma[J]. Mol Ther Nucleic Acids,2022,27:670-684 . doi: 10.1016/j.omtn.2021.12.032 [7] Dong P,Xiong Y,Konno Y,et al. Long non-coding RNA DLEU2 drives EMT and glycolysis in endometrial cancer through HK2 by competitively binding with miR-455 and by modulating the EZH2/miR-181a pathway[J]. J Exp Clin Cancer Res,2021,40(1):216. doi: 10.1186/s13046-021-02018-1 [8] Yu T,Zhou F,Tian W,et al. EZH2 interacts with HP1BP3 to epigenetically activate WNT7B that promotes temozolomide resistance in glioblastoma[J]. Oncogene,2023,42(6):461-470. doi: 10.1038/s41388-022-02570-w [9] Ren J,Yu H,Li W,et al. Downregulation of CBX7 induced by EZH2 upregulates FGFR3 expression to reduce sensitivity to cisplatin in bladder cancer[J]. Br J Cancer,2023,128(2):232-244. doi: 10.1038/s41416-022-02058-0 [10] Sun J X,Xu J Z,Liu C Q,et al. The association between human papillomavirus and bladder cancer: Evidence from meta-analysis and two-sample mendelian randomization[J]. J Med Virol,2023,95(1):e28208. doi: 10.1002/jmv.28208 [11] Kim H S,Seo H K. Immune checkpoint inhibitors for urothelial carcinoma[J]. Investig Clin Urol,2018,59(5):285-296. doi: 10.4111/icu.2018.59.5.285 [12] Su H,Jiang H,Tao T,et al. Hope and challenge: Precision medicine in bladder cancer[J]. Cancer Med,2019,8(4):1806-1816. doi: 10.1002/cam4.1979 [13] Patel V G,Oh W K,Galsky M D. Treatment of muscle-invasive and advanced bladder cancer in 2020[J]. CA Cancer J Clin,2020,70(5):404-423. doi: 10.3322/caac.21631 [14] Qu H C,Huang Y,Mu Z Y,et al. Efficacy and safety of chemotherapy regimens in advanced or metastatic bladder and urothelial carcinomas: An updated network meta-analysis[J]. Front Pharmacol,2019,10:1507. [15] Duan R,Du W,Guo W. EZH2: A novel target for cancer treatment[J]. J Hematol Oncol,2020,13(1):104. doi: 10.1186/s13045-020-00937-8 [16] Sawicka-Gutaj N,Shawkat S,Andrusiewicz M,et al. EZH2 and SMYD3 expression in papillary thyroid cancer[J]. Oncol Lett,2021,21(5):342. doi: 10.3892/ol.2021.12603 [17] Li Z,Li M,Wang D,et al. Post-translational modifications of EZH2 in cancer[J]. Cell Biosci,2020,10(1):143 . doi: 10.1186/s13578-020-00505-0 [18] Hussein Y R,Sood A K,Bandyopadhyay S,et al. Clinical and biological relevance of enhancer of zeste homolog 2 in triple-negative breast cancer[J]. Hum Pathol,2012,43(10):1638-1644. doi: 10.1016/j.humpath.2011.12.004 [19] Liu L C,Chien Y C,Wu G W,et al. Analysis of EZH2 genetic variants on triple-negative breast cancer susceptibility and pathology[J]. Int J Med Sci,2022,19(6):1023-1028 . doi: 10.7150/ijms.71931 [20] Morschhauser F,Salles G,Batlevi C L,et al. Taking the EZ way: Targeting enhancer of zeste homolog 2 in B-cell lymphomas[J]. Blood Rev,2022,56:100988. doi: 10.1016/j.blre.2022.100988 [21] Qiang N,Ao J,Nakamura M,et al. Alteration of the tumor microenvironment by pharmacological inhibition of EZH2 in hepatocellular carcinoma[J]. Int Immunopharmacol,2023,118:110068. doi: 10.1016/j.intimp.2023.110068 [22] Li C,Song J,Guo Z,et al. EZH2 inhibitors suppress colorectal cancer by regulating macrophage polarization in the tumor microenvironment[J]. Front Immunol,2022,13:857808. doi: 10.3389/fimmu.2022.857808 [23] Gong H,Li Y,Yuan Y,et al. EZH2 inhibitors reverse resistance to gefitinib in primary EGFR wild-type lung cancer cells[J]. BMC Cancer,2020,20(1):1189. doi: 10.1186/s12885-020-07667-7 [24] Wang Y F,Yu L,Hu Z L,et al. Regulation of CCL2 by EZH2 affects tumor-associated macrophages polarization and infiltration in breast cancer[J]. Cell Death Dis,2022,13(8):748. doi: 10.1038/s41419-022-05169-x [25] Zhang Q,Chen X,Cao J,et al. Discovery of a novel covalent EZH2 inhibitor based on tazemetostat scaffold for the treatment of ovarian cancer[J]. J Med Chem,2023,66(3):1725-1741. doi: 10.1021/acs.jmedchem.2c01370 [26] Chen R,Gan Q,Zhao S,et al. DNA methylation of miR-138 regulates cell proliferation and EMT in cervical cancer by targeting EZH2[J]. BMC Cancer,2022,22(1):488 . doi: 10.1186/s12885-022-09477-5 [27] Ishiguro K,Kitajima H,Niinuma T,et al. Dual EZH2 and G9a inhibition suppresses multiple myeloma cell proliferation by regulating the interferon signal and IRF4-MYC axis[J]. Cell Death Discov,2021,7(1):7. doi: 10.1038/s41420-020-00400-0 [28] Yang Y X,Shen H H,Cao F,et al. Therapeutic potential of enhancer of zeste homolog 2 in autoimmune diseases[J]. Expert Opin Ther Targets,2019,23(12):1015-1030. doi: 10.1080/14728222.2019.1696309 [29] He Y,Wang N,Zhou X,et al. Prognostic value of ki67 in BCG-treated non-muscle invasive bladder cancer: A meta-analysis and systematic review[J]. BMJ Open,2018,8(4):e019635. doi: 10.1136/bmjopen-2017-019635 -





 下载:
下载: