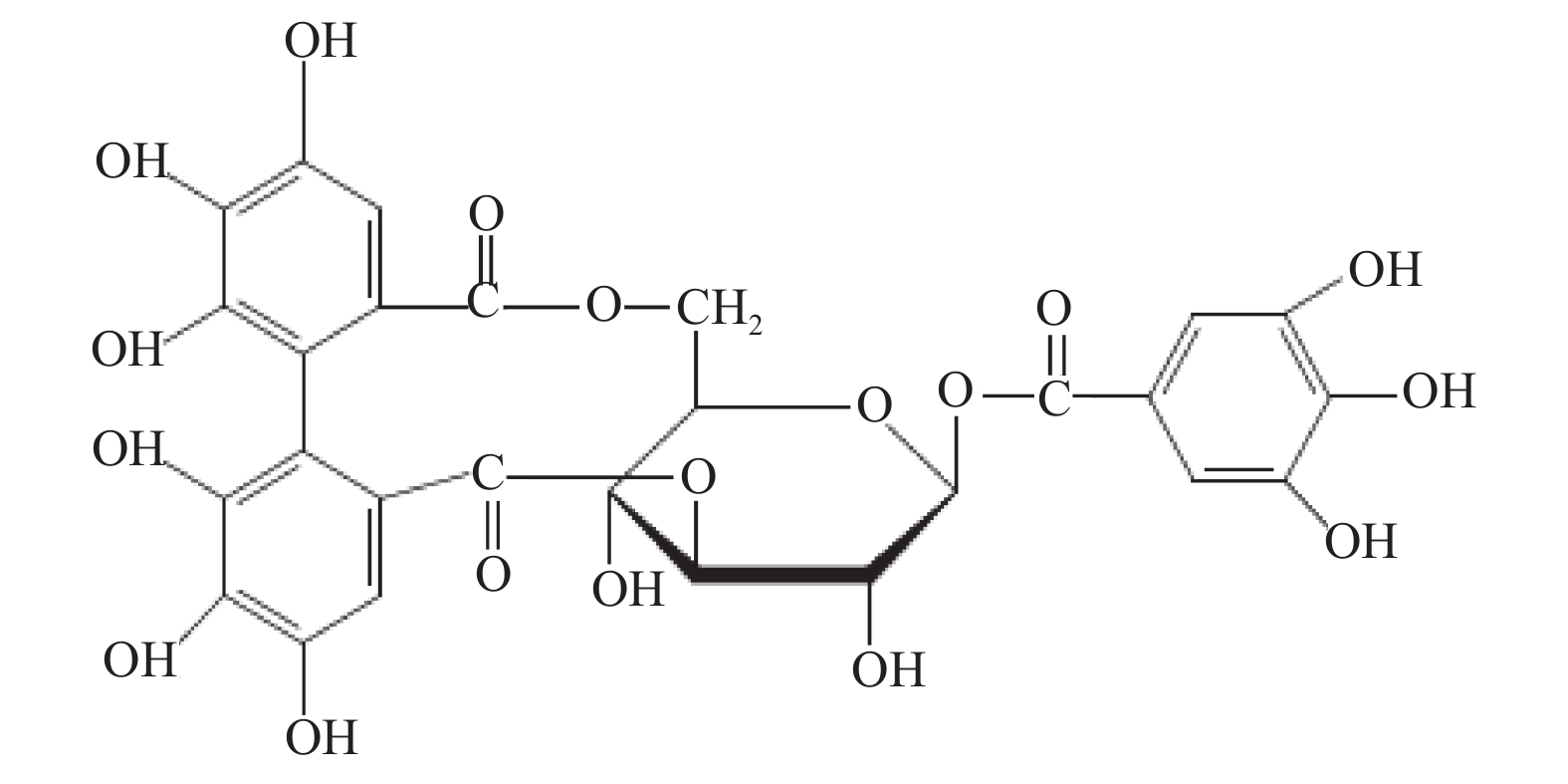
Protective Effect of Corilagin on OX-LDL-Induced HUVECs Cell Damage and Its Impact on the Expression of the MyD88 Signaling Pathway
-
摘要:
目的 探讨不同浓度和时间的柯里拉京(Corilagin)处理对氧化性低密度脂蛋白(oxidative low-density lipoprotein,ox-LDL)诱导人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)损伤的保护作用,以及其对MyD88信号通路表达调控的影响。 方法 体外培养HUVECs复制ox-LDL诱导损伤模型,利用形态学及免疫学方法鉴定HUVECs细胞,MTT法确定复制ox-LDL损伤HUVECs模型的最佳条件,根据不同处理将细胞分为正常组(Normal)、模型组(Model)、Corilagin(3.125、6.25、12.5、25、50 µmol/L)组、阳性对照(VE 10 µmol/L、Simvastain 1 µmol/L)组。观察Corilagin对ox-LDL诱导损伤的HUVECs保护作用;Western blot和RT-qPCR 方法检测HUVECs细胞中MyD88、P65、TNF-α、MCP-1表达变化。 结果 经形态学及免疫学方法鉴定,所培养细胞为HUVECs;70 mg/L的ox-LDL刺激12 h是复制ox-LDL损伤HUVECs模型的最佳条件;MTT结果显示,与ox-LDL组比较,Corilagin组细胞活力明显升高(P < 0.01);RT-qPCR和Western blot结果表明,与Normal组比,ox-LDL组MyD88、P65、TNF-α及MCP-1的mRNA和蛋白表达升高(P < 0.01);与ox-LDL组比较,Corilagin组及阳性对照组的MyD88、P65、TNF-α及MCP-1的mRNA和蛋白表达降低(P < 0.01),且Corilagin组呈现剂量依赖下调MyD88、P65、TNF-α及MCP-1的mRNA和蛋白表达。 结论 随着时间和浓度的增加,Corilagin能明显提高ox-LDL诱导损伤的HUVECs细胞活力,其保护作用与抑制MyD88信号通路有关。 -
关键词:
- Corilagin /
- 人脐静脉内皮细胞HUVECs /
- 氧化型低密度脂蛋白 /
- 动脉粥样硬化
Abstract:Objective To investigate the protective effects of different concentrations and durations of corilagin treatment on oxidative low-density lipoprotein (ox-LDL)-induced damage in human umbilical vein endothelial cells (HUVECs), as well as its effects on the expression regulation of the MyD88 signaling pathway. Methods In vitro cultured HUVECs were used to replicate the ox-LDL-induced damage model. Morphological and immunological methods were employed to identify HUVECs cells. The MTT assay was used to determine the optimal conditions for replicating the ox-LDL-induced damage model in HUVECs. Cells were divided into different groups based on different treatments: normal group, model group, Corilagin (3.125, 6.25, 12.5, 25, 50 µmol/L) group, and positive control (VE 10 µmol/L, Simvastatin 1 µmol/L) group. The protective effect of corilagin on ox-LDL-induced damage in HUVECs was observed. Western blot and RT-qPCR methods were used to detect the expression changes of MyD88, P65, TNF-α, and MCP-1 in HUVECs cells. Results The cultured cells were confirmed as HUVECs by using morphological and immunological methods. The best condition for replicating ox-LDL-induced damage to HUVECs was 12 hours of treatment with 70 mg/L of ox-LDL. MTT results showed that compared with the ox-LDL group, the corilagin group had a significantly higher cell viability (P < 0.01). RT-qPCR and Western blot results showed that compared with the control group, the mRNA and protein expression of MyD88, P65, TNF-α, and MCP-1 were increased in the ox-LDL group (P < 0.01). Compared with the ox-LDL group, the mRNA and protein expression of MyD88, P65, TNF-α, and MCP-1 were decreased (P < 0.01) in the corilagin group and positive control group, and the corilagin group showed a dose-dependent downregulation of the mRNA and protein expression of MyD88, P65, TNF-α, and MCP-1. Conclusion With the increase of time and concentration, corilagin can significantly improve the cell viability of HUVECs induced by ox-LDL damage, and its protective effect is associated with the inhibition of the MyD88 signaling pathway. -
Key words:
- Corilagin /
- HUVECs /
- Ox-LDL /
- Atherosclerosis
-
图 5 Corilagin对OX-LDL损伤HUVECs的保护作用(
$\bar x \pm s $ ,n = 6)A:Corilagin对OX-LDL损伤HUVECs作用12 h对细胞活力的影响;B:Corilagin对OX-LDL损伤HUVECs作用24 h对细胞活力的影响;C:Corilagin对OX-LDL损伤HUVECs作用48 h对细胞活力的影响。与正常组相比,##P < 0.01,与模型组相比,**P < 0.01。
Figure 5. Protective effect of Corilagin on OX-LDL-damaged HUVECs (
$\bar x \pm s $ ,n = 6)图 6 Corilagin对OX-LDL诱导的HUVECs中P65、MCP-1、MyD88和TNF-α的mRNA表达的影响(
$\bar x \pm s $ ,n = 6)A:不同浓度Corilagin对OX-LDL诱导的HUVECs中MYD88 mRNA表达的影响;B:不同浓度Corilagin对OX-LDL诱导的HUVECs中P65 mRNA表达的影响;C:不同浓度Corilagin对OX-LDL诱导的HUVECs中MCP-1mRNA表达的影响;D:不同浓度Corilagin对OX-LDL诱导的HUVECs中TNF-αmRNA表达的影响。与正常组相比,##P < 0.01,与模型组相比,*P < 0.05,**P < 0.01。
Figure 6. Effect of Corilagin on mRNA expression of P65,MCP-1,MyD88 and TNF-α in OX-LDL-induced HUVECs(
$\bar x \pm s $ ,n = 6)图 7 Corilagin对OX-LDL诱导的HUVECs中P65、MCP-1、MyD88和TNF-α的蛋白表达的影响(
$\bar x \pm s $ ,n = 3)A:Western blot 检测Corilagin对OX-LDL诱导的HUVECs中P65、MCP-1、MyD88和TNF-α的蛋白表达的影响;B:Corilagin对OX-LDL诱导的HUVECs中MYD88蛋白表达的影响;C:Corilagin对OX-LDL诱导的HUVECs中P65蛋白表达的影响;D:Corilagin对OX-LDL诱导的HUVECs中MCP-1蛋白表达的影响;E:Corilagin对OX-LDL诱导的HUVECs中TNF-α蛋白表达的影响。与正常组相比,##P < 0.01;与模型组相比,*P < 0.05,**P < 0.01。
Figure 7. Effect of Corilagin on protein expression of P65,MCP-1,MyD88 and TNF-α in OX-LDL-induced HUVECs (
$\bar x \pm s $ ,n = 3)表 1 引物序列
Table 1. Primer sequences
基因名 引物序列 长度(bp) β-actin F-CGTGCGTGACATCAAAGAGA 178 R-CAAGAAGGAAGGCTGGAAAA MyD88 F-CTGGGGGCACTGTGGATT 174 R-CGCTGCTGGGGAGAAAAC P65 F-CAACCAAAACAGAGGGGATT 160 R-TTGTGACCAACTGAACGATA TNF-α F-CTCCTCACCCACACCGTC 226 R-AACACCCATTCCCTTCAC MCP-1 F-TGACCCCAAGAAGGAATG 180 R-GAGGTGGTTGTGGAAAAG -
[1] Shah P K. Inflammation,infection and atherosclerosis[J]. Trends Cardiovas Med,2019,29(8):468-472. doi: 10.1016/j.tcm.2019.01.004 [2] Sharma T,Romeo F,Mehta J L. LOX-1: Implications in atherosclerosis and myocardial ischemia[J]. Excli J,2022,21(1):273-278. [3] Gao W,Liu H,Yuan J,et al. Exosomes derived from mature dendritic cells increase endothelial inflammation and atherosclerosis via membrane TNF-α mediated NF-κB pathway[J]. J Cell Mol Med,2016,20(12):2318-2327. doi: 10.1111/jcmm.12923 [4] Xiong X,Lu W,Zhang K,et al. Pterostilbene reduces endothelial cell apoptosis by regulation of the Nrf2-mediated TLR-4/MyD88/NF-κB pathway in a rat model of atherosclerosis[J]. Exp Ther Med,2020,20(3):2090-2098. [5] Chen T,Luo W,Wu G,et al. A novel MyD88 inhibitor LM9 prevents atherosclerosis by regulating inflammatory responses and oxidative stress in macrophages[J]. Toxicol Appl Pharm,2019,370(1):44-55. [6] Hosseini H,Li Y,Kanellakis P,et al. Toll-like receptor (TLR)4 and MyD88 are essential for atheroprotection by peritoneal B1a B cells[J]. J Am Heart Assoc,2016,5(11):e002947. doi: 10.1161/JAHA.115.002947 [7] Basurto L,Gregory M A,Hernández S B,et al. Monocyte chemoattractant protein-1 (MCP-1) and fibroblast growth factor-21 (FGF-21) as biomarkers of subclinical atherosclerosis in women[J]. Exp Gerontol,2019,124(1):110624-110631. [8] Yu H,Cao H,Yu H. MicroRNA-98 inhibition accelerates the development of atherosclerosis via regulation of dysfunction of endothelial cell[J]. Clin Exp Hypertens,2023,45(1):2206068. doi: 10.1080/10641963.2023.2206068 [9] 夏欣,杨媛,李发靖,等. 柯里拉京的心脑血管保护作用及机制研究进展[J]. 医学综述,2022,28(2):229-234. [10] Tao Y,Zhang L,Yang R,et al. Corilagin ameliorates atherosclerosis by regulating MMP-1,-2,and -9 expression in vitro and in vivo[J]. Eur J Pharmacol,2021,906(1):174200-174210. [11] 郭英,陈鹏,谢建平,等. Corilagin对血管内皮细胞的保护作用及LOX-1蛋白表达的影响[J]. 中成药,2012,34(1):151-154. [12] 郭英,陈鹏,谢建平,等. Corilagin对HUVEC的保护作用及LOX-1 mRNA表达的影响[J]. 时珍国医国药,2011,22(10):2419-2421. doi: 10.3969/j.issn.1008-0805.2011.10.044 [13] Gunta S P,O'keefe J H,O'keefe E L,et al. PCSK9 inhibitor,ezetimibe,and bempedoic acid: Evidence-based therapies for statin-intolerant patients[J]. Prog Cardiovasc Dis,2023,13(5):e068915. [14] Zhu K,Wang X,Weng Y,et al. Sulfated galactofucan from sargassum thunbergii attenuates atherosclerosis by suppressing inflammation via the TLR4/MyD88/NF-κB signaling pathway[J]. Cardiovasc Drug Ther,2022,10(1):7383-7397. [15] Park H J,Zhang Y,Georgescu S P,et al. Human umbilical vein endothelial cells and human dermal microvascular endothelial cells offer new insights into the relationship between lipid metabolism and angiogenesis[J]. Stem Cell Rev,2006,2(2):93-102. doi: 10.1007/s12015-006-0015-x -






 下载:
下载: