ZNF384 Regulates Metastasis of Hepatocellular Carcinoma via GCLM
-
摘要:
目的 探讨ZNF384通过调控GCLM对肝细胞癌(hepatocellular carcinoma,HCC)增殖和转移的影响及具体调控机制。 方法 分别在HCC细胞系HepG2和HuH7中转染si-ZNF384和pcDNA-GCLM。Western blot检测ZNF384和GCLM蛋白表达以及上皮间质转化(epithelial-mesenchymal transition,EMT)标志物N-cadherin、Vimentin、E-cadherin的表达,CCK-8检测细胞增殖活力,Transwell检测细胞迁移。双荧光素酶报告基因实验验证ZNF384和GCLM结合关系。荧光原位杂交(fluorescence in situ hybridization,FISH)技术检测ZNF384和GCLM在HepG2细胞中的定位。 结果 ZNF384和GCLM在HepG2和HuH7细胞中表达升高(P < 0.05),敲降ZNF384抑制HepG2和HuH7细胞增殖(P < 0.001)、迁移(P < 0.001)以及间质标志物N-cadherin(P < 0.01)和Vimentin(P < 0.01)的表达,促进上皮标志物E-cadherin的表达(P < 0.01)。数据库以及双荧光素酶实验证实ZNF384与GCLM启动子结合。过表达GCLM逆转敲降ZNF384对HepG2和HuH7细胞增殖、迁移以及EMT的抑制作用(P < 0.05)。 结论 敲降ZNF384通过抑制GCLM,抑制HCC细胞增殖和转移。 Abstract:Objective To investigate the effect of ZNF384 on the proliferation and metastasis of HCC by regulating GCLM and demonstrate the specific mechanism. Methods si-ZNF384 and pcDNA-GCLM were transfected into HepG2 and HuH7 cell lines of HCC, respectively. Western blot was carried out to detect the expressions of ZNF384 and GCLM proteins as well as the expressions of EMT-markers N-cadherin, Vimentin and E-cadherin. CCK-8 assessed cell proliferative activity. Transwell assay was conducted to measure cell migration. Dual-luciferase experiment verified the binding relationship between ZNF384 and GCLM. The localization of ZNF384 and GCLM in HepG2 cells was detected by FISH assay. Results The expressions of ZNF384 and GCLM in HepG2 and HuH7 cells were increased(P < 0.05). Knockdown of ZNF384 inhibited the proliferation(P < 0.001) and migration(P < 0.001) of HepG2 and HuH7 cells, suppressed the expression of interstitial markers N-cadherin(P < 0.01) and Vimentin(P < 0.01), and promoted the expression of epithelial marker E-cadherin(P < 0.01). Database and dual-luciferase experiments confirmed that ZNF384 is bound to the promoter of GCLM. Overexpression of GCLM reversed the inhibitory effect of knocking down ZNF384 on the proliferation, migration and EMT of HepG2 and HuH7 cells(P < 0.05). Conclusion Knocking down ZNF384 can repress the proliferation and metastasis of HCC cells by inhibiting GCLM. -
Key words:
- Hepatocellular carcinoma /
- ZNF384 /
- GCLM /
- Proliferation /
- Metastasis
-
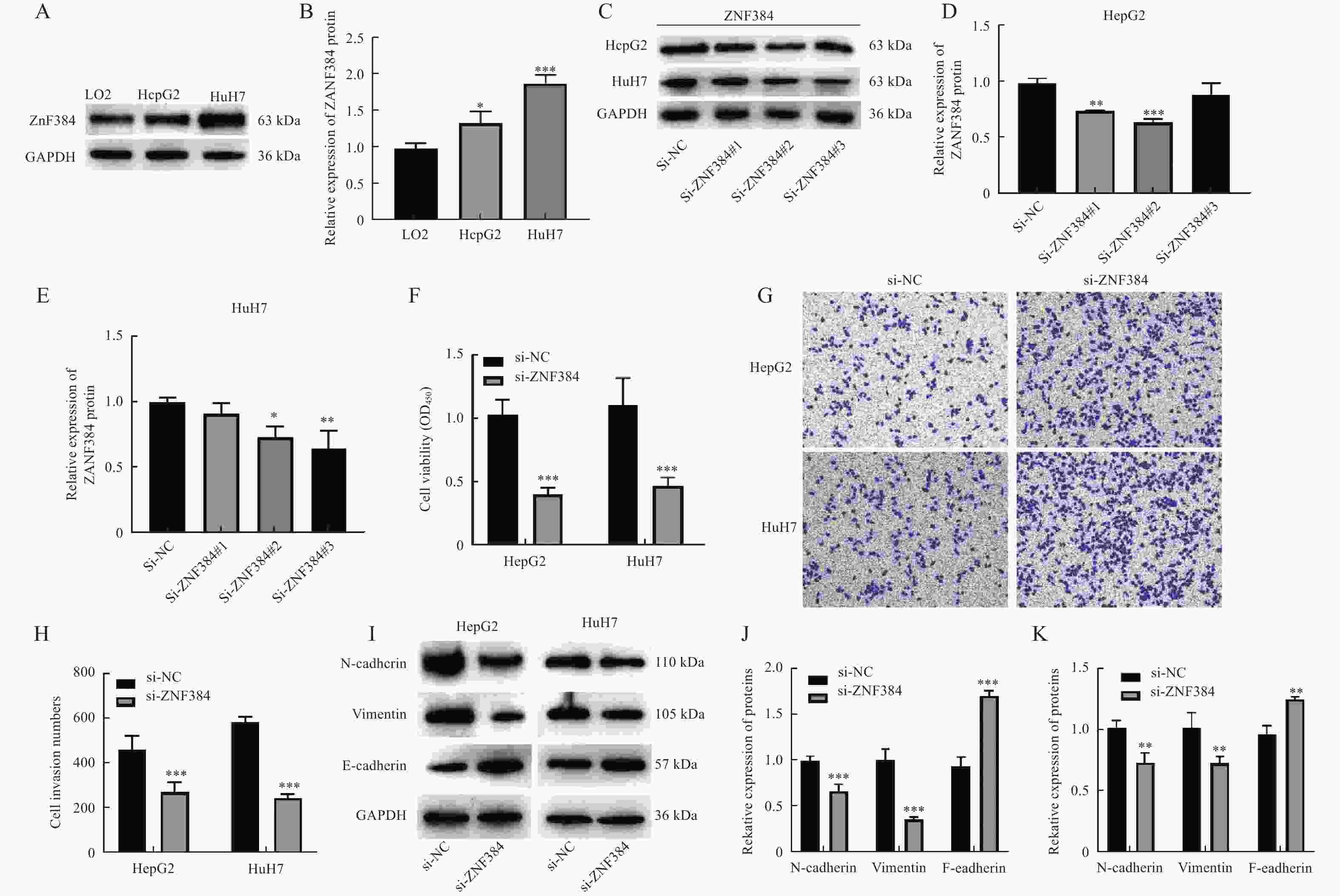
图 1 敲降ZNF384抑制HCC细胞增殖和转移
A~B:Western blot检测HCC细胞系中ZNF384蛋白表达,与LO2组相比,*P < 0.05,***P < 0.001。C~E:Western blot检测敲降ZNF384对ZNF384蛋白表达的作用;F:CCK-8检测细胞增殖活力;G~H:Transwell检测细胞迁移能力;I-K:Western blot检测EMT相关标志物的表达。与si-NC组相比,*P < 0.05,**P < 0.01,***P < 0.001。
Figure 1. Knockdown of ZNF384 inhibited the proliferation and metastasis of HCC cells
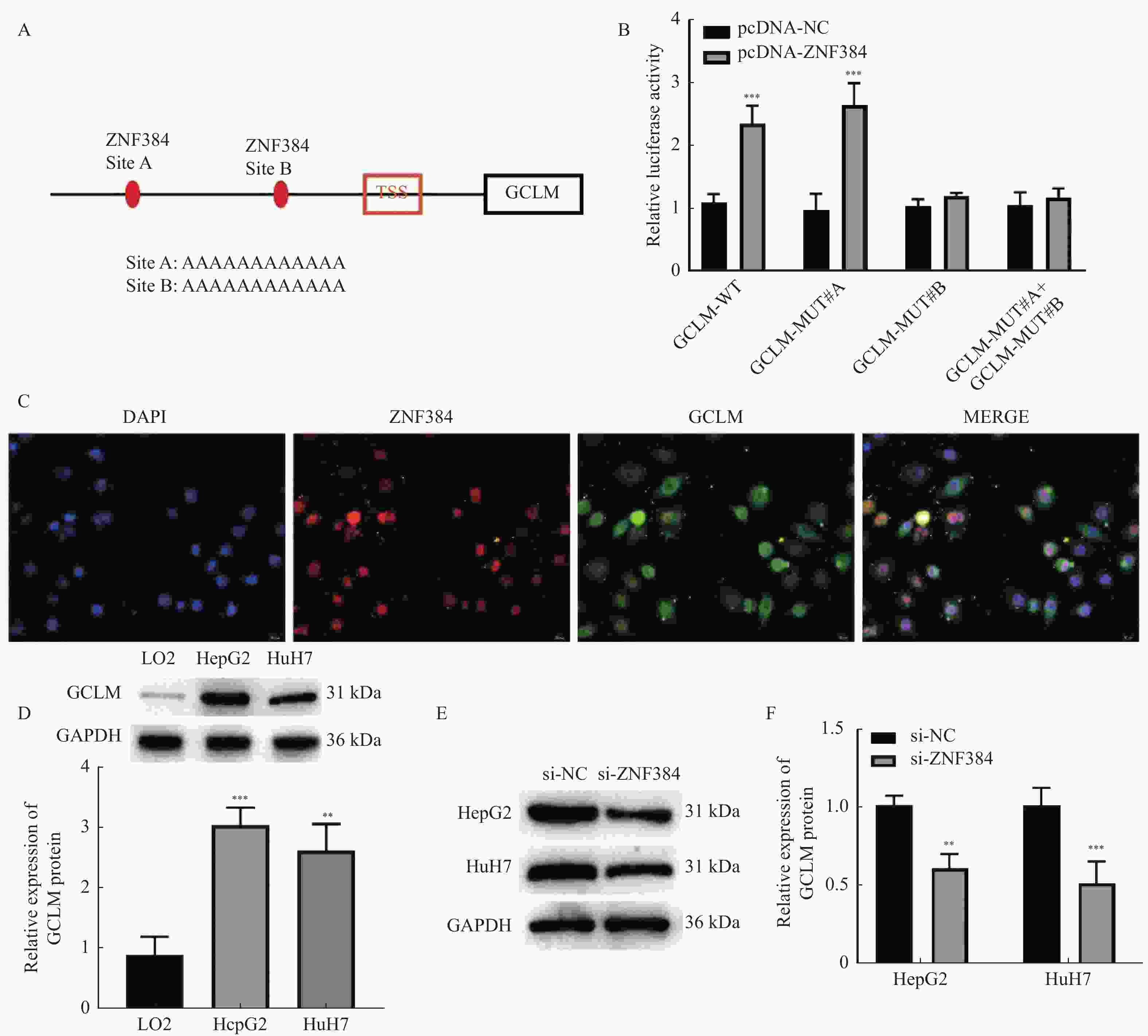
图 2 ZNF384作为转录因子调控GCLM的表达
A:AnimalTFD3.0数据库预测ZNF384与GCLM的启动子结合位点;B:双荧光素酶报告基因实验验证ZNF384与GCLM的结合关系,与pcDNA-NC组相比,***P < 0.001;C:FISH检测ZNF384和GCLM在HepG2细胞中的定位;D:Western blot检测HCC细胞中GCLM的蛋白表达,与LO2组相比,**P < 0.01,***P < 0.001;E~F:Western blot检测敲降ZNF384对GCLM蛋白表达的作用。与si-NC组相比,**P < 0.01,***P < 0.001。
Figure 2. ZNF384 as a transcription factor regulated the expression of GCLM
图 3 ZNF384调控GCLM抑制肝细胞癌细胞的增殖和转移
A~C:Western blot检测ZNF384和GCLM在HepG2和HuH7细胞中的表达;D:CCK-8检测细胞增殖活力;E~G:Transwell检测细胞迁移能力;H~J:Western blot检测EMT相关标志物N-cadherin、Vimentin和E-cadherin的蛋白表达。*P < 0.05,**P < 0.01,***P < 0.001。
Figure 3. ZNF384 suppressed the proliferation and metastasis of HCC cells by regulating GCLM
-
[1] Brown Z J,Tsilimigras D I,Ruff S M,et al. Management of hepatocellular carcinoma: A review[J]. JAMA Surg,2023,158(4):410-420. doi: 10.1001/jamasurg.2022.7989 [2] Xie D,Shi J,Zhou J,et al. Clinical practice guidelines and real-life practice in hepatocellular carcinoma: A Chinese perspective[J]. Clin Mol Hepatol,2023,29(2):206-216. doi: 10.3350/cmh.2022.0402 [3] Liu S,Liu X,Lin X,et al. Zinc finger proteins in the war on gastric cancer: Molecular mechanism and clinical potential[J]. Cells,2023,12(9):1314. doi: 10.3390/cells12091314 [4] Singh J K,Smith R,Rother M B,et al. Zinc finger protein ZNF384 is an adaptor of Ku to DNA during classical non-homologous end-joining[J]. Nat Commun,2021,12(1):6560. doi: 10.1038/s41467-021-26691-0 [5] Meng Q X,Wang K N,Li J H,et al. ZNF384-ZEB1 feedback loop regulates breast cancer metastasis[J]. Mol Med,2022,28(1):111. doi: 10.1186/s10020-022-00541-1 [6] Yan Z,Zhou Y,Yang Y,et al. Zinc finger protein 384 enhances colorectal cancer metastasis by upregulating MMP2[J]. Oncol Rep,2022,47(3):49. doi: 10.3892/or.2022.8260 [7] He L,Fan X,Li Y,et al. Overexpression of zinc finger protein 384 (ZNF 384),a poor prognostic predictor,promotes cell growth by upregulating the expression of Cyclin D1 in Hepatocellular carcinoma[J]. Cell Death Dis,2019,10(6):444. doi: 10.1038/s41419-019-1681-3 [8] Yang H, Wang J, Huang Z Z, et al. Cloning and characterization of the 5'-flanking region of the rat glutamate-cysteine ligase catalytic subunit[J]. Biochem J, 2001, 357(Pt 2): 447-455. [9] Yang H,Li G,Qiu G. Bioinformatics analysis using ATAC-seq and RNA-seq for the identification of 15 gene signatures associated with the prediction of prognosis in hepatocellular carcinoma[J]. Front Oncol,2021,11:726551. [10] Tsai M C,Yen Y H,Chang K C,et al. Elevated levels of serum urokinase plasminogen activator predict poor prognosis in hepatocellular carcinoma after resection[J]. BMC Cancer,2019,19(1):1169. doi: 10.1186/s12885-019-6397-3 [11] Luo Y,Teng F,Fu H,et al. Immunotherapy in liver transplantation for hepatocellular carcinoma: Pros and cons[J]. World J Gastrointest Oncol,2022,14(1):163-180. doi: 10.4251/wjgo.v14.i1.163 [12] Gauthier A,Ho M. Role of sorafenib in the treatment of advanced hepatocellular carcinoma: An update[J]. Hepatol Res,2013,43(2):147-154. doi: 10.1111/j.1872-034X.2012.01113.x [13] Fang Y,Zhan Y,Xie Y,et al. Integration of glucose and cardiolipin anabolism confers radiation resistance of HCC[J]. Hepatology,2022,75(6):1386-1401. doi: 10.1002/hep.32177 [14] Zhu L,Bai W,Cheng Q,et al. ZNF384-related fusion genes in acute lymphoblastic leukemia[J]. Cancer Control,2023,30:10732748231182787. [15] Grammatico S,Vitale A,La Starza R,et al. Lineage switch from pro-B acute lymphoid leukemia to acute myeloid leukemia in a case with t(12;17)(p13;q11)/TAF15-ZNF384 rearrangement[J]. Leuk Lymphoma,2013,54(8):1802-1805. doi: 10.3109/10428194.2012.753450 [16] Sim J,Park J,Kim S,et al. Association of Tim-3/Gal-9 Axis with NLRC4 inflammasome in glioma malignancy: Tim-3/Gal-9 induce the NLRC4 inflammasome[J]. Int J Mol Sci,2022,23(4):2028. doi: 10.3390/ijms23042028 [17] Mori S,Takeuchi T,Ishii Y,et al. Identification of APOBEC3B promoter elements responsible for activation by human papillomavirus type 16 E6[J]. Biochem Biophys Res Commun,2015,460(3):555-560. doi: 10.1016/j.bbrc.2015.03.068 [18] Xiao Y,Yang K,Liu P,et al. Deoxyribonuclease 1-like 3 inhibits hepatocellular carcinoma progression by inducing apoptosis and reprogramming glucose metabolism[J]. Int J Biol Sci,2022,18(1):82-95. doi: 10.7150/ijbs.57919 [19] Kendig E L,Chen Y,Krishan M,et al. Lipid metabolism and body composition in Gclm(-/-) mice[J]. Toxicol Appl Pharmacol,2011,257(3):338-348. doi: 10.1016/j.taap.2011.09.017 [20] Wang T,Li C,Han B,et al. Neuroprotective effects of danshensu on rotenone-induced parkinson's disease models in vitro and in vivo[J]. BMC Complement Med Ther,2020,20(1):20. doi: 10.1186/s12906-019-2738-7 [21] Wang S, Wang H, Zhu S, et al. Systematical analysis of ferroptosis regulators and identification of GCLM as a tumor promotor and immunological biomarker in bladder cancer[J]. Front Oncol, 2022, 24(12): 1040892. [22] Inoue Y,Tomisawa M,Yamazaki H,et al. The modifier subunit of glutamate cysteine ligase (GCLM) is a molecular target for amelioration of cisplatin resistance in lung cancer[J]. Int J Oncol,2003,23(5):1333-1339. [23] Wu N,Zhu D,Li J,et al. CircOMA1 modulates cabergoline resistance by downregulating ferroptosis in prolactinoma[J]. J Endocrinol Invest,2023,46(8):1573-1587. doi: 10.1007/s40618-023-02010-w [24] Cheng M L,Lu Y F,Chen H,et al. Liver expression of Nrf2-related genes in different liver diseases[J]. Hepatobiliary Pancreat Dis Int,2015,14(5):485-491. doi: 10.1016/S1499-3872(15)60425-8 -





 下载:
下载: