Correlation between PEAR1 Gene Polymorphisms and Ischemic Stroke
-
摘要:
目的 分析PEAR1基因多态性与缺血性脑卒中相关性,为缺血性脑卒中发病机制的进一步研究提供科学依据,为疾病防治提供新的思路。 方法 收集昆明医科大学附属延安医院神经内科门急诊或住院确诊为急性缺血性脑卒中患者150例作为实验组,同期150例健康体检者作为对照组,应用聚合酶链反应-限制性片断长度多态性(PCR-RFLP)方法分析PEAR1基因rs12041331位点单核苷酸多态性(SNP),并测序验证基因型。 结果 卡方检验显示缺血性脑卒中组和正常对照组PEAR1基因rs12041331G > A位点GG、GA、AA基因型和G、A等位基因频率间的差异有统计学意义(P < 0.05);缺血性脑卒中组的糖尿病、高血压比例较正常对照组多,同型半胱氨酸(HCY)水平较正常对照组高,差异有统计学意义(P < 0.05);Logistic回归分析显示PEAR1基因rs12041331G > A位点突变可能是缺血性脑卒中发生的危险因素。 结论 PEAR1基因rs12041331G > A位点基因多态性与缺血性脑卒中发生相关。rs12041331G > A位点基因可作为缺血性脑卒中风险预测的候选基因。 -
关键词:
- 缺血性脑卒中 /
- 单核苷酸多态性 /
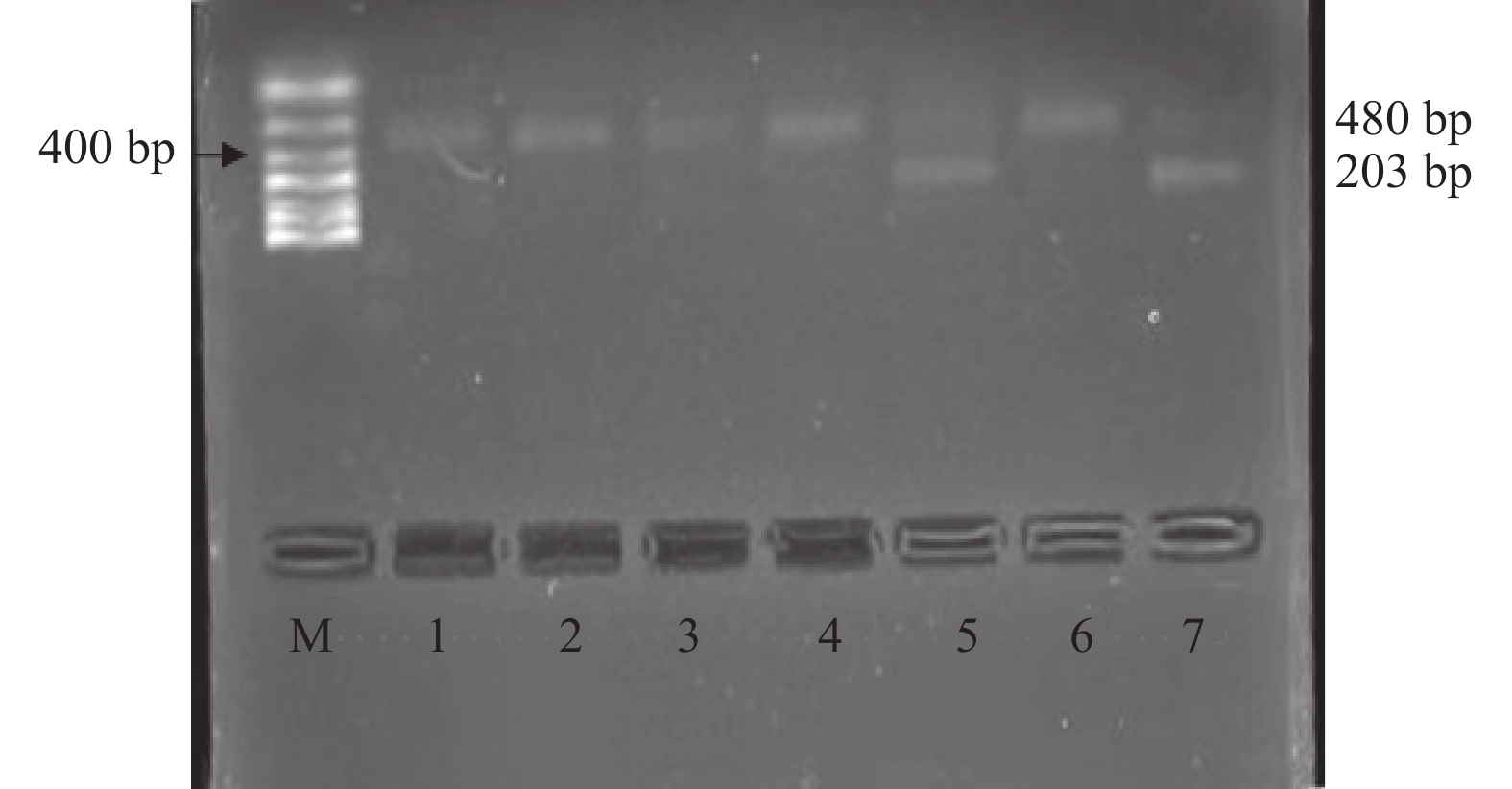
- 聚合酶链反应-限制性片断长度多态性
Abstract:Objective To analyze the correlation between PEAR1 gene polymorphism and ischemic stroke, so as to provide a scientific basis for further research on the pathogenesis of ischemic stroke, and provide new ideas for disease prevention and treatment Methods A total of 150 patients with acute ischemic stroke in the Department of Neurology, Yan’ an hospital affiliated to the Kunming Medical University were selected as the experimental group and 150 healthy persons as the control group, a polymerase chain reaction-restriction fragment length polymorphism(PCR-RFLP) was used to analyze the Single-nucleotide polymorphism at rs12041331 in PEAR1 gene. The genotypes were verified by sequencing. Results Chi-square test results showed that between the ischemic stroke group and control group, the distribution of GG, GAandAA genotypes and allele frequency of G, A on PEAR1 gene rs12041331G > A polymorphism site had significant differences(p < 0.05). The proportion of diabetes mellitus and hypertension and the level of homocysteine homocysteine(HCY) in the ischemic stroke group were significantly higher than those in the control group(p < 0.05).Logistic regression analysis showed that mutations at the PEAR1 gene rs12041331G > A site might be a risk factor for ischemic stroke. Conclusion The polymorphism of PEAR1 gene rs12041331G > A site is associated with ischemic stroke Genetic predisposition. The PEAR1 gene rs12041331G > A site may be a candidate gene for ischemic stroke risk prediction. -
表 1 缺血性脑卒中组和正常对照组一般资料比较[n(%)/
$\bar x \pm s$ ]Table 1. Comparison of general data between ischemic stroke group and normal control group[n(%)/
$\bar x \pm s $ ]分类 缺血性脑卒中组
(n=150)正常对照组
(n=150)t/χ2 P 性别 男 95(63) 88(59) 0.687 0.478 女 55(36) 62(41) 年龄(岁) 63.75±9.67 63.66±8.81 0.087 0.143 高血压 115 (76.67) 40 (26.67) 75.083 <0.001* 糖尿病 58 (38.67) 12 (8.00) 39.429 <0.001* TC(mmol/L) 4.37±0.97 4.45±0.84 −0.743 0.458 TG(mmol/L) 1.64±0.86 1.61±0.67 0.314 0.754 HDL-C(mmol/L) 1.16±0.35 1.22±0.32 −4.161 0.450 LDL-C(mmol/L) 2.69±0.85 2.77±0.64 −0.841 0.401 HCY(μmol/L) 13.78±12.62 10.27±1.86 3.374 0.001* 高HCY 104(69.33) 83(55.33) 6.261 0.017* *P<0.05。 表 2 缺血性脑卒中组和正常对照组的Hardy-Weinberg遗传平衡检验(n)
Table 2. Hardy-weinberg genetic balance test in ischemic stroke group and normal control group(n)
基因位点 基因型 观测值(n) 理论值(n) χ2 P 正常对照组
rs12041331G > AGG 114 111 2.10 0.25 GA 31 36 AA 5 3 缺血性脑卒中组rs12041331G > A GG 62 59 1.09 0.50 GA 64 70 AA 24 21 表 3 缺血性脑卒中组和正常对照组PEAR1基因rs12041331G > A位点基因型分布和等位基因频率的比较[n(%)]
Table 3. Comparison of genotype distribution and allele frequency of PEAR1 gene rs12041331G>A between ischemic stroke group and normal control group[n(%)]
位点 基因型/
等位基因正常
对照组缺血性
脑卒中组χ2 P rs12041331G
>AGG 114(76) 62(41) GA 31(21) 64(43) 39.275 <0.001* AA 5(3) 24(16) G 129(86) 94(63) 21.402 <0.001* A 21(14) 56(37) *P<0.05。 表 4 缺血性脑卒中发生影响因素的Logistic回归分析
Table 4. Logistic regression analysis of influencing factors of ischemic stroke
相关因素 回归系数 标准误 Wald OR 95%CI P 糖尿病 0.865 0.392 4.86 2.374 (1.101,5.121) 0.027* 高血压 1.856 0.302 37.886 6.398 (3.543,11.553) < 0.001* HCY 0.171 0.048 12.523 1.187 (1.079,1.305) < 0.001* GG −1.503 0.253 35.268 0.222 (0.135,0.365) < 0.001* GA 1.050 0.261 16.224 2.857 (1.714,4.761) < 0.001* AA 1.709 0.506 11.388 5.524 (2.047,14.905) < 0.001* *P < 0.05。 -
[1] 中国中西医结合学会急救医学专业委员会,方邦江,李志军,等. 中国急性缺血性脑卒中中西医急诊诊治专家共识[J]. 中华危重病急救医学,2018,30(3):193-197. [2] 李昕,杨建中. 急性缺血性脑卒中静脉溶栓后出血转化危险因素的研究进展[J]. 中华脑血管病杂志(电子版),2023,17(1):9-15. [3] 申利娜,姬利红. PEAR1基因多态性与服用阿司匹林缺血性脑卒中患者复发的相关性分析[J]. 中国药物滥用防治杂志,2021,27(4):617-620. [4] 桑坤琳,唐婕,王玲玲. PEAR1、GSTP1基因型与脑梗死预后的相关性分析[J]. 北华大学学报(自然科学版),2023,24(2):206-211. [5] Kauskot A,DiMichele M,Loyen S,et al. A novel mechanism of sustained platelet α IIbβ 3 activation via PEAR1[J]. Blood:The Journal of the American Society of Hematology,2012,119(17):4056-4065. [6] Xiang Q,Zhou S,Lewis J P,et al. Genetic variants of PEAR1 are associated with platelet function and antiplatelet drug efficacy: A systematic review and meta-analysis[J]. Current Pharmaceutical Design,2017,23(44):6815-6827. [7] 中华医学会神经病学分会,中华医学会神经病学分会脑血管病学组. 中国急性缺血性脑卒中诊治指南2018[J]. 中华神经科杂志,2018,51(9):666-682. [8] 崔君,蒯圣旺. 低剂量CT颅脑灌注成像诊断缺血性脑卒中的临床价值研究[J]. 中国CT和MRI杂志,2021,19(9):13-15. [9] 郭健. 中国脑卒中及其危险因素的流行特征变化趋势(2002—2013年)[J]. 中华预防医学杂志, 2019, 53(2): 211. [10] 上官醉飞,毛其芬,张鹏,等. HCYHDL-C比值与急性缺血性脑卒中的关联性分析[J]. 浙江临床医学,2023,25(4):578-580. [11] Faraday N,Yanek L R,Yang X P,et al. Identification of a specific intronic PEAR1 gene variant associated with greater platelet aggregability and protein expression[J]. Blood:The Journal of the American Society of Hematology,2011,118(12):3367-3375. [12] 李天瑜,袁晋青. 血小板内皮聚集受体1与血小板功能的基础与临床研究进展[J]. 中国分子心脏病学杂志,2020,20(4):3445-3448. [13] Yang J,Bao Z,Hu G,et al. Impact of platelet endothelial aggregation receptor 1 genotypes and DNA methylation on platelet reactivity in patients with recurrent ischemic stroke treated with clopidogrel[J]. Arch Med Sci.,2023,19(2):518-522. doi: 10.5114/aoms/159180 [14] 石秀锦,胡志旭,彭文星,等. GPⅢa PLA2、PEAR1、PTGS1基因多态性与阿司匹林临床抗血栓疗效关联性研究[J]. 中国药物应用与监测,2018,15(1):1-4. [15] 石洪晨,李清,付文亭. 长期服用阿司匹林脑梗死患者的复发因素及PEAR1基因多态性分布情况[J]. 中国药物滥用防治杂志,2023,29(6):987-989,994. -






 下载:
下载: