Study on Immune Function and Drug Resistance of Tuberculosis Patients Co-infected with HBV,HCV and HIV in Yunnan
-
摘要:
目的 探讨云南地区结核病患者合并感染HBV、HCV、HIV中合并感染率、免疫功能及耐药性状况。 方法 收集2020年4月至2023年3月昆明市第三人民医院收治的2271例云南地区结核病患者进行HBV、HCV、HIV血清学检测,同时进行淋巴细胞检测及结核菌的耐药基因检测,分析结核病分别感染HBV、HCV、HIV的感染率、免疫功能及耐药性。 结果 2271例结核病患者中,结核病合并HBV感染499例,感染率21.97%;合并HCV感染196例,感染率8.63%;合并HIV感染166例,感染率7.31%;单纯结核患者1410例,占比62.09%。结核病合并HBV、HCV、HIV感染率在不同年龄组比较,差异具有统计学意义(P < 0.01)。结核病合并HBV、HCV患者中CD3+、CD4+和CD8+T细胞的绝对数量表达较高,且两者的差异均具有统计学意义(P < 0.05);结核病合并HIV患者CD3+、CD4+T细胞的绝对数量表达较低,CD8+T细胞的绝对数量表达上升,两者的差异具有统计学意义(P < 0.01)。CD3+、CD4+、CD8+T细胞绝对数量在结核合并HIV的女性患者中表达较高,且差异均具有统计学意义(P < 0.05);各年龄段中,结核合并HIV患者CD3+、CD8+T细胞绝对数量在46~65岁组最低,差异均有统计学意义(P < 0.05)。2271例结核病患者中,耐任意1种一线药(单耐药)有391例,总体耐药率17.22%;其中,合并HBV耐药52例,耐药率10.42%;合并HCV耐药10例,耐药率5.10%;合并HIV耐药40例,耐药率24.10%;单纯结核患者耐药289例,耐药率20.50%。其中最多的是单耐药耐利福平33例,占19.88%。 结论 云南地区结核及合并HBV感染率最高,结核合并HIV患者的免疫功能最差,结核合并HIV的耐药率最高,单耐药以耐利福平最多;结核属于慢性消耗性疾病,免疫功能较一般人群差,易合并HBV感染,结核患者感染HIV有加重免疫功能减低及耐药性产生的趋势。 Abstract:Objective To explore the co-infection rate, immune function and drug resistance status among tuberculosis patients co-infected with HBV, HCV and HIV in Yunnan. Methods A total of 2271 TB patients in Yunnan province admitted to the Third People's Hospital of Kunming from April 2020 to March 2023 were collected for HBV, HCV, HIV serological tests, lymphocyte tests and drug resistance gene detection, and analysis of TB infection of HBV, HCV, HIV infection, immune function and resistance. Results Among the 2271 TB patients, 499 cases were infected with TB and HBV, the infection rate was 21.97%. 196 cases were infected with HCV, the infection rate was 8.63%. 166 cases were infected with HIV, the infection rate was 7.31%. There were 1410 patients with simple tuberculosis, accounting for 62.09%. The infection rates of tuberculosis combined with HBV, HCV and HIV were statistically significant in different age groups(P < 0.01). The absolute number expression of CD3+, CD4+ and CD8+T cells was higher in TB patients with HBV and HCV, and the differences between the two were statistically significant(P < 0.05).The absolute number expression of CD3+ and CD4+T cells was lower in TB patients with HIV, and the absolute number expression of CD8+T cells was increased, and the difference between the two was statistically significant(P < 0.01). The absolute number of CD3+, CD4+ and CD8+T cells was higher in female patients with tuberculosis and HIV, and the differences were statistically significant(P < 0.05). In all age groups, the absolute number of CD3+ and CD8+T cells in tuberculosis patients with HIV was the lowest in 46-65 years old group, and the differences were statistically significant(P < 0.05). Among the 2271 TB patients, 391 were resistant to any first-line drug(single drug resistance), and the overall drug resistance rate was 17.22%. Among them, 52 cases were combined with HBV drug resistance, the resistance rate was 10.42%. There were 10 cases with HCV drug resistance, the drug resistance rate was 5.10%. 40 cases were combined with HIV drug resistance, the drug resistance rate was 24.10%. Drug resistance in 289 patients with simple tuberculosis was 20.50%. Among them, 33 cases were single drug resistant rifampicin, accounting for 19.88%. Conclusion Tuberculosis has the highest rate of co-infection with HBV, and the immune function of TB patients co-infected with HIV is the worst. The drug resistance rate of TB patients co-infected with HIV is also the highest, with resistance to rifampicin being the most common. TB is a chronic wasting disease, with poorer immune function compared to the general population, making it more susceptible to HBV infection. TB patients who are also infected with HIV tend to have worsened immune function and increased drug resistance. -
Key words:
- Tuberculosis /
- Hepatitis B virus /
- Hepatitis C virus /
- Human immunodeficiency virus /
- Drug resistance /
- Yunnan region
-
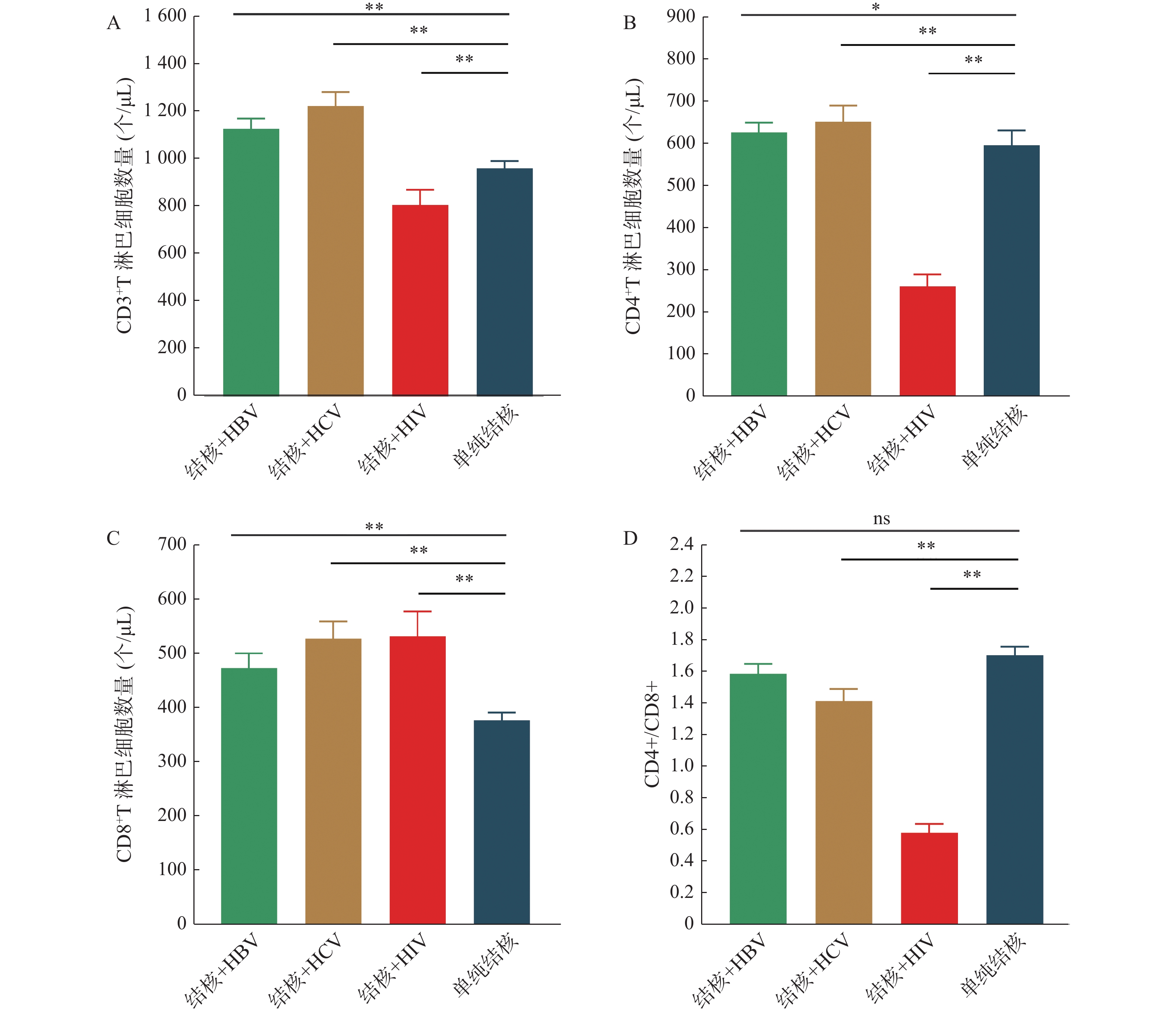
图 1 结核及合并HBV、HCV、HIV免疫指标分析
A:各组血清CD3+T淋巴细胞数量的平均数和SE;B:各组血清CD4+T淋巴细胞数量的平均数和SE;C:各组血清CD8+T淋巴细胞数量的平均数和SE;D:各组血清CD4+/CD8+淋巴细胞数量的平均数和SE。各组血清T淋巴细胞表达情况分析,直方图显示了每组的平均数和SE,各组间差异的显著性用Mann-Whitney 检验。与单纯结核比较,*P < 0.05,**P < 0.01。
Figure 1. Analysis of immunologic indicators of tuberculosis and combined HBV,HCV,and HIV
表 1 结核及合并HBV、HCV、HIV感染分析 [n(%)]
Table 1. Analysis of tuberculosis and co-infection with HBV,HCV and HIV [n(%)]
分类 结核+HBV 结核+HCV 结核+HIV 单纯结核 χ2 P 性别 男 350 (70.14) 147 (75.0) 128(77.11) 992 (70.35) 4.971 0.174 女 149 (29.86) 49 (25.0) 38 (22.89) 418 (29.65) 年龄(岁) ≤18 12 (2.40) 2 (1.02) 0 (0.00) 52 (3.69) 81.53 0.001* 19~45 223 (44.69) 77 (39.29) 80 (48.19) 556 (39.43) 46~65 210 (42.08) 103(52.55) 69 (41.57) 487 (34.54) ≥66 54 (10.82) 14 (7.14) 17 (10.24) 315 (22.34) 合计 499 196 166 1410 各年龄组组内比较,*P < 0.05。 表 2 结核及合并HBV、HCV、HIV免疫指标情况 ($\bar x \pm s$)
Table 2. Tuberculosis and combined HBV,HCV,and HIV immune indicators ($\bar x \pm s$)
相关指标 结核+HBV 结核+HCV 结核+HIV 单纯结核 U P CD3+T(个/μL) 1126 ± 41.41** 1220 ± 57.64** 806.6 ± 62.71** 958.7 ± 30.57 7041 0.001** CD4+T(个/μL) 626.3 ± 22.78* 650.9 ± 38.49** 262.7 ± 28.45** 595.4 ± 35.17 22236 0.03* CD8+T(个/μL) 472.7 ± 26.45** 526.1 ± 31.35** 530.5 ± 45.88** 376.8 ± 13.43 7234 0.004** CD4+/CD8+ 1.58 ± 0.06 1.41 ± 0.08** 0.58 ± 0.05** 1.70 ± 0.05 9423 0.002** 与单纯结核比较,*P < 0.05;**P < 0.01。 表 3 结核合并HIV不同性别和年龄段免疫指标情况 ($ \bar x \pm s$)
Table 3. Immunological indicators of tuberculosis combined with HIV by sex and age ($ \bar x \pm s $)
分类 CD3+T(个/μL) CD4+T(个/μL) CD8+T(个/μL) CD4+/CD8+ 性别 男 (n=128) 763.7 ± 64.04* 241.9 ± 25.70* 508.7 ± 51.10* 0.61 ± 0.06 女 (n=38) 944.3 ± 155.8* 316.1 ± 82.58* 613.6 ± 98.28* 0.47 ± 0.11 年龄(岁) ≤18 (n=0) — — — — 19~45 (n=80) 845.2 ± 99.01# 224.6 ± 32.84 589.9 ± 78.55# 0.46 ± 0.06 46~65 (n=69) 743.0 ± 80.89 296.0 ± 49.88 452.3 ± 49.24 0.73 ± 0.09 ≥66 (n=17) 893.8 ± 198.7# 307.0 ± 65.12 669.0 ± 139.8# 0.47 ± 0.10 与男性比较,*P < 0.05;与46~65岁比较,#P < 0.05;—:无数据。 表 4 结核病与HBV、HCV、HIV共感染耐药情况 [n(%)]
Table 4. Tuberculosis and HBV,HCV,HIV co-infection drug resistance [n(%)]
分类 结核+HBV 结核+HCV 结核+HIV 单纯结核 χ2 P 性别 男 37 (71.15) 6 (60.0) 22 (55.0) 208 (71.97) 5.306 0.151 女 15 (28.85) 4 (40.0) 18 (45.0) 81 (28.03) 年龄(岁) ≤18 1 (1.92) 0 (0.00) 0 (0.00) 8 (2.77) 9.622 0.382 19-45 20 (38.46) 2 (20.0) 22 (55.0) 123 (42.56) 46-65 22 (42.31) 6 (60.0) 14 (35.0) 96 (33.22) ≥66 9 (17.31) 2 (20.0) 4 (10.0) 62 (21.45) 合计 52 10 40 289 表 5 结核病与HBV、HCV、HIV共感染各抗结核药耐药情况 [n(%)]
Table 5. Tuberculosis and HBV,HCV,HIV co-infection by anti-tuberculosis drug resistance [n(%)]
分类 结核+HBV (n=52) 结核+HCV (n=10) 单纯结核(n=289) χ2 P 异烟肼 22 (42.31) 3 (30.0) 172 (59.52) 6.862 0.333 利福平 40 (76.92) 8 (80.0) 183 (63.32) 链霉素 13 (25) 2 (20.0) 80 (27.68) 乙胺丁醇 12 (23.08) 2 (20.0) 98 (33.91) -
[1] Massimo D P,Maria T M,Luisa Bi,et al. Evaluation of LIAISON®XL System for HBs Ag,and anti-HCV and anti-HIV/Ag p24[J]. Journal of Medical Virology,2017,89(8):489-496. [2] 秦志华,顾尔莉,施军卫,等. 抗结核治疗导致乙型肝炎病毒再激活相关性研究[J]. 中国热带医学,2022,22(2):138-142. [3] 马世武,王嘉睿,朱娅梅. 结核合并丙型肝炎病毒感染同时治疗的药物选择[J]. 中华肝脏病杂志,2022,30(1):113-116. [4] 卢春容,房宏霞,陆普选,等. WHO 2021年全球结核病报告: 全球与中国关键数据分析[J]. 新发传染病电子杂志,2021,6(4):368-372. [5] 肺结核诊断 WS 288—2017[J]. 中国感染控制杂志, 2018, 17(7): 642-652. [6] 周颖. 结核分枝杆菌异烟肼耐药性与脂肪酸合成代谢基因accD1和mcr相关性的初步研究[D]. 长春: 吉林农业大学, 2020. [7] 王钰婷,陶必林,李忠奇,等. 全球结核分枝杆菌谱系分布与耐药分析[J]. 中华疾病控制杂志,2022,26(11):1248-1251,1295. [8] Chakaya J,Khan M,Ntoumi F,et al. Global tuberculosis report 2020-reflections on the Global TB burden,treatment and prevention efforts[J]. International Journal of Infectious Diseases,2021,113 Suppl 1(Suppl 1):S7-S12. [9] 梁思敏. 新疆南疆地区抗结核药物性肝损伤危险因素分析及列线图预测模型的构建[D]. 乌鲁木齐: 新疆医科大学, 2023. [10] 叶洁桐. 化瘀柔肝方联合恩替卡韦治疗乙肝肝硬化的临床观察[J]. 中国中医药科技,2022,29(6):1028-1030. [11] 晁春梅,哏传香,金正英,等. 2015-2019年云南省献血者血清阳性隐匿性乙肝病毒感染流行病学特征[J]. 热带医学杂志,2021,21(5):650-652+669. [12] 李涛, 闫翔宇, 杜昕, 等. 中国肺外结核流行现状的全国性调查研究[C]. 中国防痨协会, 2023, 2(1): 198-199. [13] 王新霞,吴晓美,童涌. 艾滋病患者结核杆菌感染与其免疫功能及HIV载量的关系[J]. 中国现代医生,2022,60(6):8-11+50. [14] 张凌,陈玉萍,李琴. HIV感染者HBV HCV TP及TB检测结果研究[J]. 基层医学论坛,2021,25(26):3792-3794. [15] 唐柳生, 黄于萍, 雷振, 等. 223株艾滋病合并感染结核分枝杆菌临床分离株的耐药特征[C]. 中国防痨协会, 2023, 2(1): 363-365. [16] 王娟娟,施旭东,肖园园,等. 南京地区HIV/AIDS患者分枝杆菌感染分布及耐药性分析[J]. 临床检验杂志,2021,39(2):148-150. [17] 王印,朱迎春,周锐峰,等. HIV/AIDS合并结核病患者196株结核分枝杆菌耐药分析[J]. 重庆医学,2017,46(9):1203-1205. [18] 古丽米拉·达列力汗,宋玉霞,李弘,等. 艾滋病合并结核病患者结核分枝杆菌耐药分析[J]. 传染病信息,2022,35(3):245-247,258. [19] 律彤. 云南省利福平耐药肺结核患者经济负担现状及影响因素研究[D]. 昆明: 昆明医科大学, 2022. -






 下载:
下载: