CD147 Mediates Cervical Cancer Cell Pyroptosis and Proliferation through AIM2 Inflammasome
-
摘要:
目的 探讨跨膜蛋白CD147表达量变化对AIM2炎症小体介导的宫颈癌细胞焦亡及增殖的影响。 方法 采用Western blot 实验检测 CD147 在宫颈癌细胞 SiHa(HPV+)、C33a(HPV-) 和正常宫颈上皮细胞 H8(HPV+) 、HCer Epic(HPV-)中的表达水平;通过慢病毒转染 SiHa细胞下调CD147的表达,根据不同处理分为SiHa组、阴性对照组(shCD147-NON)、敲低组1(shCD147-1)和敲低组2(shCD147-2),通过Western blot、RT-qPCR和观察细胞绿色荧光表达验证转染效果;通过Western blot 和 RT-qPCR 检测CD147和AIM2炎症小体相关因子 AIM2、Caspase-1、IL-18、GSDMD蛋白和 mRNA 的表达;检测细胞培养上清中乳酸脱氢酶(LDH) 释放度,荧光倒置显微镜下观察细胞的形态;CCK-8 实验检测细胞的增殖能力;细胞克隆实验检测细胞集落形成能力。 结果 Western blot 结果显示,与 HCerEpic细胞比较,SiHa 细胞中 CD147 蛋白表达最高(P < 0.05) ; CD147低表达慢病毒有效下调了SiHa细胞 CD147表达水平(P < 0.05);Western blot 及 RT-qPCR实验结果表明,与SiHa组相比, shCD147-1 组和 shCD147-2 组AIM2、Caspase-1、IL-18、GSDMD蛋白和 mRNA 表达明显升高(P < 0.05);乳酸脱氢酶(LDH)释放实验显示,与SiHa组相比,shCD147组LDH释放度明显升高(P < 0.05);荧光倒置显微镜下显示,shCD147组出现肿胀和空泡化,表现出典型的细胞焦亡现象;与SiHa组相比,shCD147-1组和shCD147-2组细胞增殖能力和集落形成能力明显降低(P < 0.05)。 结论 CD147低表达有效上调宫颈癌 SiHa 细胞AIM2炎症相关因子的表达,诱发细胞焦亡,抑制细胞的增殖和克隆。 Abstract:Objective To investigate the effect of transmembrane protein CD147 expression on AIM2 inflammasome-mediated pyroptosis and proliferation of cervical cancer cells. Methods Western Blot was used to detect the expression of CD147 in cervical cancer cell lines SiHa(HPV+) and C33a(HPV-) and normal cervical epithelial cells H8(HPV+) and HCer Epic(HPV-). SiHa cells were transfected with lentivirus to down-regulate the expression of CD147. According to the different treatments, SiHa cells were divided into SiHa group, negative control group(shCD147-NON), knockdown group 1(shCD147-1) and knockdown group 2(shCD147-2). The transfection effect was verified by Western Blot, RT-qPCR and green fluorescence expression. The protein and mRNA expressions of AIM2, Caspase-1, IL-18 and GSDMD were detected by Western Blot and RT-qPCR. The lactate dehydrogenase(LDH) release was measured in the cell culture supernatant, and the cell morphology was observed under the fluorescence inverted microscope; the proliferation ability of cells was measured by CCK-8 and the colony formation ability was measured by cell cloning experiments. Results Western Blot results showed that CD147 protein expression in SiHa cells was the highest compared with that in HCerEpic cells. CD147 low expression lentivirus effectively down-regulated the expression of CD147 in SiHa cells. The results of Western Blot and RT-qPCR experiments showed that the expression of AIM 2, Caspase-1, IL-18, GSDMD protein and mRNA increased in shCD147-1 and shCD147-2 group(P < 0.05). Lactate dehydrogenase(LDH) release assay showed that compared with the SiHa group, the shCD147 group had a significant increase in LDH release(P < 0.05). Fluorescence inverted microscope showed that the shCD147 group had swelling and vacuolization, showing typical pyroptosis. Compared with the SiHa group, the shCD147-1 and shCD147-2 groups had significantly reduced the cell proliferation and colony formation ability(P < 0.05). Conclusion Low expression of CD147 effectively up-regulates the expression of AIM2 inflammation-related factors in cervical cancer SiHa cells, induces the pyroptosis, and inhibits the cell proliferation and cloning. -
Key words:
- Cervical cancer /
- CD147 /
- AIM2inflammasome /
- Pyroptosis /
- Proliferation
-
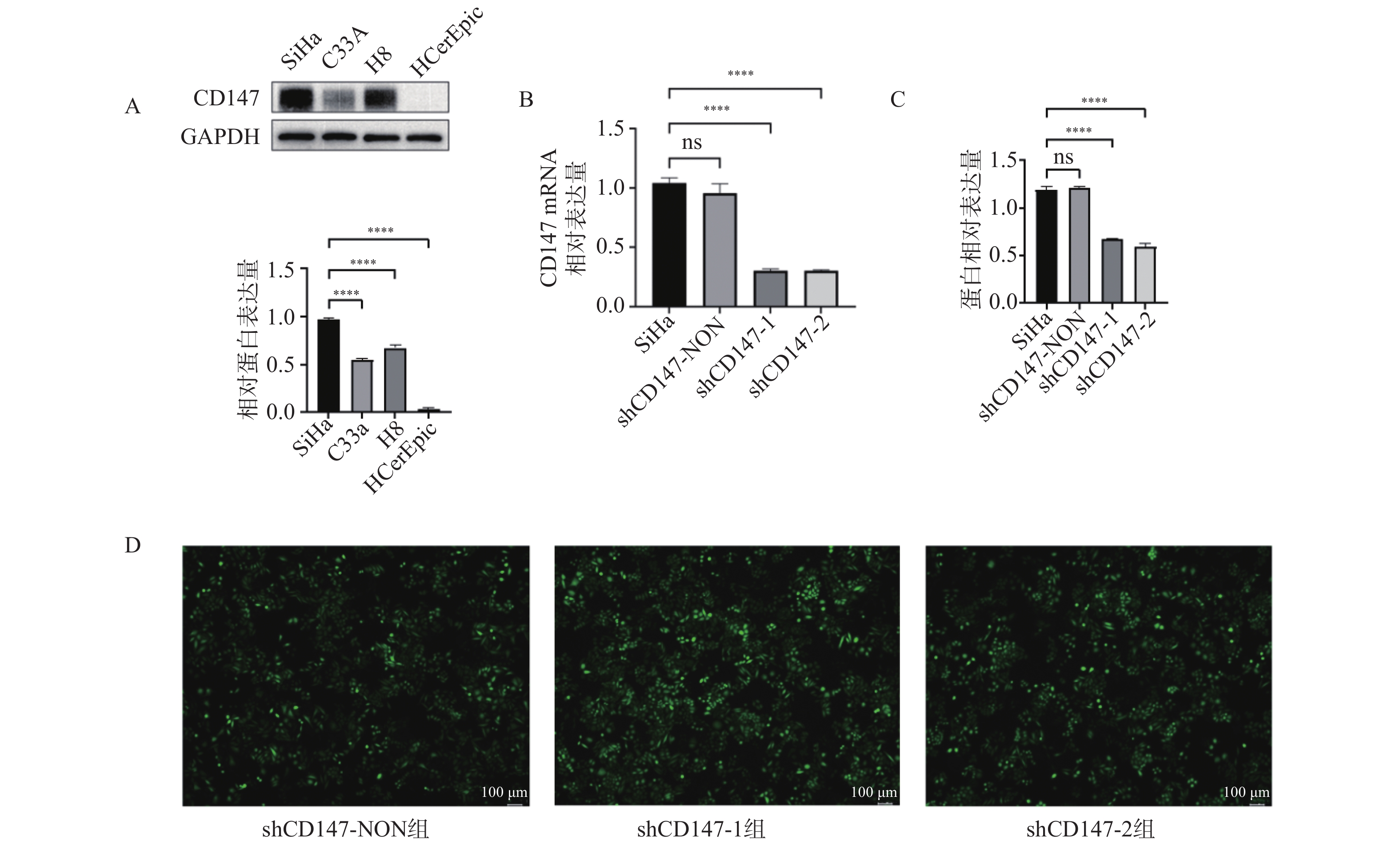
图 1 检测 CD147在宫颈癌细胞中的表达水平及慢病毒转染效率
A:CD147蛋白在宫颈癌及正常宫颈上皮细胞中的相对表达量;B:转染慢病毒后CD147的 mRNA 的表达情况;C:转染慢病毒后CD147蛋白的相对表达量;D:慢病毒转染CD147细胞后绿色荧光表达情况 ( 标尺为100 μm);ns:差异无统计学意义;****P < 0.0001。
Figure 1. The expression level of CD147 in cervical cancer cells and the transfection efficiency of lentivirus were detected
表 1 RT-qPCR检测基因的引物序列
Table 1. Primer sequences of genes detected by RT-qPCR
基因 引物序列 CD147 F-TGTTCGTGCTGCTGGGATTCG
R-GAGCCAAGGTCTTCTACGGTAGTGAIM2 F-TATCGGCACAGTGGTTTCTTAGAGG
R-GGGCTGAGTTTGAAGCGTGTTGCaspase-1 F-CCCACATCCTCAGGCTCAGAAG
R-TGCGGCTTGACTTGTCCATTATTGIL-18 F-TGGCTGCTGAACCAGTAGAAGAC
R-GAGGCCGATTTCCTTGGTCAATGGSDMD F-CCAGAAGAAGACGGTCACCATCC
R-TGGAACGCTTGTGGCCTGTCGAPDH F-TGCACCACCAACTGCTTAGC
R-GGCATGGACTGTGGTCATGAG -
[1] Sung H,Ferlay J,Siegel R L,et al. Global cancer statistics 2020: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2021,71(3):209-249. doi: 10.3322/caac.21660 [2] Kendrick A A,Schafer J,Dzieciatkowska M,et al. Cd147: A small molecule transporter ancillary protein at the crossroad of multiple hallmarks of cancer and metabolic reprogramming[J]. Oncotarget,2017,8(4):6742-6762. doi: 10.18632/oncotarget.14272 [3] Dana P,Kariya R,Vaeteewoottacharn K,et al. Upregulation of cd147 promotes metastasis of cholangiocarcinoma by modulating the epithelial-to-mesenchymal transitional process[J]. Oncol Res,2017,25(7):1047-1059. doi: 10.3727/096504016X14813899000565 [4] Schroder K,Tschopp J. The inflammasomes[J]. Cell,2010,140(6):821-832. doi: 10.1016/j.cell.2010.01.040 [5] Shi J,Gao W,Shao F. Pyroptosis: Gasdermin-mediated programmed necrotic cell death[J]. Trends Biochem Sci,2017,42(4):245-254. doi: 10.1016/j.tibs.2016.10.004 [6] Rao Z,Zhu Y,Yang P,et al. Pyroptosis in inflammatory diseases and cancer[J]. Theranostics,2022,12(9):4310-4329. doi: 10.7150/thno.71086 [7] Kumari P,Russo A J,Shivcharan S,et al. Aim2 in health and disease: Inflammasome and beyond[J]. Immunol Rev,2020,297(1):83-95. doi: 10.1111/imr.12903 [8] Fidler T P,Xue C,Yalcinkaya M,et al. The aim2 inflammasome exacerbates atherosclerosis in clonal haematopoiesis[J]. Nature,2021,592(7853):296-301. doi: 10.1038/s41586-021-03341-5 [9] 郭文涛. Cd147调控srebps影响宫颈癌细胞脂肪酸合成及侵袭迁移能力的实验研究[D]. 乌鲁木齐: 新疆医科大学硕士学位论文, 2020. [10] Lee C L,Lam M P,Lam K K,et al. Identification of cd147 (basigin) as a mediator of trophoblast functions[J]. Hum Reprod,2013,28(11):2920-2929. doi: 10.1093/humrep/det355 [11] Yang H,Chen B. Cd147 in ovarian and other cancers[J]. Int J Gynecol Cancer,2013,23(1):2-8. doi: 10.1097/IGC.0b013e3182749139 [12] Poli G,Fabi C,Bellet M M,et al. Epigenetic mechanisms of inflammasome regulation[J]. Int J Mol Sci,2020,21(16):5758. doi: 10.3390/ijms21165758 [13] Wang L,Sun L,Byrd K M,et al. Aim2 inflammasome's first decade of discovery: Focus on oral diseases[J]. Front Immunol,2020,11(8):1487. [14] Lee S,Karki R,Wang Y,et al. Aim2 forms a complex with pyrin and zbp1 to drive panoptosis and host defence[J]. Nature,2021,597(7876):415-419. doi: 10.1038/s41586-021-03875-8 [15] Du T,Gao J,Li P,et al. Pyroptosis,metabolism,and tumor immune microenvironment[J]. Clin Transl Med,2021,11(8):e492. doi: 10.1002/ctm2.492 [16] Yu P,Zhang X,Liu N,et al. Pyroptosis: Mechanisms and diseases[J]. Signal Transduct Target Ther,2021,6(1):128. doi: 10.1038/s41392-021-00507-5 [17] Pushkarsky T,Zybarth G,Dubrovsky L,et al. Cd147 facilitates hiv-1 infection by interacting with virus-associated cyclophilin A[J]. Proc Natl Acad Sci USA,2001,98(11):6360-6365. doi: 10.1073/pnas.111583198 [18] Majno G,Joris I. Apoptosis,oncosis,and necrosis. An overview of cell death[J]. Am J Pathol,1995,146(1):3-15. [19] Butera A,Quaranta M T,Crippa L,et al. Cd147 targeting by ac-73 induces autophagy and reduces intestinal fibrosis associated with tnbs chronic colitis[J]. J Crohns Colitis,2022,16(11):1751-1761. doi: 10.1093/ecco-jcc/jjac084 [20] Kulyar M F,Yao W,Ding Y,et al. Cluster of differentiation 147 (cd147) expression is linked with thiram induced chondrocyte's apoptosis via bcl-2/bax/caspase-3 signalling in tibial growth plate under chlorogenic acid repercussion[J]. Ecotoxicol Environ Saf,2021,213(4):112059. [21] 曹勋荣,吕桂雪,魏雯雯. Rna干扰抑制cd147表达对宫颈癌细胞增殖、转移和侵袭能力的影响[J]. 中国免疫学杂志,2023,39(2):349-353,358. doi: 10.3969/j.issn.1000-484X.2023.02.023 -






 下载:
下载: