The Association of Intestinal Flora Metabolite TMAO with Non-alcoholic Fatty Liver Disease
-
摘要:
目的 检测NAFLD患者血清氧化三甲胺(TMAO)及其前体代谢物水平,及肠道中直肠真杆菌、多形拟杆菌、乳酸杆菌和双歧杆菌的表达量,探讨肠道菌群代谢物TMAO在NAFLD病程进展中的作用。 方法 随机选取118例受试者,分为NAFLD组86例和健康对照组32例,采用高效液相色谱串联质谱法检测受试者血清中TMAO及其前体代谢物的水平,qRT-PCR法检测粪便中目标细菌DNA的表达量。 结果 NAFLD患者血清TMAO、三甲胺(TMA)及胆碱水平明显升高(P<0.05),肝脏脂肪含量与TMAO的水平具有正相关性(P<0.05);NAFLD患者粪便中乳酸杆菌、直肠真杆菌表达量增加(P < 0.05),双歧杆菌、多形拟杆菌表达量减少(P < 0.05);血清TMAO水平与粪便中直肠真杆菌的数量呈正相关(r=0.280,P<0.05),与双歧杆菌的数量呈负相关(r=-0.332,P<0.05)。 结论 血清TMAO水平与NAFLD的严重程度呈正相关,NAFLD患者肠道菌群结构失衡,且与TMAO存在关联,推断肠道菌群可能通过代谢生成TMAO在NAFLD病程进展中起重要作用。 Abstract:Objective To explore the role of TMAO from gut microbiota in non-alcoholic fatty liver disease (NAFLD), we detected the serum level of TMAO and its precursor metabolites in NAFLD, as well as the expression level of Eubacterium rectum, Bacteroidetes multiforme, Lactobacillus and bifidobacterium in the intestinal flora. Methods We collected 118 subjects and divided into NAFLD group (86 cases) and healthy control group (32 cases) randomly. We also detected the serum level of TMAO and its precursor metabolites in subjects by high performance liquid chromatography tandem mass spectrometry detection (LC-MS), and the expression of target bacterial DNA was detected by qRT-PCR. Results Serum TMAO, TMA and choline levels were significantly increased in NAFLD (P<0.05), and liver fat content was positively correlated with TMAO (P<0.05). The expression level of Lactobacillus and Eubacterium rectum in NAFLD group were increased (P<0.05); the expression level of Bifidobacterium and Bacteroides multiform were decreased (P<0.05).The serum TMAO level was positively correlated with Eubacterium rectum (r=0.280, P<0.05), and negatively correlated with Bifidobacterium (r=-0.332, P<0.05). Conclusion The level of TMAO in serum shows a positive correlation with NAFLD. The structure of intestinal flora in individuals with NAFLD is altered and linked to TMAO. This suggests that the intestinal flora may have a significant impact on the development of NAFLD through TMAO. -
Key words:
- Non-alcoholic fatty liver disease /
- TMAO /
- TMA /
- Intestinal flora
-
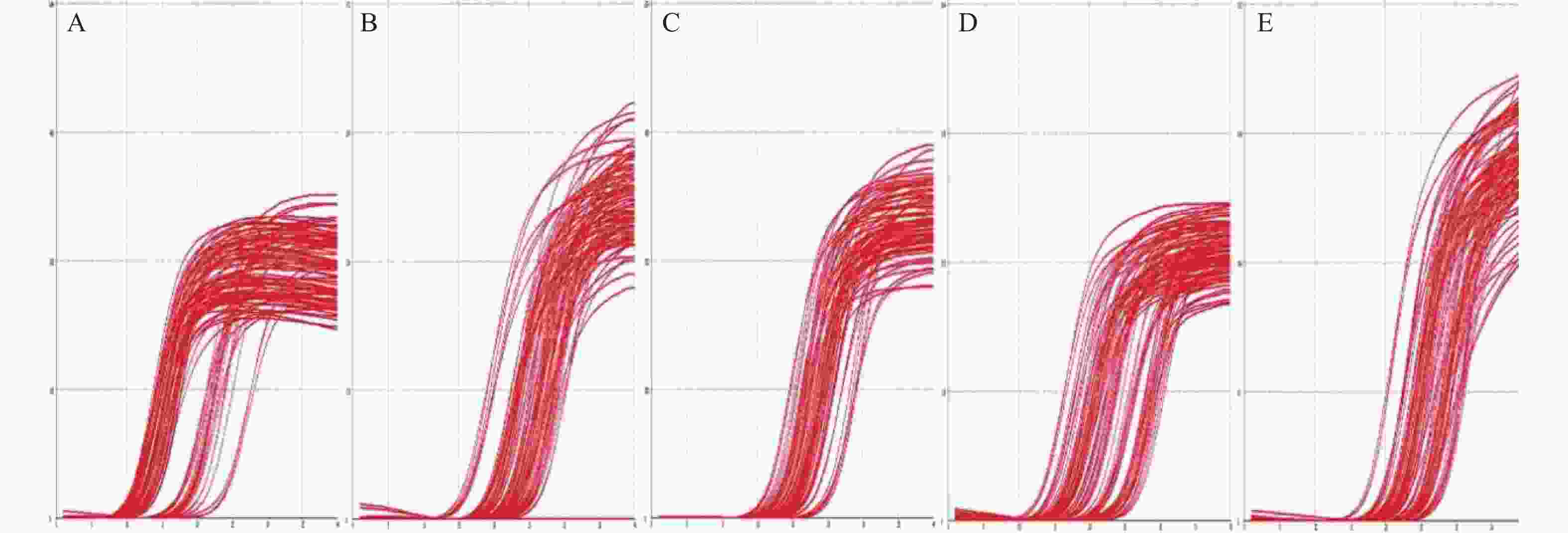
表 1 引物及内参序列
Table 1. The sequences of primer and internal reference
细菌名称 序列(5′-3′) 直肠真杆菌 F: GGGTGACCGGCCACATTGGG R: ATCAGACTTGCCGCACCGCC 乳酸杆菌 F: AGCAGTAGGGAATCTTCCA R: CACCGCTACACATGGAG 双歧杆菌 F:GATTCTGGCTCAGGATGAACGC R: CTGATAGGACGCGACCCAT 多行拟杆菌 F: CCGCCTCCGTTAGCTGCGTG R: ACGTAGGCTGCACAGCCGGT GAPDH(内参) F: TCGGCATCATCGAAGGTCTG R: TGCCATTCAGTTCTGGCAGT F:上游引物 R:下游引物 表 2 2组受试者的一般临床指标比较 [M(P25,P75) /$ \bar x \pm s $]
Table 2. Comparison of the general data between the two groups [M(P25,P75) /$ \bar x \pm s $]
临床指标 NAFLD组(n=86) 健康对照组(n=32) Z/t P 性别(男/女) 49/37 12/20 3.543 0.060 年龄(岁) 50.63±15.02 40.34±12.47 3.454 0.001* BMI(kg/m2) 25.01±3.04 21.06±2.23 6.794 <0.001* 腰围(cm) 93.5(84.75,102.25) 81.5(75.25,84.0) −5.911 <0.001* 臀围(cm) 99.5(94.0,105.0) 93.0(89.25,95.75) −4.318 <0.001* FPG(mmol/L) 5.77(5.05,7.67) 4.96(4.09,5.25) −4.147 <0.001* HbA1C(%) 6.65(5.70,9.25) 5.45(5.33,5.58) −6.861 <0.001* HOMA-IR 2.46(0.52,3.82) 0.27(0.23,0.50) −6.435 <0.001* TC(mmol/L) 4.65±1.17 4.45±0.75 0.873 0.385 TG(mmol/L) 2.25(1.64,3.33) 0.89(0.70,1.30) −5.203 <0.001* HDL-C(mmol/L) 1.03±0.26 1.34±0.33 −5.386 <0.001* LDL-C(mmol/L) 2.93±1.06 2.71±0.59 1.128 0.262 AST(IU/L) 21.00(16.05,27.33) 21.35(14.60,25.28) −1.595 0.111 ALT(IU/L) 23.75(15.68,36.90) 15.15(12.23,20.18) −3.562 <0.001* γ-GGT(U/L) 46.50(23.00,83.00) 18.50(13.25,27.50) −5.238 <0.001* TBA(µmol/L) 3.85(2.20,7.15) 1.6(0.95,3.10) −2.177 0.030* UA(µmol/L) 390.92±124.92 328.80±70.15 2.657 0.009* GFR(mL/min) 103.05(82.25,130.81) 84.86(69.03,107.11) −2.851 0.004* *P < 0.05。 表 3 2组受试者TMAO及其前体代谢物比较 [M(P25,P75) /$ \bar x \pm s $]
Table 3. Comparison of TMAO and its precursor metabolites between the two groups [M(P25,P75) /$ \bar x \pm s $]
代谢物 NAFLD组(n=86) 健康对照组(n=32) Z/t P TMAO(ng/mL) 240.20(148.97,386.84) 136.94(100.40,246.37) −3.584 <0.001* TMA(ng/mL) 186.88(146.30,278.83) 141.84(114.62,231.03) −2.312 0.021* 胆碱(ng/mL) 1882.20±442.22 1582.59±538.60 3.079 0.003* 甜菜碱(ng/mL) 4121.55±973.57 4175.00±855.83 −0.274 0.785 左旋肉碱(ng/mL) 7736.19±2334.51 8084.90±1703.53 −0.771 0.442 *P < 0.05。 表 4 肝脏脂肪含量与TMAO、TMA及胆碱相关性
Table 4. Correlation between liver fat content and TMAO,TMA and choline
项目(n=118) 相关系数(r) P TMAO 0.250 0.043* TMA 0.182 0.143 胆碱 0.173 0.166 *P < 0.05。 表 5 2组受试者4种肠道菌群表达量比较 [M(P25,P75)]
Table 5. Comparison of the expression levels of intestinal microbiota in the two groups [M(P25,P75)]
肠道菌群 NAFLD组(n=86) 健康对照组(n=32) Z P 直肠真杆菌 3.24(1.64,10.60) 0.93(0.27,2.12) −4.240 <0.001* 乳酸杆菌 9.71(0.16,26.26) 1.06(0.46,5.18) −2.450 0.014* 多形拟杆菌 0.62(0.10,3.57) 2.80(0.35,11.08) −2.217 0.027* 双歧杆菌 0.05(0.004,0.30) 1.18(0.26,2.90) −5.453 <0.001* *P < 0.05。 表 6 TMAO水平与4种肠道菌群表达量相关性(n=118)
Table 6. Correlation between TMAO and the expression levels of intestinal microflora(n=118)
项目 相关系数(r) P 直肠真杆菌 0.280 0.004* 乳酸杆菌 0.163 0.097 多形拟杆菌 −0.161 0.101 双歧杆菌 −0.332 0.001* *P < 0.05。 表 7 饮食结构在2组间的差异
Table 7. Differences in dietary structure between the two groups
是否按时就餐 膳食搭配(荤/素) 每日饮水量(ml) 鸡蛋 牛奶 鱼类 红肉 动物内脏 水果 油腻油炸食物 甜食饮料 Z −0.473 −3.251 −0.136 −0.091 −0.226 −3.500 −0.882 −0.313 −0.898 −0.073 −0.482 P 0.636 0.001* 0.892 0.928 0.821 <0.001* 0.378 0.755 0.369 0.942 0.630 *P < 0.05,食物种类食用频率均为每周次数。 表 8 肝脏脂肪含量与饮食结构的相关性(n=118)
Table 8. Correlation between liver fat content and diet structure(n=118)
项目(n=118) 相关系数(r) P 膳食搭配(荤/素) 0.345 0.004* 鱼类(每周次数) −0.289 0.019* *P < 0.05。 -
[1] 张金俊,吕梦,陈浩,等. 我国成人非酒精性脂肪性肝病患病率的meta分析[J]. 职业与健康,2023,39(21):3000-3003. [2] Xiao S Y,Xie W H,Zhang Y H,et al. Changing epidemiology of cirrhosis from 2010 to 2019: Results from the Global Burden Disease study 2019[J]. Ann Med,2023,55(2):2252326. doi: 10.1080/07853890.2023.2252326 [3] Fang J,Yu C H,Li X J,et al. Gut dysbiosis in nonalcoholic fatty liver disease: Pathogenesis,diagnosis,and therapeutic implications[J]. Front Cell Infect Microbiol,2022,8(12):997018. [4] Nawrot M,Peschard S,Lestavel S,et al. Intestine-liver crosstalk in type 2 diabetes and non-alcoholic fatty liver disease[J]. Metabolism,2021,10(123):154844. [5] Wang Z,Klipfell E,Bennett B J. Gut flora metabolism of phosphatidylcholine promotes cardiovascular disease[J]. Nature,2011,472(7341):57-63. doi: 10.1038/nature09922 [6] Janeiro M H,Ramírez M J,Milagro F I,et al. Implication of Trimethylamine N-Oxide (TMAO) in disease: Potential biomarker or new therapeutic target[J]. Nutrients,2018,10(10):1398. doi: 10.3390/nu10101398 [7] Jalandra R,Dalal N,Yadav A K,et al. Emerging role of trimethylamine-N-oxide (TMAO) in colorectal cancer[J]. Appl Microbiol Biotechnol,2021,105(20):7651-7660. doi: 10.1007/s00253-021-11582-7 [8] Tang W H,Wang Z,Kennedy D J. Gut microbiota-dependent trimethylamine N-oxide (TMAO) pathway contributes to both development of renal insufficiency and mortality risk in chronic kidney disease[J]. Circ Res,2015,116(3):448-455. doi: 10.1161/CIRCRESAHA.116.305360 [9] Le ó n-Mimila P,Villamil-Ramírez H,Li X S,et al. Trimethylamine N-oxide levels are associated with NASH in obese subjects with type 2 diabetes[J]. Diabetes Metab,2021,47(2):101183. doi: 10.1016/j.diabet.2020.07.010 [10] 中华医学会肝脏病学分会脂肪肝和酒精性肝病学组. 非酒精性脂肪性肝病诊疗指南[J]. 中国肝脏病杂志(电子版),2010,2(4):43-48. doi: 10.3969/j.issn.1674-7380.2010.04.013 [11] Motamed N,Faraji A H,Khonsari M R,et al. Fatty liver index (FLI) and prediction of new cases of non-alcoholic fatty liver disease: A population-based study of northern Iran[J]. Clin Nutr,2020,39(2):468-474. doi: 10.1016/j.clnu.2019.02.024 [12] Xia M F,Lin H D,Yan H M,et al. The association of liver fat content and serum alanine aminotransferase with bone mineral density in middle-aged and elderly Chinese men and postmenopausal women[J]. J Transl Med,2016,13(14):11. [13] 薛平燕,江艳,徐玉善,等. 肠道菌群结构在非酒精性脂肪性肝病患者中的改变[J]. 昆明医科大学学报,2020,41(11):62-67. doi: 10.12259/j.issn.2095-610X.S20201120 [14] Eslam M,Sanyal A J,George J,et al. MAFLD: A consensus-driven proposed nomenclature for metabolic associated fatty liver disease[J]. Gastroenterology,2020,158(7):1999-2014. doi: 10.1053/j.gastro.2019.11.312 [15] Angelico F,Baratta F,Pastori D,et al. Statins and non-alcoholic fatty liver disease[J]. Liver Int,2019,39(9):1787. doi: 10.1111/liv.14134 [16] Polyzos S A,Kountouras J,Mantzoros C S. Obesity and nonalcoholic fatty liver disease: From pathophysiology to therapeutics[J]. Metabolism,2019,3(92):82-97. [17] Cusi K,Isaacs S,Barb D,et al. American association of clinical endocrinology clinical practice guideline for the diagnosis and management of nonalcoholic fatty liver disease in primary care and endocrinology clinical settings: Co-Sponsored by the American association for the study of liver diseases(AASLD)[J]. Endocr Pract,2022,28(5):528-562. doi: 10.1016/j.eprac.2022.03.010 [18] Hemmati M,Kashanipoor S,Mazaheri P,et al. Importance of gut microbiota metabolites in the development of cardiovascular diseases (CVD)[J]. Life Sci,2023,15(329):121947. [19] Saaoud F,Liu L,Xu K,et al. Aorta- and liver-generated TMAO enhances trained immunity for increased inflammation via ER stress/mitochondrial ROS/glycolysis pathways[J]. JCI Insight,2023,8(1):e158183. doi: 10.1172/jci.insight.158183 [20] Flores-Guerrero J L,Post A,Dijk P R,et al. Circulating trimethylamine-N-oxide is associated with all-cause mortality in subjects with nonalcoholic fatty liver disease[J]. Liver Int,2021,41(10):2371-2382. doi: 10.1111/liv.14963 [21] Chen Y M,Liu Y,Zhou R F,et al. Associations of gut-flora-dependent metabolite trimethylamine-N-oxide,betaine and choline with non-alcoholic fatty liver disease in adults[J]. Sci Rep,2016,8(6):19076. [22] Gao X,Liu X F,Xu J,et al. Dietary trimethylamine N-oxide exacerbates impaired glucose tolerance in mice fed a high fat diet[J]. J Biosci Bioeng,2014,118(4):476-481. doi: 10.1016/j.jbiosc.2014.03.001 [23] Yu D X,Shu X O,Xiang Y B,et al. Higher dietary choline intake is associated with lower risk of nonalcoholic fatty liver in normal-weight Chinese women[J]. J Nutr,2014,144(12):2034-2040. doi: 10.3945/jn.114.197533 [24] Ji Y,Yin Y,Sun L J,et al. The molecular and mechanistic insights based on gut-liver axis: Nutritional target for non-alcoholic fatty liver disease (NAFLD) Improvement[J]. Int J Mol Sci,2020,21(9):3066. doi: 10.3390/ijms21093066 [25] Muralitharan R R,Marques F Z. Diet-related gut microbial metabolites and sensing in hypertension[J]. J Hum Hypertens,2021,35(2):162-169. doi: 10.1038/s41371-020-0388-3 [26] Cho C E,Taesuwan S,Malysheva O V,et al. Trimethylamine-N-oxide (TMAO) response to animal source foods varies among healthy young men and is influenced by their gut microbiota composition: Arandomized controlled trial[J]. Mol Nutr Food Res,2017,61(1):1600324. doi: 10.1002/mnfr.201600324 -





 下载:
下载: