Association between Myeloperoxidase-463G/A Gene Polymorphism and Essential Hypertension in Yi Nationality
-
摘要:
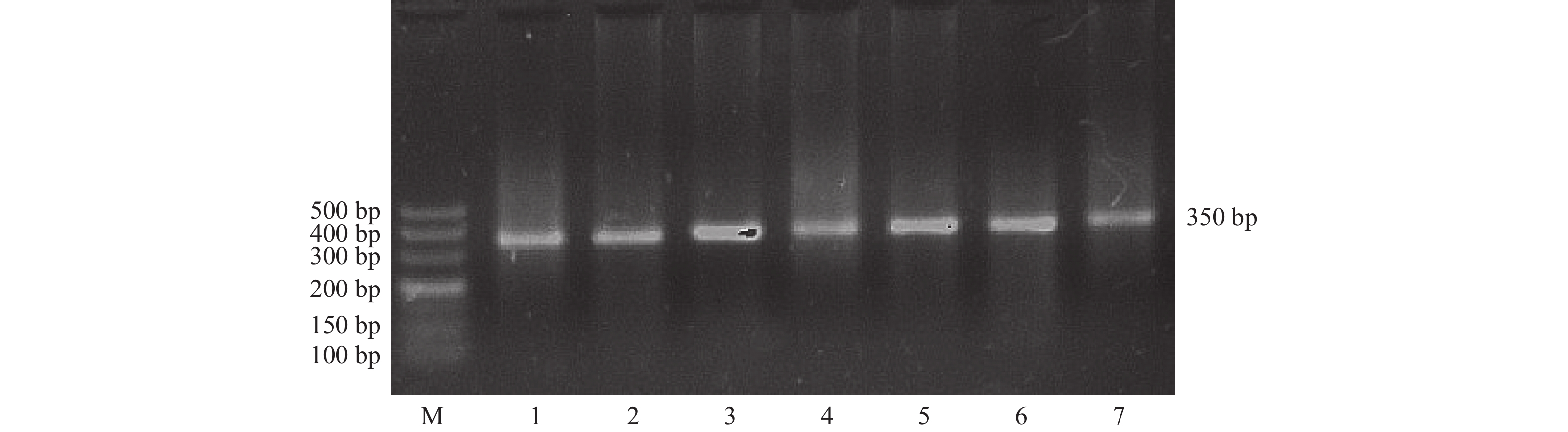
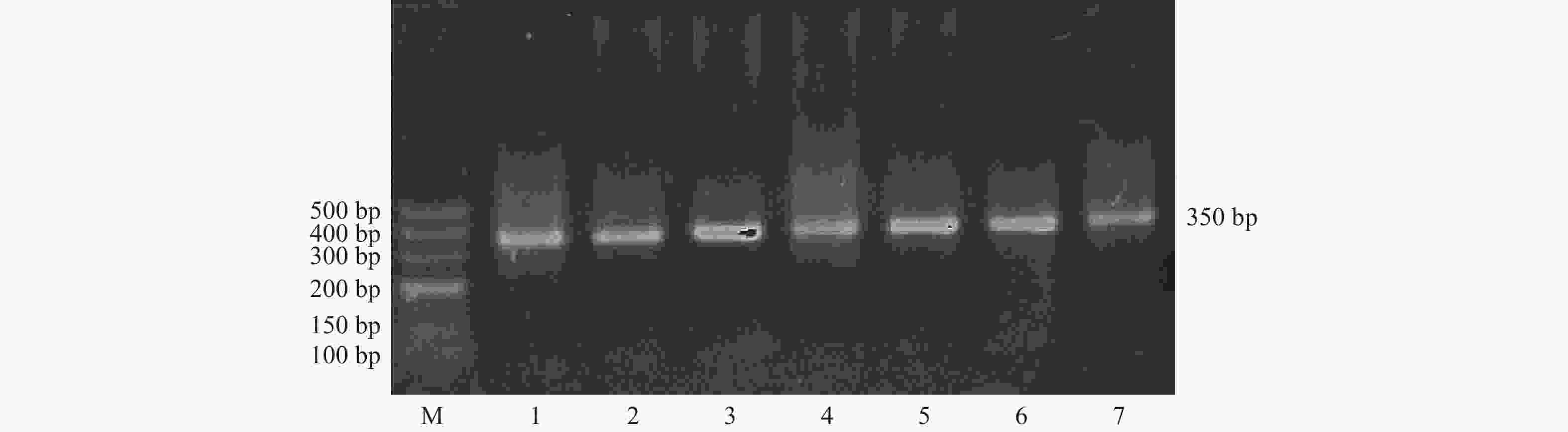
目的 研究髓过氧化物酶(MPO)-463G/A基因的多态性与云南彝族原发性高血压(EH)的相关性。 方法 应用聚合酶链反应-限制性片段长度多态性(PCR-RELP)技术,检测2007年1月至2008年11月由昆明医科大学第一附属医院采自云南省双河乡彝族高血压患者(EH组,n = 86)和彝族正常人(对照组,n = 100)的MPO-463G/A基因多态性,并计算GG、GA、AA基因型频率及G、A基因频率,再进行关联分析。 结果 在EH组和对照组中,MPO基因-463G/A 多态的基因型频率GG为66.28%、52.00%,GA+AA为33.72%、48.00%,等位基因G频率为79.65%、69.50%,等位基因A频率为20.35%、30.50%,2组基因型频率和基因频率分别相比,差异均具有统计学意义(P < 0.05)。彝族女性EH组和女性对照组中GG和GA+AA基因型频率分别为74.50%、49.30%和25.50%、50.70%,等位基因G和A的频率分别为85.50%、69.00%和14.50%、31.00%,2组基因型频率和基因频率分别相比,差异均具有统计学意义(P <0.05),EH组A基因频率明显低于对照组。彝族男性 EH 组和男性对照组的基因型频率和基因频率分别比较,差异均无统计学意义(P > 0.05)。 结论 MPO基因-463G/A 多态与云南彝族女性原发性高血压具有相关性,是彝族女性高血压的易感基因。该位点A基因的表达在彝族女性EH的发生过程中起保护性作用。 Abstract:Objective To study the correlation between the polymorphism of myeloperoxidase-463G/A gene and essential hypertension of Yi nationality in Yunnan Province. Methods The PCR-RFLP technique was used to detect the MPO-463G/A gene polymorphism in 86 Yi hypertensive patients and 100 normal Yi people in Shuanghe Township and Yunnan Province collected by the First Affiliated Hospital of Kunming Medical University from January 2007 to November 2008. The frequencies of the GG, GA, and AA genotypes and the G and A allele frequencies were calculated, followed by association analysis. Results The genotype frequencies of MPO gene-463G/A polymorphism in EH group and control group GG were 66.28%, 52.00%, GA+AA were 33.72%, 48.00%, respectively. The frequencies of allele G were 79.65% and 69.50%, and the frequencies of allele A were 20.35% and 30.50%, respectively. There were statistically significant differences in genotype frequency and gene frequency between the two groups(P < 0.05). The genotype frequencies of GG and GA+AA were 74.50% and 49.30% in female EH group and 25.50% and 50.70% in femal control group. The allele frequencies of G and A were 85.50% and 69.00% in EH group and 14.50% and 31.00% in control group. The differences were statistically significant(P < 0.05). The frequency of A gene in female EH group was significantly lower than that in female control group. There was no significant difference in genotype frequency and gene frequency between EH group and control group in Yi male(P > 0.05). Conclusion MPO gene-463G/A polymorphism is related to essential hypertension in Yunnan Yi women and is a susceptibility gene for hypertension in Yi women. The expression of the A allele at this locus has a protective effect during the development of EH in Yi women. -
Key words:
- Myeloperoxidase /
- Essential hypertension /
- The Yi nationality /
- Gene polymorphism
-
表 1 EH组和对照组一般临床资料比较($\bar x \pm s$)
Table 1. Comparison of the general clinical data between EH and control group ($\bar x \pm s$)
组别 n 年龄(岁) 男∶女(n) EH组 86 55.92 ± 13.58 31∶55 对照组 100 51.84 ± 15.04 29∶71 t/χ2 −1.928 1.051 P 0.055 0.305 表 2 云南省彝族人群中MPO基因−463G/A 位点的基因型及等位基因频率比较[n(%)]
Table 2. Comparison of genotype and allele frequency of MPO gene−463G/A locus in Yi people of Yunnan Province[n(%)]
组别 基因型 等位基因 n GG GA+AA n G A EH组 86 57(66.28) 29(33.72) 172 137(79.65) 35(20.35) 对照组 100 52(52.00) 48(48.00) 200 139(69.50) 61( 30.50) 总计 186 109(58.60) 77( 41.40) 372 276(74.19) 96(25.81) χ2 3.866 4.977 P 0.049* 0.026* *P < 0.05。 表 3 男、女性EH组与对照组基因型分布和等位基因比较[n(%)]
Table 3. Comparison of genotype distribution and alleles between male and female EH groups and control group[n(%)]
组别 基因型 等位基因 n GG GA+AA n G A 男性 EH组 31 16(51.60) 15(48.40) 62 43(69.40) 19(30.60) 对照组 29 17(58.60) 12(41.40) 58 41(70.70) 17(29.30) 总计 60 33(55.00) 27(45.00) 120 84(70.00) 36(30.00) χ2 0.297 0.025 P 0.586 0.873 女性 EH组 55 41(74.50) 14(25.50) 110 94(85.50) 16(14.50) 对照组 71 35(49.30) 36(50.70) 142 98(69.00) 44(31.00) 总计 126 76(60.32) 50(39.68) 252 192(76.19) 60(23.81) χ2 8.255 9.235 P 0.004* 0.002* *P < 0.05。 -
[1] Wang J,Zhang L,Wang F,et al. Prevalence,awareness,treatment,and control of hypertension in China: Results from a national survey[J]. Am J Hypertens,2014,27(11):1355-1361. doi: 10.1093/ajh/hpu053 [2] Wang Z,Chen Z,Zhang L,et al. Status of hypertension in China: Results from the China hypertension survey,2012-2015[J]. Circulation,2018,137(22):2344-2356. doi: 10.1161/CIRCULATIONAHA.117.032380 [3] 李欢,冯磊,方绕红,等. 髓过氧化物酶在临床心血管疾病中的意义和研究展望[J]. 心血管病防治知识,2022,12(3):90-94. [4] 孙恕,易松. 2023年《中国高血压防治指南》更新临床实践[J]. 心电与循环,2023,42(3):203-206,212. [5] 彭红瑜,范志祥,张延洁,等. CYP11B2基因-344C/T位点多态性在云南彝族人群中的分布[J]. 医学研究杂志,2021,50(5):121-124. [6] 莫艳萍,张彦,张红星,等. ACE基因多态性与云南彝族原发性高血压的相关性研究[J]. 昆明医学院学报,2009,30(9):67-72. [7] London S J,Lehman T A,Taylor J A. Myeloperoxidase genetic polymorphism and lung cancer[J]. Cancer Research,1997,57:5001-5003. [8] 潘世扬, 陈进步. Assessment of hepatocyte injury for hepatitis B patient by quantitative analysis of plasma DNA[C]. //第5届全国检验与临床学术会议暨国际检验与临床高峰论坛论文集, 2010, 188. [9] 毕玉华,鞠卫萍,迟晓妮,等. 髓过氧化物酶与动脉粥样硬化的关系及在脑卒中应用的研究进展[J]. 检验医学与临床,2020,17(14):2096-2100. [10] 王英,陈会霞. 髓过氧化物酶在心血管疾病诊断中的意义[J]. 中华临床实验室管理电子杂志,2019,7(3):165-168. [11] 席可,吴嘉,汪俊军. 髓过氧化物酶在慢性肾病患者中的研究进展[J]. 国际检验医学杂志,2018,39(24):3086-3089. [12] 赵倩,陈还珍. 髓过氧化物酶在心血管疾病中作用的研究进展[J]. 中西医结合心脑血管病杂志,2022,20(6):1021-1024. [13] 唐桦,诸国华,孙希鹏,等. 髓过氧化物酶在高血压发病机制中作用的研究进展[J]. 中国心血管杂志,2019,24(5):481-483. [14] 陈楦,陈宋明. 高血压病的免疫机制研究进展[J]. 汕头大学学报(自然科学版),2021,36(1):69-75. [15] 潘力行. 高血压病与炎症反应相关性的研究[J]. 中国医学创新,2014,11(7):43-45. [16] 张竞之,贾会欣,张汛,等. 高血压病与血管内皮细胞损伤的相关性研究进展[J]. 华中医学杂志,2008,32(5):377-378. [17] Kisic B,Miric D,Zoric L,et al. Xanthine oxidase activity in patients with age-related cataract associated with hypertension[J]. Braz J Med Biol Res,2018,51(5):e6129. doi: 10.1590/1414-431x20176129 [18] 周白丽,苏晓灵,刘彦民,等. 不同海拔地区高血压病患者血清髓过氧化物酶、脑利钠肽含量变化[J]. 高原医学杂志,2011,21(1):11-13. [19] 方金瑞,张支明,马丽雅,等. 髓过氧化物酶基因多态性与原发性高血压遗传易感性的研究[J]. 临床心血管病杂志,2009,25(3):202-204. [20] 马慧元,马丽雅,方金瑞,等. 髓过氧化物酶-463G/A基因多态性与原发性高血压相关性研究[J]. 中国现代医学杂志,2010,20(23):3580-3582,3587. [21] Bushueva O,Solodilova M,Ivanov V,et al. Gender-specific protective effect of the-463G>A polymorphism of myeloperoxidase gene against the risk of essential hypertension in Russians[J]. J Am Soc Hypertens,2015,9(11):902-906. doi: 10.1016/j.jash.2015.08.006 -





 下载:
下载: