Orthogonal Experiment for Optimization of Ultrasonic Extraction Process of Six Components from Geranium wilfordii Maxim
-
摘要:
目的 采用L9(34)正交实验优化老鹳草中老鹳草素、没食子酸、柯里拉京、金丝桃苷、鞣花酸、原儿茶酸6种成分的超声提取方法。 方法 在单因素实验基础上,选取甲醇体积分数、超声提取时间、料液比3个主要因素进行L9(34)正交实验,研究各因素相互作用对老鹳草中6种成分提取率的影响。 结果 老鹳草中6种成分的超声法最佳提取工艺为:甲醇溶液体积分数:60%,料液比:1.0 g/10 mL,超声波提取时间:40 min。 结论 此方法操作简便,重复性高,准确度好,可用于老鹳草中老鹳草素、没食子酸、柯里拉京、金丝桃苷、鞣花酸、原儿茶酸6种成分的同时提取。 Abstract:Objective T o optimize the ultrasonic extraction method for Geraniin, Gallic acid, Corilagin, Hyperoside, Ellagic acid, Protocatechuic acid from Geranium wilfordii Maxim by L9(34) orthogonal experiment. Methods On the basis of single factor experiments, using L9(34) orthogonal experiment, three main factors, methanol volume fraction, extraction time, solid-liquid ratio are chosen for three main component to study the effect of the interaction of various factors on the extraction rate of six components fromGeranium wilfordiiMaxim. Results The results show that the optimum extraction process are as follow: the methanol volume fraction was 60%, the solid-liquid ratio was 1∶10(g∶ml), the extraction time was 40 min. Conclusion This method is simple, repeatability and accuracy. It can be to extract Geraniin, Gallic acid, Corilagin, Hyperoside, Ellagic acid, Protocatechuic acidfrom Geranium wilfordii Maxim. -
Key words:
- Geranium wilfordii Maxim /
- Ultrasonic Extraction /
- Orthogonal Experiment /
- HPLC
-
肺癌是威胁人类健康最常见的恶性肿瘤之一,2022年全球新发肺癌人数和死亡人数高达250万例和180万例,中国新发肺癌106.06万例、死亡73.33万例,均居所有肿瘤第一位[1]。衰弱是一组由于机体的生理储备下降或多系统失调,导致机体易损性增加、抗应激能力减弱的综合征,可增加个体不良结局的风险[2−3]。肿瘤患者由于其疾病本身、心理以及治疗方式都可能是挑战患者生理储备的重要压力源,均可增加其衰弱的发生。肺癌患者症状困扰(37.7%~99.2%)和心理障碍(97.98%)发生率高且较严重[4−5],加之抗肿瘤治疗相关副反应的困扰,是衰弱的高发人群,相关研究显示肺癌患者衰弱发生高达28%~61%(平均发生率为45%)[6],是导致患者不良症状反应、治疗严重并发症及病死率上升,加重患者经济负担,降低生活质量的重要原因[7]。放射治疗是肺癌患者的主要治疗手段之一。目前国内外学者已将衰弱应用到肺癌放疗患者治疗相关并发症及康复结局的预测中,并成为肺癌放疗患者康复结局的重要预测因子[8−9],但目前肺癌衰弱现状及其影响因素的探讨多集中在手术、化疗患者,关于肺癌患者衰弱发生率与放射治疗的相关性还存在争议[10−12],缺乏客观、综合的衰弱评估,更缺乏对肺癌放疗患者衰弱发生现状及影响因素的研究。因此,本研究旨在运用主观和客观相结合的方式,调查肺癌放疗患者衰弱的发生现状,并分析其影响因素,以期为开展肺癌放疗患者衰弱管理提供参考依据。
1. 资料与方法
1.1 研究对象
本研究为横断面调查研究,采用便利抽样调查2023年1月至12月在云南省某三级甲等肿瘤专科医院放疗肺癌患者。纳入标准:(1)病理学或细胞学诊断为肺癌需接受放射治疗患者[13];(2)年龄>18岁,自愿签署知情同意书;(3)意识清楚,无认知障碍,能正常交流沟通;(4)正在接受放疗且总放疗次数 ≥ 20次。排除标准:(1)肺癌术后时间 < 3个月,放疗期间合并化疗的患者;(2)患有其他严重躯体、精神疾病者;(3)严重心、肝、肾功能衰竭及骨髓造血功能不全者。根据Kendall样本量估计方法,可取自变量个数的5~10倍[14],本研究共涉及变量25个,估计需要样本量为125~250例,共收集241例患者,满足样本量需求。本研究获云南省肿瘤医院伦理委员会批准(SLKYLX2023-031)。
1.2 研究工具
1.2.1 一般资料
调查问卷包括肺癌放疗患者年龄、性别、职业、肺癌细胞分型类型、放疗次数、合并症、血红蛋白计数、白蛋白计数等。
1.2.2 衰弱表型量表
Fried等[15]于2001年编制,多用于住院患者的衰弱测量,内容包括5项指标,不明原因体质量减轻、握力低下、体力活动减少、行走速度降、自述疲乏,总分为5分,0分为无衰弱,1~2分为衰弱前期,3分为衰弱期,本研究中将衰弱前期和无衰弱状态统称为非衰弱状态。
1.2.3 安德森症状评估量表
该量表由美国Texas大学和Anderson癌症中心编制[16],包含症状严重度和症状困扰度两部分,共13个条目,评估过去24 h癌症患者出现的伴随症状和症状困扰度。中文版安德森症状测评量表内部一致性信度在0.82~0.94之问,该量表广泛适用于不同类型和治疗的癌症患者[17]。
1.2.4 医院焦虑抑郁量表
该量表包含有焦虑和抑郁两个亚量表,各7个条目,共14个条目组成,两个量表的Cronbach's α系数分别为0.806与0.791[18]。
1.2.5 营养风险筛查2002
用于评估研究对象是否存在营养不良风险,评估内容包括:疾病严重程度评分、营养受损评分、年龄评分[19]。
1.2.6 Barthel指数
用于评估研究对象的日常活动能力,共10个条目,根据患者完成每项内容需协助的程度计分,总分100分[20]。
1.3 数据收集
由经过统一培训的调查员在放射治疗科病房招募符合纳入、排除标准的肺癌放疗患者,向患者介绍研究内容、目的,同意后签署知情同意书,现场发放纸质版问卷填写,无法自行填写者,由调查者采用问答形式协助填写。
1.4 统计学处理
采用SPSS23.0软件进行数据录入与分析。符合正态分布的计量资料采用均数±标准差($\bar x \pm s $)表示,不符合正态分布计量资料采用中位数(四分位数)M(P25,P75)表示,用Wilcoxon秩和检验;计数资料以百分数(n)%表示,组间比较采用χ2检验,等级资料采用非参数检验;采用二元Logistic探讨影响因素,以P < 0.05表示差异有统计学意义。
2. 结果
2.1 人口学资料
本研究共纳入241名肺癌放疗患者,其中男性187例(77.59%),女性54例(22.41%),平均年龄(58.95±9.16)岁,年龄范围(29~85)岁;鳞癌59例(24.48%),腺癌112例(46.47%),大细胞肺癌17例(7.05%),小细胞肺癌53例(21.99%);II期23例(9.54%),III期138例(57.26%),IV期80例(33.20%);局部转移159例(65.98%),远处转移82例(34.02%)。
2.2 肺癌放疗患者衰弱表型量表、医院焦虑抑郁量表、安德森症状评估量表评分情况
肺癌放疗患者衰弱评分,焦虑评分、抑郁评分、安德森症状评估量表评分见表1。
表 1 肺癌放疗患者衰弱表型、焦虑、抑郁、安德森症状评估量表得分[M(P25,P75),分]Table 1. Scores of frailty phenotype,anxiety,depression,and Anderson symptom assessment scale for lung cancer patients undergoing radiotherapy[M(P25,P75),points]变量 得分 衰弱表型量表评分 3.00(1.00,4.00) 医院焦虑抑郁量表 焦虑 8.00(5.00,11.00) 抑郁 7.00(3.50,10.00) 安德森症状评估量表评分 50.18(17.00,74.50) 2.3 不同社会人口特征肺癌放疗患者衰弱状况的单因素分析
年龄、放疗次数、疾病分期、转移情况、是否口服多种药物、白细胞计数、血红蛋白计数、营养风险评分等因素在肺癌放疗患者衰弱中差异具有统计学意义(P < 0.05),见表2。
表 2 不同社会人口特征肺癌放疗患者衰弱状况的单因素分析[n(%)](1)Table 2. Univariate analysis of frailty status in lung cancer radiotherapy patients with different sociodemographic characteristics[n(%)](1)项目 衰弱组 非衰弱组 χ2 P 年龄(岁) 19.527 < 0.001* < 60 57(42.86) 77(71.30) ≥ 60 76(57.14) 31(28.70) 性别 男 105(78.95) 82(75.93) 0.313 0.576 女 28(21.05) 26(24.07) 文化程度 小学及以下 50(37.59) 42(38.89) 1.401 0.705 初中 41(30.83) 37(34.26) 高中或中专 26(19.55) 15(14.89) 大专及以上 16(12.03) 14(12.96) 婚姻状况 已婚 115(86.47) 99(91.67) 1.620 0.203 其他 18(13.53) 9(8.33) 职业 农民 74(55.64) 69(63.89) 4.873 0.181 工人 11(8.27) 12(11.11) 职员 10(7.52) 9(8.33) 无业或退休 38(28.57) 18(16.67) 居住情况 3.861 0.145 与配偶同住 100(75.19) 86(79.63) 与子女同住 28(21.05) 14(12.96) 独居或养老院 5(3.76) 8(7.41) 家庭人均月收入(元) ≤ 2000 56(42.11) 56(51.85) 5.311 0.150 2001 ~4000 35(26.32) 28(25.93) 4001 ~6000 24(18.05) 9(8.33) > 6000 18(13.53) 15(13.89) 医疗费用支付方式 1.905 0.168 职工医保 52(39.10) 33(30.56) 居民医保 81(60.90) 75(69.44) 病程(月) 5.311 0.150 ≤ 6 13(9.77) 22(20.37) 7~12 43(32.33) 36(33.33) 13~24 40(30.08) 30(27.78) > 24 37(27.82) 20(18.52) 肺癌细胞分型 1.781 0.633 腺癌 31(23.31) 28(25.93) 鳞癌 61(45.86) 51(47.22) 大细胞肺癌 8(6.02) 9(8.33) 小细胞肺癌 33(24.81) 20(18.52) 临床分期 12.592 0.002* II期 10(7.52) 13(12.04) III期 66(49.62) 72(66.67) IV期 57(42.86) 23(21.30) *P < 0.05。 表 2 不同社会人口特征肺癌放疗患者衰弱状况的单因素分析[n(%)](2)Table 2. Univariate analysis of frailty status in lung cancer radiotherapy patients with different sociodemographic characteristics[n(%)](2)项目 衰弱组 非衰弱组 χ2 P 转移情况 14.125 < 0.001* 局部转移 74(55.64) 85(78.70) 远处转移 59(44.36) 23(21.30) 曾接受何种治疗 手术 11(8.27) 10(9.26) 0.451 0.930 化疗 88(66.17) 69(63.30) 手术+化疗 20(15.04) 19(17.59) 其他治疗 14(10.53) 10(9.26) 是否口服多种药物 22.897 < 0.001* 无口服药物 82(61.65) 96(88.89) 口服一种及以上药物 51(38.35) 12(11.11) 是否存在多种慢性疾病 0.909 0.363 无合并症 106(79.70) 91(84.26) 存在一种及以上合并症 27(20.30) 17(15.74) 血小板计数(109/L) 0.876 0.349 < 100 16(12.03) 9(8.33) ≥ 100 117(87.97) 99(91.67) 白细胞计数(109/L) 4,329 0.037* < 4 43(32.33) 22(20.37) ≥ 4 90(67.67) 86(79.63) 白蛋白计数(g/L) 3.195 0.074 < 35 26(19.55) 12(11.11) ≥ 35 107(80.45) 96(88.89) 血红蛋白计数(g/L) 16.856 < 0.001* < 120 65(48.87) 25(23.15) ≥ 120 68(51.13) 83(76.85) 营养风险评分(分) 43.268 < 0.001* < 3 47(35.34) 84(77.78) ≥ 3 86(64.66) 24(22.22) 放疗次数(次) 62.879 < 0.001* ≤ 10 36(27.07) 84(77.78) 11~20 46(34.59) 16(14.81) > 20 51(38.35) 8(7.41) Barthel指数(分) 135.235 < 0.001* 100(无需依赖) 23(17.29) 93(86.11) 61~99(轻度依赖) 110(82.71) 15(13.89) *P < 0.05。 2.4 不同医院焦虑抑郁量表、安德森症状评估量表评分肺癌放疗患者衰弱状况的单因素分析
衰弱组焦虑、抑郁、安德森症状评估量表评分均高于非衰弱组,焦虑、抑郁量、安德森症状评估量评分是肺癌放疗患者衰弱发生的影响因素,差异具有统计学意义(P < 0.001),见表3。
表 3 不同医院焦虑抑郁量表、安德森症状评估量表评分肺癌放疗患者衰弱状况的单因素分析[M(P25,P75)]Table 3. Univariate analysis of frailty status in lung cancer radiotherapy patients using anxiety and depression scales and Anderson symptom assessment scales from different hospitals[M(P25,P75)]变量 得分 Z P 衰弱组(n = 133) 非衰弱组(n = 108) 焦虑量表评分 9.00(5.00,11.00) 7.00(4.00,9.00) −4.349 < 0.001* 抑郁量表评分 9.00(5.00,11.00) 4.00(3.00,8.00) −6.567 < 0.001* 安德森症状评估量表评分 72.93(47.00,98.00) 23.08(7.00,35.00) −10.58 < 0.001* *P < 0.05。 2.5 肺癌放疗患者衰弱的多因素分析
以是否发生衰弱为因变量(否 = 0,是 = 1),将单因素分析中差异具有统计学意义的项目作为自变量进行Logistic回归分析,变量进入方程水准为0.05,剔除水准为0.10。结果显示,年龄( < 60岁 = 0, ≥ 60 = 1)、放疗次数(≤ 10次 = 0,10~20次 = 1,> 20次 = 2)、血红蛋白计数( < 120 = 0, ≥ 120 = 1)、Barthel指数评分(100分无依赖 = 0,61~99分有依赖 = 1)、安德森症状评估量量表、焦虑评分是肺癌放疗患者衰弱发生的影响因素,见表4。
表 4 肺癌放疗患者衰弱发生多因素分析Table 4. Multivariate analysis of frailty in lung cancer patients undergoing radiotherapy自变量 β SE Waldχ P OR 95%CI 常量 −3.455 1.340 6.609 0.010* 年龄(对照组: < 60岁) 2.291 0.664 11.892 0.001* 9.883 2.688~36.334 放疗次数(对照组:≤10次) 11~20 次 1.656 0.683 5.873 0.015* 5.240 1.373~20.001 >20次 3.095 0.829 13.931 < 0.001* 22.098 4.349~89.634 血红蛋白(对照组: < 120 g/L) −1.723 0.628 7.518 0.006* 0.178 0.052~0.612 安德森症状评估量表评分 0.072 0.015 21.806 < 0.001* 1.074 1.043~1.107 焦虑评分 −0.393 0.141 7.742 0.005* 0.675 0.512~0.890 Barthel指数评分(对照组:100分无依赖) 3.142 0.679 21.398 < 0.001* 23.151 6.115~87.647 *P < 0.05。 3. 讨论
3.1 肺癌放疗患者衰弱现状
研究结果显示肺癌放疗患者衰弱发生率为55.19%,与意大利的一项系统评价[6]研究结果相近(肺癌患者衰弱发生率28%~61%,总发生率45%),但明显高于美国学者Raghavan等[9]的一项回顾性研究结果(衰弱发生率35%),原因可能是其研究中选取的140例接受SBRT治疗的非小细胞肺癌患者均为早期,而本研究中研究对象III期、IV期患者占(90.46%),III期、IV期患者由于癌细胞对机体重要器官的损伤以及预后差等原因,患者面临更严重的症状及心理困扰,更容易发生衰弱[21];此外,云南省是中国乃至全世界肺癌高发区域,加之肺癌发病隐匿和云南省属于中国西南边境少数民族聚居地区,超过50%的患者确诊时已处于晚期,患者面临的疾病和症状负担更严重[22],导致患者衰弱发生率更高。同时两项研究中患者的治疗方式也存在较大差别,SBRT相较于传统调强放疗,放疗次数更少副反应更低[23]。英国学者Imam等[24]已证实通过实施医院衰弱风险评分分级可预测患者住院时间、再入院率、死亡率和某些特定条件治疗并发症的关系,可为实施衰弱干预提供信息决策。提示临床医护人员应早期识别患者衰弱现状、评估其严重程度,并根据评估结果制定精准化、个性化的衰弱管理策略,帮助患者延缓或逆转衰弱发生,进一步提高患者生活质量。
3.2 肺癌放疗患者衰弱的影响因素
3.2.1 年龄因素
Logistic回归分析结果显示与60岁以下的肺癌放疗患者相比,60岁及以上肺癌放疗患者发生衰弱的风险更高(OR:9.883;95%CI:2.688~36.334,P = 0.001),年龄 ≥ 60岁的肺癌放疗患者衰弱发生风险是年龄 < 60岁患者的9.883倍。中国大陆学者Hou等[25]在1项横断面研究中结果表明年龄是肺癌患者衰弱的独立预测因子,与本研究结果一致。其原因可能随着年龄增长机体各项机能指标逐渐下降,如基础代谢率下降、钙质流失、肌肉力量下降等导致患者生理功能下降有关;此外运动能力也会影响患者衰弱的发生[26],随着年龄增长机体各项机能指标逐渐下降,人体的运动能力跟运动量也在逐步下降,而本研究在调查过程中也发现大多数 ≥ 60岁的患者都表示“自己有高血压糖尿病,自从罹患肺癌后明显感觉呼吸不够用也不运动了”“自从患病后自己也不知道能做什么运动?”,患者的运动量较生病前明显下降。因此,提示临床医护人员在肺癌放疗患者衰弱管理过程中既要重视高龄患者衰弱的早发现、早诊断,也要根据患者的实际情况制定针对性功能锻炼,是帮助患者预防和缓解衰弱的有效手段。
3.2.2 放疗次数
Logistic回归分析结果显示与放疗次数 ≤ 10次相比,10次 > 放疗次数 ≤ 20、放疗次数 > 20次的肺癌放疗患者衰弱发生风险更高(OR:5.240;95%CI:1.373~20.001,P = 0.015;OR:22.098;95%CI:4.349~89.634,P = 0.015),10次 > 放疗次数 ≤ 20、放疗次数 > 20次的衰弱发生风险是放疗次数 ≤ 10的5.240倍和22.09倍。目前关于肺癌患者衰弱发生率与放射治疗次数累积的相关性还存在争议[10−12],本研究结果表明随着放疗次数增加患者衰弱风险不断上升。放射治疗作为肺癌患者主要治疗手段之一,在放疗过程中受肿瘤解剖位置的限制,其照射野区除肿瘤组织外还涉及人体的正常组织器官,在治疗肿瘤的同时也会产生放射治疗相关副反应,根据副反应发生时间分为早期效应和晚期效应,早期效应可在放疗7~10次出现,且随放疗次数增加而累积[27]。疲乏、放射性皮肤损伤、骨髓抑制等是患者常见的放疗早期效应[28−29],而疲乏是衰弱的重要评价指标,本研究中患者疲乏204例发生率(84.65%),研究结果符合患者放疗期间早期效应发生规律,结果具有可靠性。因此,医护人员应加强对多次、高剂量照射肺癌患者衰弱的评估,及时减轻患者放疗相关副反应症状困扰,减轻衰弱发生。
3.2.3 血红蛋白计数
Logistic回归分析结果显示与血红蛋白 < 120 g/L的肺癌放疗患者相比,血红蛋白 ≥ 120 g/L的肺癌放疗患者发生衰弱风险更低(OR:0.178;95%CI: 0.052~0.612, P = 0.004)。血红蛋白 ≥ 120 g/L的肺癌放疗患者衰弱发生风险是血红蛋白 < 120 g/L的肺癌放疗患者的0.178倍,中国大陆学者Ruan等[30]研究中表明贫血和低血红蛋白浓度与衰弱显著相关,与本研究结果一致。骨髓抑制作为肺癌放疗患者常见的放疗副反应,由放射性导致损伤骨髓的造血功能,使血液中的红细胞数量减少或寿命缩短,促红细胞生长素减少[31],头晕、乏力、注意力不集中等是患者的常见症状,而这些症状都是患者衰弱的重要表现。本研究血红蛋白计数 < 120 g/L患者占(37.34%),提示临床医护人员需动态监测患者的血象变化,及早发现可引起患者衰弱的敏感指标。
3.2.4 安德森症状评估量表评分、焦虑评分
Logistic回归分析安德森症状评估量表、焦虑量表评分越高肺癌放疗患者发生衰弱风险越高(OR:1.074;95%CI:1.043~1.107,P < 0.001;OR:0.675;95%CI:0.512~0.890,P = 0.005),Chen等[7]研究结果表明安德森症状评估量表得分是肺癌患者衰弱的危险因素,与本研究结果一致。肺癌患者症状困扰和发生率高且严重,疼痛、呼吸困难、咳嗽、疲乏、焦虑等是患者的常见症状[4],这些不良症状反应及其导致的一般活动能力下降引起患者发生衰弱[32]。本研究中III、IV期患者占(90.46%),患者症状困扰发生率和严重程度更高,同时放射治疗在肿瘤治疗过程中,也会产生放射治疗相关副反应,如放射治疗皮肤损伤、疲乏、放射性食管炎等[28−29],相关症状严重程度可随放疗次数增加而累积。相关研究显示多学科合作下的症状管理是缓解患者衰弱的有效手段[33],提示临床医护人员对于肺癌放疗患者要动态监测患者的症状和心理状态变化轨迹,帮助患者减轻症状困扰和紧张焦虑,早期识别、早期干预高危因素。
3.2.5 Barthel指数
Logistic回归分析结果显示与Barthel指数为100分无依赖的肺癌放疗患者相比,Barthel < 100分有依赖(OR:23.151;95%CI:6.115~87.647, P < 0.001)患者发生衰弱风险更高,Barthel < 100分有依赖的肺癌放疗患者衰弱发生风险是Barthel指数为100分无依赖的肺癌放疗患者的23.15倍。中国大陆学者Wan等[34]证实Barthel指数与患者患衰弱成负相关,与本研究结果一致。Barthel指数评估内容包括患者进食、洗澡、修饰、穿衣、转移、步行、上楼梯和洗澡等,可直观反应患者衰弱的严重程度。晚期肺癌患者由于疾病本身的症状困扰和治疗所致的相关副反应,患者日常生活能力受损严重,Barthel指数评分较低,导致衰弱更为严重。美国学者Gill等[35]研究发现通过改善居家患者身体能力的潜在障碍,可以减缓患者身体功能衰弱进展。临床医护人员应与康复医师紧密合作,根据患者Barthel指数评分有目的、有计划地为患者制定功能康复方案帮助患者缓解或延缓衰弱的发生。
研究结果显示肺癌放疗患者衰弱发生率为55.19%,年龄、放疗次数、血红蛋白计数、Barthel指数、安德森症状评估量表评分、焦虑评分是肺癌放疗患者衰弱的影响因素。因此,在肺癌放疗患者治疗过程中应重视衰弱的评估及管理,早期识别患者衰弱状态和衰弱的高危因素,以多学科合作、循证为基础有目的、有计划地为患者制定干预措施,预防或控制患者衰弱状况,减轻患者治疗相关并发症和再次入院,进一步提高患者生活质量。近年来,随着国家“优势医疗资源扩容下沉”等政策实施,2023年云南省各地州已成立10余家“肿瘤放射治疗科”,本研究结果对帮助云南省肿瘤放射治疗科临床护士提高肺癌放疗衰弱管理意识具有重要意义。但本研究仅选取云南省一家医院肺癌放疗患者调查,样本量较小,限制研究结果的普及性,今后需开展多中心大样本的纵向研究,深入探讨肺癌放疗患者衰弱的发展轨迹及人群异质性。
-
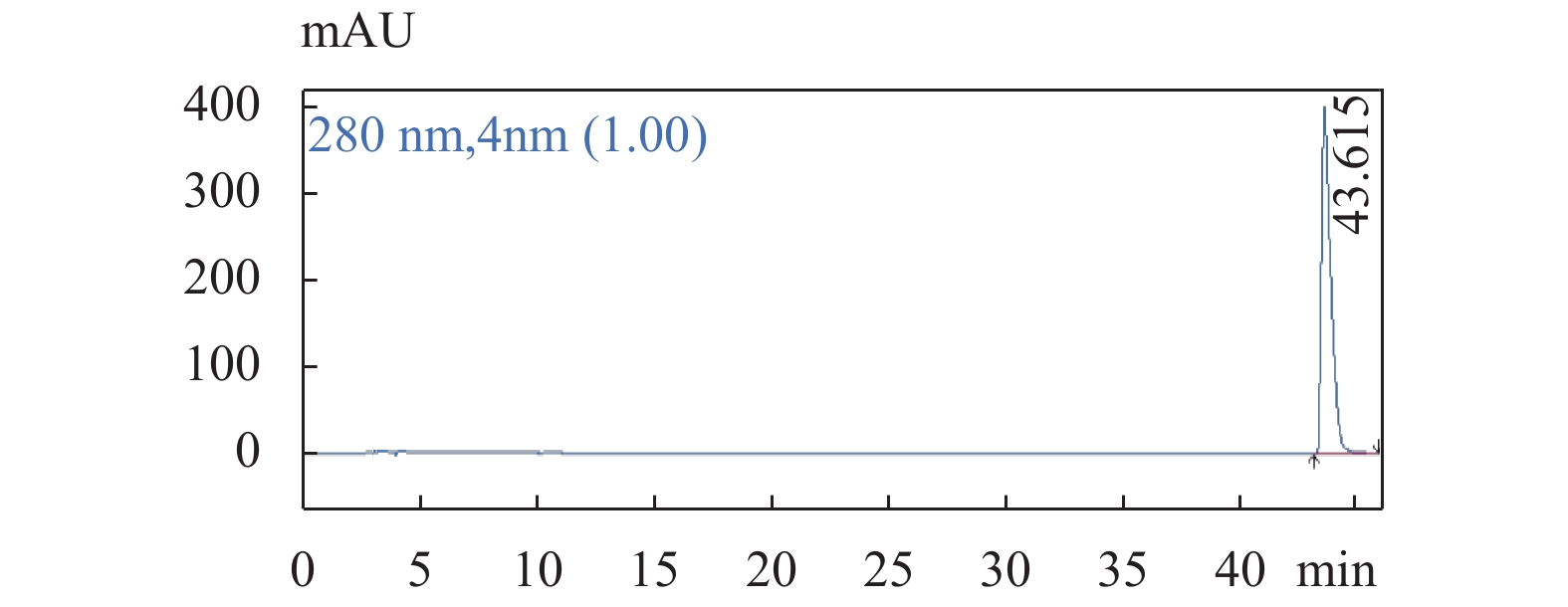
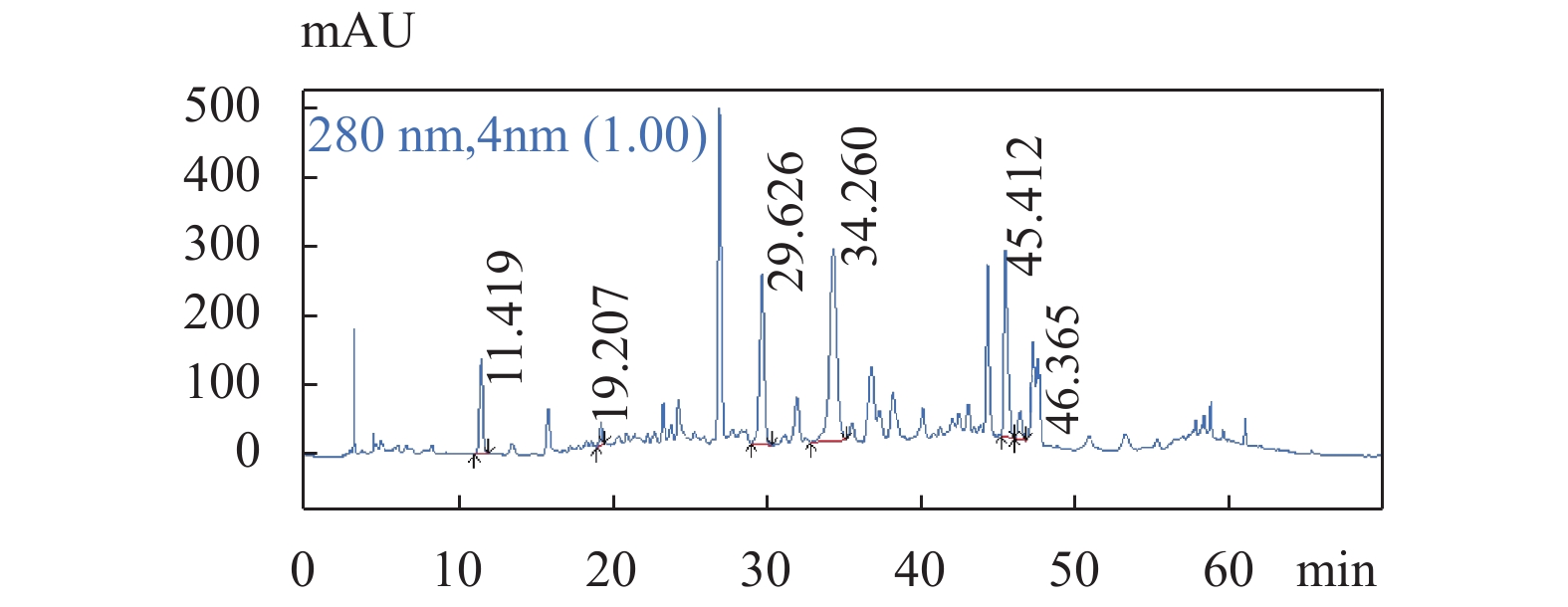
图 1 供试品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 1. The chromatogram of Geranium wilfordii Maxim
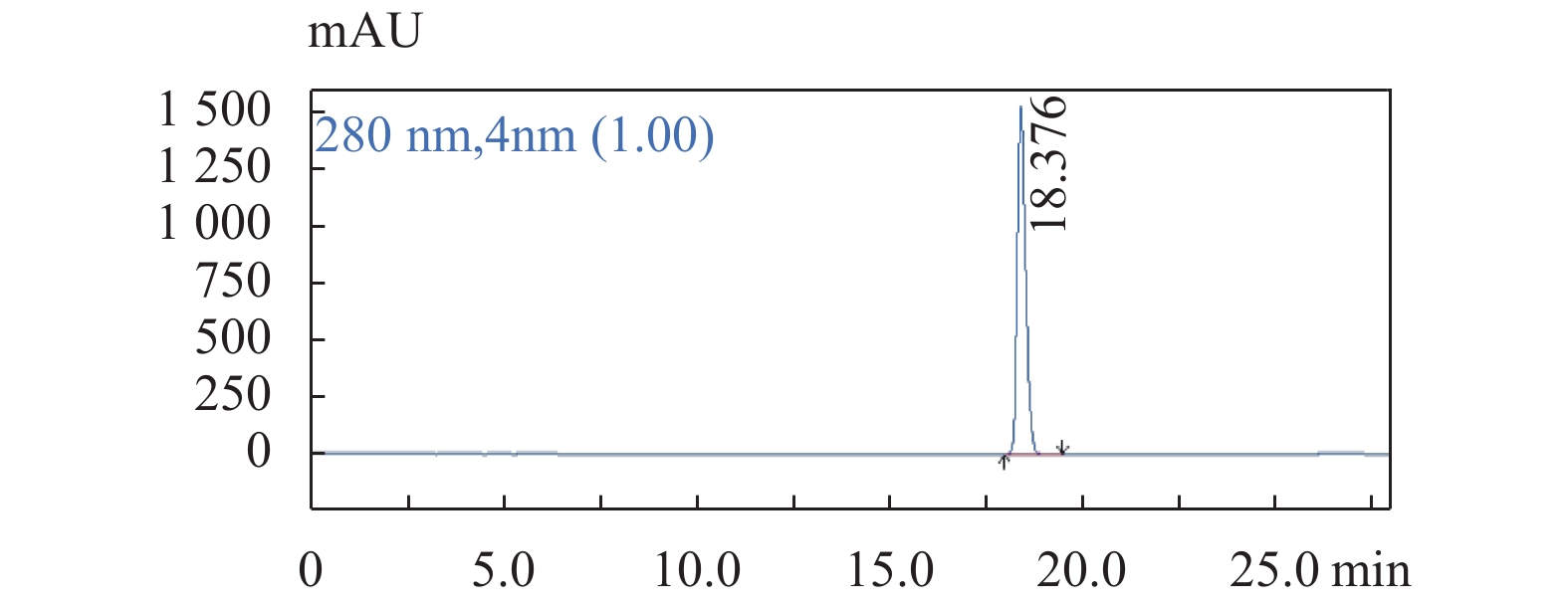
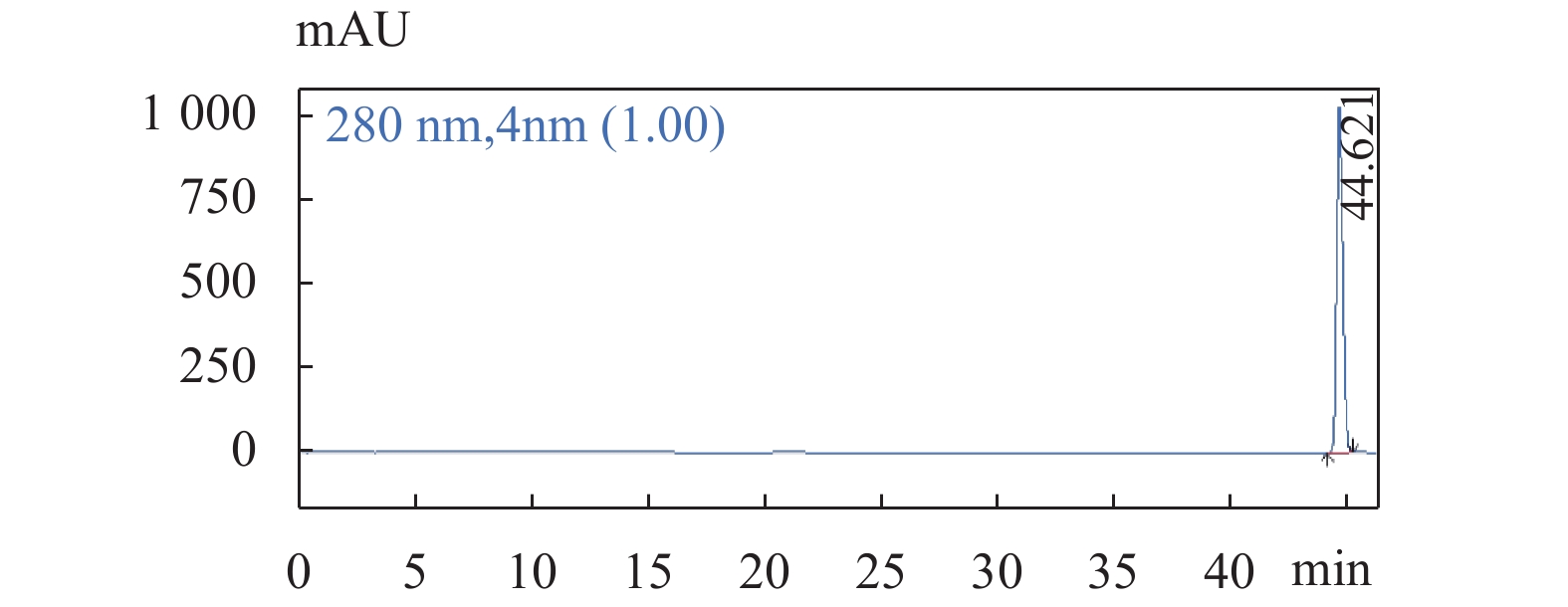
图 2 鞣花酸对照品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 2. The chromatogram of Ellagic acid
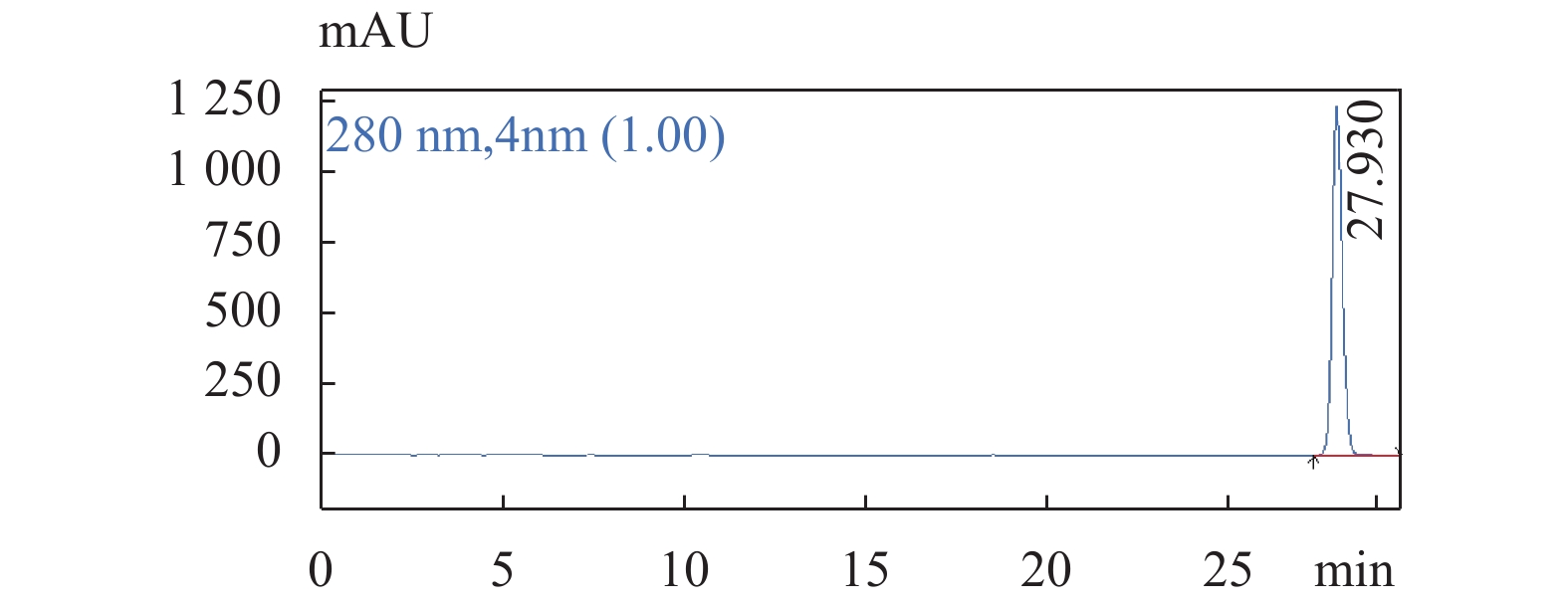
图 3 原儿茶酸对照品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 3. The chromatogram of Protocatechuic acid
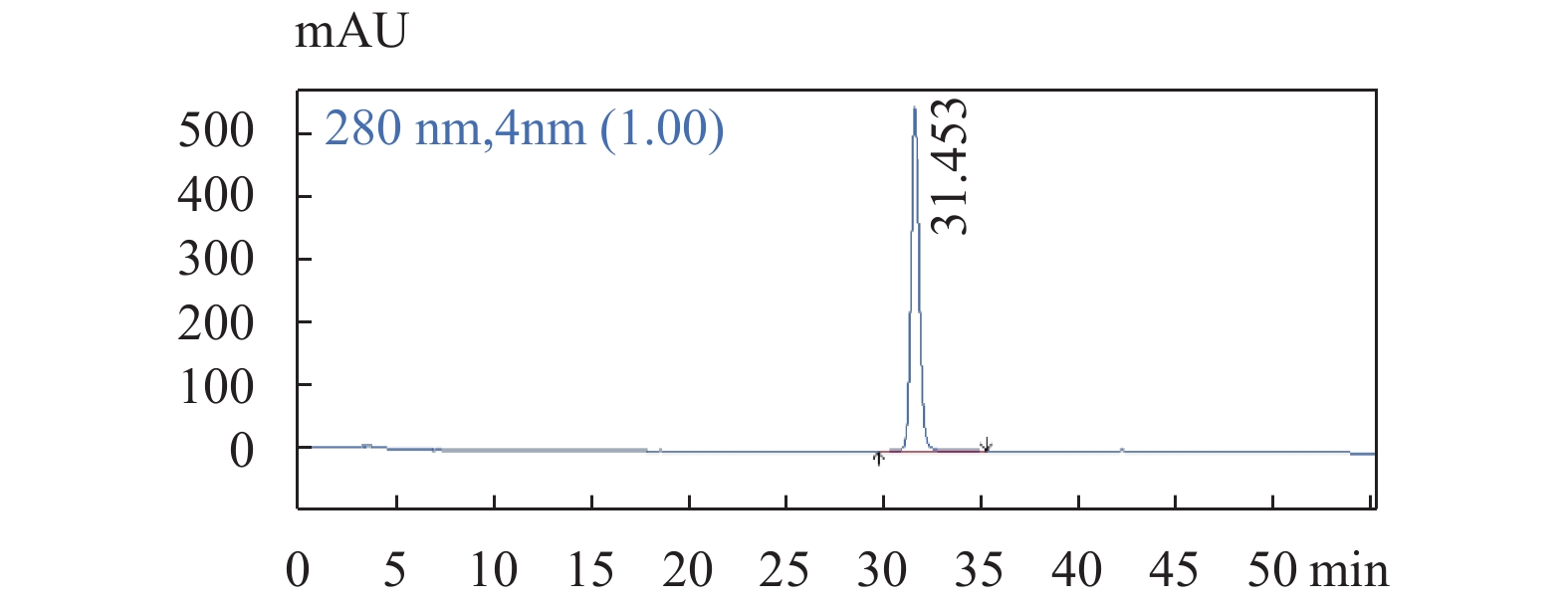
图 4 柯里拉京对照品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 4. The chromatogram of Corilagin
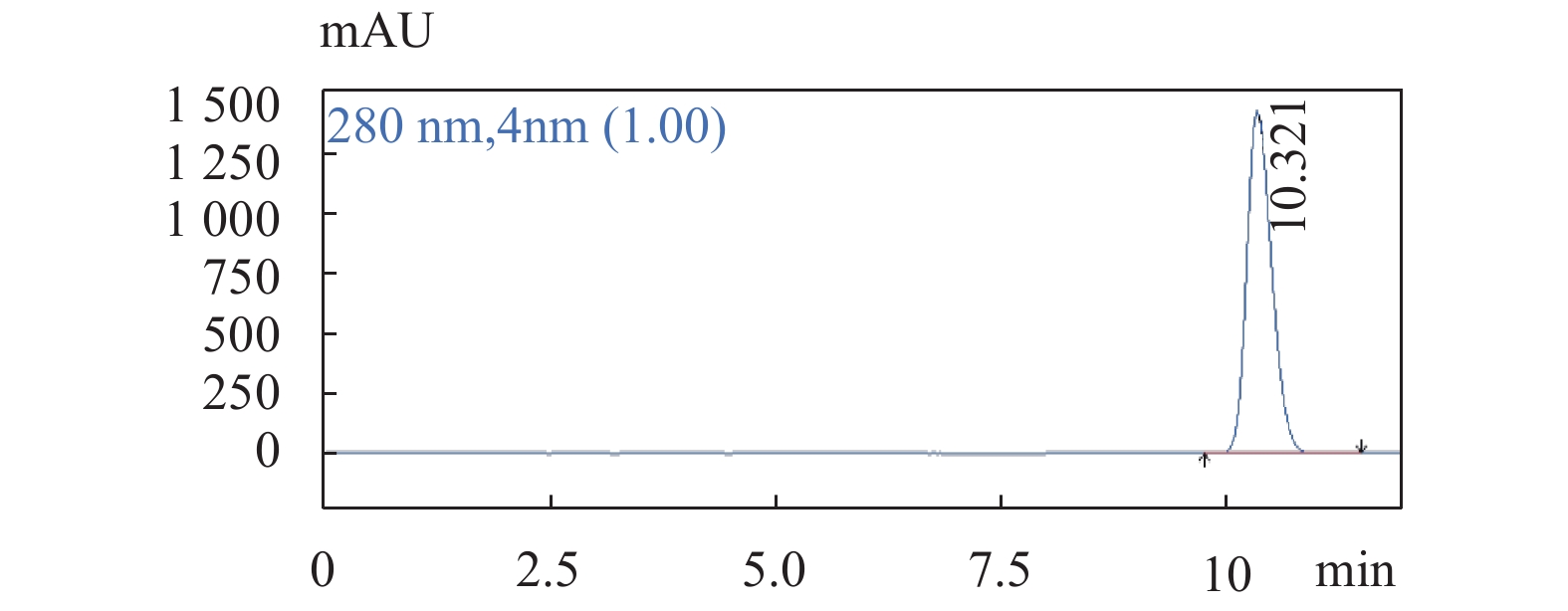
图 5 老鹳草素对照品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 5. The chromatogram of Geraniin
图 6 没食子酸对照品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 6. The chromatogram of Gallic acid
图 7 金丝桃苷对照品溶液色谱图
色谱条件:流速:1.0 mL/min;柱温:25 ℃;检测波长:280 nm;梯度洗脱程序见表1。
Figure 7. The chromatogram of Hyperoside
表 1 HPLC梯度洗脱程序表、
Table 1. The HPLC gradient elution procedures
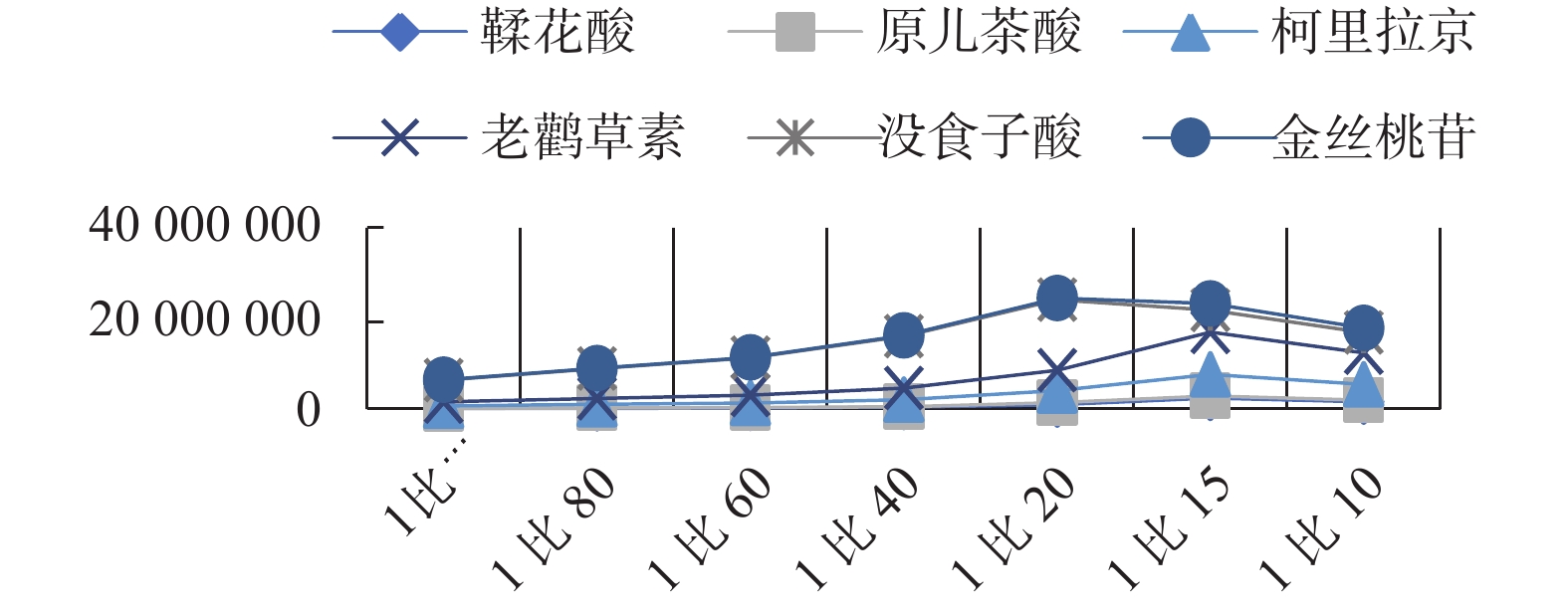
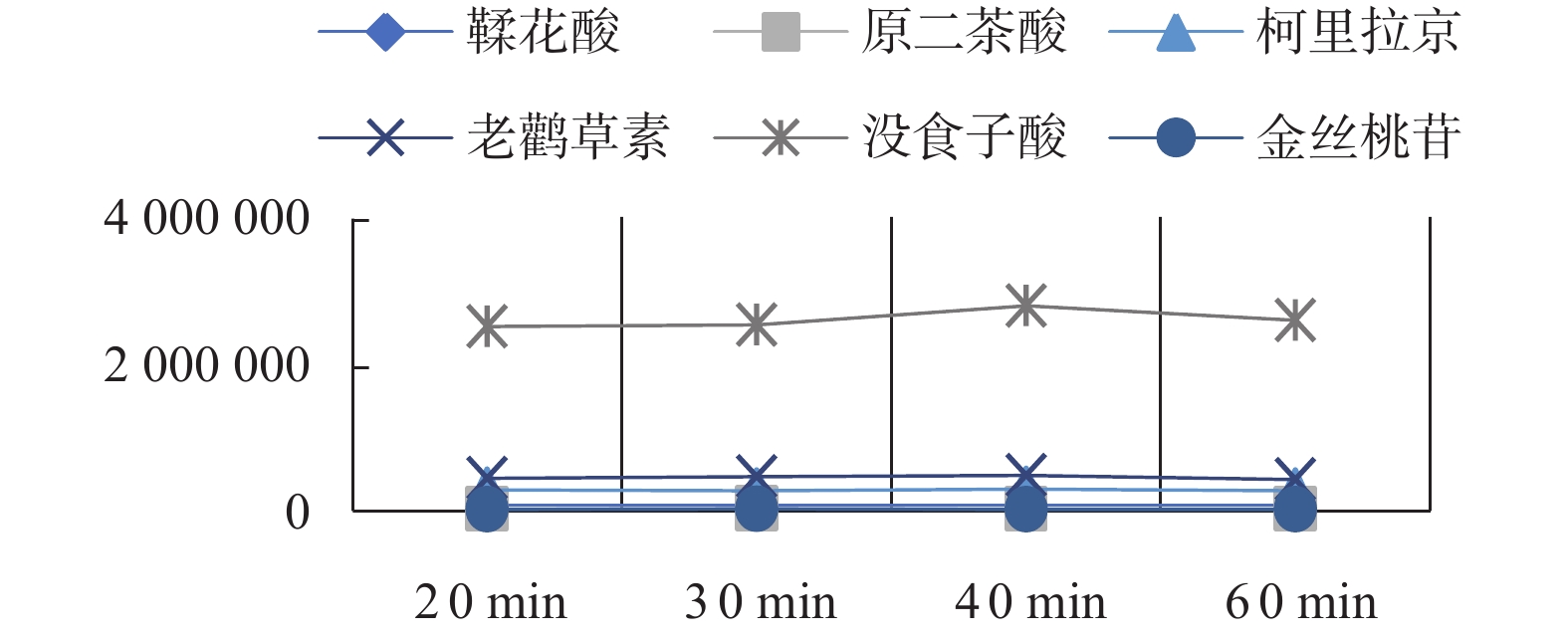
时间(min) 0.1%磷酸(Phosphoric) 乙腈(Acetonitrile) 0 96 4 10 95 5 15 88 12 20 86 14 30 85 15 40 79 21 50 79 21 60 55 45 70 55 45 表 2 因素水平表
Table 2. Factors and Levels
表 3 L9(34)正交试验表(老鹳草素)
Table 3. The results of orthogonal experiment (Geraniin)
试验 因素 老鹳草素
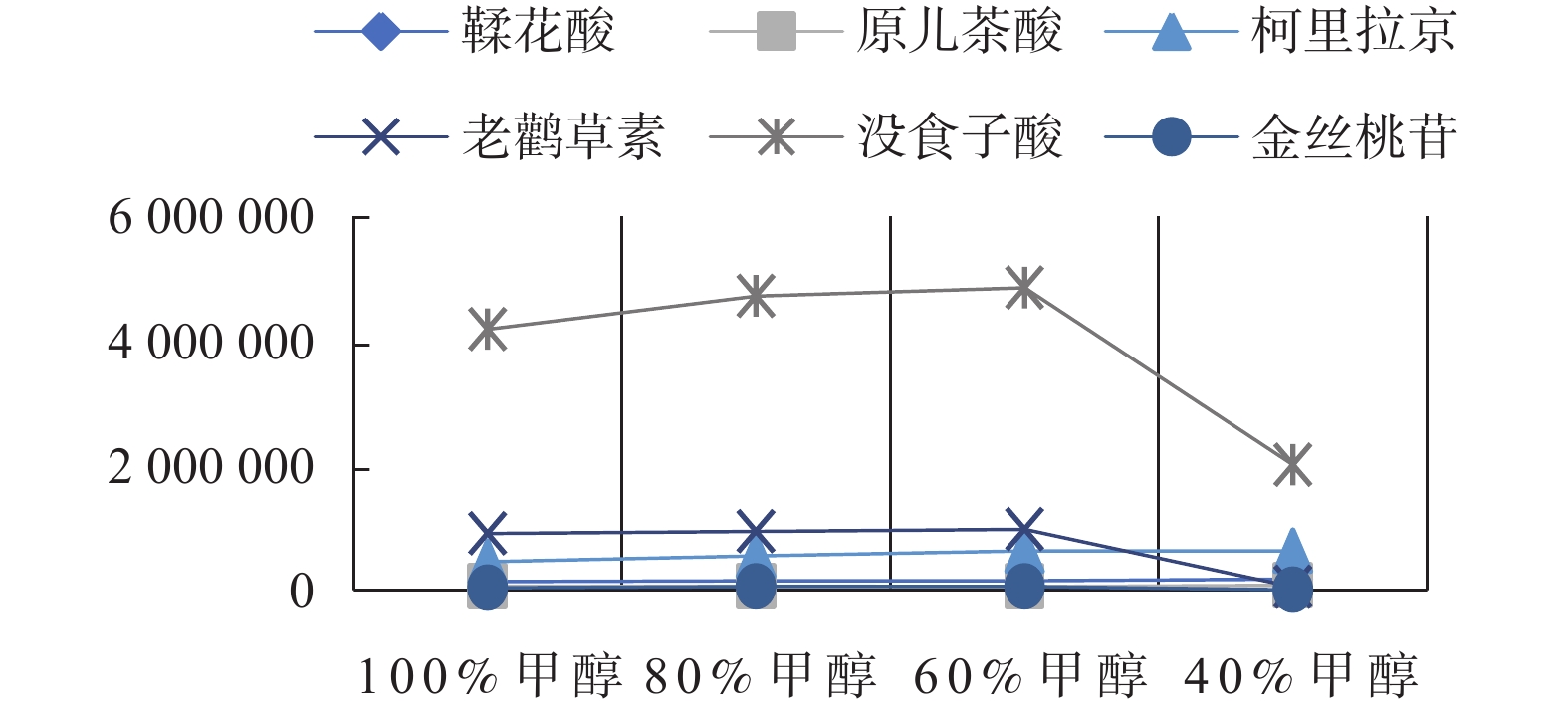
峰面积A B C 1 1 1 1 1103857 2 1 2 2 4837849 3 1 3 3 3661222 4 2 1 2 2185068 5 2 2 3 3675299 6 2 3 1 6156247 7 3 1 3 1361929 8 3 2 1 6736777 9 3 3 2 4823928 M1 9602928 4650854 13996881 T = 34542176 M2 12016614 15249925 11846845 y = 3838020 M3 12922634 14641397 8698450 m1 3200976 1550285 4665627 m2 4005538 5083308 3948948 m3 4307545 4880466 2899483 Rj R1 = 9346027 R2 = 3403080 R3 = 5942947 Sj S1 = 1963022889647 S2 = 23613509157143 S3 = 4734267721180 A:提取时间;B:料液比;C:溶剂体积分数; m1:实验因素一水平实验结果平均值;m2:实验因素二水平实验结果平均值;
m3:实验因素三水平实验结果平均值;Rj :M 值极差;Sj :反映了正交表上第 j 列所排因素的不同水平之间的差异程度,称 Sj 为第 j 列变差平方和;T:9 次实验结果之和;y:9 次实验结果平均值。在一定范围内,R值极差的大小与提取量的影响大小正比,m值大小与最佳提取条件因素成正比。表 4 L9(34)正交试验表(没食子酸)
Table 4. The results of orthogonal experiment (Gallic acid)
试验 因素 没食子酸
峰面积A B C 1 1 1 1 7314190 2 1 2 2 16280524 3 1 3 3 12562631 4 2 1 2 13938578 5 2 2 3 13910940 6 2 3 1 19201446 7 3 1 3 7694251 8 3 2 1 24710211 9 3 3 2 18204393 M1 36157345 28947018 51225846 T = 133817162 M2 47050964 54901675 48423495 y = 14868574 M3 50608854 49968469 34167822 m1 12052448 9649006 17075282 m2 15683655 18300558 16141165 m3 16869618 16656156 11389274 Rj R1 = 22278828 R2 = 7850711 R3 = 5480344 Sj S1 = 37797292060705 S2 = 126653568075958 S3 = 55783729621634 表 5 L9(34)正交试验表(柯里拉京)
Table 5. The results of orthogonal experiment (Corilagin)
试验 因素 柯里拉京
峰面积A B C 1 1 1 1 1904530 2 1 2 2 3202766 3 1 3 3 1869245 4 2 1 2 3343529 5 2 2 3 2315514 6 2 3 1 3106967 7 3 1 3 2468583 8 3 2 1 4962727 9 3 3 2 2490196 M1 6976540 7716642 9974224 T = 25664055 M2 8766010 10481006 9036490 y = 2851562 M3 9921506 7466408 6653342 m1 2325513 2572214 3324741 m2 2922003 3493669 3012163 m3 3307169 2488803 2217781 Rj R1 = 2997684 R2 = 1714997 R3 = 3268164 Sj S1 = 14677993215 S2 = 18657924733 S3 = 1954110905333 表 6 L9(34)正交试验表(金丝桃苷)
Table 6. The results of orthogonal experiment (Hyperoside)
试验 因素 金丝桃苷
峰面积A B C 1 1 1 1 477208 2 1 2 2 482219 3 1 3 3 332298 4 2 1 2 553354 5 2 2 3 325225 6 2 3 1 640846 7 3 1 3 402090 8 3 2 1 716723 9 3 3 2 450258 M1 901338 364870 1480455 T = 3378937 M2 1107751 1535964 1187781 y = 375437 M3 1369849 1478104 710701 m1 300446 121623 493485 m2 369250 511988 395927 m3 456616 492701 236900 Rj R1 = 1115586 R2 = 428214 R3 = 767403 Sj S1 = 36756108434 S2 = 290455567127 S3 = 100642735244 表 7 L9(34)正交试验表(鞣花酸)
Table 7. The results of orthogonal experiment (Ellagic acid)
试验 因素 鞣花酸
峰面积A B C 1 1 1 1 2275146 2 1 2 2 1022426 3 1 3 3 716270 4 2 1 2 1485928 5 2 2 3 704427 6 2 3 1 1477116 7 3 1 3 868155 8 3 2 1 1545919 9 3 3 2 1044160 M1 4013842 4629228 5298180 T = 11139544 M2 3667471 3272771 3552514 y = 1237727.1 M3 3458233 3237545 2288851 m1 1337947 1543076 1766060 m2 1222490 1090924 1184171 m3 1152744 1079182 762950 Rj R1 = 428113 R2 = 131567 R3 = 389794 Sj S1 = 52494689151 S2 = 419777559602 S3 = 1522250079819 表 8 L9(34)正交试验表(原儿茶酸)
Table 8. The results of orthogonal experiment (Protocatechuic acid)
试验 因素 原儿茶酸
峰面积A B C 1 1 1 1 477208 2 1 2 2 482219 3 1 3 3 332298 4 2 1 2 553354 5 2 2 3 325225 6 2 3 1 640846 7 3 1 3 402090 8 3 2 1 716723 9 3 3 2 450258 M1 1291724 1432652 1834777 T = 4380219 M2 1519425 1524167 1485830 y = 486691 M3 1569071 1423401 1059613 m1 430575 477551 611592 m2 506475 508056 495277 m3 523024 474467 353204 Rj R1 = 543053 R2 = 38337 R3 = 509458 Sj S1 = 14581556354 S2 = 2068250330 S3 = 100478249341 -
[1] 国家药典委员会. 中华人民共和国药典[S]. 北京: 中国医药出版社, 2020: 126. [2] 罗宏,尹海波. 中药老鹳草的研究[J]. 长春中医药大学学报,2010,26(2):285-286. [3] 车环宇,刘畅,孙仁爽. 老鹳草鞣质体外抗氧化作用研究[J]. 通化师范学院学报,2013,34(10):37-38. doi: 10.3969/j.issn.1008-7974.2013.10.012 [4] 李倩,买吾拉江·阿不都热衣木,徐芳,等. 老鹳草素药理研究进展[J]. 中国中医药信息杂志,2016,23(8):125-128. doi: 10.3969/j.issn.1005-5304.2016.08.034 [5] 王如意,刘纲勇,梁晓欣,等. HPLC法同时测定野老鹳草中5种活性成分的含量[J]. 中国药房,2016,27(21):2972-2975. doi: 10.6039/j.issn.1001-0408.2016.21.29 [6] 谷静逸,尹海波,赵容,等. 辽宁省5种老鹳草中5种活性成分的含量测定[J]. 中国实验方剂学杂志,2016,22(6):26-29. [7] 曹波,尹海波,贾晓晴,等. HPLC 法同时测定3种老鹳草中7种成分[J]. 中成药,2016,38(6):1338-1342. [8] 罗燕平,戚微岩,吴小东,等. 老鹳草素的研究进展[J]. 药物生物技术,2016,23(3):279-282. [9] 江尚飞,潘伦,杨宗发,等. 中药有效成分常用提取新工艺研究进展[J]. 中国药业,2014,23(17):1-3. [10] 王吉华,尹海波. 正交试验法优选老鹳草酚酸类成分的提取工艺[J]. 中药材杂志,2012,35(6):986-989. [11] 刘娟,罗仓学,魏丽娜,等. 地椒总黄酮超声提取工艺优化及抗氧化活性研究[J]. 食品科技,2020,45(1):268-273. [12] 翟豫州,王玉梅,王世杰,等. 正交实验法优化盐地碱蓬中多糖的超声提取工艺[J]. 广东化工,2021,48(15):29-31. [13] 邓莹,刘杰,李香,等. 正交试验法优选玄参中肉桂酸的超声提取工艺[J]. 广东化工,2021,30(20):32-35. [14] 潘娅,郑德俊. 正交试验法优选藤黄酸超声提取工艺[J]. 广东化工,2021,48(2):1-2. [15] 彭华,宋霞,张春. 正交法优化‘胭脂萝卜’红色素超声提取工艺[J]. 中国农学通报,2021,37(27):132-138. -






 下载:
下载:
 下载:
下载: