Clinical Characteristics, Diagnosis and Treatment of Diabetes Mellitus with Pulmonary Mucormycosis
-
摘要:
目的 探讨肺毛霉菌病(pulmonary mucormycosis,PM)的危险因素、临床表现和诊治方法,以期提高肺毛霉菌病的诊断率,降低死亡率。 方法 收集2011年1月至2021年8月在昆明市延安医院呼吸与危重症医学一科经病理确诊的PM患者4例,分析其临床特征、临床症状、影像学表现及诊治方法、预后情况。 结果 4例PM中女性2例,男性2例。4例均合并2型糖尿病,1例合并高血压,1例合并慢性肾功能衰竭、长期口服激素治疗。胸部CT表现主要为斑片状、片絮状高密度影、支气管管腔狭窄。4例PM患者均经组织病理学检查确诊。确诊后1例因大咯血死亡,2例给予全身使用抗真菌药物联合支气管镜介入治疗,1例因不耐受全身抗真菌治疗行支气管镜介入治疗。经治疗后3例临床症状明显改善。 结论 PM 为一种罕见的侵袭性真菌病,好发于糖尿病、肾功能衰竭、免疫功能低下患者。临床症状缺乏特异性,确诊主要依赖于病原学和组织学检查。临床经验提示,抗真菌药物联合支气管镜下介入治疗可改善患者预后,但仍需进一步扩大样本量观察其疗效确切性。 Abstract:Objective To explore the risk factors, clinical symptoms, diagnosis and treatment of pulmonary mucormycosis (PM) so as to improve the diagnostic rate of PM and reduce the mortality. Methods 4 patients (2 females and 2 males) with pulmonary mucormycosis confirmed by pathology in the First Department of Respiratory and Critical Care Medicine of Yan'an Hospital of Kunming City from January 2011 to August 2021 were collected and their clinical data, risk factors, clinical symptoms, imaging findings, treatment and prognosis were analyzed. Results All 4 patients were complicated with type 2 diabetes, 1 patient with hypertension, 1 patient with chronic renal failure and was treated with long-term oral hormone therapy. The main chest imaging findings were mainly patchy, patchy high-density shadows and bronchial lumen stenosis. All the 4 patients were diagnosed as PM by pathological biopsy. After the diagnosis, 1 patient died of massive hemoptysis, 2 patients were treated with systemic antifungal drugs combined with bronchoscopic intervention and 1 patient was treated with bronchoscopic intervention due to intolerance to systemic antifungal therapy. The clinical symptoms of the 3 patients were improved significantly after the treatment. Conclusion PM is a rare invasive fungal disease, which occurs frequently in patients with diabetes, renal failure and immune deficiency. The clinical symptoms are lack of specificity, and the diagnosis mainly depends on the etiology and histological examination. Our clinical experience suggests that antifungal drugs combined with bronchoscopic interventional therapy can improve the outcomes of patients with PM, but further expanded sample size is still needed to observe the efficacy of the treatment. -
Key words:
- Pulmonary mucormycosis /
- Clinical characteristics /
- Treatment
-
2型糖尿病(Type 2 diabetes mellitus,T2DM)是由多种因素导致血糖升高的代谢紊乱性疾病,胰岛素抵抗是其主要诱因[1],肾脏损害是糖尿病严重的并发症,也是临床上终末期肾病的首位病因[2]。因此,阐明T2DM合并肾脏损伤的机制,寻找有效的药物治疗成为当前的重要问题。
肾素血管紧张素系统(renin angiotensin s-ystem,RAS)在T2DM及其并发症的发生和发展中具有重要的地位,RAS的激活可增加胰岛素抵抗,促进炎性反应,引起肾炎[3]。血管紧张素Ⅱ 1型受体(angiotensin Ⅱ receptor 1 type, AT1)的表达增加可引起TGF-β1的生成增多,激活RAS导致糖尿病肾病的发生发展[4]。另外,糖尿病患者肾脏中肾小球硬化导致肾功能减退,基质金属蛋白酶9(matrix metalloproteinase, MMP9)通过水解细胞外基质,减轻糖尿病肾脏的恶化[5-7]。所以,抑制RAS的激活和增加细胞外基质的水解将是治疗的关键。
人参皂苷Rg1是我国传统名贵药材人参和三七等主要活性物质[8]。具有抗衰老[9]、抗心肌损伤[10-12]、减缓认知功能障碍[13]、减轻糖尿病并发症如肝损伤[14]、勃起功能障碍[15]的功能。但在T2DM合并肾脏损伤中,人参皂苷Rg1是否抑制RAS的激活和促进细胞外基质的降解,从而保护肾脏的功能未见报道,因此,本研究拟通过建立T2DM的动物模型,探讨人参皂苷Rg1对肾脏组织RAS的激活和促进细胞外基质的降解影响,为人参皂苷Rg1治疗T2DM合并肾脏损伤提供理论依据。
1. 材料与方法
1.1 动物模型及分组
SPF级雄性 SD 大鼠60只(实验所涉及到的实验动物程序均经昆明医科大学实验动物伦理委员会批准,动物合格证号:53004100000079),体重 180~200 g,适应性喂养2周后,分为正常对照组10只,高糖高脂组50只。高糖高脂组喂养高糖高脂饲料8周后,35 mg/kg腹腔注射链脲佐菌素(streptozocin,STZ)1次,1周后测空腹血糖,血糖 ≥ 11.1 mmol/L为造模成功;选择造模成功大鼠分为模型对照组、Rg1低剂量治疗组(25 mg/kg·d)、Rg1中剂量治疗组(50 mg/kg·d)、Rg1高剂量治疗组(100 mg/kg·d)和二甲双胍对治疗组(100 mg/kg·d),每组10只,灌胃给药4周。
1.2 取材
灌胃结束后,以10%水合氯醛麻醉大鼠(6.25 mL/kg),取血离心获得血清后于-80 ℃保存用于检测生化指标;取部分左侧肾脏组织4%甲醛固定后,石蜡包埋用于HE染色,剩余肾脏组织于-80 ℃冰箱保存,用于Western blot检测蛋白质表达。
1.3 血生化指标检测
全自动生化分析仪测定Scr、BUN和UA含量。
1.4 肾体比检测
各组大鼠麻醉前,称取其体重。麻醉处死后取左侧肾脏称取体重,计算肾重量/体重的比值。
1.5 HE染色检测肾脏病理改变
取石蜡包埋后的肾脏组织,通过切片机将组织切为5 µm薄片后经过烤片,二甲苯脱蜡30 min,95%酒精-50%酒精各浸泡2 min,苏木精染色5 min,流水冲洗30 min放入氨水中4 s。1%伊红浸泡3 min,再进行脱水后用中性树脂封片,显微镜下一个样本随机选取6个视野采集图片。
1.6 Western blot检测
从-80 ℃取出肾脏组织称取100 mg,在EP管中加入组织裂解液1 mL,提取总蛋白,采用BCA蛋白定量法定量。取40 µg的蛋白质经SDS-PAGE电泳后采用湿转法把蛋白转移至PVDF膜上,转膜完成后5%脱脂牛奶封闭2 h,加入一抗AT1(Wanleibio)、TGF-β1(Abcam)、MMP9(Wanleibio)和β-actin(Abcam)(1∶1000),孵育过夜后,PBS洗3次,二抗孵育2 h后洗涤,加入ECL发光液,置于凝胶成像系统中进行曝光,保存图片。采用 ImagePro-plus6.0软件进行灰度分析,以β-actin作为内参,分析结果。
1.7 统计学处理
通过SPSS25.0进行统计学处理,计量资料服从正态分布的以均数±标准差( $\bar x\pm s $)表示,组间比较采用单因素方差分析法,P < 0.05为差异有统计学意义,应用GraphPad Prism6.0版进行图片制作。
2. 结果
2.1 生化指标检测
与正常组比较,模型组血BUN增加(P < 0.001),与模型组比较,低、中剂量Rg1组大鼠BUN降低( P < 0.01)。与正常组比较,模型组Scr改变无统计学意义,不同剂量Rg1治疗组与模型组相比无统计学差异。UA值在正常组、模型组大鼠以及Rg1不同治疗组中的改变均无统计学意义,见 表1。
表 1 血生化指标( $\bar x \pm s $)Table 1. Blood biochemical index ( $\bar x \pm s $)检测指标 正常组(n = 6) 模型组(n = 6) 低剂量Rg1(n = 6) 中剂量Rg1(n = 6) 高剂量Rg1(n = 6) 二甲双胍(n = 6) 尿素氮 4.93 ± 0.562 10.00 ± 0.628# 6.41 ± 0.509* 7.74 ± 0.296* 7.18 ± 0.614* 12.97 ± 0.848* 肌酐 41.67 ± 3.667 43.22 ± 2.253 44.86 ± 2.865 42.22 ± 1.913 48.22 ± 3.643 50.33 ± 2.744 尿酸 5.50 ± 0.269 5.00 ± 0.289 5.13 ± 0.350 5.89 ± 0.824 6.00 ± 0.373* 5.75 ± 0.366 与正常组相比较具有统计学意义,#P < 0.05;与模型组比较有统计学意义, *P < 0.05。 2.2 左肾重、肾体积以及肾体比
与正常组比较,模型组左侧肾脏的重量增加(P < 0.05),与模型组比较,各剂量Rg1组和二甲双胍组治疗后左肾重减轻( P < 0.05)。与正常组比较,模型组大鼠体重降低( P < 0.05),低、中、高3个剂量Rg1和二甲双胍治疗后体重与模型组相比无统计学意义。与正常组大鼠相比,模型组大鼠肾脏系数增大,提示可能有肾脏充血、水肿或是肥大增生。给与Rg1以及二甲双胍治疗后肾脏系数降低( P < 0.05),见 表2。
表 2 肾脏指标( $\bar x \pm s $)Table 2. Kidney indicators ( $\bar x \pm s $)检测指标 正常组(n = 6) 模型组(n = 6) 低剂量Rg1(n = 6) 中剂量Rg1(n = 6) 高剂量Rg1(n = 6) 二甲双胍(n = 5) 左肾重 1.84 ± 0.131 2.22 ± 0.082# 1.90 ± 0.052* 1.43 ± 0.114* 1.58 ± 0.091* 1.90 ± 0.110* 体重 570.50 ± 17.480 376.80 ± 7.016# 395.30 ± 11.070 366.50 ± 4.403 367.00 ± 8.450 398.20 ± 9.932 肾重/体重 0.32 ± 0.022 0.59 ± 0.024# 0.48 ± 0.008* 0.39 ± 0.030* 0.43 ± 0.028* 0.48 ± 0.021* 与正常组比较具有统计学意义,#P < 0.05;与模型组比较有统计学意义, *P < 0.05。 2.3 肾脏HE染色结果
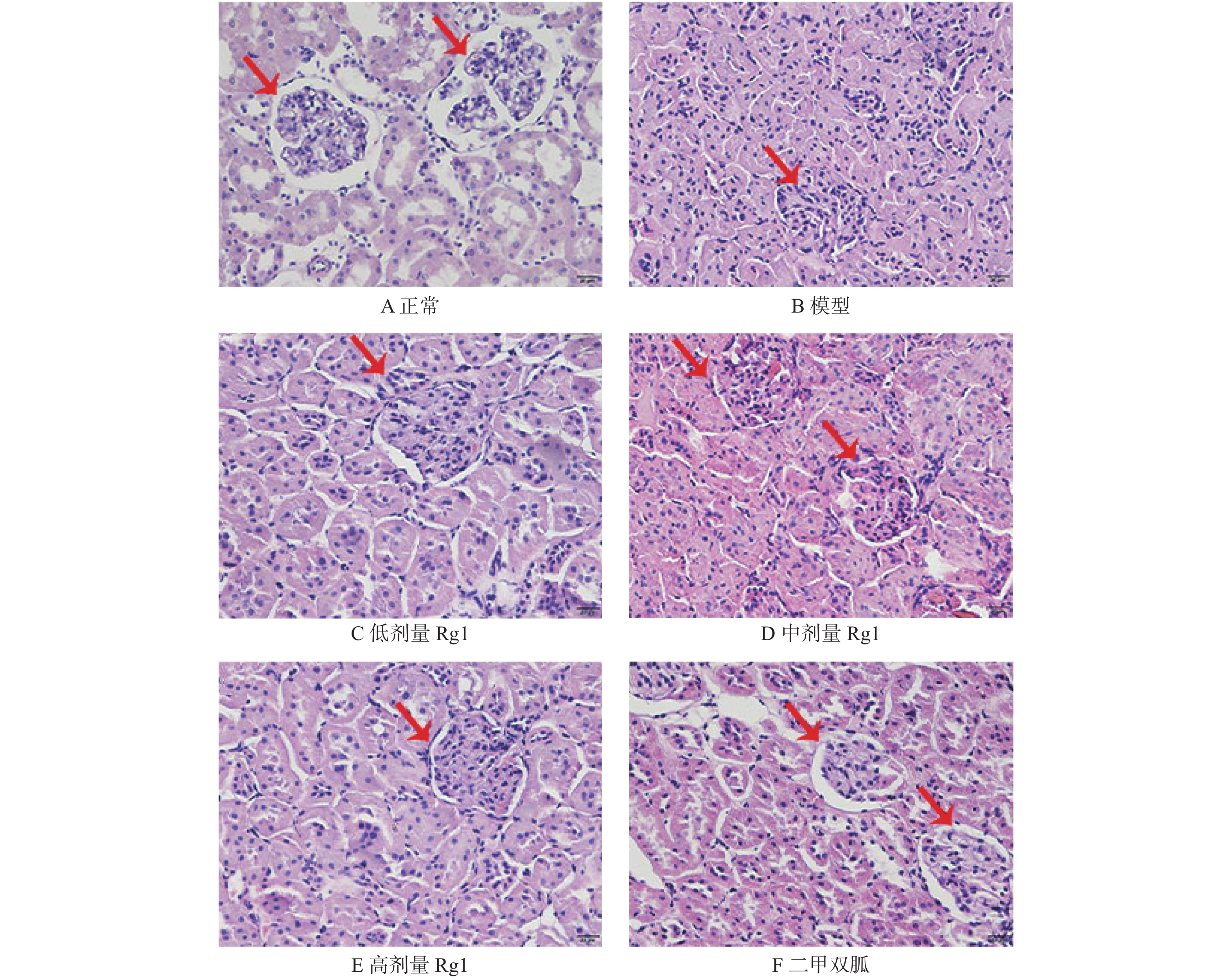
与正常组相比,模型组大鼠的肾脏肾小球体积增大、细胞数目增多。系膜基质增多,系膜区增宽。炎性细胞浸润,肾小囊消失肾小管上皮细胞出现水肿以及坏死脱落。给与各剂量Rg1和二甲双胍治疗后,肾小球体积减小,炎性细胞浸润程度下降,肾小囊部分可见,见图1。
2.4 肾脏Western blot检测结果
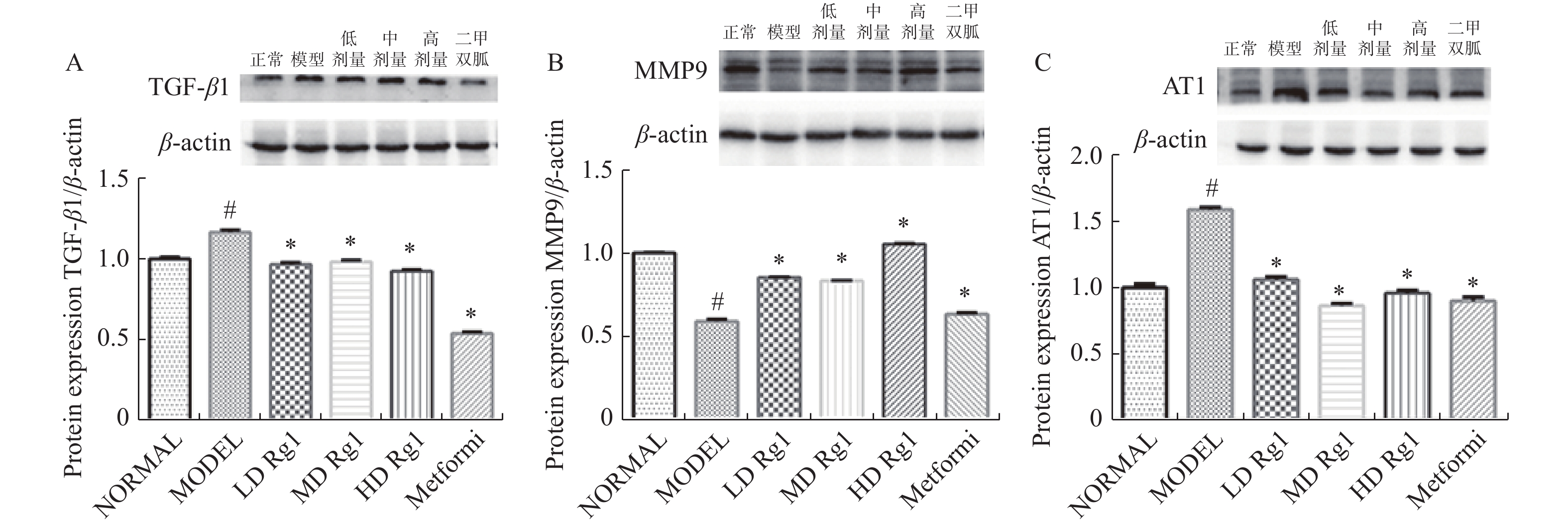
与正常组相比,模型组肾脏组织TGF-β1分泌增多,模型组与正常组相比有统计学意义P < 0.05,给与Rg1不同剂量和二甲双胍治疗后TGF-β1分泌减少,剂量组和模型组相比有统计学意义 P < 0.05。MMP9在糖尿病模型组大鼠肾脏中的表达低于正常组,模型组与正常组相比有统计学意义 P < 0.05。给与Rg1不同剂量和二甲双胍治疗后,MMP9的表达较模型组相比升高,有统计学意义 P < 0.05。AT1在糖尿病大鼠模型组肾脏中的表达高于模型组,模型组与正常组相比有统计学意义 P < 0.05。给与Rg1不同剂量以及二甲双胍治疗后AT1表达下降明显,接近正常组,Rg1不同剂量治疗组以及二甲双胍组与模型组相比具有统计学意义 P < 0.05,见 图2。
3. 讨论
杨敬等[16]研究发现人参皂苷Rg1可显著改善肾损伤大鼠血清氧化应激指标,下调血清炎性因子水平以及肾组织TGF-β1、MCP-1 mRNA表达。沈晓燕等研究发现Rg1可通过抑制NOX4介导的ROS氧化应激和NLRP3炎症小体激活来延缓肾脏衰老,减轻与衰老相关的肾损伤和纤维化[17]。在本研究中从血生化数据中可看出采用高糖高脂饮食 + 小剂量链脲佐菌素(STZ)建立的2型糖尿病大鼠BUN值显著升高,而尿酸值以及肾脏系数指标下降,本研究从大体角度对人参皂苷Rg1治疗肾脏损伤的表型进行了描述,说明人参皂苷Rg1可以保护大鼠肾脏受损。这与其他研究结论一致[18-20]。
陈少霞等研究发现局部肾素血管紧张素系统的过度激活引起肾脏足细胞、内皮细胞、系膜细胞、肾小管上皮细胞的损害,导致肾脏病理改变,引起一系列临床表现。其他研究也证明了肾素血管紧张素系统的过度激活可能会引起肾脏的损伤[21-22],肾素血管紧张素系统的激活表现为血管紧张素受体AT1表达增加[23],使用AT1抑制剂可以降低糖尿病大鼠肾脏受损程度[24],本研究免疫印迹结果显示糖尿病大鼠肾脏中AT1表达增加,说明RAS系统的激活参与了糖尿病大鼠肾脏受损的分子调节。
糖尿病早期肾损害表现为系膜细胞增殖、大量细胞外基质生成并异常聚集,TGF-β1与系膜细胞增殖有关,早期2型糖尿病TGF-β1分泌升高[25-26]。本研究免疫印迹结果显示糖尿病大鼠肾脏中TGF-β1表达增高,这可能是由于RAS系统激活所致。MMP9在糖尿病大鼠肾脏表达减少,糖尿病大鼠肾脏中细胞外基质ECM不能被正常代谢从而促进肾脏受损。人参皂苷Rg1保护糖尿病大鼠肾脏受损的分子机制可能是Rg1抑制RAS系统激活,抑制TGF-β1的表达,从而促进ECM的水解,减缓肾脏受损程度。
根据本实验研究结果分析发现,人参皂苷Rg1可有效缓解2型糖尿病大鼠的症状,减少糖尿病大鼠的肾脏损伤,其作用机制是Rg1对RAS系统的作用,调控了炎性因子的表达,从而实现对肾脏功能的良性调节。人参皂苷Rg1可以作为2型糖尿病引起肾脏损伤的预防药物,但其作用机制有待更深入研究。
-
表 1 4例肺毛霉菌病患者的临床特征n(%)
Table 1. Clinical characteristics of 4 patients with PM n(%)
临床特征 占比 女性 2(50) 男性 2(50) 年龄(中位数)(岁) 54(48~61) 合并基础疾病情况 糖尿病 4(100) 慢性肾功能衰竭 1(25) 高血压 1(25) 表 2 肺毛霉菌病患者的临床表现、胸部影像学改变 n(%)
Table 2. Clinical features, computed tomographic presentation of patients with PM n(%)
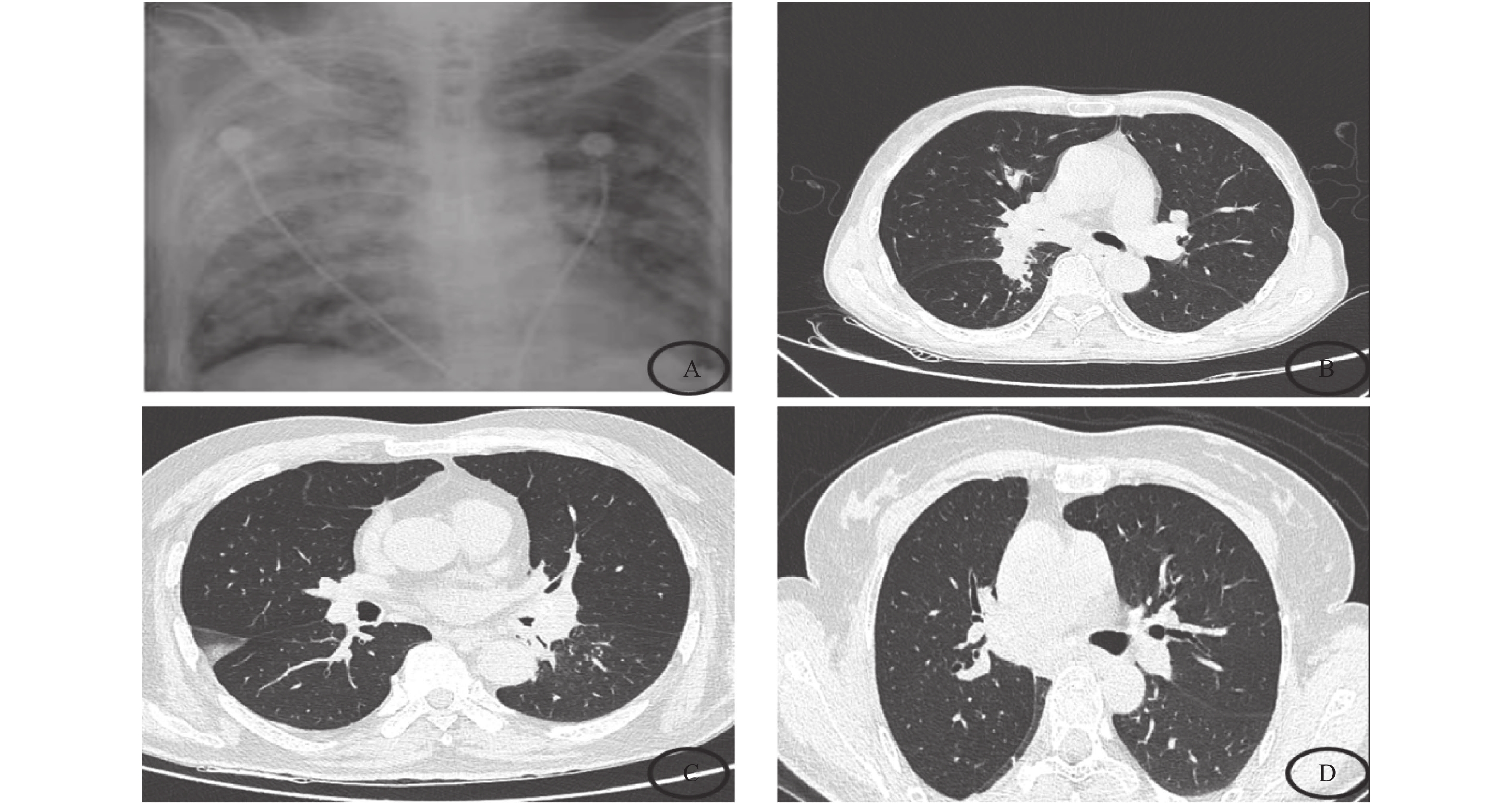
临床表现+影像学改变 占比 咳嗽 4(100) 呼吸困难 3(75) 咳痰 2(50) 发热 1(25) 病变部位 中央型 3(75) 外周型 1(25) 左肺 3(75) 右肺 2(50) 上叶 3(75) 中叶 3(50) 下叶 4(75) -
[1] Guinea J,Escribano P,Vena A,et al. Increasing incidence of mucormycosis in a large Spanish hospital from 2007 to 2015:Epidemiology and microbiological characterization of the isolates[J]. PLos One,2017,12(6):e0179136. doi: 10.1371/journal.pone.0179136 [2] Kontoyiannis D P,Wessel V C,Bodey G P,et al. Zygomycosis in the 1990s in a tertiary-care cancer center[J]. Clin Infect Dis,2000,30(6):851-856. doi: 10.1086/313803 [3] Tedder M,Spratt J A,Anstadt M P,et al. Pulmonary mucormycosis:Results of medical and surgical therapy[J]. Ann Thorac Surg,1994,57(4):1044-1050. doi: 10.1016/0003-4975(94)90243-7 [4] Chamilos G,Lewis R E,Kontoyiannis D P. Delaying amphotericin B-based frontline therapy significantly increases mortality among patients with hematologic malignancy who have zygomycosis[J]. Clin Infect Dis,2008,47(4):503-509. doi: 10.1086/590004 [5] Linden P K. Amphotericin B lipid complex for the treatment of invasive fungal infections[J]. Expert Opin Pharmacother,2003,4(11):2099-2110. doi: 10.1517/14656566.4.11.2099 [6] 中华医学会呼吸病学分会感染学组, 中华结核和呼吸杂志编辑委员会. 肺真菌病诊断和治疗专家共识[S]. 中华结核和呼吸杂志, 2007, 30(11): 821-834. [7] 梁志欣, 金芬华, 余丹阳等. 5例病理确诊的肺毛霉菌病临床分析[J]. 临床肺科杂志, 2012, 17(3): 418-420. [8] Cohen-Abbo A,Bozeman P M,Patrick C C. Cunninghamella infections:Review and report of two cases of Cunninghamella pneumonia in immunocompromised children[J]. Clin Infect Dis,1993,17(2):173-177. doi: 10.1093/clinids/17.2.173 [9] Rüping M J,Heinz W J,Kindo A J,et al. Forty-one recent cases of invasive zygomycosis from a global clinical registry[J]. J Antimicrob Chemother,2010,65(2):296-302. doi: 10.1093/jac/dkp430 [10] Pozo Laderas J C,Pontes Moreno A,Pozo Salido C,et al. Disseminated mucormycosis in immunocompetent patient:A disease that also exsists[J]. Rev Iberoam Micol,2015,32(2):63-70. doi: 10.1016/j.riam.2014.01.006 [11] Farmakiotis D,Kontoyiannis D P. Mucormycoses[J]. Infect Dis Clin North Am,2016,30(1):143-163. doi: 10.1016/j.idc.2015.10.011 [12] Lee F Y,Mossad S B,Adal K A. Pulmonary mucormycosis:The last 30 years[J]. Arch Intern Med,1999,159(12):1301-1309. doi: 10.1001/archinte.159.12.1301 [13] Feng J,Sun X. Characteristics of pulmonary mucormycosis and predictive risk factors for the outcome[J]. Infection,2018,46(4):503-512. doi: 10.1007/s15010-018-1149-x [14] Danion F,Aguilar C,Catherinot E,et al. Mucormycosis:New developments into a persistently devastating infection[J]. Semin Respir Crit Care Med,2015,36(5):692-705. doi: 10.1055/s-0035-1562896 [15] Chitasombat M N,Kontoyiannis D P. Treatment of mucormycosis in transplant patients:Role of surgery and of old and new antifungal agents[J]. Curr Opin Infect Dis,2016,29(4):340-345. doi: 10.1097/QCO.0000000000000277 [16] 邓莉萍, 杨莹, 邓治平. 支气管镜下注入两性霉素B脂质体治疗肺毛霉菌病 [J]. Chinese Journal of Respiratory and Critical Care Medicine, 2018, 17(4): 416-417. [17] Mihara T,Kakeya H,Izumikawa K,et al. Efficacy of aerosolized liposomal amphotericin B against murine invasive pulmonary mucormycosis[J]. J Infect Chemother,2014,20(2):104-108. doi: 10.1016/j.jiac.2013.09.002 [18] Panigrahi M K,Manju R,Kumar S V,et al. Pulmonary mucormycosis presenting as nonresolving pneumonia in a patient with diabetes mellitus[J]. Respiratory Care,2014,59(12):201-205. doi: 10.4187/respcare.03205 [19] Virally M L,Riveline J P,Virally J,et al. Pulmonary mucormycosis in a diabetic patient with HIV[J]. Diabetes Care.,2002,25(11):2105. doi: 10.2337/diacare.25.11.2105 -






 下载:
下载:

 下载:
下载: