Value Evaluation of New Markers AFP-L3 and PIVKAⅡ in the Diagnosis of Liver Cancer
-
摘要:
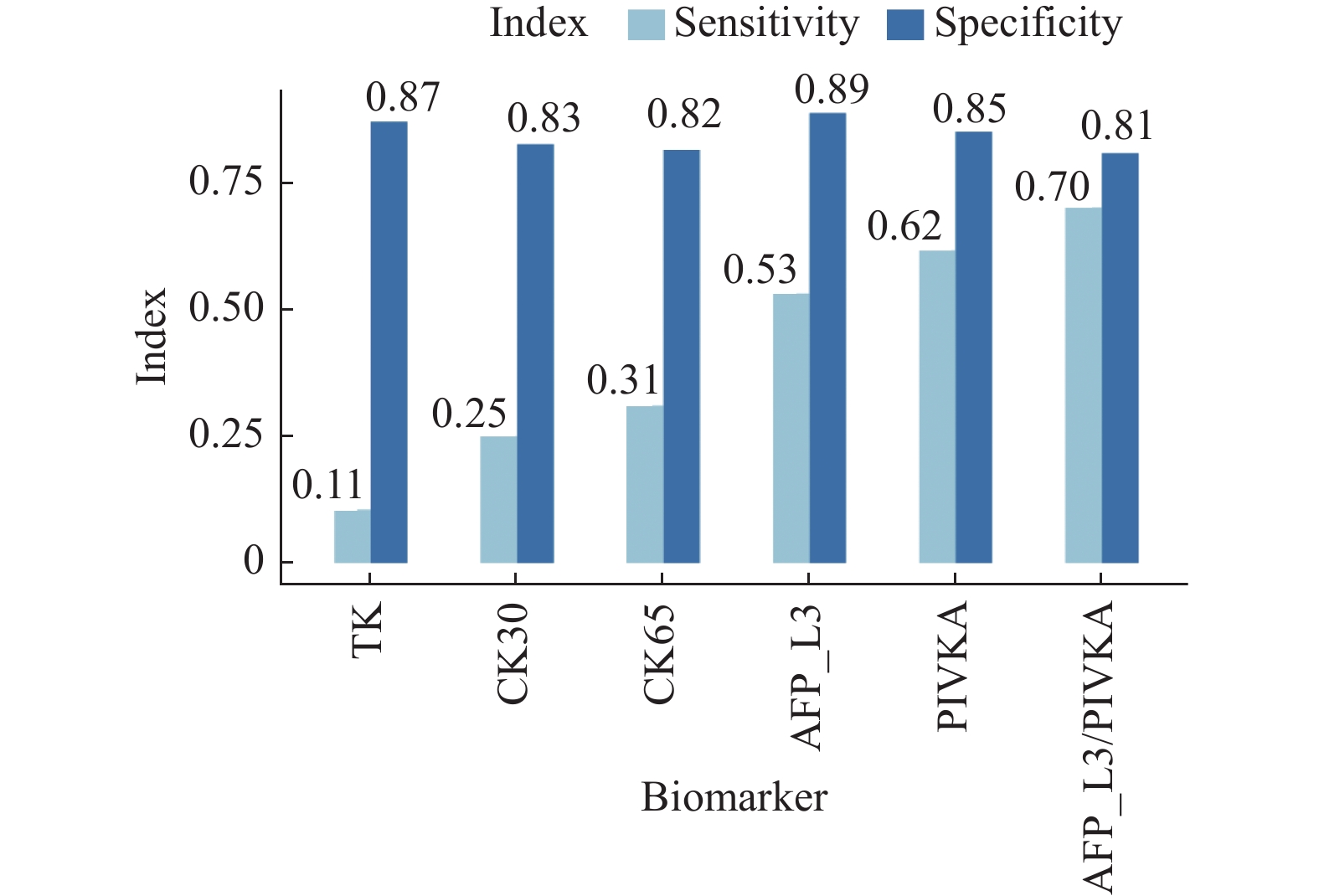
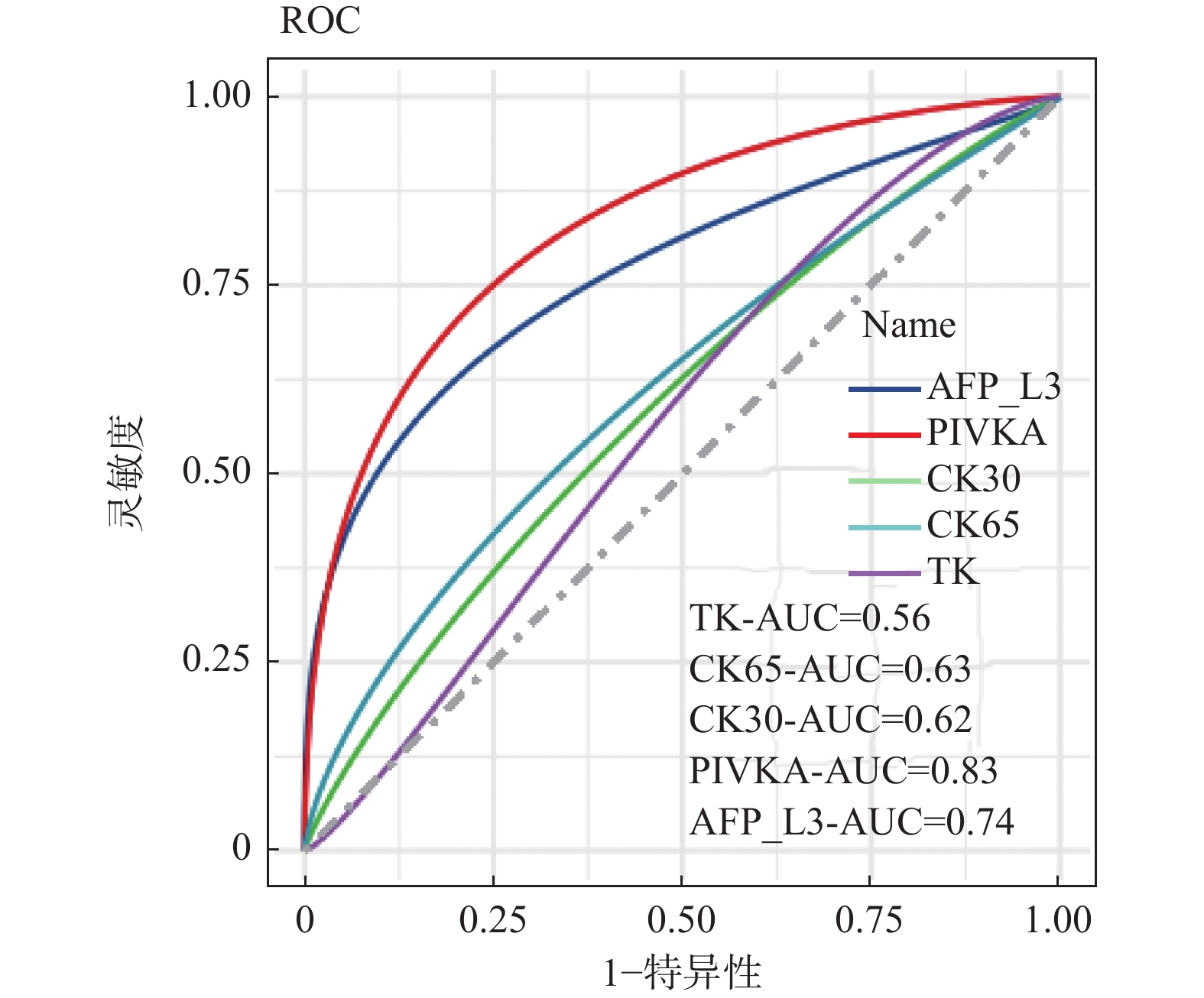
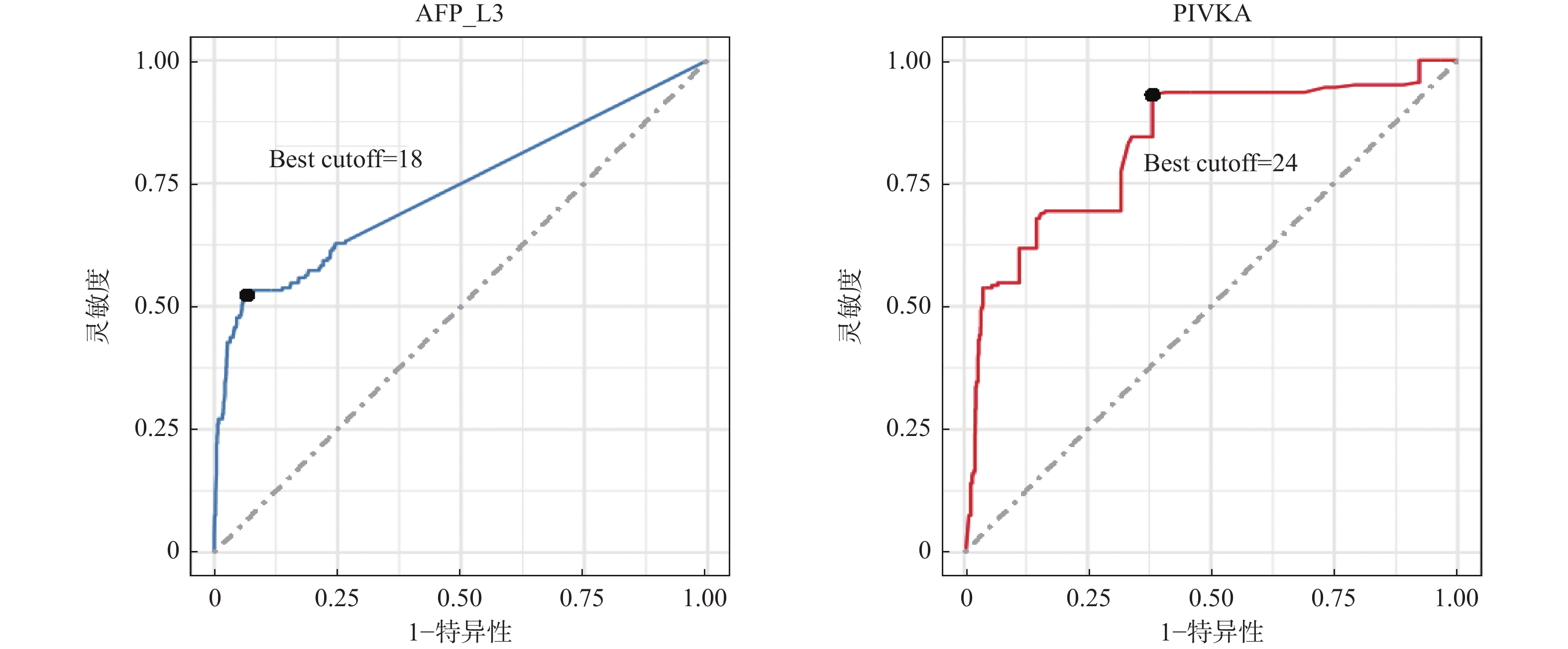
目的 探讨甲胎蛋白异质体L3(alpha-fetoprotein variants L3,AFP-L3)和维生素K缺乏或拮抗剂-Ⅱ诱导的蛋白质(protein induced by vitamin K absence or antagonist II,PIVKAⅡ)在肝癌诊断中的的价值。 方法 收集2019年1月至2022年1月期间青岛市第六人民医院收治的3 066例患有慢性肝脏疾病患者作为研究对象。比较AFP-L3、PIVKAⅡ、CK65、CK30、TK1在肝炎、肝硬化以及肝癌间的水平差异,评估特异性、敏感度,应用受试者工作特征曲线(receiver operating characteristic,ROC)曲线评估生物标志物及提出最优截断点。 结果 AFP-L3和PIVKA在肝硬化组中表达高于肝炎组(P < 0.0001),CK65、CK30和TK在肝硬化组中表达低于肝炎组(P < 0.001)。肝癌组中AFP-L3、CK65、CK30和PIVKA表达显著高于肝硬化组(P < 0.0001),TK在肝癌组中的表达低于肝硬化组(P > 0.05)。在纳入研究的5种生物标志物中,AFP-L3具有最高的特异度(0.89),PIVKAⅡ具有最高的灵敏度(0.62),且联合应用AFP-L3和PIVKAⅡ灵敏度达到0.70,特异度达到0.81,有相较于单个标志物更优的表现。ROC曲线分析表明PIVKAⅡ具有更高的诊断价值(24)。 结论 在肝癌筛查中AFP-L3比PIVKAⅡ特异性高,联合AFP-L3和PIVKAⅡ诊断可其在肝癌中的诊断价值。 -
关键词:
- 肝癌 /
- 甲胎蛋白异质体L3 /
- 维生素K缺乏或拮抗剂-Ⅱ诱导的蛋白质 /
- 诊断价值
Abstract:Objective To investigate the diagnostic value of AFP-L3 and PIVKAⅡ in liver cancer. Methods A total of 3066 patients with chronic liver disease who were admitted to Qingdao Sixth People’s Hospital from January 2019 to January 2022 were selected as objects of the research. The levels of AFP-L3, PIVKAⅡ, CK65, CK30, and TK1 in hepatitis, liver cirrhosis, and liver cancer were compared. The specificity and sensitivity were evaluated, and the ROC curve was used to evaluate the biomarkers and propose the optimal cutoff point. Results The expression of AFP-L3 and PIVKA in the liver cirrhosis group was higher than that in the hepatitis group (P < 0.0001), while the expression of CK65, CK30, and TK in liver cirrhosis group was lower than that in the hepatitis group (P < 0.001). The expression of AFP-L3, CK65, CK30 and PIVKA in the liver cancer group was significantly higher than that in the liver cirrhosis group (P < 0.0001), while the expression of TK in the liver cancer group was lower than that in the liver cirrhosis group (P > 0.05). Among the five biomarkers included in the study, AFP-L3 had the highest specificity (0.89) and PIVKAⅡ had the highest sensitivity (0.62), and the combined application of AFP-L3 and PIVKAⅡ had a sensitivity of 0.70 and a specificity of 0.81, which was better than a single marker. The analysis of ROC curve showed that PIVKAⅡ had a higher diagnostic value (24). Conclusion AFP-L3 is more specific than PIVKAⅡ in liver cancer screening, and the combination of AFP-L3 and PIVKAⅡ diagnosis may have diagnostic value in liver cancer. -
多囊卵巢综合征(polycystic ovarian syndrome,PCOS)是一种以雄激素过高、稀发排卵或无排卵、卵巢多囊改变为特征的病变,病因至今尚不清楚,通常与许多内分泌和代谢紊乱相关,如促黄体生成素(luteinizing hormone,LH)升高、中枢性肥胖、雄激素过高、血脂异常、胰岛素抵抗、2型糖尿病(type 2 diabetes mellitus,T2DM)和高胰岛素血症[1],其中过量的LH和高浓度胰岛素可促进卵巢间质、卵泡细胞合成过多的雄激素。利拉鲁肽是长效的胰高血糖素样肽-1受体激动剂(GLP-1 RA),可以增加胰岛素敏感性,改善中枢性肥胖及非酒精性脂肪性肝脏疾病,并降低心血管疾病(cardiovascular disease,CVD)的风险,有研究表明利拉鲁肽联合二甲双胍在改善PCOS患者内分泌和代谢紊乱时有协同作用[2−3],本研究分析了利拉鲁肽联合二甲双胍改善多囊卵巢综合征患者糖脂代谢、性激素水平及生殖功能的有效性。
1. 资料与方法
1.1 检索方法
在PubMed、万方医学网、万方数据库、CNKI中国知网、维普期刊、谷歌学术、百度学术中进行检索,检索的关键词是:利拉鲁肽、二甲双胍、利拉鲁肽联合二甲双胍、多囊卵巢综合征,检索词之间用 “OR”,英文关键词:Liraglutide,Metformin,Liraglutide Combined with Metformin,Polycystic Ovarian Syndrome(PCOS),文献发表时间为2011年1月至2022年8月。
1.2 纳入及排除标准
纳入标准:(1)所有公开发表的关于利拉鲁肽联合二甲双胍及二甲双胍治疗多囊卵巢综合征的中英文文献;(2)研究对象:临床诊断为多囊卵巢综合征的患者,分为联合治疗组(利拉鲁肽联合二甲双胍组)和对照组(二甲双胍组),为随机对照研究;(3)纳入的研究所包含的具体疗效指标见表1。排除标准:符合以下任意一项则被排除:(1)重复发表的文献;(2)数据不详细或不完整的文献;(3)综述、基础研究类、个案报道、回顾性研究的文献。
表 1 纳入荟萃分析的16篇文献资料Table 1. 16 studies included in the meta-analysis第一作者/发表年份 研究起始时间 联合治疗组(n) 对照组(n) 分组方法 治疗时间(周) 疗效指标 黄昭穗,2015[4] 2011.3 -2014.3 87 85 随机数字表法 24 ①②③④⑤⑥⑦⑧⑨⑩⑪⑫⑬⑭⑮⑯⑰ 郝建民,2020[5] 2017.6 -2018.12 93 93 随机数字表法 12 ①②④⑤⑥⑨⑰ 郑亮,2022[6] 2018.5 -2020.12 75 75 随机抽签法 24 ①②③④⑤⑥⑦⑧⑨⑩⑪⑫⑬⑭⑮⑯⑰ 赵丹,2019[7] 2015.1 -2018.10 30 30 患者选择不同治疗方案 24 ①②③④⑥⑦⑧⑨⑰ 谭明灯,2022[8] 2018.11 -2020.11 46 46 随机数字表法 16 ①②③④⑦⑧⑨⑩⑪⑫⑬⑭⑮⑯⑰ 王爱媛,2020[9] 2018.1 -2020.2 30 30 奇偶数法 4 ①②③④⑥ 杨莉,2022[10] 2018.5 -2020 .550 50 随机数字表法 24 ①②④⑥⑦⑧⑨ 杨茜,2021[11] 2017.3 -2020.3 50 50 奇偶数法 12 ①②④⑤⑥⑦⑧⑨⑭⑮⑯⑰ 张波,2019[12] 2017.1 -2019.1 42 42 随机数字表法 16 ①②③⑩⑪⑫⑬⑰ 宛光彩,2021[13] 2018.1 -2019.1 30 30 随机数字表法 24 ①②③④⑦⑧⑰ 孙海云,2021[14] 2019.3 -2020.3 56 56 随机分组 16 ①④⑤⑥⑦⑧⑨⑰ 孙晖,2020[15] 2018.1 -2020.1 37 37 随机数字表法 24 ①②③④⑦⑧⑨⑭⑮⑰ 仉媛媛,2020[16] 2018.1 -2019.6 41 41 随机分组 12 ①②④⑤⑨ Vesna Salamun,2018[17] 2014.9 -2015.5 13 14 随机分组 12 ①②④⑤⑥⑨⑰ Mojca Jensterle
Sever,2014[18]2011.11 -2012.5 11 14 随机分组 12 ①②④⑤⑥⑨⑪⑫⑬⑰ Chuan Xing,2022[19] 2021.1 -2022.1 27 25 随机分组 12 ①④⑤⑥⑦⑧⑨ 联合治疗组:利拉鲁肽+二甲双胍;对照组:二甲双胍,疗效指标:①空腹血糖,②餐后2 h血糖,③糖化血红蛋白,④胰岛素抵抗指数,⑤空腹胰岛素,⑥BMI,⑦促黄体生成素,⑧促卵泡刺激素,⑨总睾酮,⑩总胆固醇,⑪甘油三酯,⑫低密度脂蛋白,⑬高密度脂蛋白,⑭建立月经周期,⑮正常排卵率,⑯自然受孕率,⑰胃肠道反应。 1.3 数据提取
依据纳入标准及排除标准对所有检索到的文献由2名研究人员进行人工检索,将符合要求的文献资料纳入荟萃分析,提取的资料内容见表1。
1.4 统计学处理
采用ReviewManager5.4软件进行分析,数值资料采用均数差(mean difference,MD)及95%可信区间(95%CI)表示,分类资料采用比值比OR及95%CI表示,若异质性检验结果为P > 0.10、I2 < 50%,可认为多个同类研究具有同质性,采用固定效应模型分析,当异质性检验结果为P ≤ 0.10、I2>50%,可认为多个研究结果有异质性,可使用随机效应模型计算合并统计量。P < 0.05为差异有统计学意义。
2. 结果
2.1 文献检索结果
使用上述关键词在数据库进行检索,共检索到相关文献46篇,其中重复文献资料12篇,对剩余的34篇文献资料进行全文筛选,16篇文献资料符合纳入标准,最终将这16项研究纳入数据分析,共纳入
1436 例患者,研究时间为2011年3月至2022年1月,纳入荟萃分析的文献资料,见表1。2.2 荟萃分析的结果
2.2.1 空腹血糖及餐后2 h血糖
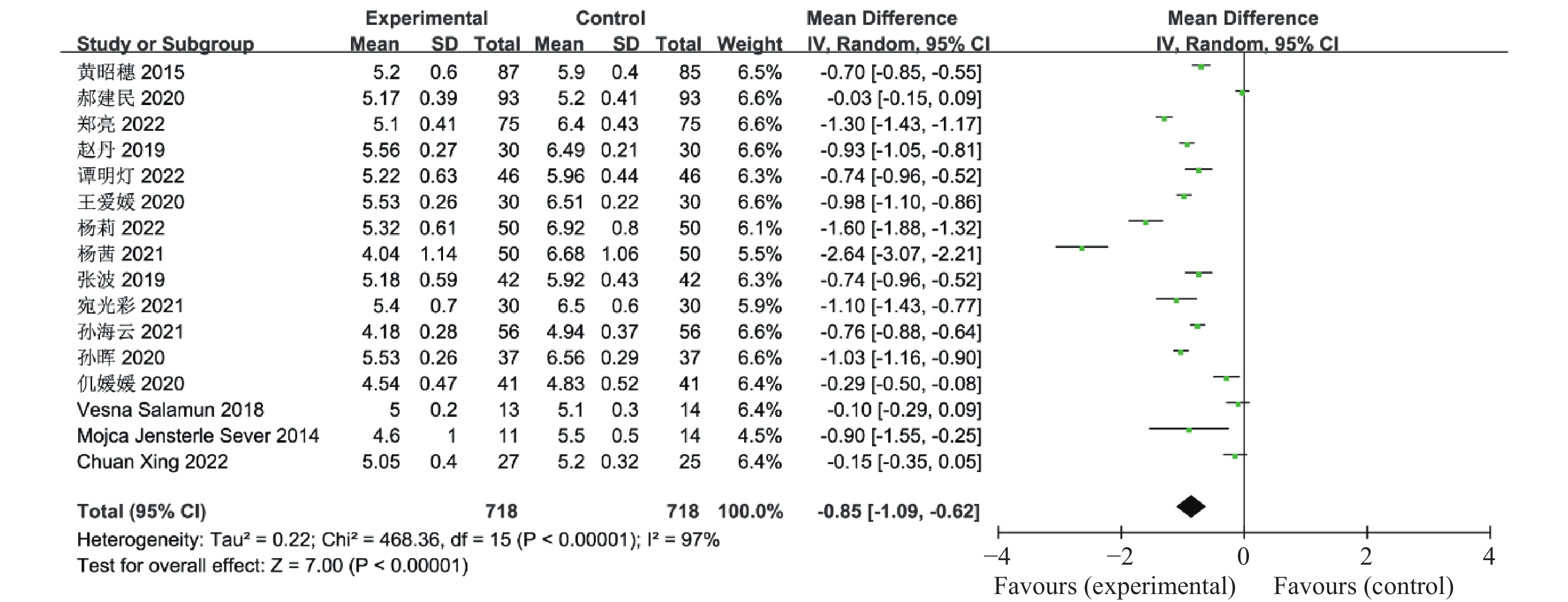
16篇文献报道了联合治疗组及对照组对空腹血糖的影响,其中包括了1 436例患者,异质性检验P <
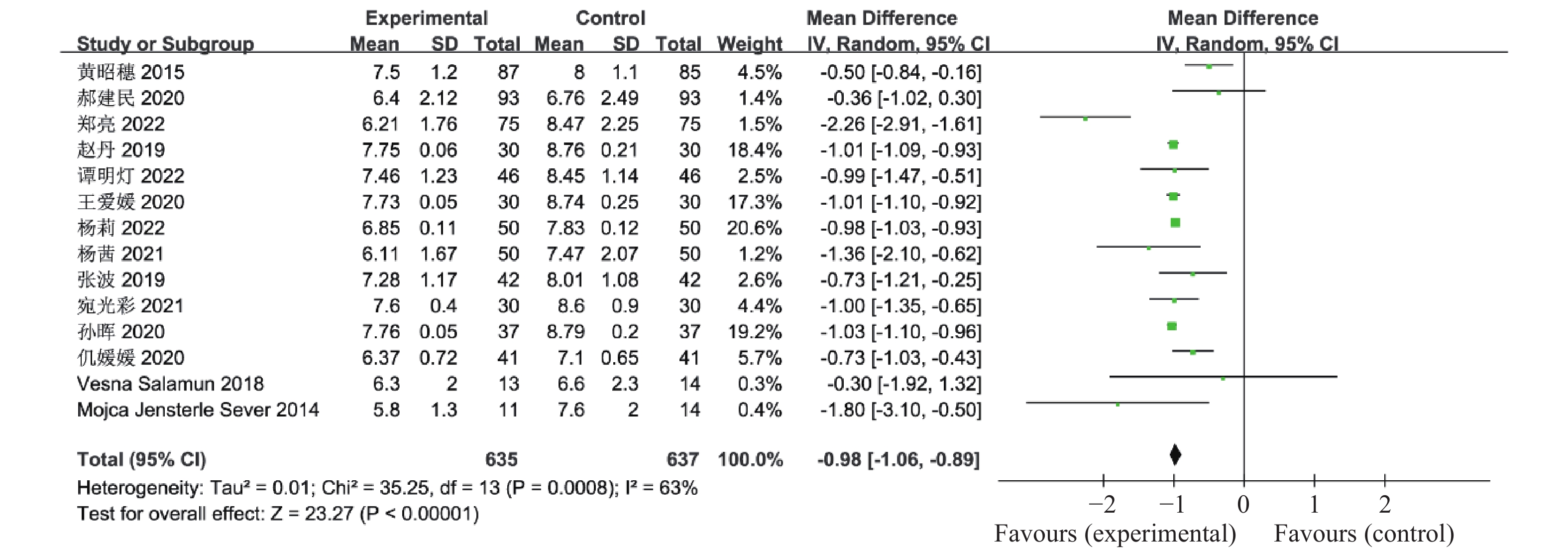
0.00001 、I 2 = 97%,认为这16个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示联合治疗组降低空腹血糖的效果明显优于对照组(OR = -0.85,95%CI -1.09~-0.62,P <0.00001 ),见图1。有14篇文献报道了联合治疗组及对照组对餐后2 h血糖的影响,其中包括了1272 例患者,异质性检验P =0.0008 、I2 = 63%,认为这14个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示联合治疗组降低餐后2 h血糖的效果明显优于对照组(OR = -0.98,95%CI -1.06~-0.89,P <0.00001 ),见图2。2.2.2 糖化血红蛋白(HbA1C)
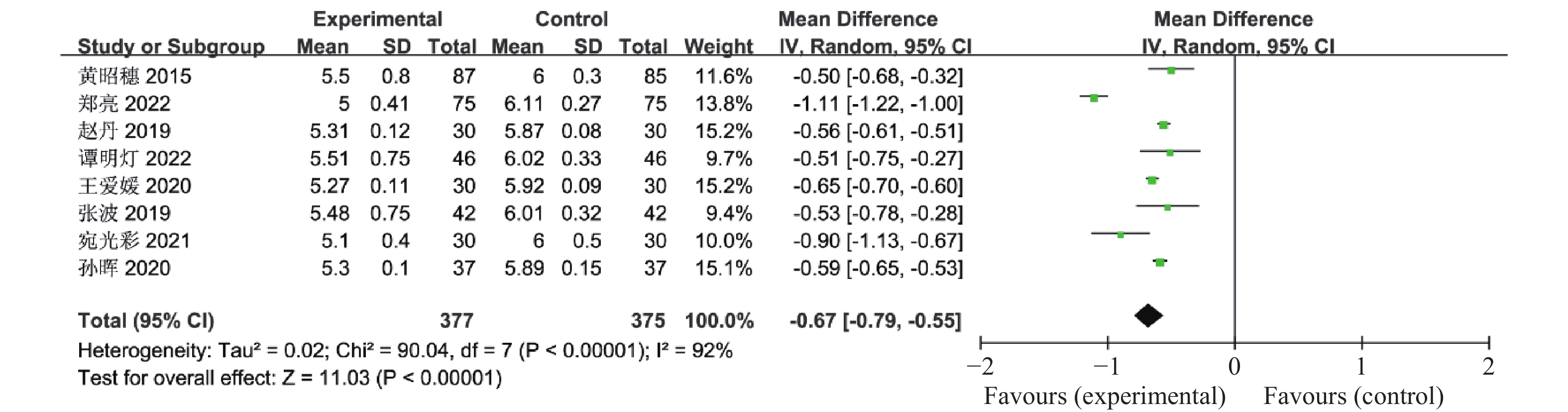
有8篇文献报道了联合治疗组及对照组对糖化血红蛋白(HbA1C)的影响,共752例患者,异质性检验P <
0.00001 、I2 92%,认为这8个研究资料具有异质性,合并效应量OR采用随机效应模型,与对照组比较,联合治疗组可明显降低患者的糖化血红蛋白量(OR = -0.67,95%CI -0.79~-0.55,P <0.00001 ),见图3。2.2.3 胰岛素抵抗指数(HOMA-IR)
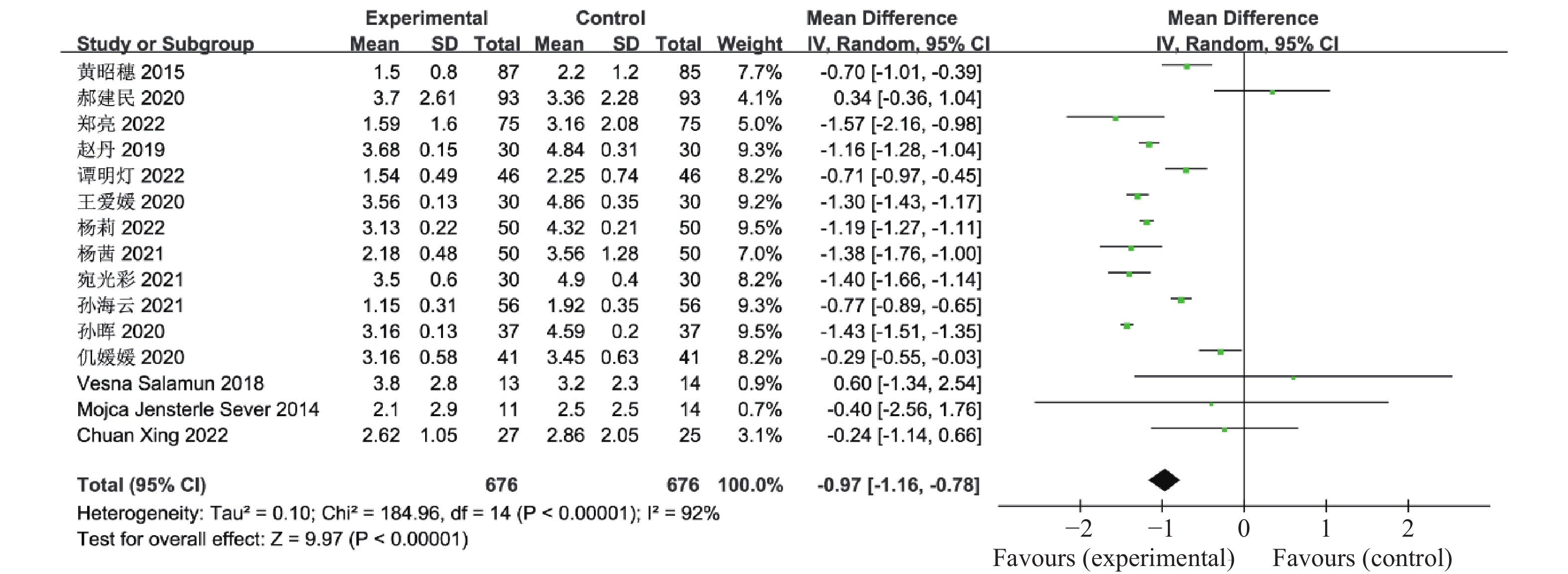
15篇文献报道了联合治疗组及对照组对胰岛素抵抗指数(HOMA-IR)的影响,共
1352 例患者,异质性检验(I2 92%,P <0.00001 )显示各研究间有异质性,采用随机效应模型合并分析,OR合并 -0.97,95%CI -1.16~-0.78,P <0.00001 ,认为联合治疗组可明显降低患者胰岛素抵抗指数(HOMA-IR),见图4。2.2.4 空腹胰岛素( fasting insulin ,FINS)
有8篇文献报道了联合治疗组及对照组对FINS的影响,共794例患者,异质性检验(I2 86%,P <
0.00001 )显示各研究间有异质性,合并效应量OR采用随机效应模型,与对照组比较,联合治疗组可降低患者FINS水平(OR = -2.47,95%CI -3.95~-1.00,P = 0.001),见图5。2.2.5 体重指数( body mass index ,BMI)
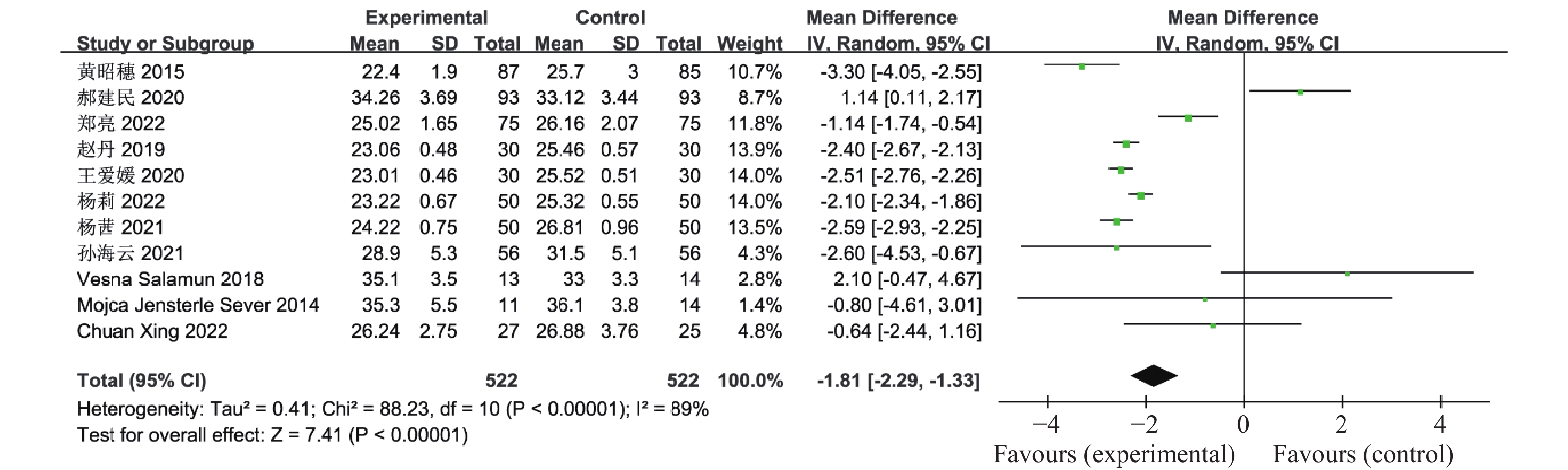
11篇文献报道了联合治疗组及对照组对BMI的影响,共
1044 例患者,异质性检验P <0.00001 、I2 = 89%,认为这11个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示与对照组比较,联合治疗组可显著降低患者BMI值(OR = -1.81,95%CI -2.29~-1.33,P <0.00001 ),见图6。2.2.6 性激素
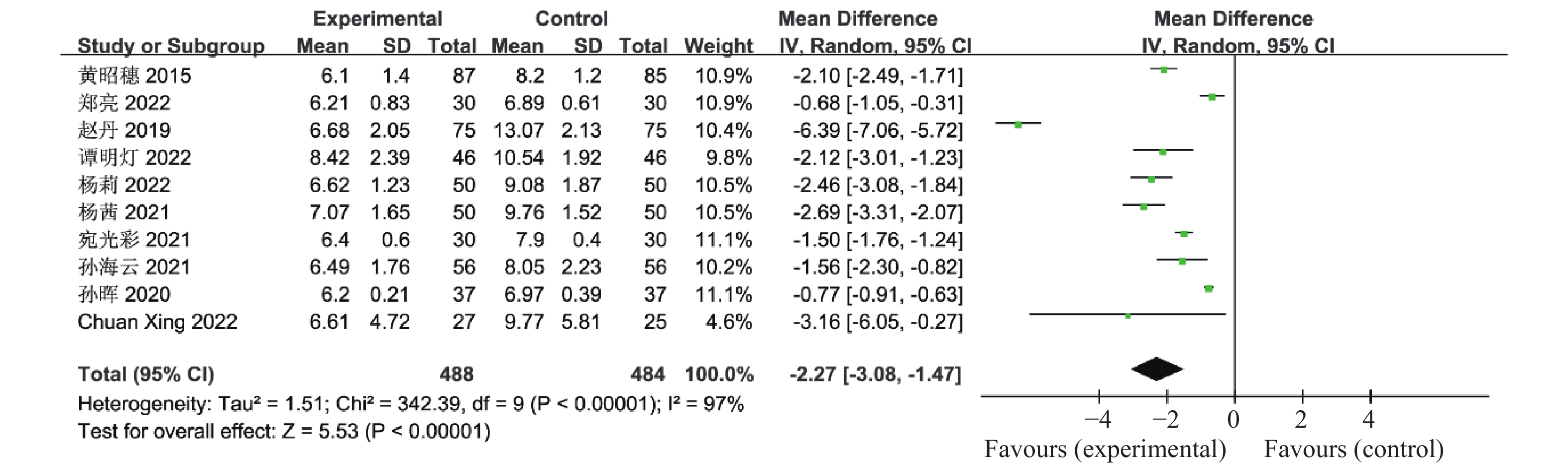
本研究分析了联合治疗组对多囊卵巢综合征患者性激素的影响,其中有10篇文献报道了联合治疗组及对照组对促黄体生成素(LH)的影响,其中包括了972例患者,异质性检验P <
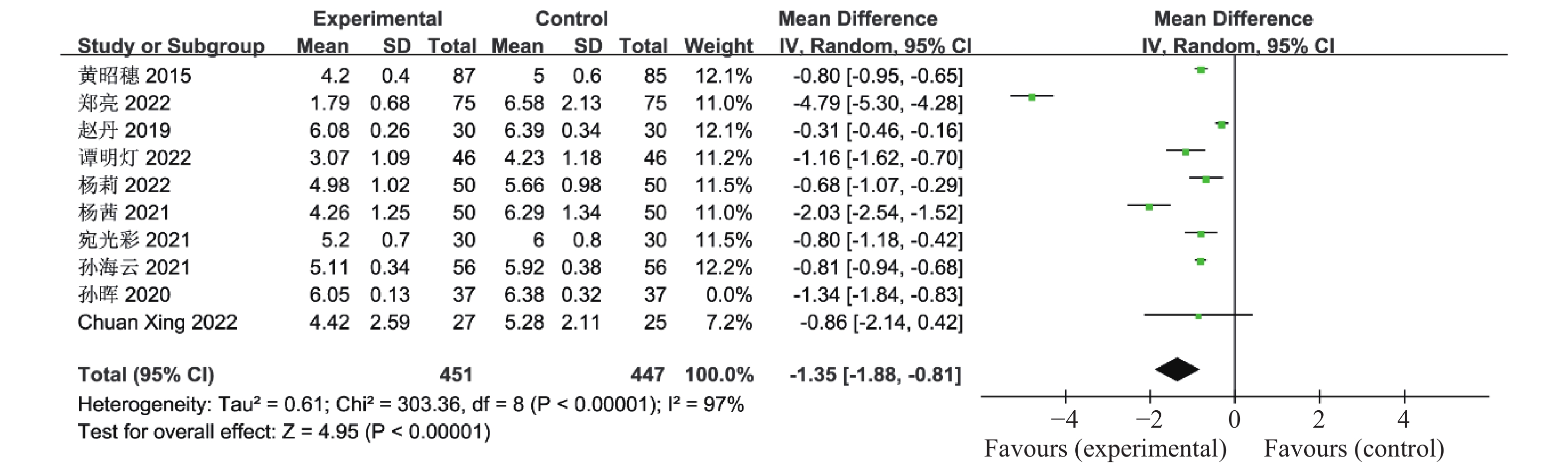
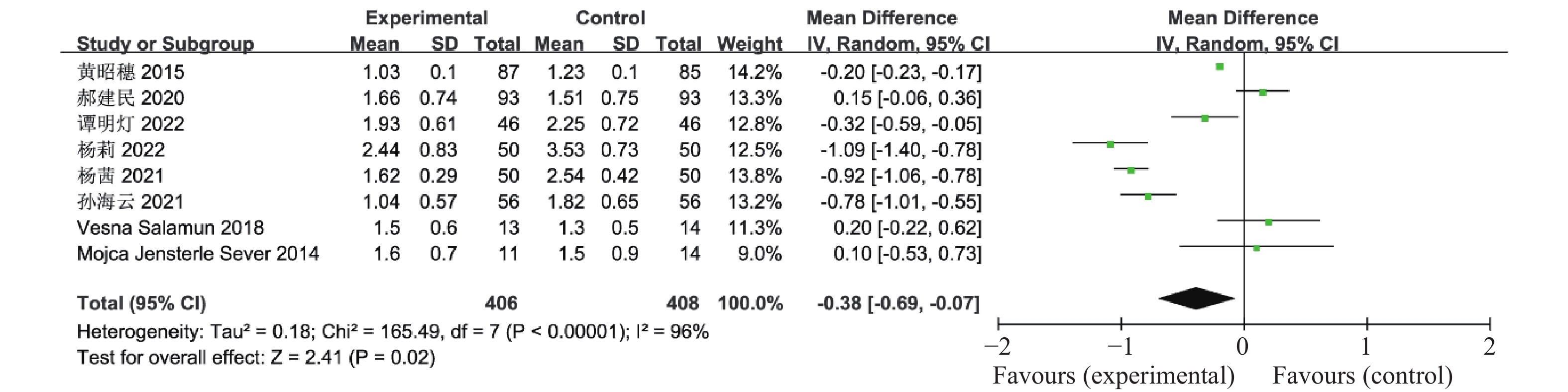
0.00001 、I2 = 97%,认为这10个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示联合治疗组降低LH的效果明显优于对照组(OR = -2.27,95%CI -3.08~-1.47,P <0.00001 ,图7)。有10篇文献报道了联合治疗组及对照组对卵泡刺激素(FSH)的影响,共898例患者,异质性检验P <0.00001 、I2 = 97%,认为这10个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示与对照组比较,联合治疗组可显著降低患者FSH(OR = -1.35,95%CI -1.88~-0.81,见P <0.00001 ),见图8。有8篇文献报道了联合治疗组及对照组对总睾酮的影响,共814例患者,异质性检验P <0.00001 、I2 96%,认为这8个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示与对照组比较,联合治疗组可显著降低患者总睾酮(OR = -0.38,95%CI-0.69~-0.07,P = 0.02),见图9。2.2.7 血脂
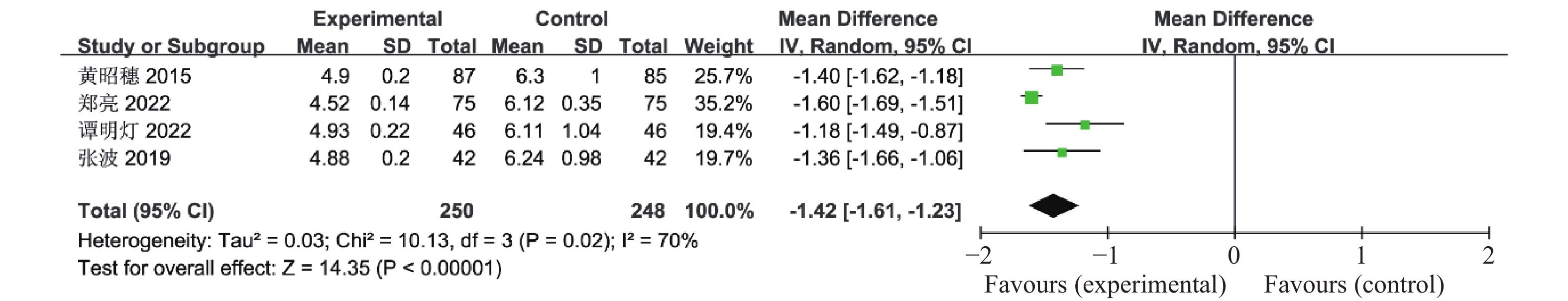
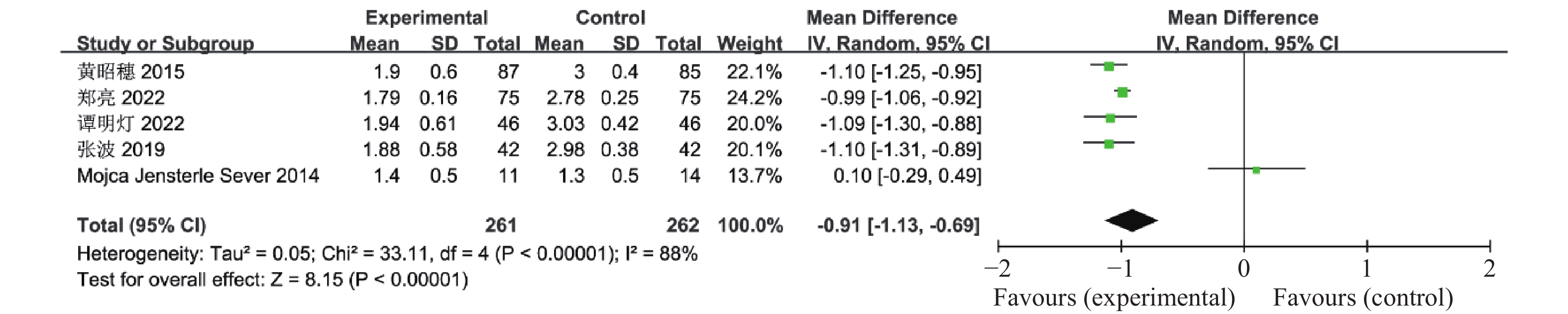
本研究分析了联合治疗组对多囊卵巢综合征患者血脂(总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL-C)、高密度脂蛋白(HDL-C))的影响,其中有4篇文献报道了联合治疗组及对照组对TC的影响,其中包括了498例患者,异质性检验P = 0.02、I2 = 70%,认为这4个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示联合治疗组可显著降低患者TC水平(OR = -1.42,95%CI -1.61~-1.23,P <
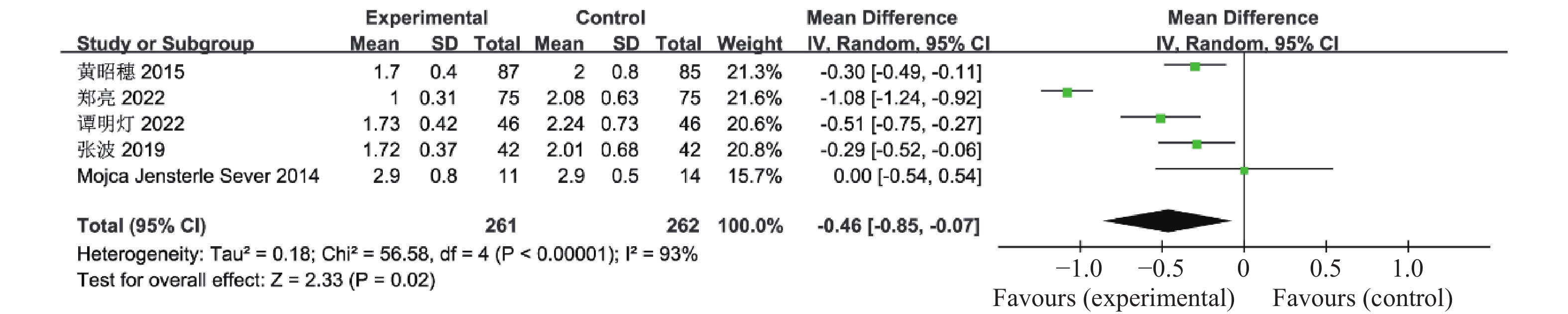
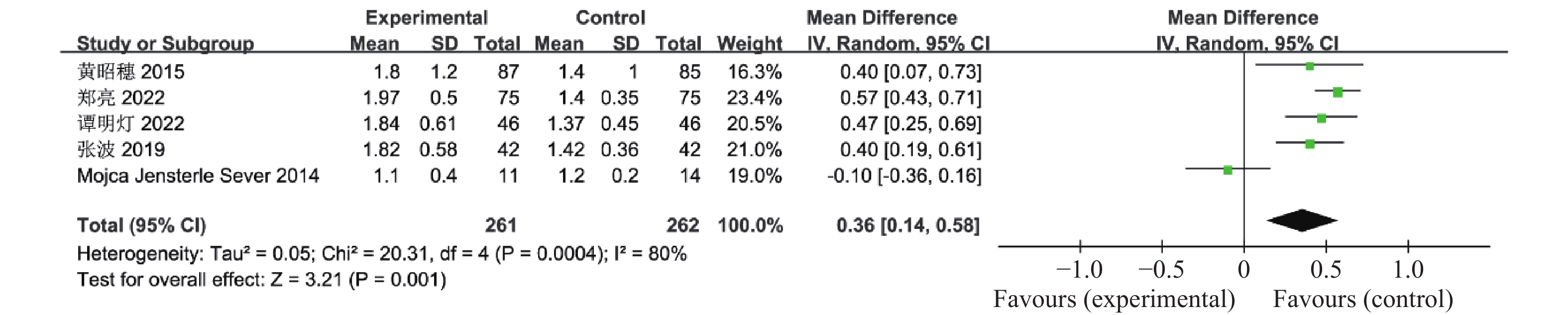
0.00001 ),见图10。有5篇文献报道了联合治疗组及对照组对TG的影响,共523例患者,异质性检验P <0.00001 、I2 88%,认为这5个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示与对照组比较,联合治疗组可显著降低多囊卵巢综合征患者TG水平(OR = -0.91,95%CI -1.13~-0.69,P <0.00001 ),见图11。有5篇文献报道了联合治疗组及对照组对LDL-C的影响,共523例患者,异质性检验P <0.00001 、I2 93%,认为这5个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示与对照组比较,联合治疗组可显著降低患者LDL-C(OR =-0.46,95%CI -0.85~-0.07,P = 0.02),见图12。有5篇文献报道了联合治疗组及对照组对HDL-C的影响,其中包括了523例患者,异质性检验P =0.0004 、I2 80%,认为这5个研究资料具有异质性,因此合并效应量采用随机效应模型,结果显示联合治疗组升高HDL-C的效果优于对照组(OR = 0.36,95%CI 0.14~0.58,P = 0.001),见图13。2.2.8 月经周期
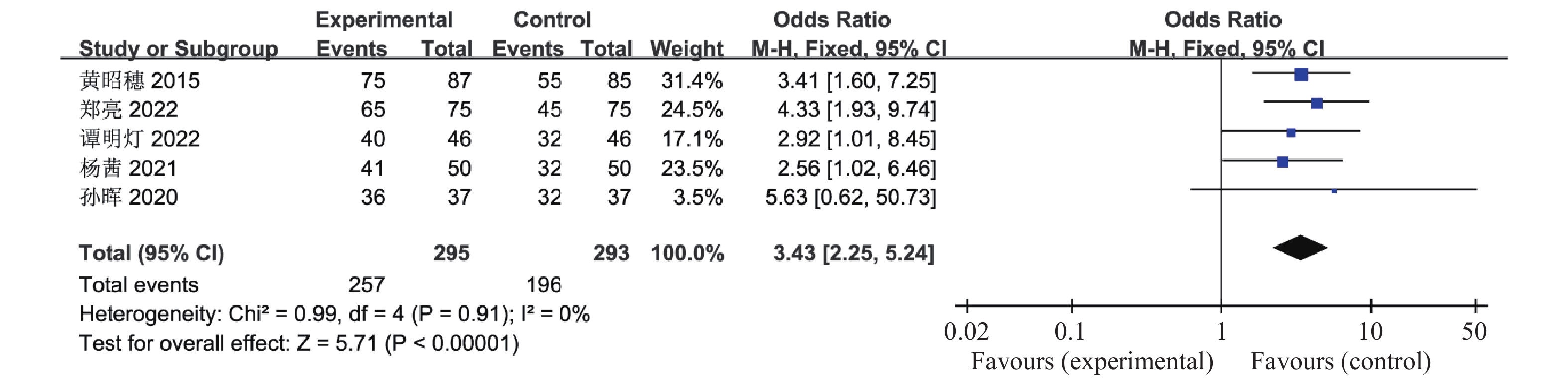
有5篇文献报道了联合治疗组及对照组对多囊卵巢综合征患者月经周期的影响,共588例患者,这5篇研究资料具有同质性(χ2 0.99,I2 0%,P = 0.91),因此合并效应量OR采用固定效应模型,OR合并 = 3.43,95%CI 2.25~5.24,P <
0.00001 ,可认为联合治疗组促使多囊卵巢综合征患者月经周期的建立,见图14。2.2.9 生殖功能
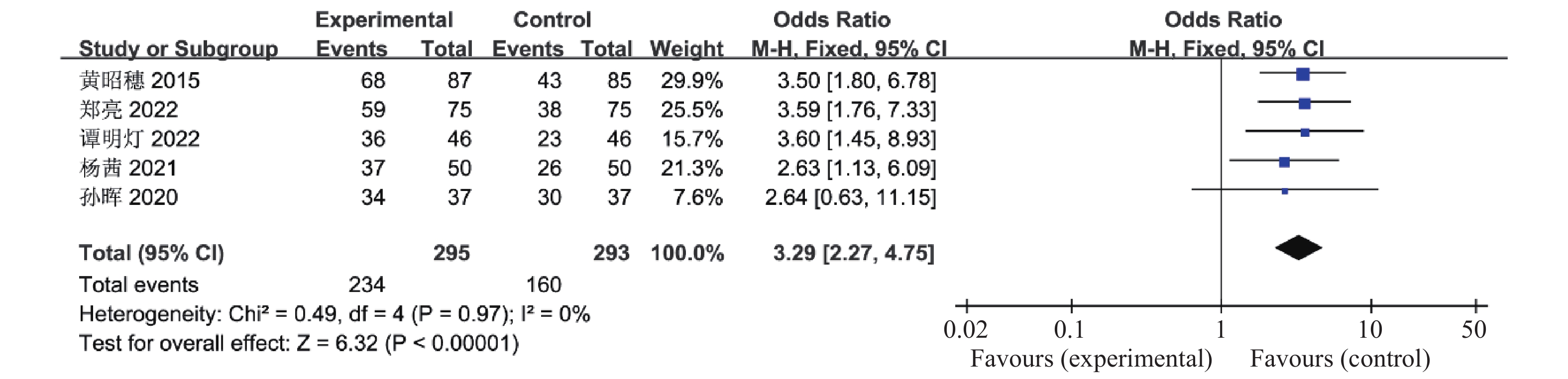
本研究分析了联合治疗组对多囊卵巢综合征患者生殖功能(正常排卵率、自然受孕率)的影响,有5篇文献报道了联合治疗组及对照组对多囊卵巢综合征患者正常排卵率的影响,共588例患者,这5篇研究资料具有同质性(异质性检验χ2 0.49,I2 0%,P = 0.97),因此合并效应量采用固定效应模型,结果分析显示与对照组比较,联合治疗组可提高多囊卵巢综合征患者的正常排卵率(OR = 3.29,95%CI 2.27~4.75,P <
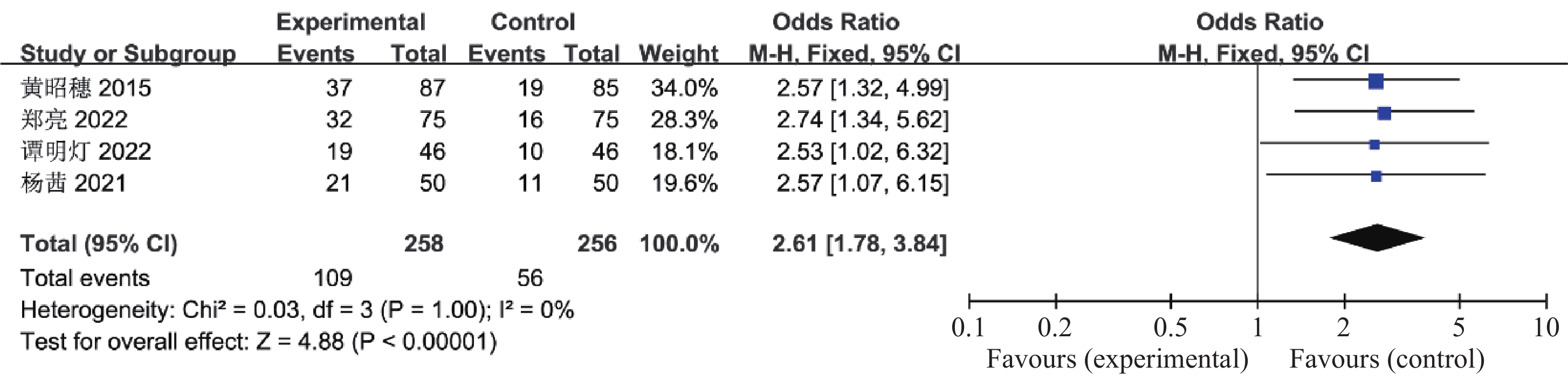
0.00001 ),见图15。有4篇文献报道了联合治疗组及对照组对多囊卵巢综合征患者正常排卵率的影响,共514例患者,异质性检验χ2 0.03,P = 1.00、I2 0%,认为这4个研究资料具有同质性,因此合并效应量采用固定效应模型,结果分析显示与对照组比较,联合治疗组可提高多囊卵巢综合征患者得自然受孕率(OR = 2.61,95%CI 1.78~3.84,P <0.00001 ),见图16。2.2.10 胃肠道反应
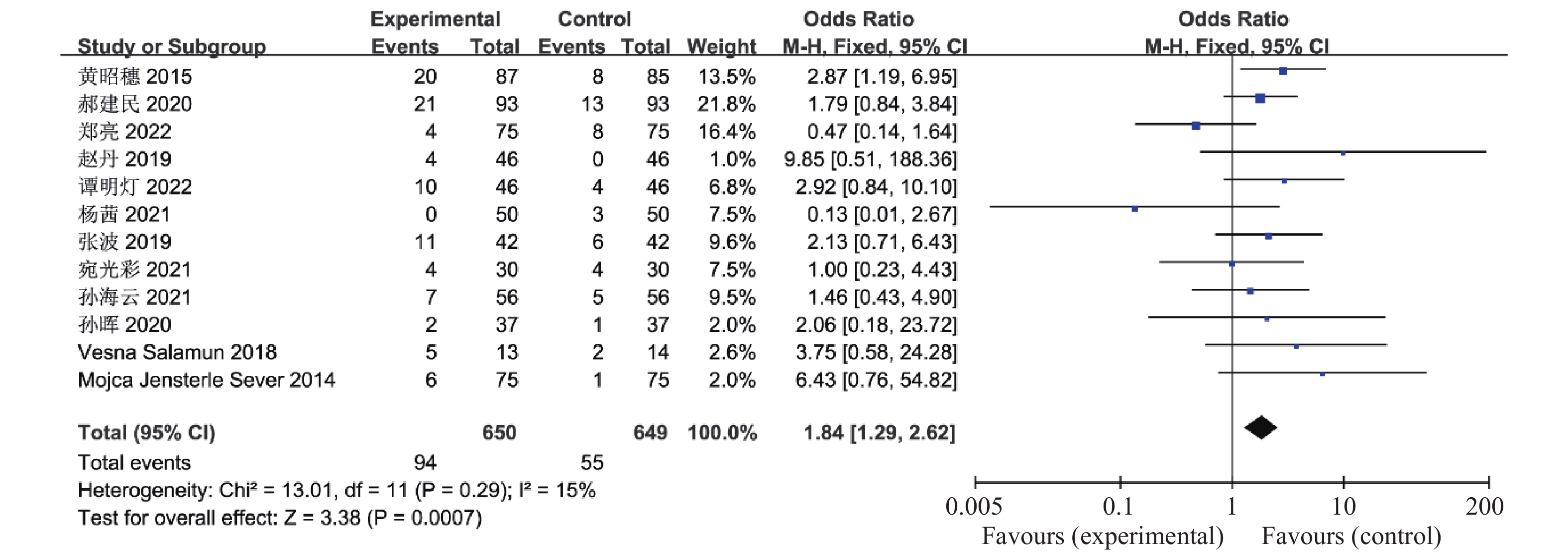
本研究分析了联合治疗组对多囊卵巢综合征患者胃肠道反应的影响,有12篇文献报道了联合治疗组及对照组对多囊卵巢综合征患者胃肠道反应的影响,共
1299 例患者,这12篇研究资料具有同质性(χ2 13.01,I2 15%,P = 0.29,)因此合并效应量OR采用固定效应模型,OR合并 = 1.84,95%CI 1.29~2.62,P =0.0007 ,可认为联合治疗组患者的胃肠道反应明显高于对照组,见图17。2.3 偏倚分析
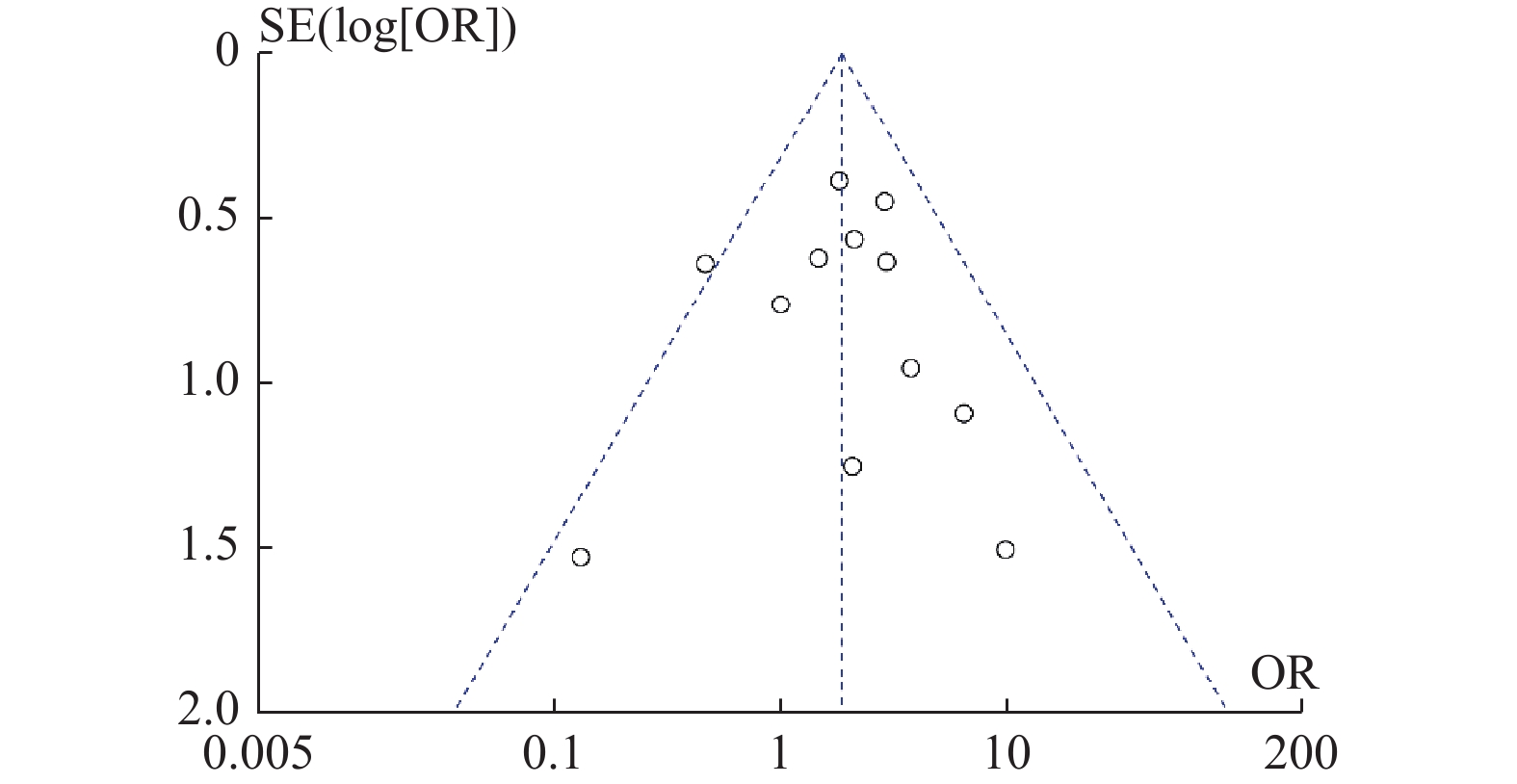
对多囊卵巢综合征患者胃肠道反应相关的12篇已发表的论文做漏斗图观察发表偏倚,图像左右基本对称,可认为该研究发表偏倚的可能性较小,故所得结论相对可靠,绘制的漏斗图见图18。
3. 讨论
多囊卵巢综合征(polycystic ovarian syndrome,PCOS)又称Stein-Leventhal综合征,病因至今尚不清楚,其发病可能与多基因异常和必要的环境因素共同作用有关,发病率逐年上升[20]。近年来胰高血糖素样肽-1受体激动剂(GLP-1 RA)逐渐用于多囊卵巢综合征的治疗,常用的有艾塞那肽(半衰期为2.4 h的短效药物)和利拉鲁肽(半衰期为13 h的长效药物)[3],因利拉鲁肽不会引起低血糖、作用持久、使用便捷,还可以降低心血管疾病(CVD)的风险、减轻体重、改善胰岛素抵抗[21],已逐渐广泛应用于临床。
肥胖与PCOS的发生发展存在相互促进的作用,肥胖患者的胰岛素抵抗及高胰岛素血症促进PCOS的发展,可能的机制是胰岛素抵抗可导致机体代偿性形成高胰岛素血症,过多的胰岛素与LH的协同作用可使卵泡细胞和卵巢间质细胞的合成过多的雄激素,高胰岛素血症可使游离雄激素增加,因此,胰岛素抵抗和高胰岛素血症被认为在多囊卵巢综合征雄激素过量的发病机制中起着核心作用[2],可见PCOS和血糖异常之间有非常明确的联系,胰岛素增敏剂也在PCOS的治疗中应用越来越广泛。二甲双胍可增强胰岛素的敏感性,改善胰岛素的抵抗,同时减少糖异生及促进肠道细胞分泌胰高血糖素样肽-1 [22]。欧洲内分泌学会(european society of endocrinology,ESE)已推荐二甲双胍作为PCOS治疗的的首选药物[23]。利拉鲁肽是1种长效的GLP-1 RA,与人类胰高血糖素样肽-1具有97%的同源性[24],是用于治疗2型糖尿病的新药物,它可增加葡萄糖摄入诱导的内源性胰岛素分泌,抑制胰高血糖素分泌,从而改善葡萄糖稳态,并抑制食欲和胃运动,也被用于肥胖的治疗。1项随机研究显示,利拉鲁肽联合二甲双胍对改善高胰岛素血症和IR有协同作用,联合治疗能够更好地降低雄激素水平[25]。研究发现,利拉鲁肽与二甲双胍联合使用治疗PCOS可能效果会更突出,因为具有协同作用[24],在减轻体重、胰岛素抵抗、高雄激素症和改善基础血糖水平、餐后血糖水平、月经周期及排卵方面,两种药物联合使用被证明优于任何一种单一药物[2-3,24]。减轻体重似乎是GLP-1 RA在PCOS表现中获得有益效果的主要作用,体重减轻5%~10%对多囊卵巢综合征的表现有重要的影响,其中包括生育能力、雄激素水平、高血压、胰岛素敏感性、血糖控制和其他代谢指标的显著改善[26−27]。
利拉鲁肽不会增加低血糖的风险,具有良好的安全性,最常见的不良反应是轻度至中度胃肠道症状(呕吐、腹胀、恶心),胃肠道不良反应呈剂量依赖性,有报道显示使用GLP-1 RA时胃肠道不适的发生率约40%[28],这是多达5%的研究参与者停止治疗的原因。为了减少胃肠道反应的出现,在采用利拉鲁肽联合二甲双胍的治疗方案时,可减少利拉鲁肽的使用剂量,同时显示出更好的抗雄激素作用[25],近年来多家医疗机构的PCOS临床研究试验结果显示,联合治疗后PCOS患者的生殖功能、体重、胰岛素抵抗和CVD生物标志物均有显著改善[24],其他影响包括缓解焦虑、抑郁,增加前驱糖尿病的缓解率,降低游离睾酮和游离雄激素指数,改善血脂异常、异位脂肪堆积及非酒精性脂肪性肝病[1,3,25,28]。本研究有一定的局限性与不足:(1)纳入的研究资料大部分是中文文献,可能存在选择偏倚;(2)纳入的研究资料来自多个研究中心,一致性稍差;(3)荟萃分析的样本量较少,需大样本的随机对照试验研究进一步验证现有的结论。总体而言,利拉鲁肽联合二甲双胍治疗PCOS时具有协同作用,改善多囊卵巢综合征糖脂代谢、性激素水平并提高了排卵率,同时还可预防PCOS的远期并发症。
-
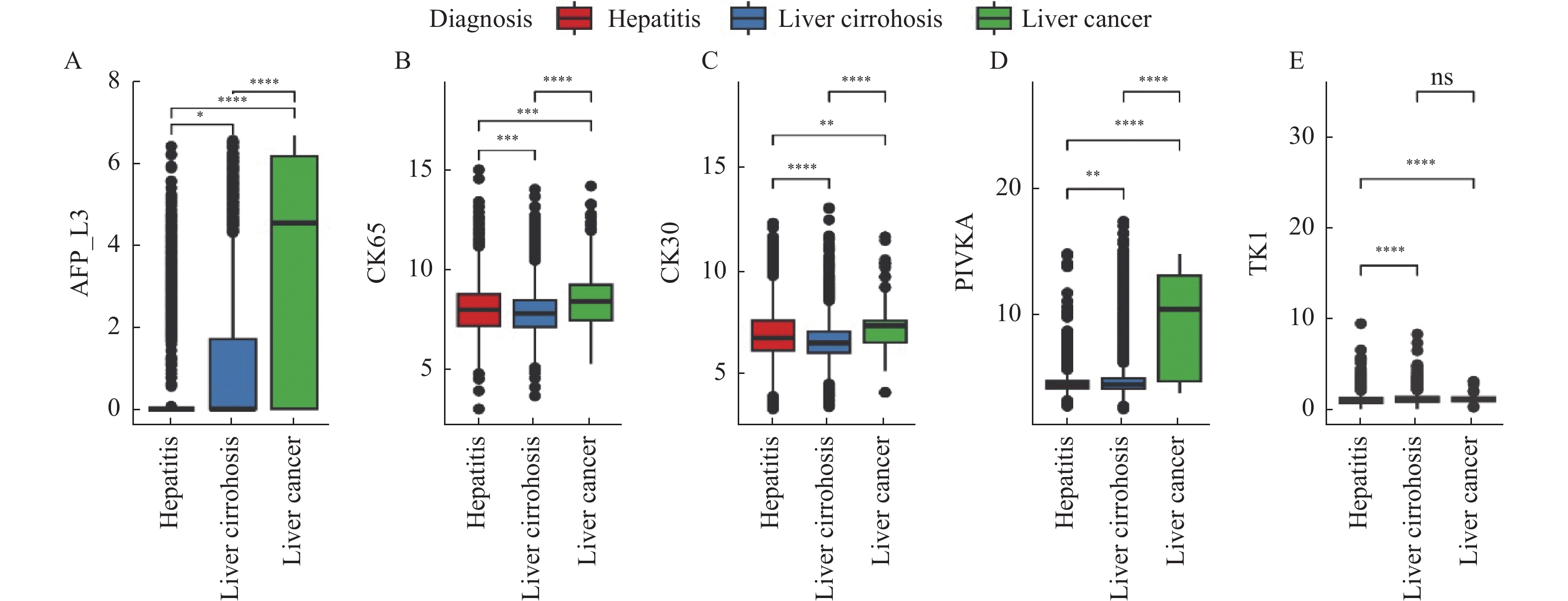
图 1 5种生物标志物在不同肝脏疾病中的测出水平比较
A:AFP-L3;B:CK65;C:CK30;D:PIVKA;E:TK1。图中性别的统计数据表示为[n(%)],年龄、AFP-L3 (%)、PIVKAⅡ (mAU/mL)、CK65 (U/L)、CK30 (U/L)、TK1 (Pmol/L)的统计数据表示为M(P25,P75),*P < 0.05,**P < 0.01,***P < 0.001,****P < 0.0001,ns:差异无统计学意义。
Figure 1. Comparison of measured levels of five biomarkers in different liver diseases
表 1 临床信息与生物标志物在不同肝脏疾病中的总结[n(%)/M(P25,P75)]
Table 1. Summary of Clinical Characteristics and Biomarker Levels [n(%)/M(P25,P75)]
项目 肝炎组(n = 1194) 肝硬化组(n = 1673) 肝癌组(n = 199) 共计(n = 3066) Kruskal Wallis P 性别 女 496 (41.54) 582 (34.79) 12 (6.03) 1090 (35.55) / / 男 698 (58.46) 1091 (65.21) 187 (93.97) 1976 (64.45) 年龄(岁) 48.15 (39.00,57.00) 54.80 (48.00,62.00) 55.17 (48.00,62.00) 52.23 (44.75,61.00) 206.20 < 0.001* AFP-L3 2.2576 (0.00,0.00) 5.1586 (0.00,2.25) 32.44 (0.00,70.30) 5.92 (0.00,2.88) 200.40 < 0.001* PIVKAⅡ 124.98 (17.50,27.00) 1239.51 (17.08,31.38) 6357.29 (26.09,9021.65) 1137.65 (17.67,30.04) 185.10 < 0.001* CK65 502.10 (142.38,432.58) 376.23 (137.39,348.73) 876.49 (163.88,602.46) 457.72 (142.32,392.97) 47.41 < 0.001* CK30 222.41 (69.50,191.44) 159.56 (64.52,130.58) 233.51 (88.66,200.63) 188.84 (66.89,160.22) 78.64 < 0.001* TK1 2.10 (0.57,1.32) 1.80 (0.72,1.50) 1.54 (0.82,1.43) 1.90 (0.67,1.42) 41.65 < 0.001* *P < 0.05。 -
[1] Lee S E,Alcedo K P,Kim H J,et al. Alternative splicing in hepatocellular carcinoma[J]. Cell Mol Gastroenterol Hepatol,2020,10(4):699-712. doi: 10.1016/j.jcmgh.2020.04.018 [2] Wallace M C,Preen D,Jeffrey G P,et al. The evolving epidemiology of hepatocellular carcinoma: A global perspective[J]. Expert Rev Gastroenterol Hepatol,2015,9(6):765-779. doi: 10.1586/17474124.2015.1028363 [3] Anwanwan D,Singh S K,Singh S,et al. Challenges in liver cancer and possible treatment approaches[J]. Biochim Biophys Acta Rev Cancer,2020,1873(1):188314. doi: 10.1016/j.bbcan.2019.188314 [4] Siegel R L,Miller K D,Fuchs H E,et al. Cancer statistics,2021[J]. CA Cancer J Clin,2021,71(1):7-33. doi: 10.3322/caac.21654 [5] Daniele B, Bencivenga A, Megna A S, et al. Alpha-fetoprotein and ultrasonography screening for hepatocellular carcinoma[J]. Gastroenterology, 2004, 127(5 Suppl 1): S108-S112. [6] Liu S,Wang M,Zheng C,et al. Diagnostic value of serum glypican-3 alone and in combination with AFP as an aid in the diagnosis of liver cancer[J]. Clin Biochem,2020,79:54-60. doi: 10.1016/j.clinbiochem.2020.02.009 [7] Ibrahim H M,Elghannam M Z,Elkhawaga O a Y,et al. Evaluation of serum alpha fetoprotein-L3 as an accuracy novel biomarker for the early diagnosis of hepatocellular carcinoma in Egyptian patients[J]. Saudi J Biol Sci,2021,28(10):5760-5764. doi: 10.1016/j.sjbs.2021.06.020 [8] Chaiteerakij R,Zhang X,Addissie B D,et al. Combinations of biomarkers and Milan criteria for predicting hepatocellular carcinoma recurrence after liver transplantation[J]. Liver Transpl,2015,21(5):599-606. doi: 10.1002/lt.24117 [9] Liebman H A,Furie B C,Tong M J,et al. Des-gamma-carboxy (abnormal) prothrombin as a serum marker of primary hepatocellular carcinoma[J]. N Engl J Med,1984,310(22):1427-1431. doi: 10.1056/NEJM198405313102204 [10] 王贵强,王福生,庄辉,等. 慢性乙型肝炎防治指南(2019年版)[J]. 中国病毒病杂志,2020,10(1):1-25. [11] 中国抗癌协会肝癌专业委员会. 中国肿瘤整合诊治指南(CACA)-肝癌部分[J]. 肿瘤综合治疗电子杂志,2022,8(3):31-63. [12] Wei W,Zeng H,Zheng R,et al. Cancer registration in China and its role in cancer prevention and control[J]. Lancet Oncol,2020,21(7):e342-e349. doi: 10.1016/S1470-2045(20)30073-5 [13] Broadfield L A,Duarte J a G,Schmieder R,et al. Fat induces glucose metabolism in nontransformed liver cells and promotes liver tumorigenesis[J]. Cancer Res,2021,81(8):1988-2001. doi: 10.1158/0008-5472.CAN-20-1954 [14] Franssen B,Jibara G,Tabrizian P,et al. Actual 10-year survival following hepatectomy for hepatocellular carcinoma[J]. HPB (Oxford),2014,16(9):830-835. doi: 10.1111/hpb.12206 [15] Zhou J M,Wang T,Zhang K H. AFP-L3 for the diagnosis of early hepatocellular carcinoma: A meta-analysis[J]. Medicine (Baltimore),2021,100(43):e27673. [16] Chen Y,Luo C,Zhao M,et al. Administration of a PTEN inhibitor BPV(pic) attenuates early brain injury via modulating AMPA receptor subunits after subarachnoid hemorrhage in rats[J]. Neurosci Lett,2015,588:131-136. doi: 10.1016/j.neulet.2015.01.005 [17] Li J,Gao T,Gu S,et al. An electrochemical biosensor for the assay of alpha-fetoprotein-L3 with practical applications[J]. Biosens Bioelectron,2017,87:352-357. doi: 10.1016/j.bios.2016.08.071 [18] Wei T,Zhang W,Tan Q,et al. Electrochemical assay of the alpha fetoprotein-l3 isoform ratio to improve the diagnostic accuracy of hepatocellular carcinoma[J]. Anal Chem,2018,90(21):13051-13058. doi: 10.1021/acs.analchem.8b04045 [19] Kotwani P,Chan W,Yao F,et al. DCP and AFP-L3 are complementary to AFP in predicting high-risk explant features: Results of a prospective study[J]. Clin Gastroenterol Hepatol,2022,20(3):701-703.e2. doi: 10.1016/j.cgh.2021.01.043 [20] Fang Y S,Wu Q,Zhao H C,et al. Do combined assays of serum AFP,AFP-L3,DCP,GP73,and DKK-1 efficiently improve the clinical values of biomarkers in decision-making for hepatocellular carcinoma? A meta-analysis[J]. Expert Rev Gastroenterol Hepatol,2021,15(9):1065-1076. doi: 10.1080/17474124.2021.1900731 [21] Abdel-Aziz M M,Elshal M F,Abass A T,et al. Comparison of AFP-L3 and p53 antigen concentration with alpha-fetoprotein as serum markers for hepatocellular carcinoma[J]. Clin Lab,2016,62(6):1121-1129. [22] Hadi H,Wan Shuaib W M A,Raja Ali R A,et al. Utility of PIVKA-II and AFP in differentiating hepatocellular carcinoma from non-malignant high-risk patients[J]. Medicina (Kaunas),2022,58(8):1015. [23] Sun X,Mei J,Lin W,et al. Reductions in AFP and PIVKA-II can predict the efficiency of anti-PD-1 immunotherapy in HCC patients[J]. BMC Cancer,2021,21(1):775. doi: 10.1186/s12885-021-08428-w -






 下载:
下载:

 下载:
下载: