Analysis of Serum 25-Hydroxyvitamin D Levels in Population with Lumbar Disc Herniation in High-Altitude Areas
-
摘要:
目的 探究高海拔地区腰椎间盘突出(LDH)人群血清25羟维生素D(25-OH-D)水平变化及临床意义。 方法 选取2021年8月至2022年7月昆明理工大学附属安宁市第一人民医院高海拔地区200例初治LDH患者作为研究组,另选同期、同年龄段100例健康志愿者作为对照组。比较2组一般资料、血清25-OH-D水平,并比较研究组不同临床特征患者血清25-OH-D水平,分析患者血清25-OH-D水平与临床特征的相关性。研究组经治疗3个月后评估疗效,分析初治LDH患者疗效的影响因素,比较不同疗效患者治疗后血清25-OH-D水平,分析治疗后血清25-OH-D水平与疗效的相关性。 结果 研究组血清25-OH-D水平较对照组低(P < 0.05);研究组血清25-OH-D水平与病情程度、椎间盘退变程度呈负相关(P < 0.05);单因素分析显示,年龄、体重指数、病情程度、椎间盘退变程度、治疗前血清25-OH-D水平与初治LDH患者疗效存在关联性(P < 0.05);多因素分析显示,年龄、体重指数、治疗前血清25-OH-D水平是初治LDH患者疗效的影响因素(P < 0.05);疗效良好患者治疗1个月、2个月、3个月后血清25-OH-D水平较疗效不良患者高,与疗效呈正相关(P < 0.05)。 结论 高海拔地区LDH人群25-OH-D水平降低,与病情程度、椎间盘退变程度密切相关。 Abstract:Objective To investigate the changes in serum 25 hydroxyvitamin D (25-OH-D) levels and clinical significance in people with lumbar disc herniation (LDH) in high altitude areas. Methods A total of 200 newly treated LDH patients from the high altitude area of the First People’s Hospital of Anning City Affiliated to Kunming University of Science and Technology from August 2021 to July 2022 were selected as the study group, and 100 healthy volunteers of the same age at the same period were selected as the control group.The general data and serum 25-OH-D level of the two groups were compared, and the serum 25-OH-D levels of patients with different clinical characteristics in the study group were compared, and the correlation between the serum 25-OH-D levels and clinical characteristics was analyzed. After 3 months of treatment, the efficacy of the study group was evaluated, the influencing factors of the efficacy of LDH patients under initial treatment were analyzed, the serum 25-OH-D levels of patients with different therapeutic effects were compared after treatment, and the correlation between the serum 25-OH-D levels and the efficacy was analyzed. Results The serum levels of 25-OH-D in the study group were lower than those in the control group (P < 0.05); and the serum 25-OH-D level in the study group is negatively correlated with the severity of the disease and the degree of intervertebral disc degeneration (P < 0.05). Univariate analysis showed that age, body mass index, severity of disease, degree of intervertebral disc degeneration, and serum 25-OH-D level before treatment were correlated with the curative effect of LDH patients (P < 0.05). Multivariate analysis showed that age, body mass index and serum 25-OH-D level before treatment were the influencing factors for the curative effect of LDH patients (P < 0.05). The serum 25-OH-D level in the patients with good curative effect was higher than that in the patients with poor curative effect after 1 month, 2 months and 3 months, and was positively correlated with the curative effect(P < 0.05). Conclusions The decrease of 25-OH-D level in LDH population at high altitude is closely related to the degree of disease and disc degeneration. -
随着生育政策及社会经济形态的转变,高龄产妇(年龄≥35岁)数量日益增多。在妊娠及分娩过程中易损伤到盆底结构及功能,患盆底功能障碍性疾病(pelvic fIoor dysfunction,PFD)风险较高。诸多研究发现[1-2],高龄产妇产后患盆底疾病风险远高于适龄产妇,且影响因素较多,一旦发生势必会对产妇生活质量造成严重影响,应给予高度重视。早期评估诊断盆底功能及结构变化对于预防及降低PFD疾病发生有着重要意义。盆底超声为评估PFD疾病的主要辅助检查技术之一,具有安全无创等优势。二维超声[3]、三维超声[4]为临床常用盆底超声技术,可量化评估观察盆底解剖结构形态学变化情况。但由于盆底结构较为复杂,误诊漏诊风险较高,仍需对超声技术诊断效能作进一步明确。基于此,本研究将对比盆底二维,三维超声评估适龄、高龄产妇产后早期盆底结构及功能的变化,旨在明确盆底超声诊断效能,为临床精准诊疗提供参考依据,现报道如下。
1. 资料与方法
1.1 一般资料
选择本院2021年7月至2022年12月就诊的产后早期(6~8周)高龄产妇86例作为观察组,选择同期就诊的产后早期适龄产妇50例作为对照组。观察组年龄35~43岁(38.67±4.35)岁;BMI(24.14±2.58)kg/m2;孕次0~3次(1.38±0.14)次,人工流产史6例;对照组年龄22~34岁(27.15±4.21)岁;BMI(23.97±2.64)kg/m2;孕次0~3次(1.29±0.18)次,人工流产史5例。两组除年龄资料以外各项资料进行匹配,差异无统计学意义(P > 0.05)。
纳入标准:(1)符合盆底超声诊断适应证[5];(2)高龄产妇年龄≥35岁;(3)单胎妊娠、足月、阴道自然分娩;(4)患者家属签署知情同意书。
排除标准:(1)妊娠前存在PFD疾病;(2)存在妊娠合并症、产后大出血、持续恶露、泌尿系统炎症者;(3)既往有盆腔手术史、占位性病变者;(4)产后接受盆底功能恢复治疗者。
1.2 方法
所有研究对象均接受盆底二维、三维超声诊断,所有操作均由同一位超声科医生完成。仪器选择:GE Voluson E10彩色多普勒超声诊断仪,并配备经阴道探头RM6C-D及编码对比成像软件。具体操作如下:叮嘱产妇排空大便,并保持膀胱适度充盈,选择截石体位,保持髋部微曲及轻度外展,充分暴露会阴部。检查者采用耦合剂均匀涂抹于探头表面上,并采用安全套包裹,将探头轻柔置入阴道,对其子宫双附件进行检查后,将其放置于受检者会阴部。首先进行二维超声扫描,选择盆底正中矢状切面(显示膀胱颈、膀胱、尿道、耻骨联合前下缘、后间隙等结构)进行扫描,观察盆底器官位置及运动情况,并于静息状态、Valsalva动作(深吸气后屏气向下用力,持续6 s)下测量膀胱颈位置(bladder neck position,BNP)、膀胱尿道后角(posterior urethravesical angel,PUA),并计算膀胱颈移动度(bladder neck descent,BND)、尿道旋转角(urethral rotation angel,URA)。接着开启三维超声扫描,进行盆底正中矢状切面、肛管横切面扫查(显示耻骨、直肠、尿道、阴道、肛门括约肌、肛提肌等结构),获取肛提肌裂孔图像,测量静息状态、Valsalva动作下肛提肌裂孔前后径 ( levator hiatal anteroposterior diameter,LHAP)、肛提肌裂孔左右径(levator hiatal lateral diameter,LHLP)、肛提肌裂孔面积(levator hiatal area,LHA)。
1.3 观察指标
(1)对比2组产妇盆底二维超声评估参数;(2)对比2组产妇盆底三维超声评估参数;(3)对比盆底二维、三维超声对适龄、高龄产妇产后PFD的诊断效能:以PFD疾病相关权威指南诊断标准(盆腔脏器脱垂[6]、压力性尿失禁等)为金标准,患PFD为阳性,未患为阴性,计算两种技术诊断灵敏度(真阳性/(真阳性+假阴性))、特异度(真阴性/(真阴性+假阳性))及准确性((真阳性+真阴性)/总样本数);(4)盆底二维、三维超声诊断图像。
1.4 统计学处理
将数据纳入SPSS23.0软件中分析,计量资料(盆底二维、三维超声评估参数)比较采用t检验,并以(
$\bar x \pm s$ )表示,计数资料(诊断效能)采用χ2检验,并以率(%)表示,(P < 0.05)为差异有统计学意义。2. 结果
2.1 2组产妇盆底二维超声评估参数比较
观察组静息状态BNP、PUA、Valsalva动作BNP水平、BND水平明显高于对照组(P < 0.05);而Valsalva动作PUA及URA水平对比差异无统计学意义(P > 0.05),见表1。
表 1 盆底二维、三维超声对适龄产妇产后PFD的诊断效能比较(n)Table 1. Comparison of the diagnostic efficacy of two-dimensional and three-dimensional ultrasound (n)诊断技术 金标准 灵敏度(%) 特异度(%) 准确性(%) 阳性 阴性 合计 二维超声 阳性 7 3 10 77.78(7/9) 92.68(38/41) 90.00(45/50) 阴性 2 38 40 合计 9 41 50 三维超声 阳性 8 1 9 88.89(8/9) 97.56(40/41) 96.00(48/50) 阴性 1 40 41 合计 9 41 50 χ2 − − − − 0.400 1.051 1.383 P − − − − 0.527 0.305 0.240 2.2 2组产妇盆底三维超声评估参数比较
观察组Valsalva动作LHAP、LHLP、LHA水平均明显高于对照组(P < 0.05);而静息状态LHAP、LHLP、LHA水平对比差异无统计学意义(P > 0.05),见表2。
表 2 2组产妇盆底二维超声评估参数比较($ \bar x \pm s $ )Table 2. Comparison of the two groups of puerpera pelvic floor two-dimensional ultrasound evaluation parameter between the two groups ($ \bar x \pm s $ )组别 n 静息状态 Valsalva动作 BND(cm) URA(°) BNP(cm) PUA(°) BNP(cm) PUA(°) 观察组 86 −2.34 ± 0.47* 120.47 ± 25.34* −0.59 ± 0.23* 137.45 ± 24.32 1.75 ± 0.35* 30.78 ± 6.53 对照组 50 −3.11 ± 0.56 104.68 ± 20.15 −1.74 ± 0.39 139.54 ± 25.47 1.37 ± 0.44 29.45 ± 5.84 t − 8.577 3.766 21.654 0.475 5.545 1.190 P − <0.001 <0.001 <0.001 0.636 <0.001 0.236 与对照组比较,*P < 0.05。 2.3 盆底二维、三维超声对高龄产妇产后PFD的诊断效能比较
50例适龄产妇中PFD患者9例,膀胱脱垂5例,压力性尿失禁4例,及阴道、直肠脱垂。盆底二维、三维对比无差异(P > 0.05)。86例高龄产妇中PFD患者27例,其中盆底脱垂15例,压力性尿失禁12例。盆底三维超声诊断灵敏度(92.59%)、准确性(91.53%)明显高于二维超声(70.37%、77.91%),P < 0.05,见表3、表4。
表 3 2组产妇盆底三维超声评估参数比较($ \bar x \pm s $ )Table 3. Comparison of pelvic floor three-dimensional ultrasound evaluation parameters between the two groups ($ \bar x \pm s $ )组别 n 静息状态 Valsalva动作 LHAP(cm) LHLP(cm) LHA(cm2) LHAP(cm) LHLP(cm) LHA(cm2) 观察组 86 5.45 ± 1.26 3.01 ± 0.84 16.41 ± 2.54 6.07 ± 1.34* 4.16 ± 1.22* 25.25 ± 2.76* 对照组 50 5.12 ± 1.23 3.07 ± 0.58 15.72 ± 2.36 5.54 ± 1.25 3.73 ± 0.85 20.66 ± 2.52 t − 1.486 0.447 1.567 2.279 2.200 9.649 P − 0.140 0.656 0.119 0.024 0.030 <0.001 与对照组比较,*P < 0.05。 表 4 盆底二维、三维超声对高龄产妇产后PFD的诊断效能比较(n)Table 4. Comparison of the diagnostic effcacy of two-dimensional and three-dimensional ultrasound of pelvic floor for PFD in older women (n)诊断技术 金标准 灵敏度(%) 特异度(%) 准确性(%) 阳性 阴性 合计 二维超声 阳性 19 11 30 70.37(19/27) 70.37(48/59) 77.91(67/86) 阴性 8 48 56 合计 27 59 86 三维超声 阳性 25 5 30 92.59(25/27) 91.53(54/59) 91.86(79/86) 阴性 2 54 56 合计 27 59 86 χ2 − − − − 4.418 2.603 6.525 P − − − − 0.036 0.107 0.011 2.4 盆底二维、三维超声诊断图像
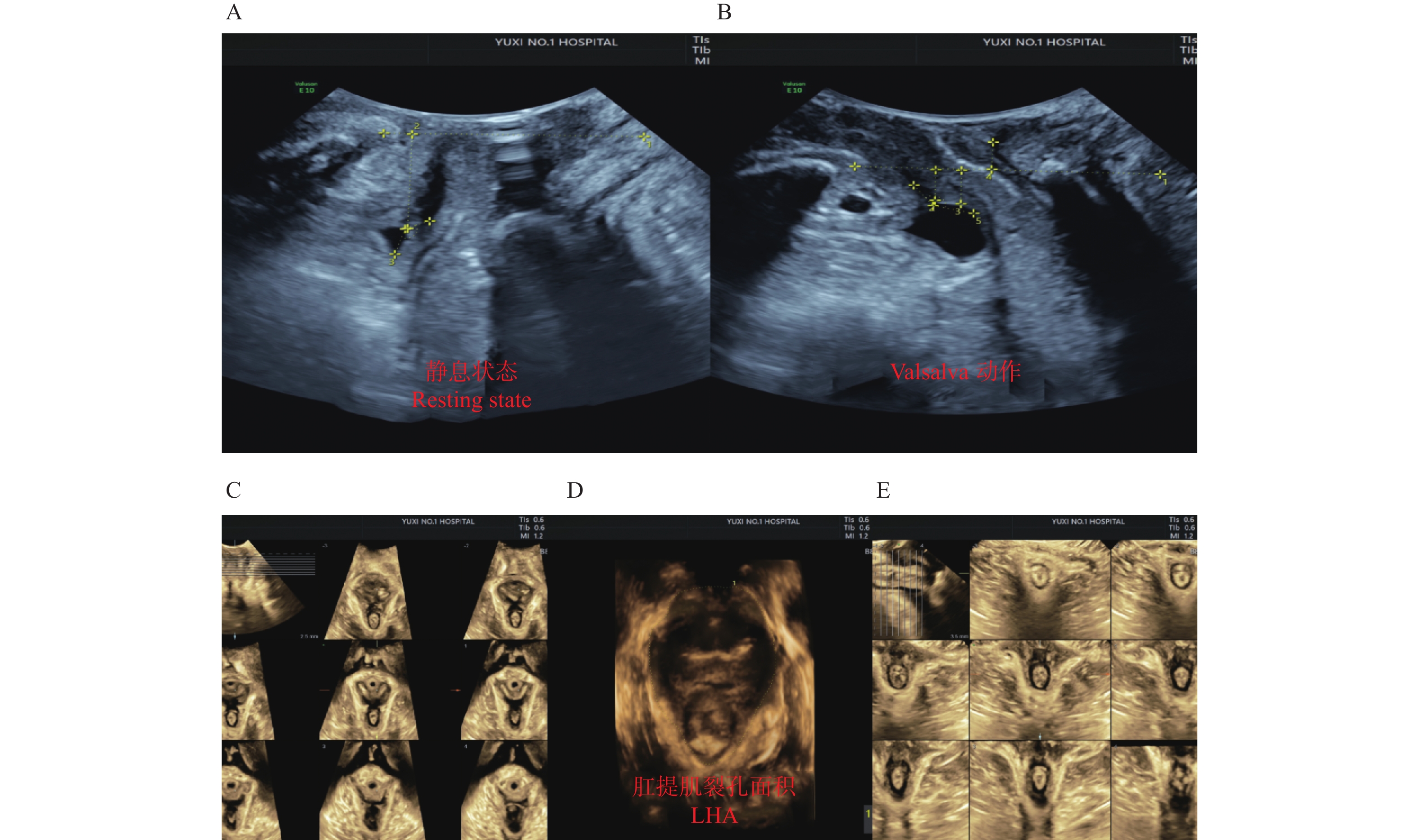
适龄、高龄产妇患者盆底二维、三维超声诊断图像分别见图1、图2,其中A为静息状态下盆底正中矢状切面;B为Valsalva动作下盆底正中矢状切面;C为断层成像模式观察肛提肌连续性,层间距2.5 mm(中间3幅图依次显示耻骨联合开放、正在关闭、已关闭状态;D为肛提肌裂孔;E为断层成像模式观察肛门括约肌连续性,其中左侧为肛门内括约肌下缘,右侧为外括约肌上缘。
3. 讨论
妊娠及分娩为引起女性盆底结构及功能损伤的主要因素,妊娠期间由于子宫体积增长,机体为适应妊娠会出现支持盆腔器官组织过度延伸,达到一定程度时将肌肉将可能丧失收缩恢复能力;分娩过程中阴道周围支持组织受到牵拉、扩张,甚或肌肉纤维断裂,继而导致盆底肌损伤。而进行产后盆底功能检测对于PFD早期诊断及预防有着重要意义。盆底超声为临床产后检查评估盆底结构主要技术,可观察盆底解剖结构形态学变化,继而评估其组织功能状态,为临床诊治及疗效评估提供客观依据。二维经阴道超声是评估的主要筛查工具,具有简单、可重复性、成像清晰等特征,可用于评估膀胱、膀胱颈、尿道等组织形态变化,辅助盆底功能及结构评估[7-9]。三维超声具有较高空间分辨率,可通过多平面成像及图像重建后处理,为临床评估盆底结构及功能提供可靠数据[10-12]。
本研究显示,观察组静息状态BNP、PUA、Valsalva动作BNP水平、BND水平明显高于对照组(P < 0.05);而Valsalva动作PUA及URA水平对比差异无统计学意义(P > 0.05)。观察组Valsalva动作LHAP、LHLP、LHA水平均明显高于对照组(P < 0.05);而静息状态LHAP、LHLP、LHA水平对比差异无统计学意义(P > 0.05)。说明相较于适龄产妇,高龄产妇产后早期更易出现肛提肌、膀胱等盆底组织功能及结构变化,适龄产妇变化不大。李宁等[13]研究报道,高龄产妇的Valsalva动作LHA水平高于适龄产妇,该结果与本研究结果一致。其原因在于相较于适龄产妇,高龄产妇的生理功能出现逐步下降,尤其是盆底肌群收缩反应时间延长,速度减慢,盆底肌肉、神经长时间处于压迫状态,出现盆底组织损伤概率较高;此外盆底肌肉组织中胶原、弹性蛋白含量降低,无法维持正常收缩功能,出现超声异常征象。盆底三维超声诊断灵敏度、准确性明显高于二维超声。此处已删减研究报道,孕妇的盆底肌肉不仅受到与分娩相关的机械损伤的影响,还受到怀孕期间生理变化的影响,继而使得提肌裂孔增大[14]。其原因在于虽然二维超声可以全面评估显示盆底结构,但该技术无法显示示肛提肌、盆膈裂孔等结构,而三维超声可通过多平面成像及图像重建后处理,更加准确、立体显示盆底结构组织及结构变化,该技术对于测量肛提肌裂孔各参数有着较高精确度,其中肛提肌裂孔可进一步反映肛提肌顺应性,继而提高临床诊断效能[15]。
综上所述,高龄产妇产后早期更易出现盆底功能及结构变化,相较于二维超声,盆底三维超声更有助于提高PFD诊断效能。
-
表 1 2组一般资料、25-OH-D水平对比[(
$\bar x \pm s $ )/n(%)]Table 1. General data and comparison of 25-OH-D levels between the two groups [(
$\bar x \pm s $ )/n(%)]项目 研究组
(n = 200)对照组
(n = 100)t/χ2 P 性别 0.817 0.366 男 115(57.50) 52(52.00) 女 85(42.50) 48(48.00) 年龄(岁) 47.26 ± 8.13 45.91 ± 7.86 1.371 0.171 体重指数(kg/m2) 23.46 ± 2.17 23.20 ± 1.95 1.011 0.313 职业类型 0.440 0.507 脑力劳动 120(60.00) 56(56.00) 体力劳动 80(40.00) 44(44.00) 吸烟 1.085 0.298 是 53(26.50) 21(21.00) 否 147(73.50) 79(79.00) 饮酒 0.629 0.533 是 33(16.50) 13(13.00) 否 167(83.50) 87(87.00) 25-OH-D(ng/ml) 20.41 ± 6.18 33.56 ± 8.24 15.488 < 0.001 表 2 研究组不同临床特征患者25-OH-D水平对比(
$\bar x \pm s $ ,ng/mL)Table 2. Comparison of 25-OH-D levels in patients with different clinical characteristics in the study group (
$\bar x \pm s $ ,ng/mL)指标 n 25-OH-D t P 年龄(岁) < 40 86 21.19 ± 6.79 1.504 0.134 ≥40 114 19.82 ± 6.05 体重指数(kg/m2) < 24 126 21.03 ± 6.56 1.794 0.074 ≥24 74 19.35 ± 6.10 性别 男 115 20.86 ± 6.53 1.166 0.245 女 85 19.80 ± 6.11 职业类型 脑力劳动 120 20.79 ± 6.48 1.048 0.296 体力劳动 80 19.84 ± 5.97 病变部位 L3~4 58 20.79 ± 6.32 0.321 0.726 L4~5 65 20.58 ± 6.20 L5~S1 77 19.98 ± 6.04 病情程度 轻度 76 23.51 ± 6.39 21.770 < 0.001 中度 65 20.29 ± 6.02 重度 59 16.55 ± 5.43 椎间盘退变程度 轻度 82 23.74 ± 6.41 28.789 < 0.001 中度 70 19.83 ± 5.97 重度 48 15.57 ± 5.16 表 3 血清25-OH-D水平与临床特征的相关性
Table 3. Correlation between serum 25-OH-D level and clinical features
指标 年龄 体重指数 性别 职业类型 病变部位 病情程度 椎间盘退变程度 25-OH-D r 0.216 0.225 0.193 0.171 0.154 −0.527 −0.584 P 0.103 0.097 0.125 0.184 0.216 < 0.001 < 0.001 表 4 初治LDH患者疗效的单因素分析[(
$\bar x \pm s $ )/n(%)]Table 4. Univariate analysis of curative effect of initial treatment of LDH patients [(
$\bar x \pm s $ )/n(%)]项目 疗效良好(n = 116) 疗效不良(n = 84) t/χ2/u P 性别 0.9 男5 0.339 男 70(60.34) 45(53.57) 女 46(39.66) 39(46.43) 年龄(岁) 44.19±7.25 51.50±8.09 6.702 < 0.001 体重指数(kg/m2) 23.09±1.83 23.97±2.14 3.124 0.002 职业类型 2.494 0.114 脑力劳动 75(64.66) 45(53.57) 体力劳动 41(35.34) 39(46.43) 文化水平 0.560 0.576 初中及小学 21(18.10) 17(20.24) 高中及中专 46(39.66) 35(41.67) 大专及以上 49(42.24) 32(38.10) 吸烟 1.470 0.225 是 27(23.28) 26(30.95) 否 89(76.72) 58(69.05) 饮酒 2.554 0.110 是 15(12.93) 18(21.43) 否 101(87.07) 66(78.57) 治疗期间是否正常工作 1.946 0.163 是 92(79.31) 73(86.90) 否 24(20.69) 11(13.10) 病变部位 0.639 0.523 L3~4 31(26.72) 27(32.14) L4~5 39(33.62) 26(30.95) L5~S1 46(39.66) 31(36.90) 病情程度 3.000 0.003 轻度 54(46.55) 22(26.19) 中度 36(31.03) 29(34.52) 重度 26(22.41) 33(39.29) 椎间盘退变程度 2.593 0.010 轻度 56(48.28) 26(30.95) 中度 39(33.62) 31(36.90) 重度 21(18.10) 27(32.14) 治疗前25-OH-D(ng/m) 22.18±6.28 17.97±5.63 4.885 < 0.001 表 5 初治LDH患者疗效的多因素分析
Table 5. Multi-factor analysis of curative effect of initial treatment of LDH patients
变量 β S.E. Wald χ2 OR 95%CI P 下限 上限 年龄 1.493 0.402 13.790 4.450 2.103 9.415 < 0.001 体重指数 1.206 0.386 9.767 3.341 1.637 6.820 < 0.001 25-OH-D −1.335 0.451 8.762 0.263 0.116 0.597 < 0.001 表 6 不同疗效患者治疗前后血清25-OH-D水平(
$ \bar x \pm s$ ,ng/mL)Table 6. Serum 25-OH-D levels in patients with different therapeutic effects before and after treatment (
$\bar x \pm s $ ,ng/mL)疗效 n 治疗1个月后 治疗2个月后 治疗3个月后 良好 116 22.63 ± 6.42 23.21 ± 6.37 23.58 ± 6.26 不良 84 18.02 ± 5.71 17.86 ± 5.83 18.24 ± 5.77 t 5.247 6.073 6.151 P < 0.001 < 0.001 < 0.001 表 7 治疗后血清25-OH-D水平与疗效的相关性
Table 7. Correlation between serum 25-OH-D level and therapeutic effect after treatment
指标 治疗1个月后 治疗2个月后 治疗3个月后 疗效 r 0.468 0.491 0.523 P < 0.001 < 0.001 < 0.001 -
[1] Rogerson A,Aidlen J,Jenis LG. Persistent radiculopathy after surgical treatment for lumbar disc herniation: causes and treatment options[J]. Int Orthop,2019,43(4):969-973. doi: 10.1007/s00264-018-4246-7 [2] Zhang R,Zhang S J,Wang X J. Postoperative functional exercise for patients who underwent percutaneous transforaminal endoscopic discectomy for lumbar disc herniation[J]. Eur Rev Med Pharmacol Sci,2018,22(1 Suppl):15-22. [3] Ravichandran D,Pillai J,Krishnamurthy K. Genetics of intervertebral disc disease: A review[J]. Clin Anat,2022,35(1):116-120. doi: 10.1002/ca.23803 [4] Yang Q,Liu Y,Guan Y,et al. Vitamin D receptor gene polymorphisms and plasma levels are associated with lumbar disc degeneration[J]. Sci Rep,2019,9(1):7829. doi: 10.1038/s41598-019-44373-2 [5] Martineau A R,Jolliffe D A,Greenberg L,et al. Vitamin D supplementation to prevent acute respiratory infections: individual participant data meta-analysis[J]. Health Technol Assess,2019,23(2):1-44. doi: 10.3310/hta23020 [6] 中华医学会疼痛学分会脊柱源性疼痛学组. 腰椎间盘突出症诊疗中国疼痛专家共识[J]. 中国疼痛医学杂志,2020,26(1):2-6. [7] Pfirrmann C W,Metzdorf A,Zanetti M,et al. Magnetic resonance classification of lumbar intervertebral disc degeneration[J]. Spine (Phila Pa,1976,),2001,26(17):1873-1878. [8] 杜会玲,刘长坯. MRI影像学在游泳运动员腰椎间盘突出病情评估与疗效评价中的应用[J]. 影像科学与光化学,2022,40(6):1581-1585. [9] Kim J H,Ham C H,Kwon W K. Current knowledge and future therapeutic prospects in symptomatic intervertebral disc degeneration[J]. Yonsei Med J,2022,63(3):199-210. doi: 10.3349/ymj.2022.63.3.199 [10] Laasik R,Lankinen P,Kivimäki M,et al. Return to work after lumbar disc herniation surgery: an occupational cohort study[J]. Acta Orthop,2021,92(6):638-643. doi: 10.1080/17453674.2021.1951010 [11] 赵玉敏,胡艳萍. 腰椎间盘突出症合理补充维生素D的临床意义[J]. 中国基层医药,2016,23(23):3. [12] Ertugrul B,Akgun B,Artas G,et al. Evaluation of BMP-2,VEGF,and vitamin D receptor levels in the ligamentum flavum of patients with lumbar spinal stenosis and disc herniation[J]. Turk Neurosurg,2022,32(1):91-96. [13] Liu C,Kuang X,Li K,et al. Effects of combined calcium and vitamin D supplementation on osteoporosis in postmenopausal women: a systematic review and meta-analysis of randomized controlled trials[J]. Food Funct,2020,11(12):10817-10827. doi: 10.1039/D0FO00787K [14] Yang R,Chen J,Zhang J,et al. 1,25-dihydroxyvitamin D protects against age-related osteoporosis by a novel VDR-Ezh2-p16 signal axis[J]. Aging Cell,2020,19(2):e13095. [15] Chang S W,Lee H C. Vitamin D and health-the missing vitamin in humans[J]. Pediatr Neonatol,2019,60(3):237-244. doi: 10.1016/j.pedneo.2019.04.007 [16] Żebrowska A,Sadowska-Krępa E,Stanula A,et al. The effect of vitamin D supplementation on serum total 25(OH) levels and biochemical markers of skeletal muscles in runners[J]. J Int Soc Sports Nutr,2020,17(1):18. doi: 10.1186/s12970-020-00347-8 [17] 赵海洋,朱建民,张银网. 上海地区中老年人维生素D与骨密度之间的相关性调查[J]. 中国骨质疏松杂志,2014,20(3):292-296. [18] Kim T H,Lee B H,Lee H M,et al. Prevalence of vitamin D deficiency in patients with lumbar spinal stenosis and its relationship with pain[J]. Pain Physician,2013,16(2):165-76. [19] Tong T,Liu Z,Zhang H,et al. Age-dependent expression of the vitamin D receptor and the protective effect of vitamin D receptor activation on H2O2-induced apoptosis in rat intervertebral disc cells[J]. J Steroid Biochem Mol Biol,2019,190(1):126-138. [20] 王俊武,陈东,南利平,等. 中老年腰椎间盘退变程度与椎旁肌退变及维生素D水平的相关性研究[J]. 中国脊柱脊髓杂志,2020,30(6):539-545. [21] Plaza-Manzano G,Cancela-Cilleruelo I,Fernández-de-Las-Peñas C,et al. Effects of adding a neurodynamic mobilization to motor control training in patients with lumbar radiculopathy due to disc herniation: a randomized clinical trial[J]. Am J Phys Med Rehabil,2020,99(2):124-132. doi: 10.1097/PHM.0000000000001295 [22] 吴清英. 超声波联合牵引治疗对跳水运动员腰椎间盘突出症的疗效观察[J]. 中国体育科技,2018,54(2):121-124. 期刊类型引用(6)
1. 郑秀艳,陈曦,何扬波,黄磊. 干燥方式对红托竹荪品质特性和微观结构的影响. 现代食品科技. 2024(03): 209-218 .  百度学术
百度学术2. 任梽源,刘新硕,陆时金,杨文智,李海鹰. 谷氨酸铁螯合物对缺铁性贫血小鼠的补铁效果评价. 河北大学学报(自然科学版). 2024(04): 365-372 .  百度学术
百度学术3. 李琳,陈丹,范晓禹,郑喜群,崔素萍. 英国红芸豆抗氧化肽营养价值评价及体外模拟消化分析. 黑龙江八一农垦大学学报. 2024(04): 62-70 .  百度学术
百度学术4. 杨皓博,周铭晗,范文涛. 谷氨酸转运体GLT调控星形胶质细胞与神经元交互作用对癫痫发作的影响. 中国实用神经疾病杂志. 2023(02): 239-244 .  百度学术
百度学术5. 谭智霖,谢琦,廖炎辉,王雅杰,杜磊,陈惠娴. 轻度认知障碍额叶白质~1H-MRS与认知功能的相关性. 磁共振成像. 2021(08): 6-10 .  百度学术
百度学术6. 王慧,段旭艳,陈鲁曼. 产前应激对子代抑郁的影响及其机制的研究进展. 菏泽医学专科学校学报. 2021(03): 85-88 .  百度学术
百度学术其他类型引用(5)
-






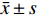
 下载:
下载:
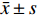
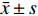
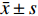
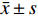


 下载:
下载: 






