Effect of PTEN Gene Expression on Apoptosis of Thyroid Cancer Cells BCPAP and FTC133 and Expression of ERK and AKT
-
摘要:
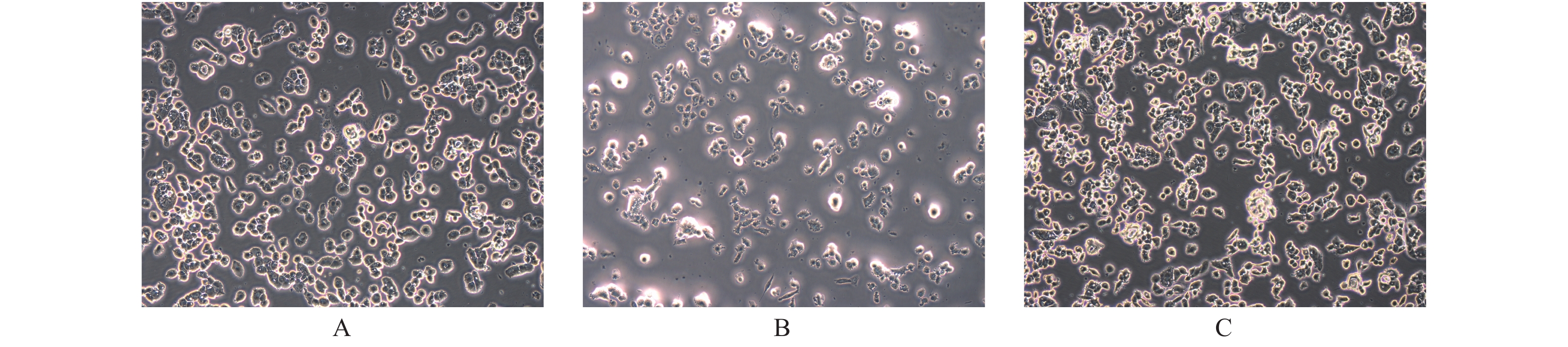
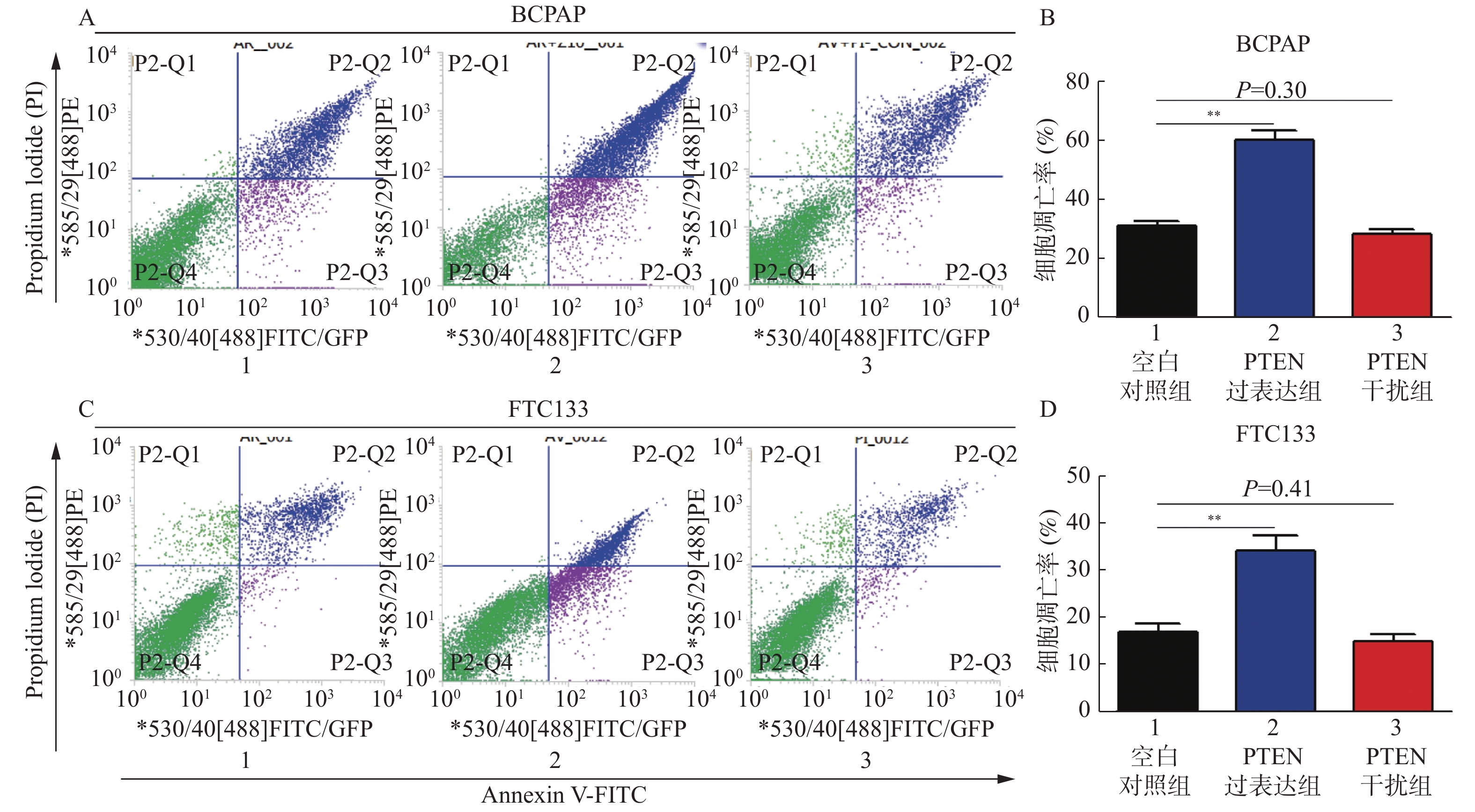
目的 探讨PTEN基因表达对甲状腺癌BCPAP细胞和FTC133细胞凋亡以及信号通路蛋白ERK和AKT表达的影响。 方法 BCPAP细胞和FTC133细胞经PTEN-pCMV6转染和si-PTEN RNA干扰后,光镜下观察细胞形态变化,MTT检测细胞活力,Annexin V-FITC和PI双染色流式细胞仪检测细胞凋亡率,Western blot检测Caspase 8、9、12、3、Bax、Bcl-2、ERK和AKT的表达水平,分析PTEN基因的不同表达与甲状腺癌BCPAP和FTC133细胞凋亡以及信号通路蛋白表达的关系。 结果 与对照组相比较,甲状腺癌BCPAP和FTC133细胞在PTEN基因过表达时,光镜下均出现细胞变形、体积缩小、核固缩等凋亡改变,细胞活力降低(P < 0.01),细胞凋亡率增加(P < 0.01),凋亡蛋白Caspase 8、9、12、3以及促凋亡蛋白Bax表达量增加(P < 0.01),抗凋亡蛋白Bcl-2表达量减低(P < 0.01),ERK和AKT表达量均较对照组减低(P < 0.05),ERK的相对表达量在FTC133细胞的减低程度显著高于BCPAP细胞(P < 0.01),AKT的相对表达量减低程度在BCPAP和FTC133,差异无统计学意义(P > 0.05);PTEN基因干扰表达减低时,光镜下BCPAP和FTC133细胞数目、细胞形态、体积及细胞核形态变化、细胞活力和细胞凋亡率变化,差异无统计学意义(P > 0.05);凋亡蛋白Caspase 8、9、12、3以及促凋亡蛋白Bax表达量减低(P < 0.01),抗凋亡蛋白Bcl-2表达量增加(P < 0.01),FTC133细胞ERK和AKT表达量分别较空白对照组均为增高(P < 0.01),BCPAP细胞ERK表达量较对照组增高(P < 0.01)。而AKT表达量与对照组比较,差异无统计学意义(P > 0.05),ERK的相对表达量增高程度在BCPAP和FTC133,差异无统计学意义(P > 0.05),AKT的相对表达量在FTC133细胞的增高程度显著高于BCPAP细胞(P < 0.05)。 结论 PTEN基因可促进BCPAP和FTC133细胞凋亡,线粒体途径、死亡受体途径和内质网激活通路均参与BCPAP和FTC133细胞凋亡的过程,ERK在PTEN基因调控BCPAP细胞凋亡发挥重要作用,而AKT和ERK均参与PTEN基因促进FTC133凋亡的过程。 Abstract:Objective To investigate the effect of PTEN gene expression on the apoptosis of BCPAP cells and FTC133 thyroid cancer cells and on the expression of signal pathway proteins ERK and AKT. Methods BCPAP cells and FTC133 cells were transfected with PTEN-pCMV6 and silenced si-PTEN RNA, before the cell microscopic morphology changes were observed. Cell viability was measured by MTT, and apoptosis rate was measured by Annexin V-FITC and PI double staining flow cytometer, respectively. Furthermore, the protein expression levels of ERK, AKT, Bax, Bcl-2, caspase 8, 9, 12 and 3 were detected by Western blot. The association between different expression of PTEN gene and the apoptosis of BCPAP and FTC133 thyroid cancer cells and the expression of signal pathway proteins were analyzed. Results Compared with control group, when the PTEN gene was overexpressed, BCPAP and FTC133 thyroid cancer cells showed microscopic apoptotic changes such as deformation, volume reduction and nuclear pyknosis. The cell viability was decreased (P < 0.01), and the cell apoptosis rate was increased (P < 0.01). The expression levels of the apoptotic proteins caspase 8, 9, 12, 3, and proapoptotic protein Bax were significantly increased (P < 0.01), and the expression of anti-apoptotic protein Bcl-2 was significantly decreased (P < 0.01), the expression of ERK and AKT were decreased (P < 0.05). The reduction degree of ERK relative expression in FTC133 cells was significantly higher than that in BCPAP cells (P < 0.01), while the reduction degree of AKT relative expression in BCPAP and FTC133 cells was not statistically significant (P > 0.05). After PTEN gene silencing, compared with the control group, the number, cell morphology, volume and nuclear morphology of BCPAP and FTC133 were not significantly different (P > 0.05). The change of cell viability and apoptosis rate were not significantly different (P > 0.05). The expression levels of apoptotic proteins caspase 8, 9, 12, 3, and proapoptotic protein Bax was significantly decreased (P < 0.01), and the expression level of anti-apoptotic protein Bcl-2 were significantly increased (P < 0.01). The expression levels of ERK and AKT in FTC133 cells were higher than those in the control group (P < 0.01), and the expression levels of ERK in BCPAP cells were higher than those in the control group (P < 0.01). Compared with the control group, there was no statistically significant difference in the expression level of AKT (P > 0.05). The relative expression level of ERK increased in BCPAP and FTC133, but there was no statistically significant difference (P > 0.05). The relative expression level of AKT increased in FTC133 cells than that in BCPAP cells (P < 0.05). Conclusion PTEN gene promotes the apoptosis of BCPAP and FTC133 cells. Mitochondrial pathway, death receptor pathway and endoplasmic reticulum activation pathway are all involved in the process of BCPAP and FTC133 cell apoptosis. ERK plays an important role in PTEN gene regulation of BCPAP cell apoptosis, while AKT and ERK both are involved in the process of PTEN gene promoting FTC133 apoptosis. -
Key words:
- PTEN /
- Thyroid cancer /
- Apoptosis /
- ERK /
- AKT
-
脑科学是近年来我国科学研究的重要方向,探讨脑神经回路的机制和寻找神经疾病的诊疗方案已成为全球神经科学研究领域的共同目标。在神经调控技术中,低强度聚焦超声(low-intensity focused ultrasound,LIFU)是一种新兴无创的治疗方法。LIFU可通过超声波透过颅骨,将声物理效应集中在特定的脑区,从而达到调节大脑活动的目的。LIFU进行神经调控的机制尚不明确,国内外学者的研究发现,不同参数的超声刺激能够兴奋或抑制神经元的活动[1-2],改变受体下游分子活性,导致电压敏感性离子通道的开放或失活[3-4]。LIFU可调控奖励回路,调节蛋白表达水平,这些为相关疾病发病机制的研究提供了理论支撑。
伏隔核(nucleus accumben,NAc)是奖赏环路的核心环节,与动机行为和奖赏行为密切联系,主要涉及药物成瘾、镇痛以及行为活动等,是研究成瘾的关键大脑核团。因此,研究LIFU对NAc的调控作用,可为药物成瘾及脑科学其他疾病提供一种新的治疗思路。c-Fos是一种即刻早期应答基因,可被多种刺激诱导激活,是一种常用的神经元兴奋性标记物[5]。结构可塑性的改变可反应神经元适应和学习记忆的变化[6]。综上,本研究通过LIFU刺激小鼠NAc脑区后,进行c-Fos蛋白测定及超微结构观察结构可塑性的改变,观察超声刺激脑区后神经元激活和结构改变情况,初步探讨超声进行神经调控的机制,为后续超声神经调控治疗脑疾病的研究提供实验依据。
1. 材料与方法
1.1 材料
1.1.1 实验动物及分组
选用SPF级的体重18~22 g(6~7周龄),雄性C57 BL/6小鼠18只(湖南斯莱克景达实验动物有限公司)。在SPF级环境下适应性饲养1周,自由进食和饮水。实验已通过昆明医科大学伦理委员会审批(审批号kmmu 2021265)。随机分成超声刺激组12只、假刺激组6只。
1.1.2 主要仪器与试剂
超声神经刺激仪(中国科学院深圳先进技术研究院),小动物麻醉机SA420(江苏塞昂斯生物科技有限公司,中国),倒置激光共聚焦显微镜N-SIM/C2 si(尼康株式会社,日本),数显脑立体定位仪SA301(江苏塞昂斯生物科技有限公司,中国),兔抗c-Fos 多克隆抗体(Abbkine公司,美国,ABP0071),IFKine驴抗兔IgG二抗(Abbkine公司,美国,A24221),FD Rapid GolgiStainTM Kit试剂盒(上海玉博生物科技有限公司,中国)。
1.2 方法
1.2.1 超声刺激
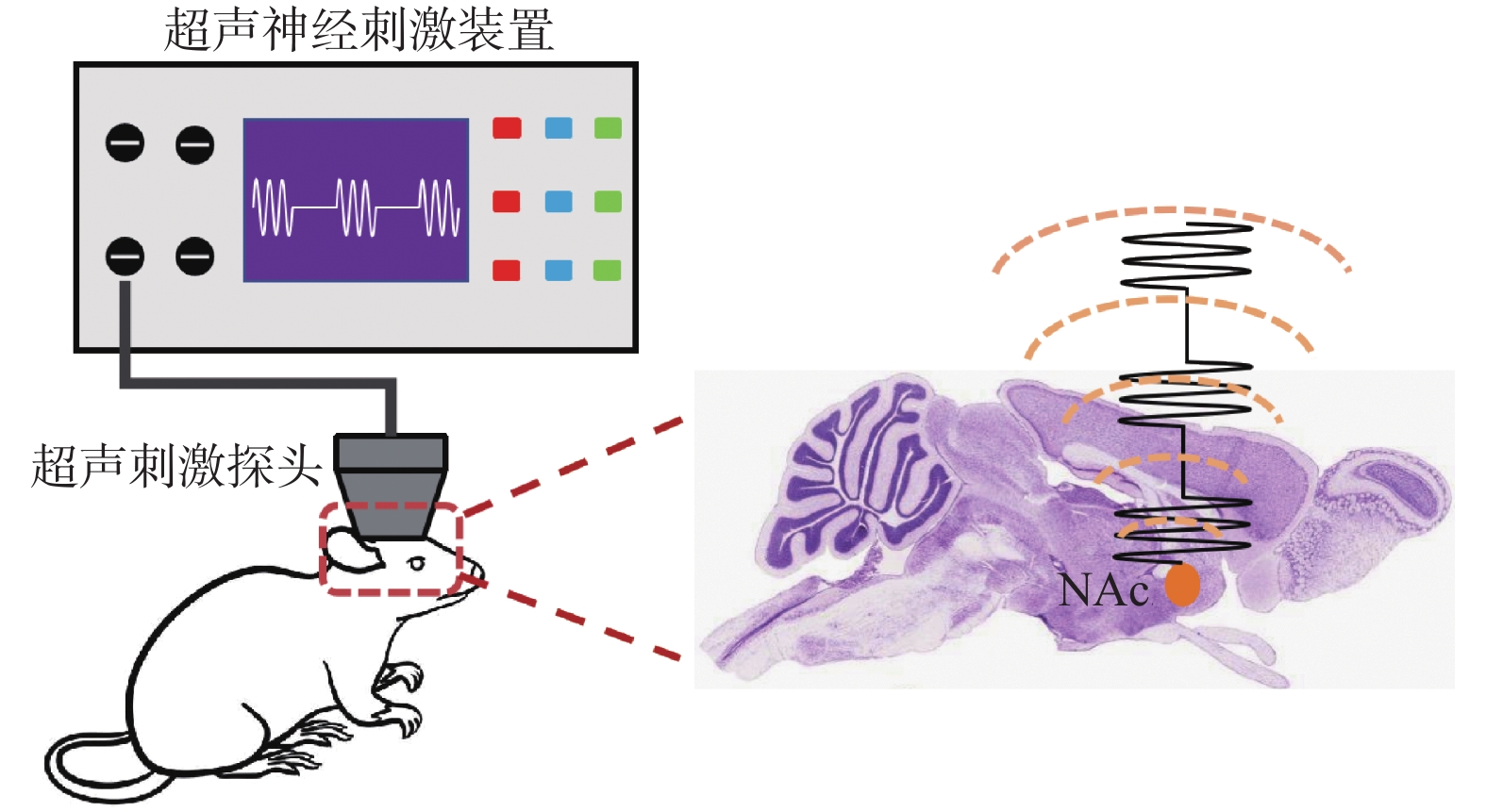
18只小鼠由呼吸面罩异氟烷麻醉后,将头部固定于脑立体定位仪上,暴露前囟,把超声刺激探头对准NAc坐标(以Bregma为坐标原点M/X:+0.5 mm,A/P:+1.18 mm,D/V:-4.50 mm)进行超声调控,见图1,超声刺激组超声调控参数为:探头频率0.5 MHz,脉冲重复频率(pulse repetition frequency,PRF)1 000 Hz,脉冲声压590 kPa,占空比为50%,刺激时间为每天10 min,持续7 d。假刺激组将超声刺激探头置于相同位置,不开电源无输出功率。18只小鼠均顺利完成整个超声刺激过程,刺激过程中无死亡或其他异常情况。
1.2.2 免疫组化测定c-Fos蛋白
最后一次刺激结束后,8%水合氯醛(0.35 mL/100 g)腹腔注射麻醉后灌注取脑,使用4%多聚甲醛4 ℃固定24 h,经15%蔗糖溶液脱水、30%蔗糖溶液梯度脱水沉底后,取出脑组织,用吸水纸吸干表面蔗糖溶液,使用OCT包埋,-22 ℃冰冻切片,片厚20 µm。0.3% Triton溶液常温孵育10 min,PBS清洗后羊血清封闭1.5 h。c-Fos兔抗多克隆抗体(1∶200)-抗,4 ℃孵育,过夜。驴抗兔IgG二抗(1∶500),常温避光孵育1.5 h。轻轻甩干后,滴入抗荧光衰减封片剂(含DAPI),封片固定。将免疫荧光染色样本置于激光共聚焦显微镜下观察,低倍镜下(蓝色荧光场)找到NAc并观察,每个标本随机取2~4个高倍视野(10×40)曝光。利用Image J软件对图片进行c-Fos阳性神经元统计,计算阳性神经元比例做归一化处理。
1.2.3 切片、高尔基染色及病理观察
最后一次刺激结束后,腹腔注射水合氯醛麻醉后灌注取脑,将脑组织浸泡在FD Rapid GolgiStainTM Kit试剂盒等体积的Solutions A 与 Solutions B 混合溶液,24 h后,换液1次,室温避光保存14 d,然后取出脑组织转至Solutions C,24 h后,换液1次,室温,避光保存2 d;使用OCT包埋,-22 ℃冰冻切片,片厚100 µm,切片放置湿盒中,避光常温15~30 min;按1∶1∶2的比例配置Solutions D,Solutions E与双蒸水混合液,然后混合液滴在脑切片上显色10 min。
将高尔基染色后的样本置于倒置激光共聚焦显微镜系统中扫描拍摄,先在低倍镜下寻找NAc,然后切换到高倍镜(40×倍镜)采集NAc神经树突、树突棘图像。利用Image J软件对图片NAc神经元树突长度进行测量,计算平均树突长度(µm/50个神经元);对固定单位内树突棘数量进行计数,计算树突棘密度(个/µm)。
1.3 统计学处理
实验数据使用 SPSS 25.0软件进行统计分析。正态分布的计量资料采用t检验,以
$\bar x \pm s $ 表示,非正态分布的计量资料采用秩和检验,以[M(P25,P75)]表示。P < 0.05为差异有统计学意义。2. 结果
2.1 超声刺激后c-Fos改变
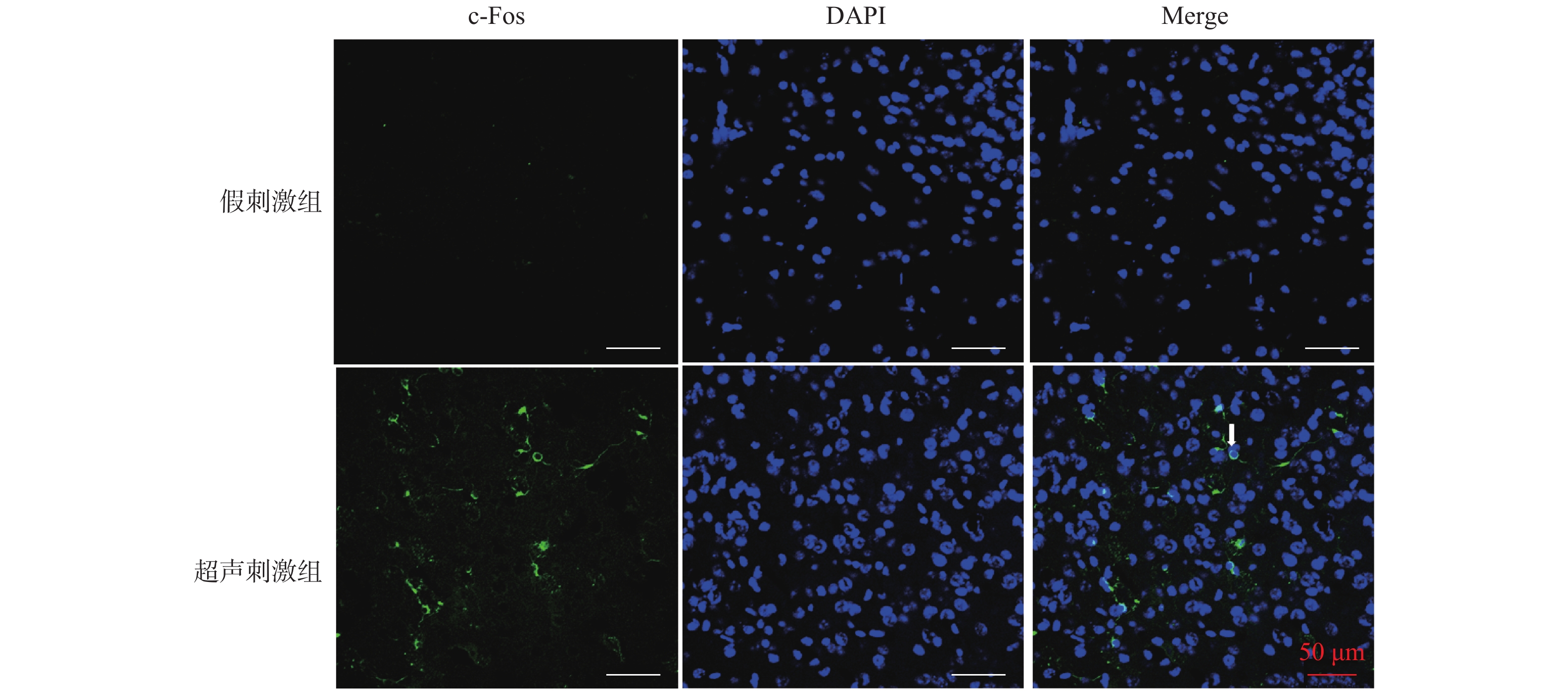
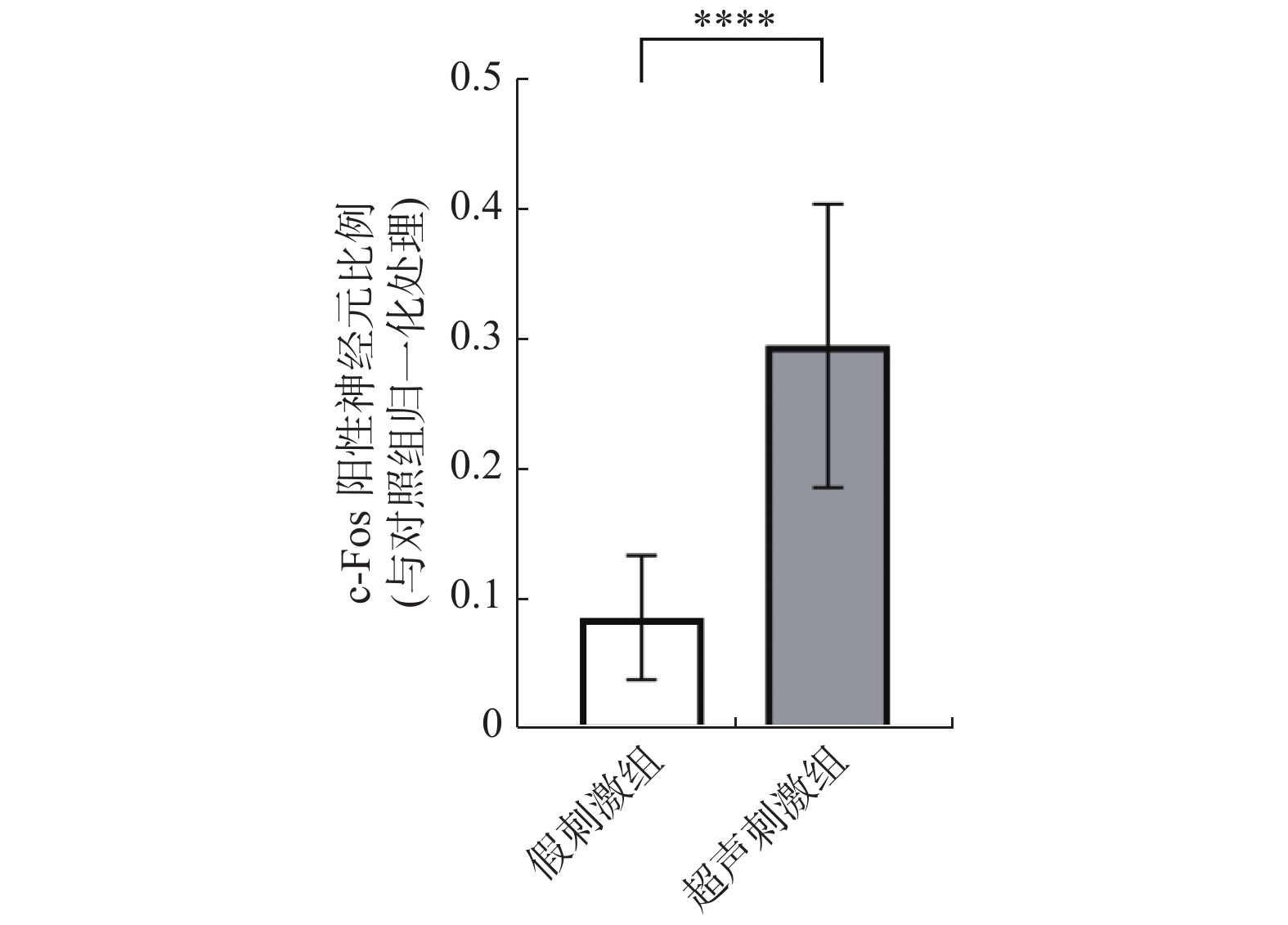
DAPI条件下所显示的为细胞核(蓝色),FITC条件下所显示的为神经元表达c-Fos蛋白(绿光),Merge为前两者组合,见图2白色箭头所示。超声刺激组表达c-Fos的神经元比例为(29.9±12.9)%,假刺激组比例为(6.3±5.8)%,2组相比,超声刺激组明显高于对照组,差异有统计学意义(P < 0.001),见表1、图2、图3。说明LIFU刺激后NAc区神经元c-Fos的表达比例显著提高。
表 1 小鼠NAc区 c-Fos阳性神经元比例统计分析($\bar x \pm s $ )Table 1. Statistical analysis of the proportion about c-Fos positive neurons in the NAc ($\bar x \pm s $ )组别 n c-Fos阳性神经元比例(%) 假刺激组 30 8.58 ± 4.78 超声刺激组 30 29.50 ± 10.91**** 与假刺激组比较,****P < 0.0001。 2.2 超声刺激后超微结构改变
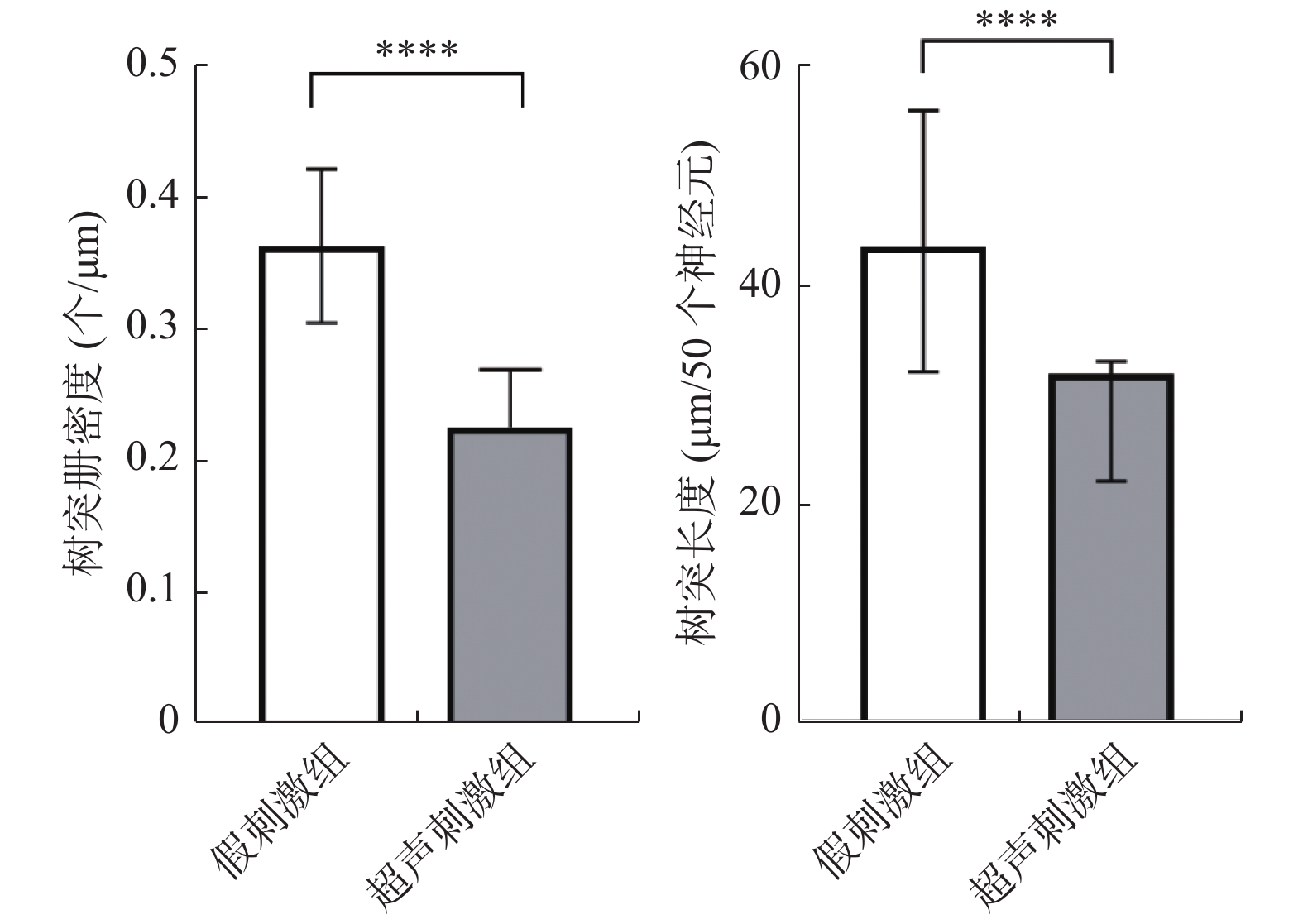
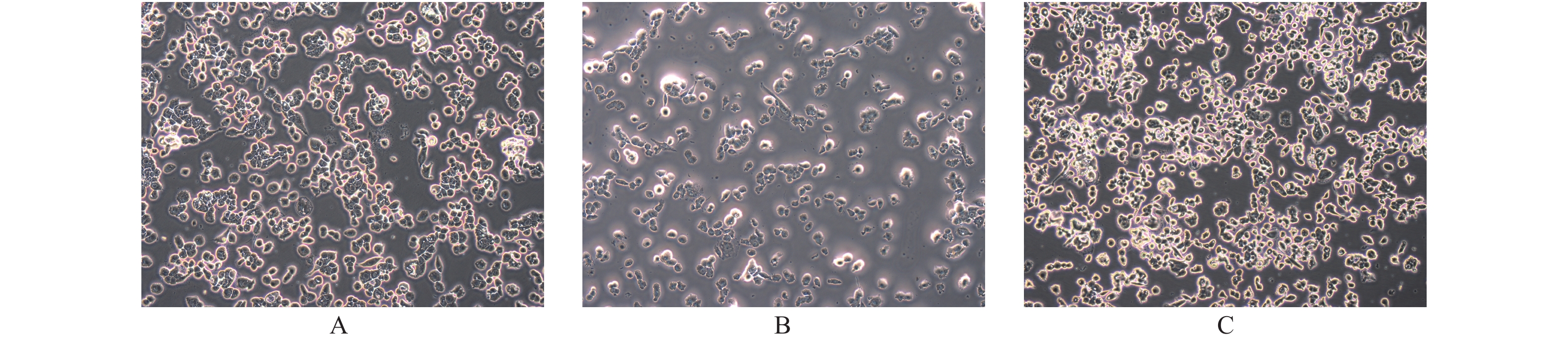
通过高尔基染色后,在倒置激光共聚焦显微镜下观察NAc区神经元,发现假刺激组的树突棘呈伪足样,有较大的棘头,而超声刺激组的树突棘呈蘑菇型或矮树桩样,且树突棘分布稀疏,数量显著减少,见图4,蓝色箭头所示为树突棘,神经元之间连接减少,甚至出现神经元连接中断。NAc区神经元树突棘密度和树突长度统计数据显示,与假刺激组相比,超声刺激后树突棘密度显著降低(P < 0.0001),树突长度显著缩短(P < 0.0001),见表2,表3、图5。
表 2 LIFU对小鼠NAc区树突棘密度的影响($\bar x \pm s $ )Table 2. Effect of LIFU on dendritic spine density in the NAc ($\bar x \pm s $ )组别 n 树突棘密度(个/µm) 假刺激组 30 0.36 ± 0.06 超声刺激组 30 0.23 ± 0.04**** 与假刺激组比较,****P < 0.0001。 表 3 LIFU对正常小鼠NAc区树突长度的影响[M(P25,P75)]Table 3. Effect of LIFU on dendritic length in the NAc [M(P25,P75)]组别 n 树突长度(µm/50个神经元) Z值 P值 假刺激组 30 43.65(32.19,56.05) −4.28 < 0.0001 超声刺激组 30 31.95(22.20,33.13) 与假刺激组比较,****P < 0.0001。 3. 讨论
调控神经核团和神经环路是脑功能及机制研究的重要方法,也是探索相关脑疾病诊疗方法的重要手段。常见的神经调控手段有电极深部脑刺激(deep brain stimulation,DBS)、经颅磁刺激(transcranial magnetic stimulation,TMS)、经颅直流电刺激(transcranial direct current stimulation,tDCS)以及光遗传学技术(Optogenetics)等,与其他神经调控方法相比,超声刺激是目前唯一一种同时具备无创、高时空分辨力等优点的神经调控方法,还可以联合CT、MRI及肌电诱发电位仪等监测设备实时调控特定脑区。
c-Fos是一种常用的神经元兴奋性标记物,对于编码和唤起记忆具有重要作用,当神经元被激活时,c-Fos表达会上调[7]。蛋白表达的检测已作为药物成瘾、脑部损伤等许多神经疾病的重要参照指标[8]。在本研究中,LIFU刺激后发现c-Fos表达显著增加,说明超声刺激能显著激活相应脑区神经元,证明了超声刺激的有效性。这与QIU等[9]的研究结果相一致。
神经元的结构可塑性与脑疾病中大脑功能的持久变化密切相关[10],目前结构可塑性的研究都集中在树突和树突棘的形态学改变上。大部分成瘾类物质如海洛因、可卡因、尼古丁等可以都可引起NAc区或内侧前额叶皮质区(medial prefrontal cortex,mPFC)的神经元树突棘密度增高和树突分支增多[11-12],但吗啡则导致NAc和mPFC树突棘密度显著降低和树突分支的减少[13]。在本研究中,笔者使用LIFU刺激正常小鼠的NAc区后,电镜观察首次发现树突棘密度降低、树突长度变短,这充分证明了超声刺激可以改变神经元的结构可塑性,且在本组超声刺激参数下(探头频率0.5 MHz,PRF 1 000 Hz,声压590 kPa,占空比50%,刺激时间10 min,连续7 d)出现了抑制性的改变。不同于Huang的研究,他发现在探头频率0.5 MHz,PRF 500 Hz,声压0.42 MPa的超声参数下对大鼠海马区域刺激后树突棘密度显著增加[14]。这表明,不同的超声刺激参数对于神经细胞结构可塑性的改变可能有着双向调控的能力。结合神经细胞结构可塑性改变基础,笔者可以设想,未来可以通过超声参数多能级的分组摸索,进一步证实超声神经调控的双向性,寻找到超声刺激在神经调控中正向和负向调控的临界点,同时也可使用LIFU在脑疾病的治疗中进行尝试。
综上所述,在本研究中,笔者发现LIFU能有效激活神经元,也能抑制性地调控NAc区神经元的结构可塑性。这充分证明了超声刺激具备干预与治疗脑疾病的潜能,尤其在药物依赖方面,将为毒品的戒治提供一种新思路。
-
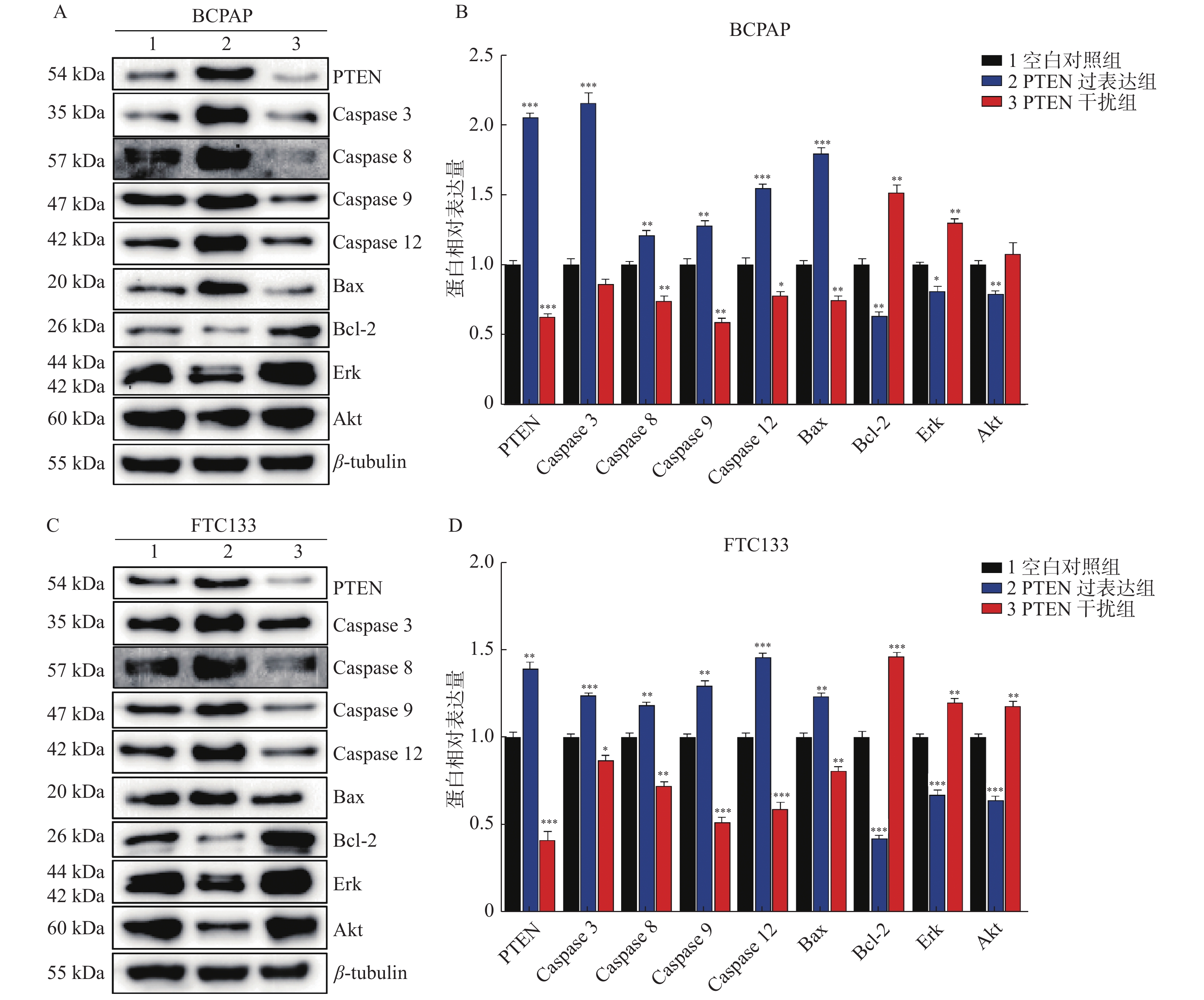
图 4 PTEN基因表达变化Western blot检测BCPAP和FTC133细胞相关蛋白表达
A:BCPAP细胞各相关因子Western印迹蛋白表达;B:BCPAP细胞各相关因子相对表达水平;C:FTC133细胞各相关因子Western印迹蛋白表达;D:FTC133细胞各相关因子相对表达水平。 与对照组比较,*P < 0.05,**P < 0.01,***P < 0.001。
Figure 4. The protein’s expression of BCPAP and FTC133 by Western blot with different PTEN expression levels
表 1 PTEN基因表达变化MTT检测BCPAP和FTC133细胞OD值及细胞活力(
$\bar x \pm s$ )Table 1. The OD and cell viability of BCPAP and FTC133 detected by MTT with different PTEN expression levels (
$\bar x \pm s$ )组别 BCPAP FTC133 OD 细胞活力(%) OD 细胞活力(%) 空白对照组 1.506 ± 0.165 100.00 ± 10.97 0.813 ± 0.123 100.00 ± 15.20 PTEN过表达组 0.345 ± 0.117* 22.92 ± 7.76* 0.040 ± 0.008* 4.91 ± 0.95* P < 0.001 < 0.001 < 0.001 < 0.001 PTEN干扰组 1.804 ± 0.086* 109.75 ± 8.17 0.943 ± 0.050* 112.66 ± 7.49 P < 0.001 0.082 0.032 0.051 与对照组比较,*P < 0.05。 表 2 PTEN基因表达变化Western blot检测BCPAP和FTC133细胞ERK和AKT表达(
$\bar x \pm s $ )Table 2. The expression of ERK and AKT of BCPAP and FTC133 by Western blot with different PTEN expression levels (
$\bar x \pm s $ )分组 BCPAP FTC133 ERK AKT ERK AKT 对照组 115.90 ± 4.41 140.04 ± 8.45 148.38 ± 5.39 126.76 ± 4.24 PTEN过表达组 95.02 ± 7.19* 112.45 ± 5.44* 101.43 ± 8.00* 82.76 ± 5.17* P 0.009 0.002 < 0.001 < 0.001 PTEN干扰组 156.47 ± 7.87* 147.49 ± 5.05 179.55 ± 6.59* 150.91 ± 6.63* P < 0.001 0.210 0.001 0.002 与对照组比较,*P < 0.05。 -
[1] Siegel R L,Miller K D,Jemal A. Cancer statistics,2017[J]. CA Cancer J Clin,2017,67(1):7-30. doi: 10.3322/caac.21387 [2] 刘志春,赵亮. PTEN和Ki-67在甲状腺癌组织中的表达及其临床意义[J]. 中国普外基础与临床杂志,2016,23(11):1348-1352. doi: 10.7507/1007-9424.20160345 [3] 陈超,张伟丽,冯长松. IncRNA PCAT19靶向miR-143-3p通过信号通路PI3K/Akt对甲状腺癌细胞增殖和凋亡的影响及机制[J]. 中国老年学杂志,2020,40(8):1712-1717. doi: 10.3969/j.issn.1005-9202.2020.08.043 [4] Seong Keun Yoo,Young Shin Song,Eun Kyung Lee,et al. Integrative analysis of genomic and transcriptomic characteristics associated with progression of aggressive thyroid cancer[J]. Nat Commun,2019,10(1):2764-2776. doi: 10.1038/s41467-019-10680-5 [5] 孙健玮. PTEN基因与肿瘤相关性的研究进展[J]. 中国当代医药,2019,26(32):20-23. doi: 10.3969/j.issn.1674-4721.2019.32.007 [6] Hanzhang Zhu,Qiaoyu Liu,Junwei Tang,et al. Alpha1-ACT functions as a tumour suppressor in hepatocellular carcinoma by inhibiting the PI3K/AKT/mTOR signalling pathway via activation of PTEN[J]. Cell Physiol Biochem,2017,41(6):2289-2306. doi: 10.1159/000475648 [7] 李金国,宋西成. 甲状腺癌相关信号传导通路的研究进展[J]. 肿瘤学杂志,2018,24(4):293-296. doi: 10.11735/j.issn.1671-170X.2018.04.B001 [8] Jahanbani I,Al Abdallah A,Ali R H,et al. Discriminatory miRNAs for the management of papillary thyroid carcinoma and noninvasive follicular thyroid neoplasms with papillary-like nuclear features[J]. Thyroid,2018,28(3):319-327. doi: 10.1089/thy.2017.0127 [9] 黄敏,倪庆峰. Beclin-1、PTEN蛋白在甲状腺癌中的表达及其意义[J]. 中国普通外科杂志,2017,26(12):1642-1646. doi: 10.3978/j.issn.1005-6947.2017.12.022 [10] 江泽友,徐灿,葛一漫. shRNA干扰IRS-1基因通过PI3K/AKT通路对人乳头状甲状腺癌细胞TPC-1增殖和转移能力的调控作用[J]. 中国免疫学杂志,2018,34(11):1674-1678. doi: 10.3969/j.issn.1000-484X.2018.11.015 [11] Rodgers S J,Ferguson D T,Mitchell C A,et al. Regulation of PI3K effector signalling in cancer by the phosphoinositide phosphatases[J]. Biosci Rep,2017,37(1):1-18. [12] 翟明慧,袁殿宝,赵峻峰,等. 过表达PTEN基因对甲状腺髓样癌细胞生长及细胞周期的影响[J]. 临床与病理杂志,2019,39(3):464-469. doi: 10.3978/j.issn.2095-6959.2019.03.002 [13] Li Za,Qiu Rb,Qiu Xc,et al. EYA2 promotes lung cancer cell proliferation by downregulating the expression of PTEN[J]. Oncotarget,2017,8(67):110837-110848. doi: 10.18632/oncotarget.22860 [14] 孙健玮,郑立民. 抑癌基因PTEN的研究进展[J]. 中国当代医药,2019,26(13):19-22. doi: 10.3969/j.issn.1674-4721.2019.13.006 [15] 陈政华. 甲状腺乳头状癌组织中血管内皮生长因子-C和PTEN蛋白的表达及其与临床病理参数的关系[J]. 中国老年杂志,2016,36(5):1124-1125. [16] Beg S,Siraj A K,Jehan Z,et al. PTEN loss is associated with follicular variant of middle eastern papillary thyroid carcinoma[J]. Br J Cancer,2015,112(12):1938-1943. doi: 10.1038/bjc.2015.169 [17] 王振,汪静宇,郭志琴,等. 同源磷酸酶-张力蛋白基因在分化型甲状腺癌组织中的表达及意义[J]. 中国基层医药,2017,24(4):536-539. doi: 10.3760/cma.j.issn.1008-6706.2017.04.014 [18] 于丰铭,徐扬. Caspase-3的研究进展[J]. 中国细胞生物学学报,2020,42(11):2072-2078. [19] 马汉宁,姬艳燕,陈伟,等. 甘草次酸通过抑制Caspase 3/Bax/Bcl-2凋亡信号通路保护心脏骤停心肺复苏大鼠心脏功能[J]. 中药药理与临床,2019,35(4):28-33. [20] Aral Kübra1,Aral Cüneyt Asım,Kapila Yvonne. The role of caspase-8,caspase-9,and apoptosis inducing factor in periodontal disease[J]. J Periodontol,2019,90(3):288-294. doi: 10.1002/JPER.17-0716 [21] Anderson S L,Townsend HGG,Singh B. Role of toll-like receptor 4 and caspase-3,-8,and-9 in lipopolysaccharide-induced delay of apoptosis in equine neutrophils.[J]. Am J Vet Res,2018,79(4):424-432. doi: 10.2460/ajvr.79.4.424 [22] Karimi A S,Tafvizi F,Tajabadi E M. Heat-killed probiotic bacteria induce apoptosis of HT-29 human colon adenocarcinoma cell line via the regulation of Bax/Bcl2 and caspases pathway[J]. Hum& Exp Toxicology,2019,38(9):1069-1081. [23] 王旭同,张永辉. 微小RNA-1269a靶向调控PTEN对肝癌细胞迁移、侵袭和PI3K/Akt信号通路的影响[J]. 临床肿瘤学杂志,2021,26(3):193-199. doi: 10.3969/j.issn.1009-0460.2021.03.001 [24] G F Zhang,J M Zhong,L Lin. MiR-19 enhances pancreatic cancer progression by targeting PTEN through PI3K/AKT signaling pathway[J]. Eur Rev Med Pharmacol Sci,2020,24(3):1098-1107. [25] Jiang Li,Qiao Yanguo,Wang Zhenghui,et al. Inhibition of microRNA-103 attenuates inflammation and endoplasmic reticulum stress in atherosclerosis through disrupting the PTEN-mediated MAPK signaling[J]. J Cell Physiol,2020,235(1):380-393. doi: 10.1002/jcp.28979 [26] 孙健玮,王剑松,刘子超,等. PTEN基因调控Raf1磷酸化对前列腺癌PC3细胞凋亡的影响[J]. 昆明医科大学学报,2020,41(1):18-25. doi: 10.3969/j.issn.1003-4706.2020.01.003 [27] LeBoeuf B,Anderson B,Young M,et al. Evaluating the effectiveness of MAPK,AKT,and mTOR inhibitors in reducing proliferation in cellular models of papillary and follicular thyroid cancer[J]. Cancer Res,2018,78(13):2887-2888. [28] 张春英,阴广维,尤鸣达,等. siRNA 靶向沉默TAK1基因对甲状腺癌细胞增殖、迁移和p38 MAPK 信号通路的抑制作用[J]. 吉林大学学报(医学版),2021,47(1):110-117. 期刊类型引用(1)
1. 段敏丹,陈雪,王悦,苏雷,史茜,贾友超,霍燃. 微小RNA多态性和非小细胞肺癌遗传易感性关系研究. 陕西医学杂志. 2017(07): 833-835+839 .  百度学术
百度学术其他类型引用(0)
-






 下载:
下载:






 下载:
下载: