The Regulation of VEGF Signal Axis by DATS and the Improvement of Formation of Placental Angiogenesis in URSA Mice
-
摘要:
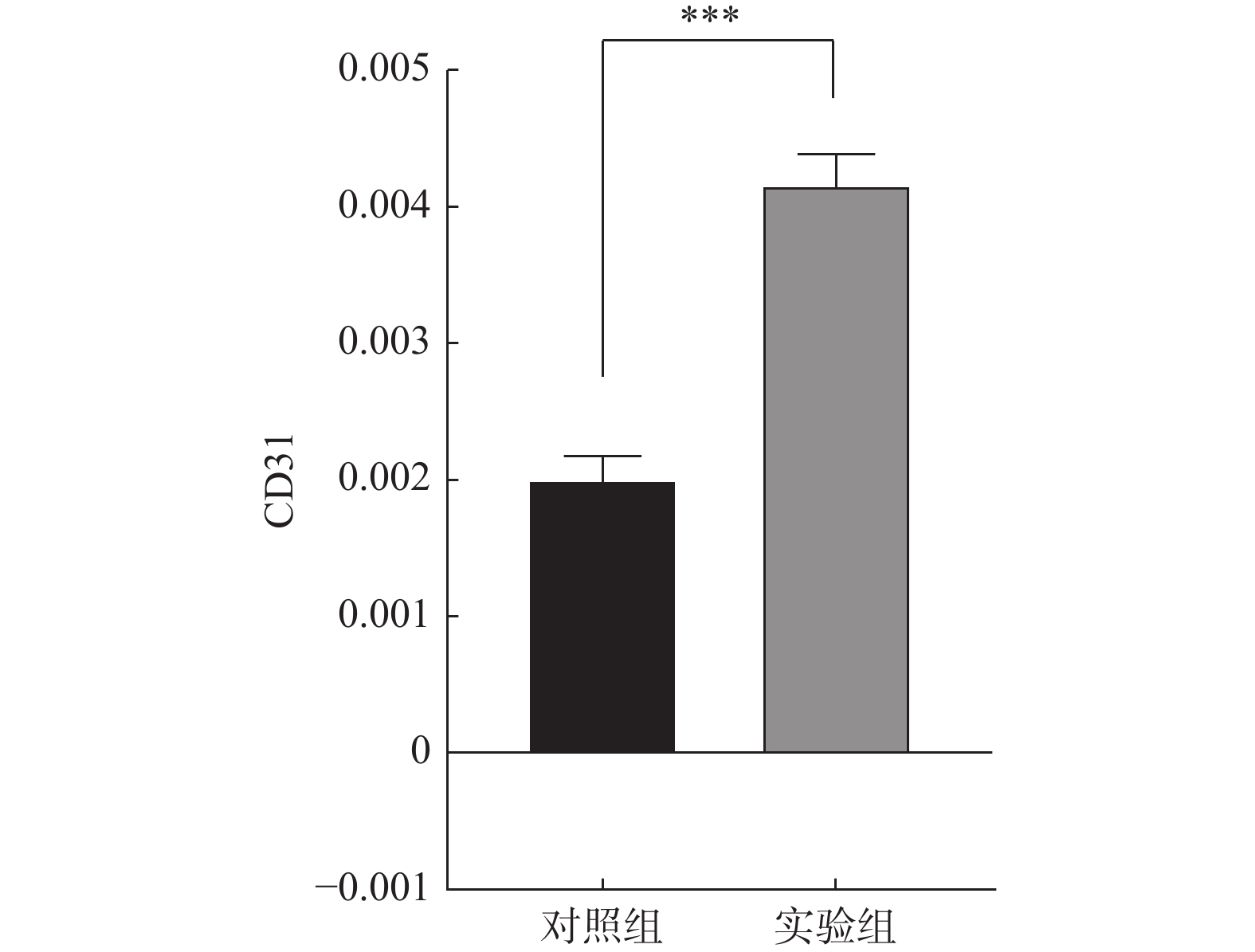
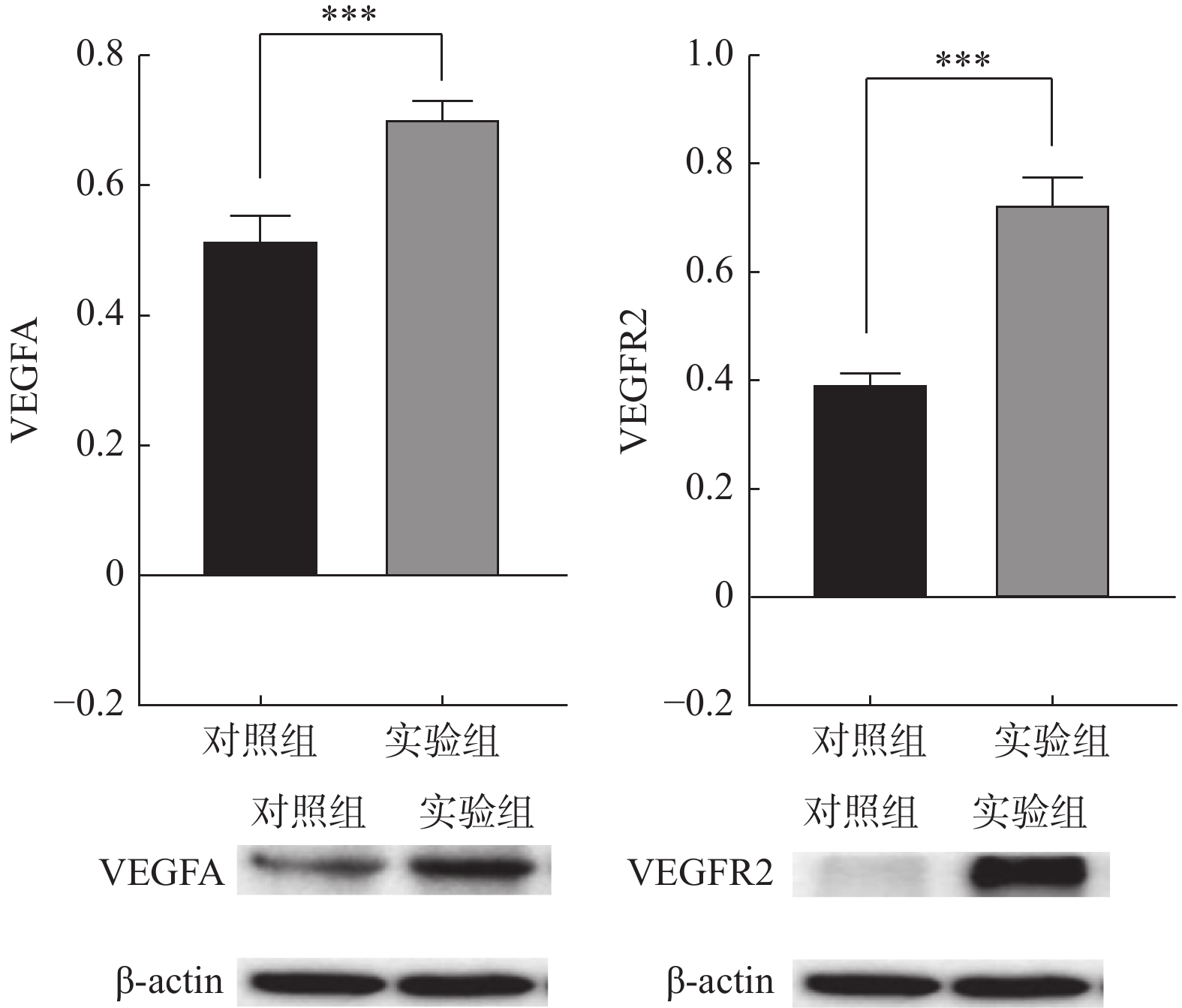
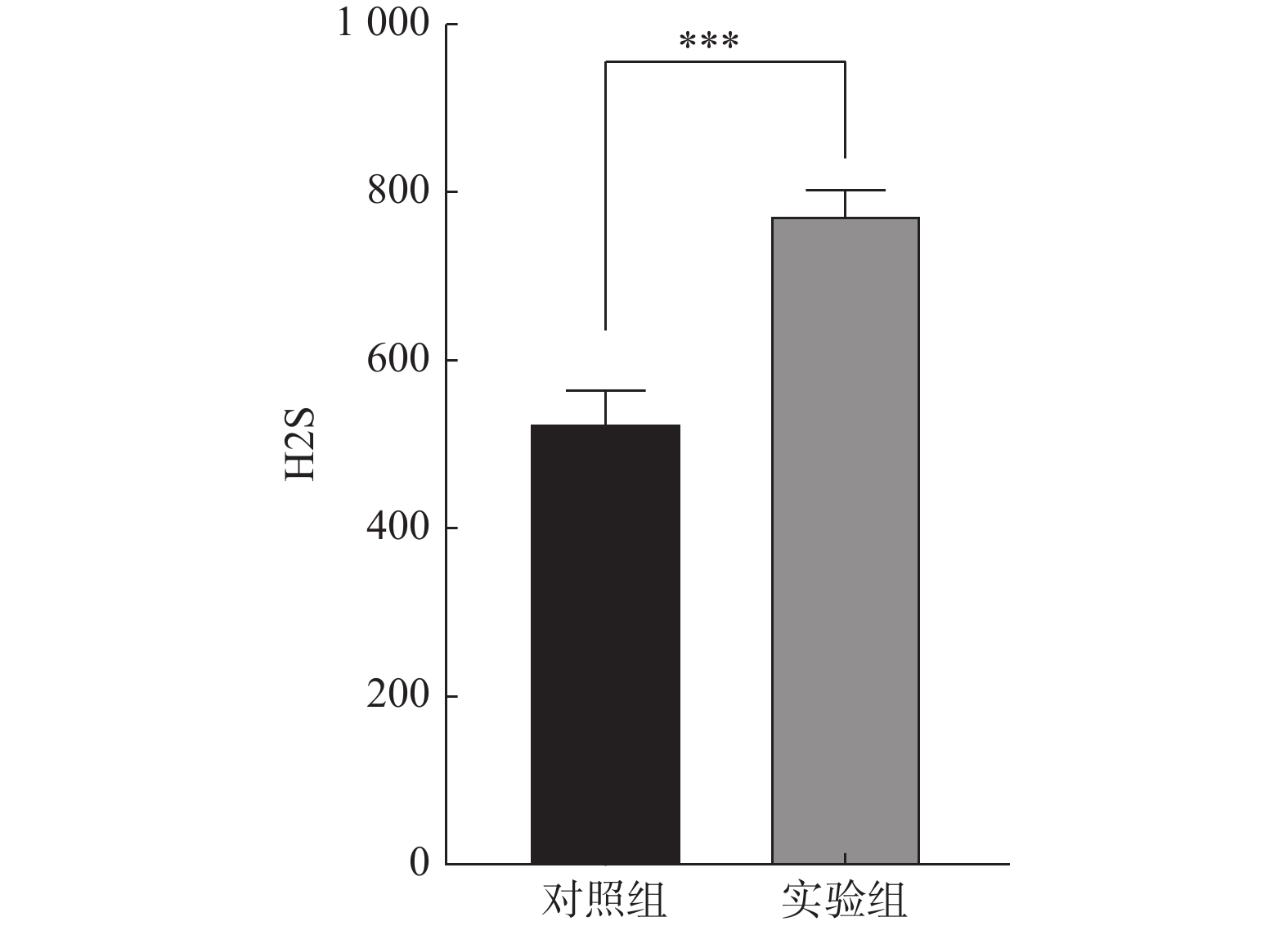
目的 探讨二烯丙基三硫醚(diallyl trisulfide,DATS)对不明原因反复自然流产(unexplained recurrent spontaneous abortion,URSA)小鼠胎盘血管生成的影响,并基于血管内皮细胞生成因子(vascular endothelial growth factor,VEGF)/血管内皮细胞生长因子受体2(vascular endothelial growth factor receptor 2 ,VEGFR-2)信号通路探索其作用机制。 方法 将16只URSA小鼠随机分为对照组与实验组,每组8只,实验组常规饲喂的同时给予纯度为98%的DATS,按照50 mg/(kg·d)配制成200 μL悬浊液进行灌胃;对照组常规饲喂的同时给予 200 μL PBS液灌胃。2组孕鼠连续给药18 d后,使用分光光度计检测胎盘组织中的硫化氢(hydrogen sulfide,H2S)含量,使用反转录酶-聚合酶链反应(RT-qPCR)检测胎盘组织中血小板-内皮细胞粘附分子(platelet endothelial cell adhesion molecule-1,CD31)、血管内皮生长因子A(vascular endothelial growth factor A,VEGFA)与VEGFR2的 mRNA相对表达量,并使用蛋白免疫印迹(Western blot)法检测胎盘组织中VEGFA与VEGFR2的蛋白表达水平。 结果 分光光度计检测结果显示:实验组(777.4922±72.9759) nmol/g H2S水平显著高于对照组(529.1824±99.7489) nmol/g (P < 0.05);RT-qPCR结果显示:实验组CD31的相对表达量(0.0042±0.0006)显著高于对照组(0.0020±0.0004)(P < 0.05)、实验组VEGFA的相对表达量(0.7073±0.0677)显著高于对照组(0.5200±0.0946)(P < 0.05)、实验组VEGFR2的相对表达量(0.7304±0.1262)显著高于对照组(0.3984±0.047)(P < 0.05);Western blot结果显示,DATS可显著提高胎盘组织中VEGFA和VEGFR2的蛋白表达水平(P < 0.05)。 结论 DATS可显著提高URSA胎盘组织中的H2S水平及胎盘组织中血管形成因子CD31、VEGFA及VEGFR2的相对表达量,并通过VEGF信号轴改善URSA小鼠胎盘血管的形成,将为DATS的临床应用提供一定的科学依据和参考价值。 Abstract:Objective The aim of this study is to investigate the effect of Diallyl trisulfide (DATS) on placental angiogenesis in mice with unexplained recurrent spontaneous abortion (URSA) and to explore its mechanism based on the vascular endothelial growth factor (VEGF)/vascular endothelial growth factor receptor-2 (VEGFR-2) signaling pathway. Methods Sixteen URSA mice selected were randomly divided into the control group and the experimental group, with 8 mice in each group. The experimental group was given 98% pure DATS (200 μL suspension prepared according to 50 mg/(kg·d) by gavage. The rats in the control group were fed conventionally and given 200 μL PBS solution by gavage. After 18 days of continuous administration, Hydrogen sulfide (H2S) content in the placental tissue was detected by spectrophotometer, and the relative expression of CD31, VEGFA and VEGFR2 mRNA in the placental tissue was detected by reverse transcriptase-polymerase chain reaction (RT-qPCR). The protein expression levels of VEGFA and VEGFR2 in placenta were detected by Western blot. Results The spectrophotometer detection showed that the H2S level in the experimental group (777.4922±72.9759) was significantly higher than that in the control group (529.1824±99.7489) (P < 0.05); The RT-qPCR results showed that the relative expression of CD31 in the experimental group (0.0042±0.0006) was significantly higher than that in the control group (0.0020±0.0004) (P < 0.05), the relative expression of VEGFA in the experimental group (0.7073±0.0677) was significantly higher than that in the control group (0.5200±0.0946)(P < 0.05), and the relative expression of VEGFR2 in the experimental group (0.7304±0.1262) was significantly higher than that in the control group (0.3984±0.047) (P < 0.05); Western blot results showed that DATS significantly increased the protein expression levels of VEGFA and VEGFR2 in placental tissue (P < 0.05). Conclusion DATS can significantly increase the level of H2S in URSA placental tissue and the relative expression levels of angiogenic factors CD31, VEGFA, and VEGFR2 in placental tissue. Through the VEGF signal axis, it can improve the formation of placental blood vessels in URSA mice. The relevant research results will provide scientific basis and reference value for the clinical application of DATS. -
Key words:
- DATS /
- VEGF signaling axis /
- URSA mice /
- Placental vessels
-
缺血性卒中(acute ischemic stroke,AIS)是我国临床常见的急性脑血管疾病之一,当供血动脉发生闭塞、狭窄时导致脑供血严重不足,引发脑组织缺血缺氧坏死,出现一系列临床表现[1]。缺血性卒中患者的治疗关键在于早期对堵塞血管的开通以及恢复脑梗死区域的血流灌注,血管内介入可实现快速开通血管恢复血供,降低颅内出血转化的风险[2−3]。替罗非班是一种Ⅱb/Ⅲa受体拮抗剂药物,可通过组织纤维蛋白原与血小板表面的糖蛋白Ⅱb/Ⅲa受体结合,降低血小板粘附活性从而预防血栓形成[4]。血管内介入治疗联合替罗非班临床疗效佳,但其安全性与有效性存在一定的个体差异[5]。相关报道指出,缺血性卒中占我国全部脑卒中的70%,治疗后致死/致残率高达35%,多见于老年人,现以成为危害我国中年人生命健康的主要疾病,免疫炎症反应是缺血性卒中发生的重要病理机制[6]。因此,寻找可预测缺血性脑卒中患者治疗后不良预后的临床敏感因子是改善其疾病预后的关键步骤。PIV是近年来临床最新提出的复合型炎症标志物,已被临床作为评估冠状动脉粥样化严重程度与疾病预后的高敏、特异性指标[7]。但是关于PIV对缺血性卒中患者血管内介入联合替罗非班治疗疾病转归的预测价值报道较少。因此,本次研究主要探讨PIV对缺血性卒中患者血管内介入联合替罗非班治疗疾病转归的预测价值。
1. 资料与方法
1.1 一般资料
选取2019年1月至2023年12月昭通市第一人民医院脑血管科收治并接受血管内介入联合替罗非班治疗的102例缺血性卒中患者作为研究对象。
发病4.5 h内,有静脉溶栓指征患者予阿替普酶(剂量0.9 mg/kg,最多使用90 mg)静脉溶栓,10%剂量1 min内静脉推注,剩余剂量静脉泵入1 h,溶栓后症状没有改善的患者立即复查头颈电脑断层血管摄影术(computed tomography angiography,CTA)。发病4.5~24 h及溶栓后头颈CTA提示大血管闭塞,符合血管内治疗指针的患者均采用SWIM技术取栓,术后立即复查头颅计算机断层扫描(computed tomography,CT)排外颅内出血后,使用的替罗菲班0.4 ug/(kg·min)微量泵入半小时后改为0.1 ug/(kg·min)维持48 h停泵,结束前6 h给予重叠阿司匹林肠溶片100 mg/d+氯吡格雷片75 mg/d双抗抗血小板聚集治疗。1个月后选取其中1种继续抗板治疗。
纳入标准:(1)首次缺血性卒中发作,符合急性缺血性脑卒中的临床诊断指南[8];(2)入院后经MRA检查或头颅CTA检查后明确责任大动脉闭塞;(3)符合血管内介入治疗指征;(4)签署知情同意书。排除标准:(1)既往接受开颅手术者;(2)合并其他器官严重疾病者;(3)合并恶性肿瘤者;(4)合并严重感染者;(5)本研究药物过敏者;(6)既往使用抗血小板聚集药物者;(7)术后颅脑CT提示颅内出血者;(8)智力低下,配合度低下者。昭通市第一人民医院医学伦理委员已对本研究审核批准。
1.2 方法
1.2.1 临床资料
收集所有研究对象的临床资料,年龄、身高、体重、体质量指数(body mass index,BMI)、性别、吸烟史(每天吸烟超过1支且时间持续1年以上)、饮酒史(每周摄入酒精量超过250 g且持续半年以上);既往疾病史(高血压史、高血脂症、糖尿病史、心房颤动史、冠心病史);实验室指标:血小板计数、淋巴细胞计数、中性粒细胞计数、单核细胞计数、甘油三脂、低密度脂蛋白胆固醇(low density lipoprotein cholesterin ,LDL-C)、高密度脂蛋白胆固醇(high-density lipoprotein,HDL-C)、总胆固醇;查体相关指标:心率、血压、PIV值、美国国立卫生院卒中量表(NIH stroke scale,NIHSS)。
1.2.2 PIV检测[9]
所有患者于入院后抽取静脉血5mL选用全自动血细胞分析仪(型号:Xn-9000,生产厂家:日本希森美康血细胞)检测中性粒细胞、单核细胞、血小板、淋巴细胞水平,并计算PIV值。PIV计算方法:PIV = (血小板×中性粒细胞×单核细胞)/淋巴细胞。
1.2.3 分组与分层[10]
根据入院后神经功能缺损程度(NIHSS评分)将患者分为3组,轻度组(0~4分),中度组(5~15分),重度组( > 16分)。根据治疗后90 d mRS评分将患者分为预后良好组63例( ≤ 2分)、预后不良组39例( > 2分)。
1.3 统计学分析
采用SPSS 21.0和R 4.2进行统计分析。在对计量资料进行分析时,首先通过正态性检验将数据分为正态分布和非正态分布两类。根据分析目标,选用相应的统计方法。正态分布数据,采用t检验或单因素方差分析(ANOVA analysis),统计描述用均数 ± 标准差来表示。非正态分布数据,采用非参数检验进行分析,统计描述用中位数(25%和75%四分位数)呈现。计数资料采用卡方检验比较组间差异。
计数资料的比较,采用了卡方检验。四格表卡方检验,当Tmin≥5,N≥40时,用person卡方检验公式;当1≤Tmin≤5,N≥40时,用校正卡方检验公式; Tmin < 1或N < 40时,用Fisher切确概率法。以P < 0.05为差异有统计学意义,P < 0.001表示差异显著。将差异分析有统计学意义的变量(P ≤ 0.05)纳入Logistic回归分析,并采用列线图(Nomogram)来展示临床预测模型以方便临床应用。采用MedCalc进行ROC曲线(receiver operating characteristic curve,ROC)分析评估变量预测效能及截断值,探讨缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的影响因素。
2. 结果
2.1 基本资料比较
102例缺血性卒中患者年龄34~87岁,平均(61.625±11.51)岁。所有患者在接受血管内介入联合替罗非班治疗后随访90 d,分为预后良好组(n = 63)与预后不良组(n = 39)。两组年龄、身高、体重、BMI、性别、吸烟史、饮酒史、既往病史(高血压病、高血脂症、糖尿病、房颤、冠心病)、单核细胞计数、甘油三脂、总胆固醇、LDL-C、HDL-C、心率、血压(收缩压、舒张压)差异无统计学意义(P > 0.05);NIHSS评分、血小板计数、淋巴细胞计数、中性粒细胞计数差异有统计学意义(P < 0.05),其中NIHSS评分、淋巴细胞计数、中性粒细胞计数(P < 0.001)差异显著,见表1。
表 1 入组患者基本资料比较 [($ \bar x \pm s $)/n(%)]Table 1. Comparison of basic data of enrolled patients [($ \bar x \pm s $)/n(%)]项目 预后良好组 (n = 63) 预后不良组 (n = 39) t/χ2/z P 年龄(岁) 60.76±11.51 62.49±11.51 −0.74 0.70 身高(cm) 162.54±7.29 163.13±6.29 −0.42 0.60 体重(kg) 61.84±9.16 62.46±6.84 −0.36 0.70 BMI(kg/m2) 23.33±2.52 23.48±2.41 −0.30 0.76 性别(n) 1.78 0.18 男 37(58.73) 28(71.79) 女 26(41.27) 11(28.21) 吸烟(n) 30(47.62) 26(66.67) 3.53 0.06 饮酒(n) 10(15.87) 11(28.21) 2.24 0.13 入院NIHSS(n) 17.80 < 0.001 轻 8(12.70) 1(2.56) 中 35(55.56) 9(23.08) 重 20(31.75) 29(74.36) 高血压(n) 33(52.38) 23(58.97) 0.42 0.50 高脂血症(n) 17(26.98) 13(33.33) 0.47 0.50 糖尿病(n) 9(14.29) 5(12.82) 0.04 0.80 心房颤动(n) 5(7.94) 4(10.26) 0.16 0.70 冠心病(n) 4(6.35) 0(0) 3.96 0.05 血小板(×109/L) 203.65±59.79 227.95±68.13 −1.89 0.05 淋巴细胞(×109/L) 1.49±0.60 1.09±0.55 3.42 < 0.001 中性粒细胞(×109/L) 7.05±3.67 10.07±3.99 −3.91 < 0.001 单核细胞(×109/L) 0.47±0.19 0.52±0.31 −0.90 0.40 甘油三酯(mmol/l) 1.34 (0.81,2.08) 1.34 (0.87,2.28) −0.39 0.69 总胆固醇(mmol/l) 4.45±0.99 4.30±1.03 0.67 0.30 LDL-C(mmol/l) 2.74±0.85 2.71±1.03 0.13 0.40 HDL-C(mmol/l) 1.11±0.30 1.09±0.25 0.29 0.60 心率(次/min) 77.22±14.95 79.03±14.62 −0.60 0.50 收缩压(mmHg) 149.87±20.02 147.82±22.64 0.48 0.70 舒张压(mmHg) 89.89±12.08 93.15±14.74 −1.22 0.20 2.2 不同严重程度患者(入院NIHSS评分分组)PIV水平对比
重度组PIV水平高于轻、中度组,中度组PIV水平高于轻度组(P < 0.05),见表2。
表 2 入院时不同NIHSS患者PIV水平比较Table 2. Comparison of PIV levels among different NIHSS patients at admission入院NIHSS分组 例数 PIV χ2 P 轻度组 9 279.9 (155.4,396.9) a 15.097 0.001* 中度组 45 308.5 (215.4,845.8) a 重度组 48 810.8 (407.2, 1524.5 )注:a表示两两比较分析,与重度组比较,*P < 0.05。 2.3 不同疾病转归患者PIV水平对比
预后良好组患者PIV水平低于预后不良组组(P < 0.05),见表3。
表 3 不同疾病转归患者PIV水平对比Table 3. Comparison of PIV levels in patients with different disease outcomes组别 n PIV Z P MRS预后 −4.192 < 0.001 预后良好 63 331.1 (221.9,662.7) 预后不良 38 1025.7 (451.5,1841.3 )2.4 PIV对缺血性卒中患者疾病转归的预测价值
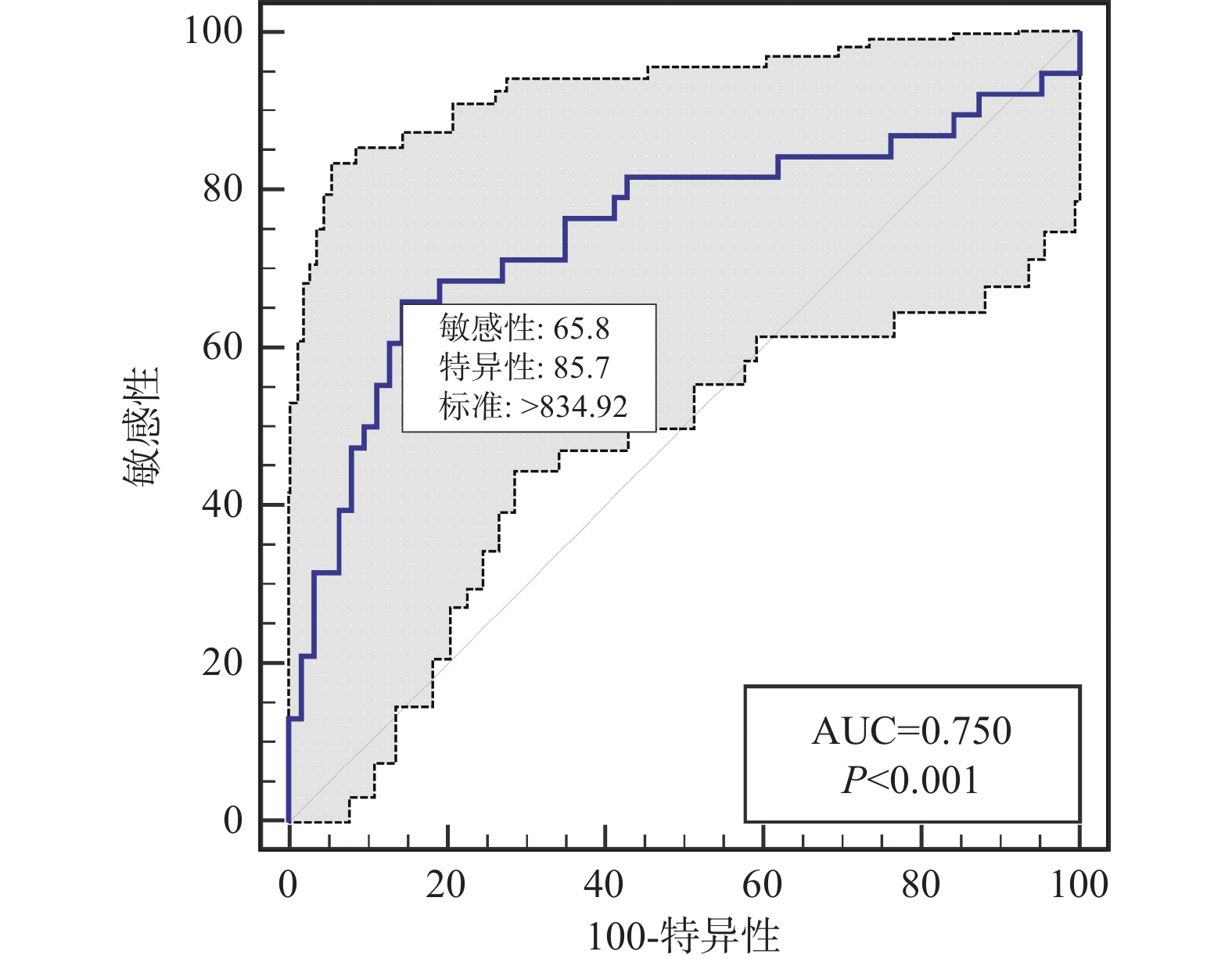
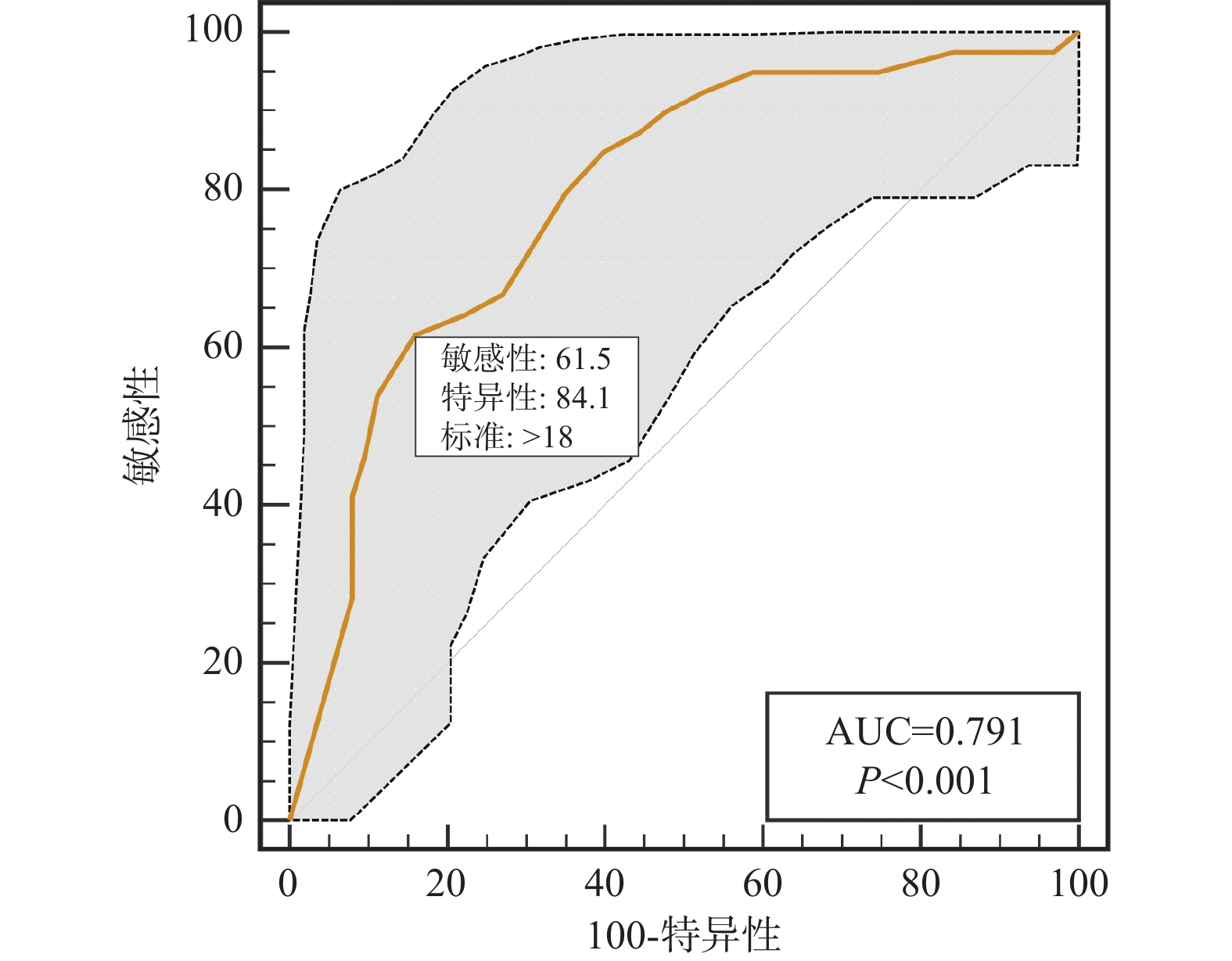
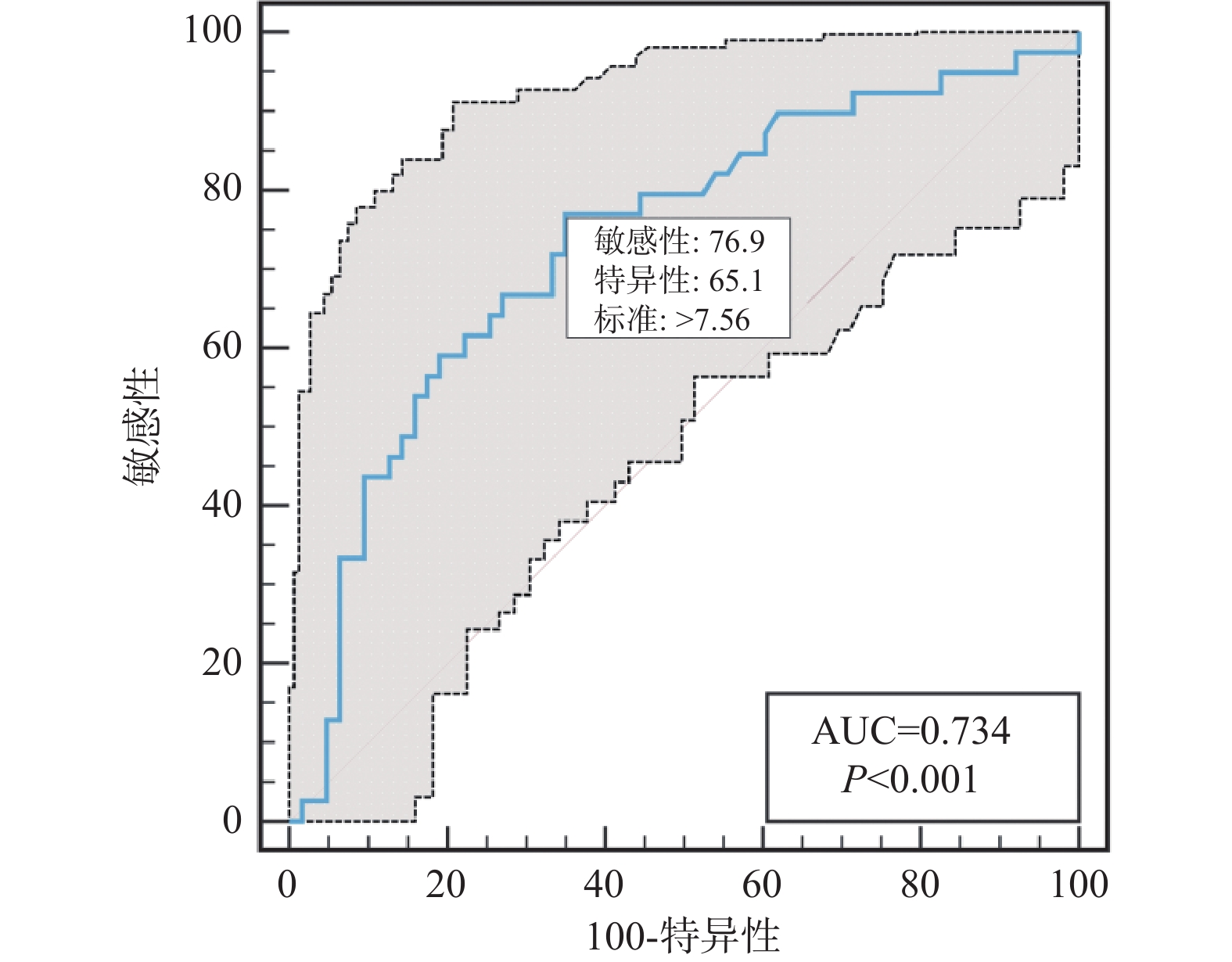
ROC结果显示,PIV预测缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的AUC为0.750(95%CI 0.654~0.831),截点值为834.92,特异度为85.71%,灵敏度为65.79%,见表4、图1。
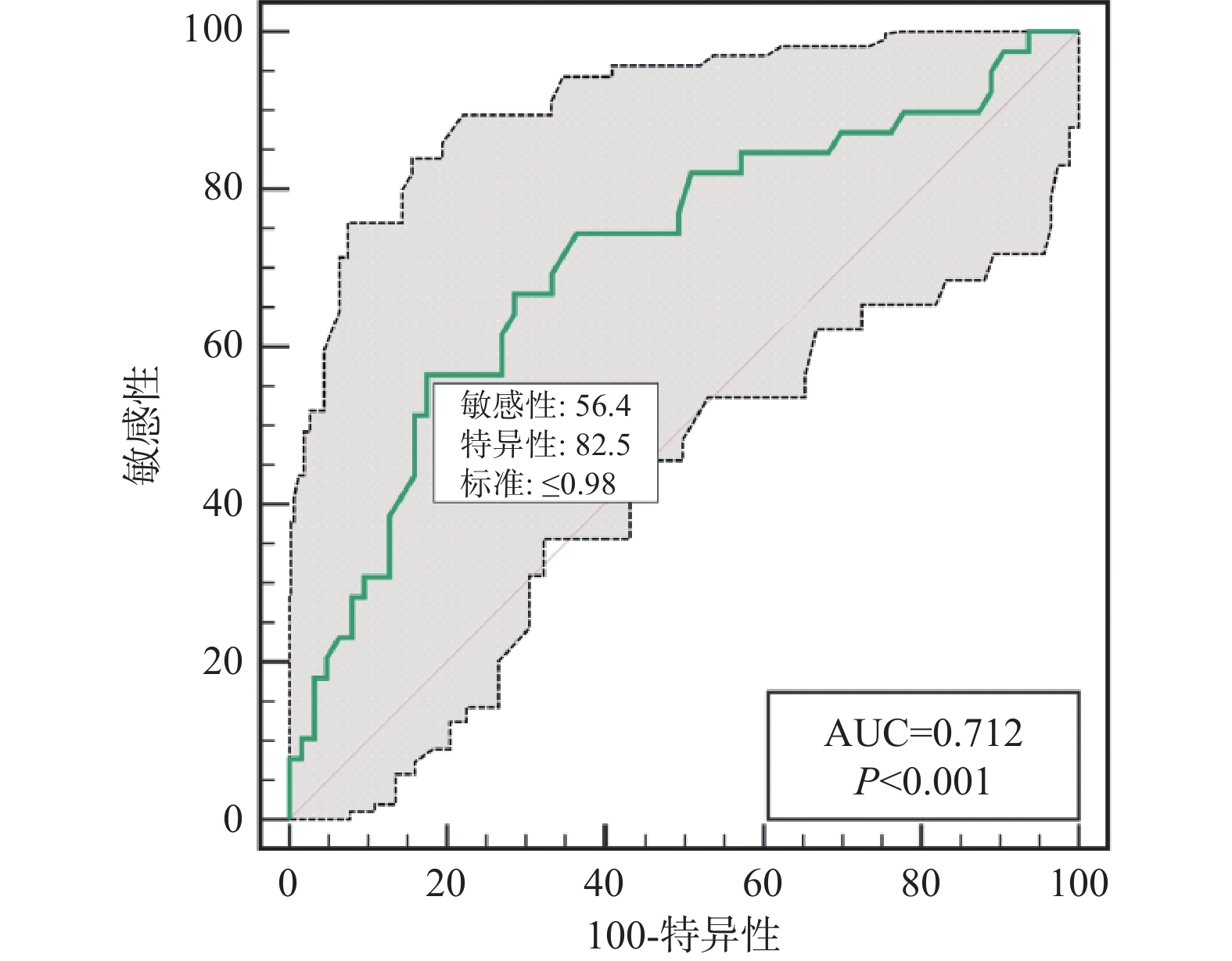
表 4 检测指标对缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的预测价值Table 4. Predictive value of the tested indicators for poor disease outcome in patients with ischemic stroke treated with endovascular intervention combined with tirofiban检测指标 AUC 95%CI 截点值 特异度(%) 灵敏度(%) NIHISS 0.791 0.699~0.865 18 84.13 61.54 PIV 0.750 0.654~0.831 834.92 85.71 65.79 淋巴细胞 0.712 0.614~0.798 0.98 82.54 56.41 中性粒细胞 0.734 0.637~0.817 7.56 65.08 76.92 同时,在ROC结果中发现NIHSS评分、淋巴细胞计数及中性粒细胞计数,似乎同样对缺血性卒中患者血管内介入联合替罗非班治疗疾病转归也有一定的预测价值,见表4、图2~4。
2.5 缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的单因素及多因素分析
将缺血性卒中患者治疗后是否发生不良预后作为因变量(否 = 0、是 = 1),将单因素分析有意义的指标:入院NIHSS评分、PIV、淋巴细胞计数及中性粒细胞计数作为自变量进行多因素Logistic回归分析,结果显示,NIHSS评分 > 18分(OR = 5.944,95%CI 2.011~19.137),PIV > 834.92(OR = 4.863,95%CI 1.410~18.685)是缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的影响因素(P < 0.05),见表5。
表 5 缺血性卒中患者血管内介入联合替罗非班治疗预后不良的单因素及多因素分析Table 5. Univariate and multivariate analysis of poor prognosis in patients with ischemic stroke treated with endovascular intervention combined with tirofiban项目 OR值a 95% CI P OR值b 95% CI P 入院NIHSS < 0.001 0.001 ≤18 — — — — > 18 8.48 3.432,22.476 5.944 2.011,19.137 PIV < 0.001 0.012 ≤834.92 — — — — > 834.92 10.192 4.066,27.574 4.863 1.410,18.685 淋巴细胞 < 0.001 0.1 > 0.98 — — — — ≤0.98 6.118 2.526,15.670 2.666 0.819,8.719 中性粒细胞 < 0.001 0.2 ≤7.56 — — — — > 7.56 6.212 2.589,16.101 2.202 0.631,7.657 注:a是单因素逻辑回归的OR值,b是多因素逻辑回归的结果。 3. 讨论
血管堵塞、血流不畅是发生缺血性卒中的主要病因,及时开通闭塞血管,清除血栓或栓子是急性缺血性卒中临床治疗的关键,血管内介入是治疗缺血性卒中患者的常用方法,通过在病变血管内溶栓、抽吸血栓或搭建支架,将血栓溶解或取出以恢复血流正常供给[11−12]。多项研究显示血管内介入联合抗血小板治疗可大幅度提升临床疗效,替罗非班可通过阻止血小板膜上相关受体相结合从而防止血栓的形成[13−14]。现缺血性脑卒中患者进行血管内介入治疗后常联合替罗非班治疗以提高临床疗效,该治疗方案也成为了目前缺血性卒中急性期的主要治疗方法。由于缺血性卒中的发病人群中老年人居多,且常伴有糖尿病、高血压等基础疾病,导致病情复杂,治疗难度大幅度增加,就算及时给予相应的临床干预预后也往往欠佳,导致神经功能受损、瘫痪、死亡等不良预后发生[15]]。因此,需要寻找合适的高敏感性指标,在缺血性卒中患者急性期治疗后用于指导该疾病预后的临床治疗,提早对不同预后的患者进行干预,更利于临床医生对病情的评估,及患者及其家属对患者预后的了解。
既往研究[16]发现,当发生缺血性卒中时机体脑组织表面细胞中的氧自由基、趋化因子等呈高水平表达,导致炎症因子水平上调破坏脑组织屏障从而造成脑组织的损伤。PIV由外国学者Fuca教授提出,通过综合淋巴细胞、血小板计数、单核细胞、中粒性细胞的计数,反应促炎与抗炎的生态平衡过程,认为其可作为全身炎症状态的潜在生物标志物[[7]。多项研究表明,PIV水平表达与心血管疾病、炎症疾病、抗中性粒细胞胞浆相关血管炎、腹膜透析发生心血管感染事件等多种疾病的不良预后有关,在国内外临床心脑血管领域备受关注[9,17- 18]。
本研究结果显示,不良预后患者的PIV高于良好预后组(P < 0.05),重度组PIV水平高于轻、中度组,中度组PIV水平高于轻度组(P < 0.05),ROC结果显示,PIV预测缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的AUC为0.750(95%CI 0.654~0.831),截点值为834.92,特异度为85.71%,灵敏度为65.79%;进一步多因素分析显示,PIV≥834.92是缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的影响因素(P < 0.05)。说明高PIV水平是缺血性卒中患者治疗后疾病转归不良的危险因素,具有较高的临床参考价值。分析原因为:(1)本研究预后不良组患者的淋巴胞数更低,既往研究表明淋巴细胞可通过抑制炎症分子从而起到抗动脉粥样硬化,降低心脑血管疾病发生风险[19−20];而预后不良组患者的中性粒细胞、血小板计数、单核细胞计数高于预后良好患者,中性粒胞具有激活单核细胞凝聚活性、增强细胞粘附力的作用,在应激状态下不仅可加速趋化因子与细胞因子的释放,还可通过调节炎性环境诱导脑细胞损伤,加剧脑血管内血液的粘稠度,最终诱发缺血性卒中的发生;血小板的聚集是冠状动脉狭窄、血栓形成的重要介质,活动度高的血小板还可刺激加速炎性物质的释放从而加快动脉粥样化的发生,而由于缺血性脑卒中患者以老年人居多,合并多种基础疾病,导致动脉内形成大量不稳定板块,当炎症因子呈高水平表达时引诱血管壁粥样化板块沉淀从而增加缺血性事件发生的的风险[21−22];(2)单核细胞是导致动脉粥样硬化斑块形成的主要细胞,还可通过调节血管平滑肌相关信号通路,诱发动脉内血管病变,加剧动脉粥样化形成;既往研究表明,缺血性卒中患者在接受治疗后脑组织细胞内自由基浓度较高,仍处于氧化失调状态,导致其中枢系统环境内氧化过多,不利于缺血性脑组织神经细胞修复,在长期随访中单核细胞表达水平不仅可预测不良心血管事件还可作为脑卒中患者疾病预后的敏感标记物[23−24]。
综上所述,PIV升高与缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良密切相关,高PIV、NIHSS评分均是缺血性卒中患者不良预后的危险因素,可作为早期识别的敏感指标,为临床治疗提供新思路,同时帮助临床医生提早做出预判,及早采取应对措施,帮助患者获得更好的预后。同时,其预测价值能更早的对患者家属进行预警,也更利于患方对疾病进展的了解。本研究是单中心回顾性研究,样本量小,可能会存在选择偏差,因此未来仍需多中心、前瞻性研究来进一步验证PIV对缺血性卒中血管内介入联合替罗非班治疗的预后不良的预测价值。
-
表 1 引物序列
Table 1. Primer sequences
基因名称 序列(5′→3′) 长度
(bp)PCR产物
长度(bp)ZNF470-F2 CCCCGGCAATCATAATGGAAA 21 95 ZNF470-R2 CTCCCTCTCAAACAAGTCTTCAC 23 ZNF545-F2 GACCTTTAGCCGTGGTTATCATC 23 88 ZNF545-R2 GGCTTTCCAGCATTCCTTACAT 22 GAPDH-F GGACCTGACCTGCCGTCTAG 20 100 GAPDH-R GTAGCCCAGGATGCCCTTGA 20 F:上游引物、正向;R:下游引物、反向。 -
[1] Practice Committee of the American Society for Reproductive Medicine. Evaluation and treatment of recurrent pregnancy loss: A committee opinion[J]. Fertil Steril,2012,98(5):1103-1111. doi: 10.1016/j.fertnstert.2012.06.048 [2] Bender Atik R,Christiansen O B,Elson J,et al. ESHRE guideline: Recurrent pregnancy loss: An update in 2022[J]. Hum Reprod Open,2023,2023(1):hoad002. [3] Hong Li Y,Marren A. Recurrent pregnancy loss: A summary of international evidence-based guidelines and practice[J]. Aust J Gen Pract,2018,47(7):432-436. doi: 10.31128/AJGP-01-18-4459 [4] 中华医学会妇产科学分会产科学组,复发性流产诊治专家共识编写组,张建平,等. 复发性流产诊治专家共识(2022)[J]. 中华妇产科杂志,2022,57(9):653-667. doi: 10.3760/cma.j.cn112141-20220421-00259 [5] Muyayalo K P,Tao D,Lin X X,et al. Age-related changes in CD4+ T and NK cell compartments may contribute to the occurrence of pregnancy loss in advanced maternal age[J]. J Reprod Immunol,2023,155(2):103790. [6] Tise C G,Byers H M. Genetics of recurrent pregnancy loss: A review[J]. Curr Opin Obstet Gynecol,2021,33(2):106-111. doi: 10.1097/GCO.0000000000000695 [7] Park S J,Min J Y,Kang J S,et al. Chromosomal abnormalities of 19,000 couples with recurrent spontaneous abortions: A multicenter study[J]. Fertil Steril,2022,117(5):1015-1025. doi: 10.1016/j.fertnstert.2022.01.011 [8] Kim M A,Kim H S,Kim Y H. Reproductive,obstetric and neonatal outcomes in women with congenital uterine anomalies: A systematic review and meta-analysis[J]. J Clin Med,2021,10(21):4797. doi: 10.3390/jcm10214797 [9] Practice committees of the American society for reproductive medicine and the society for reproductive endocrinology and infertility. Diagnosis and treatment of luteal phase deficiency: A committee opinion[J]. Fertil Steril,2021,115(6):1416-1423. doi: 10.1016/j.fertnstert.2021.02.010 [10] 复发性流产合并风湿免疫病免疫抑制剂应用中国专家共识编写组,吕良敬,赵爱民,等. 复发性流产合并风湿免疫病免疫抑制剂应用中国专家共识[J]. 中华生殖与避孕杂志,2020,40(7):527-534. [11] 国家妇幼健康研究会生殖免疫学专业委员会专家共识编写组,赵爱民,韦相才. 复发性流产合并血栓前状态诊治中国专家共识[J]. 中华生殖与避孕杂志,2021,41(10):861-875. [12] 邓玉梅,宋家美,刘仲伟,等. 淋巴细胞免疫治疗次数对复发性流产的疗效观察[J]. 昆明医科大学学报,2019,40(10):150-153. doi: 10.3969/j.issn.1003-4706.2019.10.033 [13] Dakhly D M,Bayoumi Y A,Sharkawy M,et al. Intralipid supplementation in women with recurrent spontaneous abortion and elevated levels of natural killer cells[J]. Int J Gynaecol Obstet,2016,135(3):324-327. doi: 10.1016/j.ijgo.2016.06.026 [14] Deshmukh H,Way S S. Immunological basis for recurrent fetal loss and pregnancy complications[J]. Annu Rev Pathol,2019,14(1):185-210. doi: 10.1146/annurev-pathmechdis-012418-012743 [15] 王班琴. H2S通过干扰滋养细胞入侵及调控母胎界面TH1/TH2平衡影响早孕的相关作用机制研究[D]. 济南: 山东大学博士学位论文, 2021. [16] Guerra D D,Hurt K J. Gasotransmitters in pregnancy: From conception to uterine involution[J]. Biol Reprod,2019,101(1):4-25. doi: 10.1093/biolre/ioz038 [17] 熊佳. 二烯丙基三硫醚对妊娠肥胖母鼠繁殖性能和胎盘血管发育的影响[D]. 武汉: 华中农业大学硕士学位论文, 2020. [18] Wang M,Wang Z,Miao Y,et al. Diallyl trisulfide promotes placental angiogenesis by regulating lipid metabolism and alleviating inflammatory responses in obese pregnant mice[J]. Nutrients,2022,14(11):2230. doi: 10.3390/nu14112230 [19] 杜珂珂,严育宏,廖鸿力,等. 不明原因复发性流产伴慢性子宫内膜炎诊断方法和高危因素分析[J]. 中国妇幼保健,2022,37(22):4230-4233. doi: 10.19829/j.zgfybj.issn.1001-4411.2022.22.032 [20] Zhu L,Liu M,Zhang S,et al. Foxp3 TSDR Hypermethylation is correlated with decreased tregs in patients with unexplained recurrent spontaneous abortion[J]. Reprod Sci,2021,28(2):470-478. doi: 10.1007/s43032-020-00299-z [21] 刘乐乐,路玥,王涛,等. MiRNA在不明原因复发性流产中的作用[J]. 生命的化学,2021,41(3):471-477. doi: 10.13488/j.smhx.20200500 [22] Ravikumar G,Mukhopadhyay A,Mani C,et al. Placental expression of angiogenesis-related genes and their receptors in IUGR pregnancies: Correlation with fetoplacental and maternal parameters[J]. J Matern Fetal Neonatal Med,2020,33(23):3954-3961. doi: 10.1080/14767058.2019.1593362 [23] Lu L,Kingdom J,Burton G J,et al. Placental stem villus arterial remodeling associated with reduced hydrogen sulfide synthesis contributes to human fetal growth restriction[J]. Am J Pathol,2017,187(4):908-920. doi: 10.1016/j.ajpath.2016.12.002 [24] Li W,Chen P,Pan Y,et al. Construction of a band-aid like cardiac patch for myocardial infarction with controllable H2S release[J]. Adv Sci (Weinh),2022,9(35):e2204509. doi: 10.1002/advs.202204509 [25] Li M,Liu Y,Deng Y,et al. Therapeutic potential of endogenous hydrogen sulfide inhibition in breast cancer (Review)[J]. Oncol Rep,2021,45(5):68. doi: 10.3892/or.2021.8019 [26] Matin M,Mörgelin M,Stetefeld J,et al. Affinity-enhanced multimeric VEGF (vascular endothelial growth factor) and PlGF (placental growth factor) variants for specific adsorption of sFlt-1 to restore angiogenic balance in preeclampsia[J]. Hypertension,2020,76(4):1176-1184. doi: 10.1161/HYPERTENSIONAHA.120.14974 [27] 刘鹏刚,刘彩虹,包文斌,等. 二花脸猪隐睾和正常睾丸组织学观察及PCNA/CD31蛋白差异表达分析[J]. 中国兽医科学,2023,53(3):388-395. doi: 10.16656/j.issn.1673-4696.2023.0036 [28] 夏士涛,王培宇,魏静,等. 海风藤醇提物抑制CD31因子对CSDH模型大鼠血肿外膜血管炎症影响的研究[J]. 中医药学报,2022,50(11):37-41. doi: 10.19664/j.cnki.1002-2392.220246 [29] Smink A M,Najdahmadi A,Alexander M,et al. The effect of a fast-releasing hydrogen sulfide donor on vascularization of subcutaneous scaffolds in immunocompetent and immunocompromised mice[J]. Biomolecules,2020,10(5):722. doi: 10.3390/biom10050722 [30] Guo X,Yi H,Li T C,et al. Role of vascular endothelial growth factor (VEGF) in human embryo implantation: Clinical implications[J]. Biomolecules,2021,11(2):253. doi: 10.3390/biom11020253 [31] 谢斌. CLEC14A通过VEGFA/VEGFR-2信号通路调控婴幼儿血管瘤内皮细胞增殖和血管生成的机制研究[D]. 南昌: 南昌大学博士学位论文, 2022. -






 下载:
下载:
 下载:
下载: