Determination of Norfloxacin Glucose Injection in EDTA by RP-HPLC Method
-
摘要:
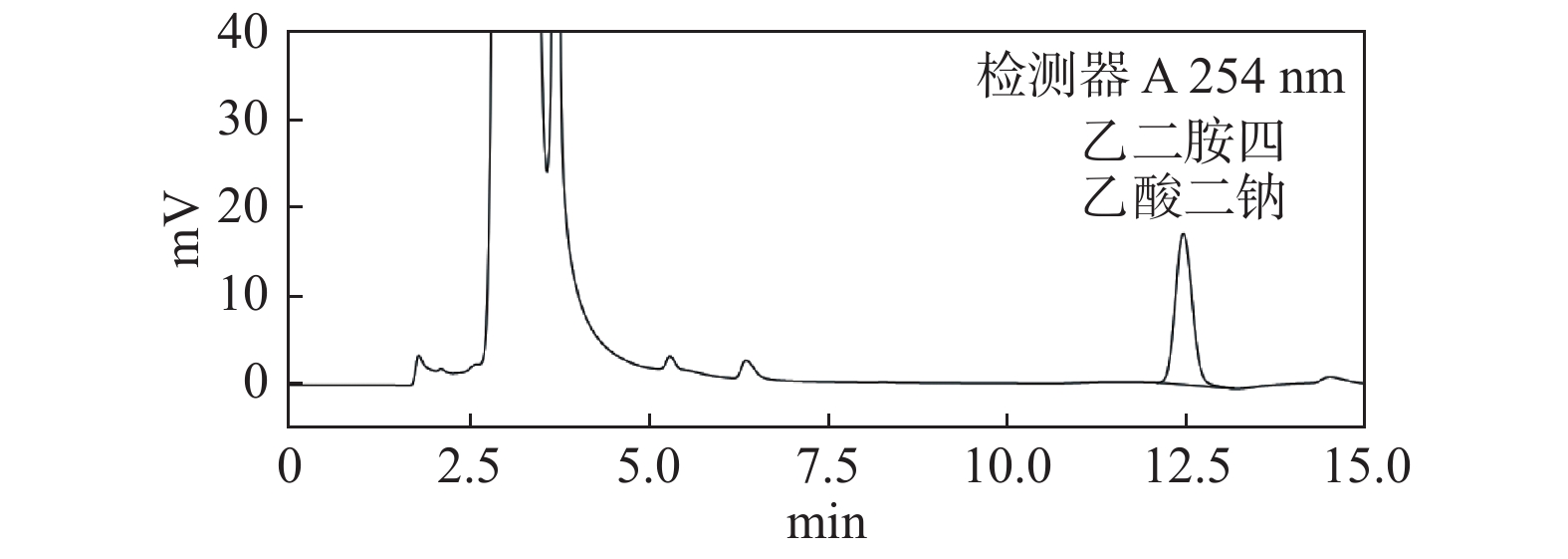
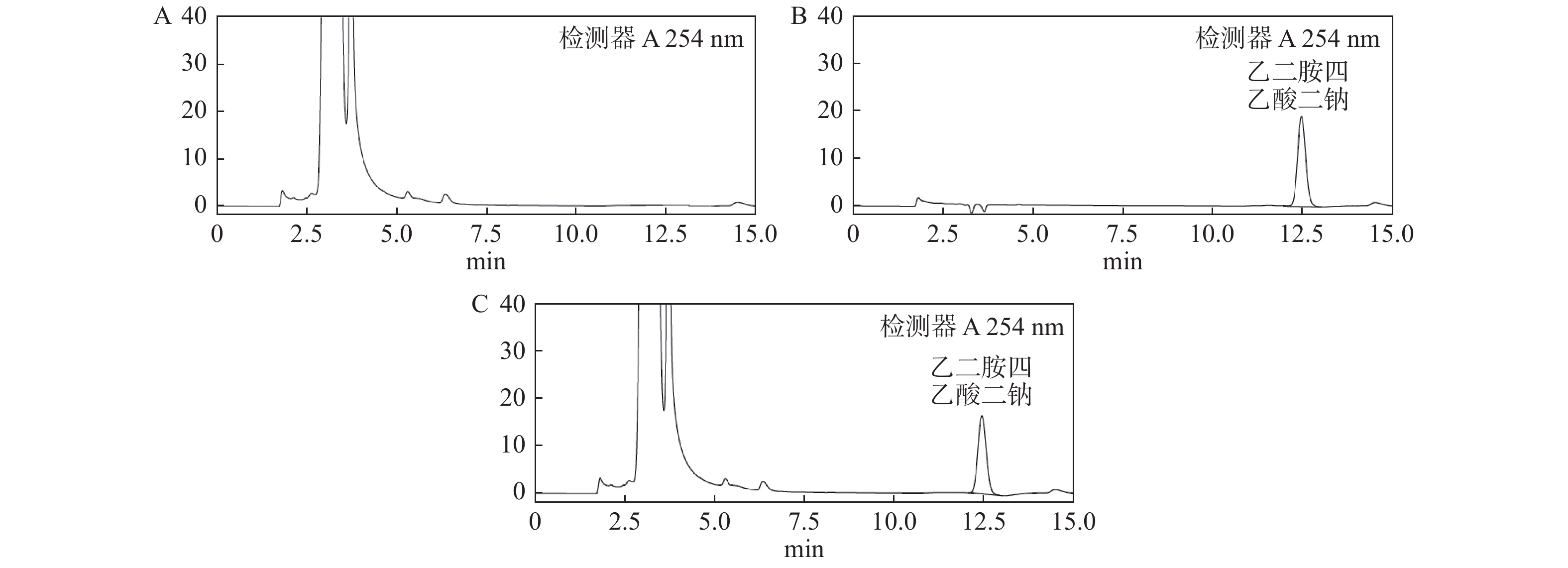
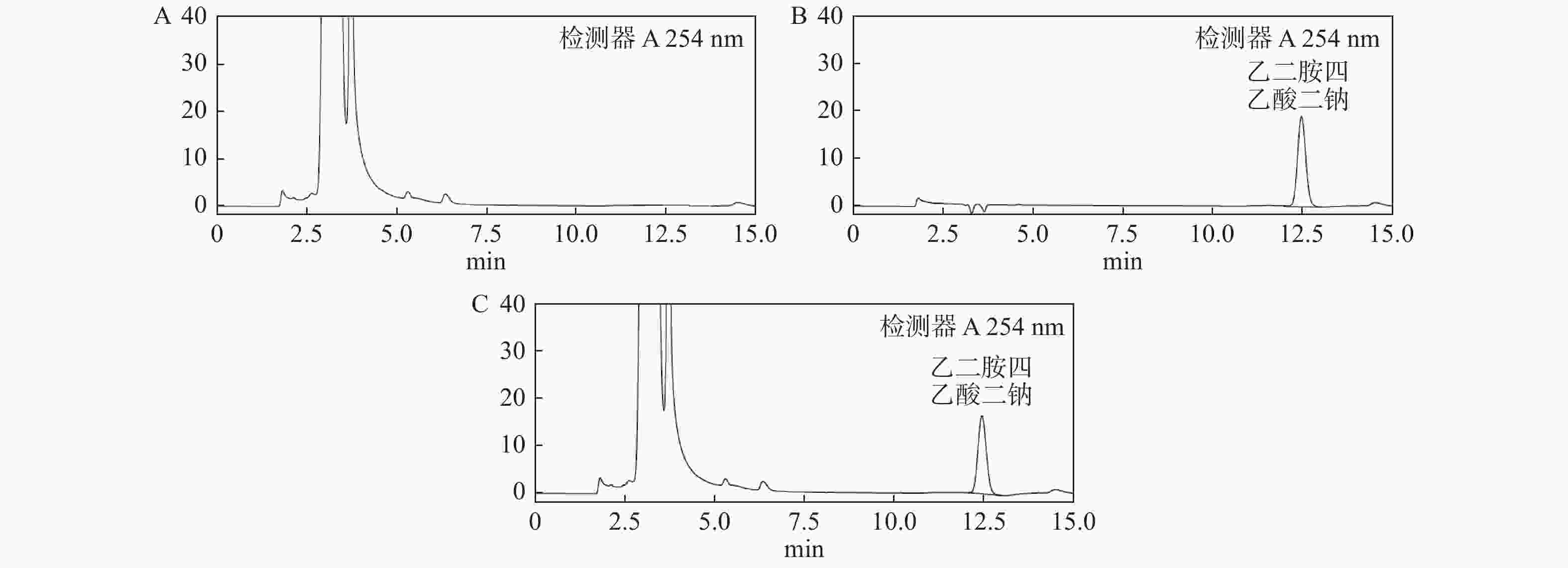
目的 建立诺氟沙星葡萄糖注射液中乙二胺四乙酸二钠的含量测定方法。 方法 选择色谱柱为(SHISEIDO C18-MGⅡ 5 µm 4.6×250 mm),流动相为乙腈:0.05 mol/L醋酸铵:水,流动相比例为70∶15∶15,流速为1.0 mL/min,进样体积为20 µL,柱温为35 ℃,检测波长为254 nm,采用三氯化铁和乙二胺四乙酸二钠反应形成螯合物后对其进行测定。 结果 乙二胺四乙酸二钠峰与其他色谱峰分离度良好;乙二胺四乙酸二钠在2.0326~200.3260 µg/mL浓度范围内与峰面积呈良好的线性关系(R2 = 0.9997),平均回收率为98.11%(n = 9)。 结论 该方法快速、简便、专属性强、精密度高、重复性好,结果准确可靠,适用于诺氟沙星葡萄糖注射液中乙二胺四乙酸二钠的含量测定。 -
关键词:
- 高效液相色谱法 /
- 诺氟沙星葡萄糖注射液 /
- 乙二胺四乙酸二钠 /
- 含量测定
Abstract:Objective To establish a method for determination of norfloxacin glucose injection in compound EDTA injection. Methods The chromatographic column was Shiseido C18-MGⅡ5 μm 4.6×250 mm, with the mobile phase of acetonitrile: 0.05 mol/L ammonium acetate: water, mobile phase ratio of 70∶15∶15, flow rate of 1.0 mL/min, injection volume of 20 L, column temperature of 35 ℃, detection wavelength of 254 nm. The chelate from ferric chloride and EDTA disodium reaction were determined. Results EDTA-2Na was detected without any interference. In the range and peak area of 2.0326 µg/mL-200.3260 µg/mL, EDTA-2Na showed a good linear relation (R2 = 0.9997), the average recovery was 98.11% (n = 9). Conclusion The method is rapid, simple, specific, reproducible, accurate and reliable, and is suitable for determination of EDTA in norfloxacin glucose injection. -
表 1 回收率(n = 9)
Table 1. Recovery rate (n = 9)
序号 EDTA-2Na加入量
(mL)实际测得量
(μg/mL)样品含量
(μg/mL)加标量
(μg/mL)回收率
(%)平均回收率
(%)RSD
(%)1 0.8 17.7539 9.8869 8.0057 98.59 98.56 0.03 2 17.7477 98.53 3 17.7506 98.56 4 1.0 19.4621 10.0040 98.36 98.26 0.17 5 19.7295 98.35 6 19.7018 98.07 7 1.2 21.6524 12.0241 96.32 97.50 1.06 8 21.7121 97.99 9 21.7340 98.20 表 2 15批样品EDTA-2Na的测定结果(μg/mL)
Table 2. Results of EDTA-2Na determination for 15 batches of samples (μg/mL)
序号 批号 处方
加入量实际
测得量平均值 RSD
(%)1 K18022001 100 97.1 97.9 1.46 2 K17100903 96.6 3 K18022002 98.1 4 K17080202 97.0 5 k17080201 96.3 6 k17110501 96.7 7 K17010802 97.3 8 K17100902 98.1 9 K18022001 99.2 10 K18022002 100.2 11 K18022004 98.3 12 K18032601 97.2 13 K18032602 99.1 14 k18010802 101.1 15 k17100901 96.6 -
[1] 杜晨成. 喹诺酮类药物的临床应用研究[J]. 智慧健康,2021,7(3):173-175. [2] 赵晓东,吕传柱,于学忠,等. 喹诺酮类抗菌药物急诊临床应用指导意见[J]. 中国急救医学,2020,40(11):1047-1056. doi: 10.3969/j.issn.1002-1949.2020.11.004 [3] 杨俾忍. 喹诺酮类抗菌药物临床应用评价[J]. 中国现代药物应用,2020,14(15):193-194. [4] 聂鲁,刘连奇,周辛波. 喹诺酮类抗菌药物发展历程与临床应用[J]. 临床药物治疗杂志,2019,17(7):12-16. doi: 10.3969/j.issn.1672-3384.2019.07.004 [5] 王春香. 药学干预对喹诺酮类抗菌药物使用情况的影响探讨[J]. 中国现代药物应用,2019,13(8):152-153. [6] 肖菊华. 诺氟沙星注射液治疗尿路感染75例病人的临床观察与护理[J]. 药物与人,2014,27(7):227. [7] 许晓文,肖佩华,刘海方. 诺氟沙星的不良反应与合理用药[J]. 今日药学,2009,19(4):27-28. [8] 徐杰远,林文鑫. 诺氟沙星的不良反应和临床应用注意[J]. 齐鲁药事,2005,35(7):441-442. [9] 易秋艳,崔学文,王灿,等. 乙二胺四乙酸二钠对异丙酚脂肪乳注射液污染微生物的影响[J]. 中国药学杂志,2019,54(18):1508-1510. [10] 刁岩忠,韩继永,陈祥峰. HPLC法测定注射用泮托拉唑钠中乙二胺四乙酸二钠的含量[J]. 药物分析杂志,2011,31(2):282-284. [11] 郑俊民. 药用辅料手册[M]. 北京: 化学工业出版社, 2005: 263. [12] 国家药典委员会. 中华人民共和国药典2010年版(二部)[S]. 北京: 中国医药科技出版社, 2010: 1206. [13] 孙春霞,韩文芳,李津. HPLC测定氯化钠滴眼液中乙二胺四乙酸二钠的含量[J]. 食品与药品,2015,17(4):270-272. doi: 10.3969/j.issn.1672-979X.2015.04.011 [14] 薛琦,杨龙华. 反相离子对高效液相色谱法测定混悬滴眼液中乙二胺四乙酸二钠含量[J]. 中国药业,2012,21(1):24-25. doi: 10.3969/j.issn.1006-4931.2012.01.013 [15] 赵磊,刘北力,蒋黄卉,等. 高效液相色谱法测定碳酸氢钠注射液中乙二胺四乙酸二钠[J]. 化学分析计量,2020,29(1):23-25. doi: 10.3969/j.issn.1008-6145.2020.01.006 [16] 郭倩倩. HPLC法测定注射用泮托拉唑钠中乙二胺四乙酸二钠的含量[J]. 北方药学,2019,16(2):2-3. [17] 胡裕迪,朱硕然,印玺璟,等. HPLC法测定泊沙康唑注射液中乙二胺四乙酸二钠的含量[J]. 中国医药工业杂志,2019,50(7):786-791. [18] 周会芹,王梅娟. RP-HPLC法测定甲硝唑氯化钠注射液中乙二胺四乙酸二钠的含量[J]. 首都医药,2013,20(14):87-88. [19] 耿志旺,刘蔚,刘茜,等. HPLC法测定丙泊酚注射液中乙二胺四乙酸二钠含量[J]. 药物分析杂志,2011,31(3):586-588. [20] 刘巨英. 浅析葡萄糖与氢氧化铜反应的变化现象[J]. 中国校外教育,2015,18(12):122. -





 下载:
下载: