Prognostic Value of Pan-immune Inflammatory Values in Patients with Ischemic Stroke Treated with Intravascular Intervention Combined with Tirofiban
-
摘要:
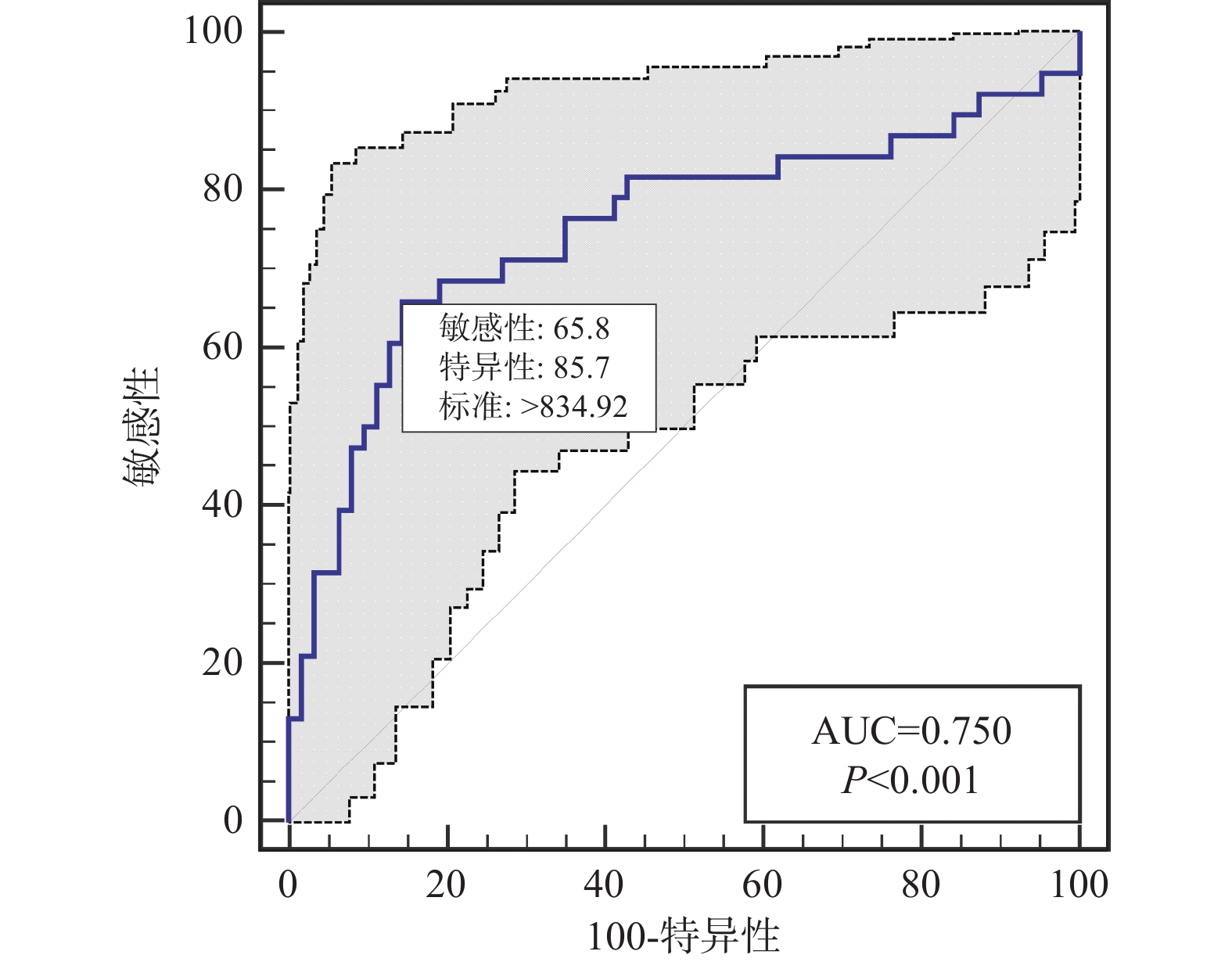
目的 探讨泛免疫炎症值(pan-immune-inflammation value,PIV)对缺血性卒中(acute ischemic stroke,AIS)患者血管内介入联合替罗非班治疗疾病转归的预测价值 方法 选取2019年1月至2023年12月昭通市第一人民医院脑血管科收治并接受血管内介入联合替罗非班治疗的102例缺血性卒中患者作为研究对象。根据入院后神经功能缺损程度将患者分为轻度组(n = 9)、中度组(n = 45)、重度组(n = 48)。根据治疗后90 d改良mRS评分将患者分为预后良好组(n = 63)和预后不良组(n = 38)。收集所有研究对象的临床资料并进行分析。采用受试者工作特性(ROC)曲线评估PIV水平对缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的预测价值;采用多因素Logistic回归探讨缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的危险因素。 结果 预后良好组PIV水平331.1(221.9,662.7)低于预后不良组 1025.7 (451.5,1841.3 )(P < 0.05)。重度组PIV水平高于轻、中度组,中度组PIV水平高于轻度组(P < 0.05)。PIV预测缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的AUC(95%CI)为0.750(95%CI 0.654~0.831),截点值为834.92,特异度为85.71%,灵敏度为65.79%。多因素分析显示,NIHSS评分 > 18分(OR = 5.944,95%CI 2.011~19.137)、PIV > 834.92(OR = 4.863,95%CI 1.410~18.685)是缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的危险因素(P < 0.05)。结论 PIV升高与缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良密切相关,高PIV、NIHSS评分均是缺血性卒中患者不良预后的危险因素,可作为早期识别的敏感指标。 Abstract:Objective To investigate the predictive value of pan-immune inflammatory values (PIV) in the prognosis of patients with ischemic stroke (AIS) treated with intravascular intervention combined with tirofiban. Methods 102 AIS cases admitted to the Department of Neurology of the First People's Hospital of Zhaotong from January 2019 to December 2023 and treated with intravascular intervention combined with Tirofiban were selected as the study objects. The patients were divided into the mild group (n = 9), moderate group (n = 45) and severe group (n = 48) according to the score of NIHSS after the admission. According to the mRS 90 days after the treatment, the cases were divided into the good prognosis group (n = 63) and poor prognosis group (n = 38). Data were collected and analyzed. The predictive value of PIV level in patients with ischemic stroke treated with intravascular intervention combined with tirofiban was evaluated by ROC. The risk factors of adverse outcomes in patients with ischemic stroke treated with intravascular intervention combined with tirofiban were investigated by multivariate Logistic regression. Results A total of 102 patients with ischemic stroke were included. The PIV level in the good prognosis group 331.1(221.9, 662.7) was lower than that in the poor prognosis group 1025.7 (451.5,1841.3 ) (P < 0.05). PIV level in the severe group was higher than that in the mild and moderate groups, and PIV level in the moderate group was higher than that in the mild group (P < 0.05). The AUC (95%CI) of PIV for predicting adverse outcomes of intravascular intervention combined with tirofiban in patients with ischemic stroke was 0.750 (95%CI 0.654~0.831), the cut-off point was 834.92, the specificity was 85.71% and the sensitivity was 65.79%. NIHSS score > 18 (OR = 5.944 95%CI 2.011~19.137), PIV > 834.92 (OR = 4.863, 95%CI 1.410~18.685) were the risk factors for the poor outcome of intravascular intervention combined with tirofiban in patients with ischemic stroke (P < 0.05).Conclusion Elevated PIV is closely related to the poor outcomes in patients with ischemic stroke treated with intravascular intervention combined with Tirofiban. High PIV and NIHSS scores are both risk factors for the poor prognosis in patients with ischemic stroke, and can be used as the sensitive indicators for the early identification. -
表 1 入组患者基本资料比较 [($ \bar x \pm s $)/n(%)/M(P25,P75)]
Table 1. Comparison of basic data of enrolled patients [($ \bar x \pm s $)/n(%)/M(P25,P75)]
项目 预后良好组 (n = 63) 预后不良组 (n = 39) t/χ2/z P 年龄(岁) 60.76±11.51 62.49±11.51 −0.74 0.70 身高(cm) 162.54±7.29 163.13±6.29 −0.42 0.60 体重(kg) 61.84±9.16 62.46±6.84 −0.36 0.70 BMI(kg/m2) 23.33±2.52 23.48±2.41 −0.30 0.76 性别(n) 1.78 0.18 男 37(58.73) 28(71.79) 女 26(41.27) 11(28.21) 吸烟(n) 30(47.62) 26(66.67) 3.53 0.06 饮酒(n) 10(15.87) 11(28.21) 2.24 0.13 入院NIHSS(n) 17.80 < 0.001* 轻 8(12.70) 1(2.56) 中 35(55.56) 9(23.08) 重 20(31.75) 29(74.36) 高血压(n) 33(52.38) 23(58.97) 0.42 0.50 高脂血症(n) 17(26.98) 13(33.33) 0.47 0.50 糖尿病(n) 9(14.29) 5(12.82) 0.04 0.80 心房颤动(n) 5(7.94) 4(10.26) 0.16 0.70 冠心病(n) 4(6.35) 0(0) 3.96 0.05 血小板(×109/L) 203.65±59.79 227.95±68.13 −1.89 0.05 淋巴细胞(×109/L) 1.49±0.60 1.09±0.55 3.42 < 0.001* 中性粒细胞(×109/L) 7.05±3.67 10.07±3.99 −3.91 < 0.001* 单核细胞(×109/L) 0.47±0.19 0.52±0.31 −0.90 0.40 甘油三酯(mmol/l) 1.34 (0.81,2.08) 1.34 (0.87,2.28) −0.39 0.69 总胆固醇(mmol/l) 4.45±0.99 4.30±1.03 0.67 0.30 LDL-C(mmol/l) 2.74±0.85 2.71±1.03 0.13 0.40 HDL-C(mmol/l) 1.11±0.30 1.09±0.25 0.29 0.60 心率(次/min) 77.22±14.95 79.03±14.62 −0.60 0.50 收缩压(mmHg) 149.87±20.02 147.82±22.64 0.48 0.70 舒张压(mmHg) 89.89±12.08 93.15±14.74 −1.22 0.20 *P < 0.05。 表 2 入院时不同NIHSS患者PIV水平比较[M(P25,P75)]
Table 2. Comparison of PIV levels among different NIHSS patients at admission [M(P25,P75)]
入院NIHSS分组 n PIV χ2 P 轻度组 9 279.9 (155.4,396.9) a 15.097 0.001* 中度组 45 308.5 (215.4,845.8) a 重度组 48 810.8 (407.2, 1524.5 )注:a表示两两比较分析,与重度组比较,*P < 0.05。 表 3 不同疾病转归患者PIV水平对比[M(P25,P75)]
Table 3. Comparison of PIV levels in patients with different disease outcomes [M(P25,P75)]
MRS预后 n PIV Z P 预后良好 63 331.1 (221.9,662.7) −4.192 <0.001* 预后不良 38 1025.7 (451.5,1841.3 )注:MRS预后两组患者PIV比较,*P < 0.05。 表 4 检测指标对缺血性卒中患者血管内介入联合替罗非班治疗疾病转归不良的预测价值
Table 4. Predictive value of the tested indicators for poor disease outcome in patients with ischemic stroke treated with endovascular intervention combined with tirofiban
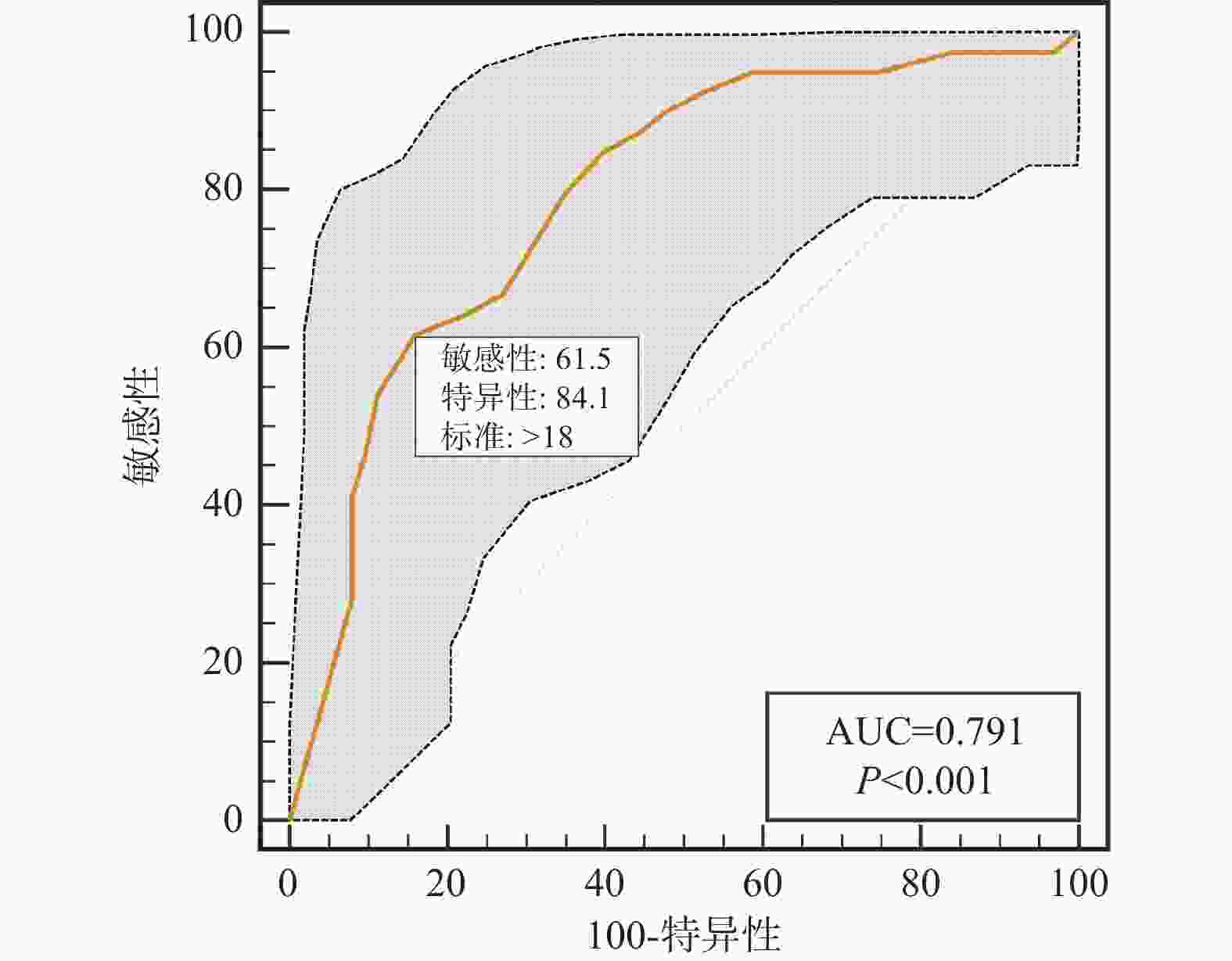
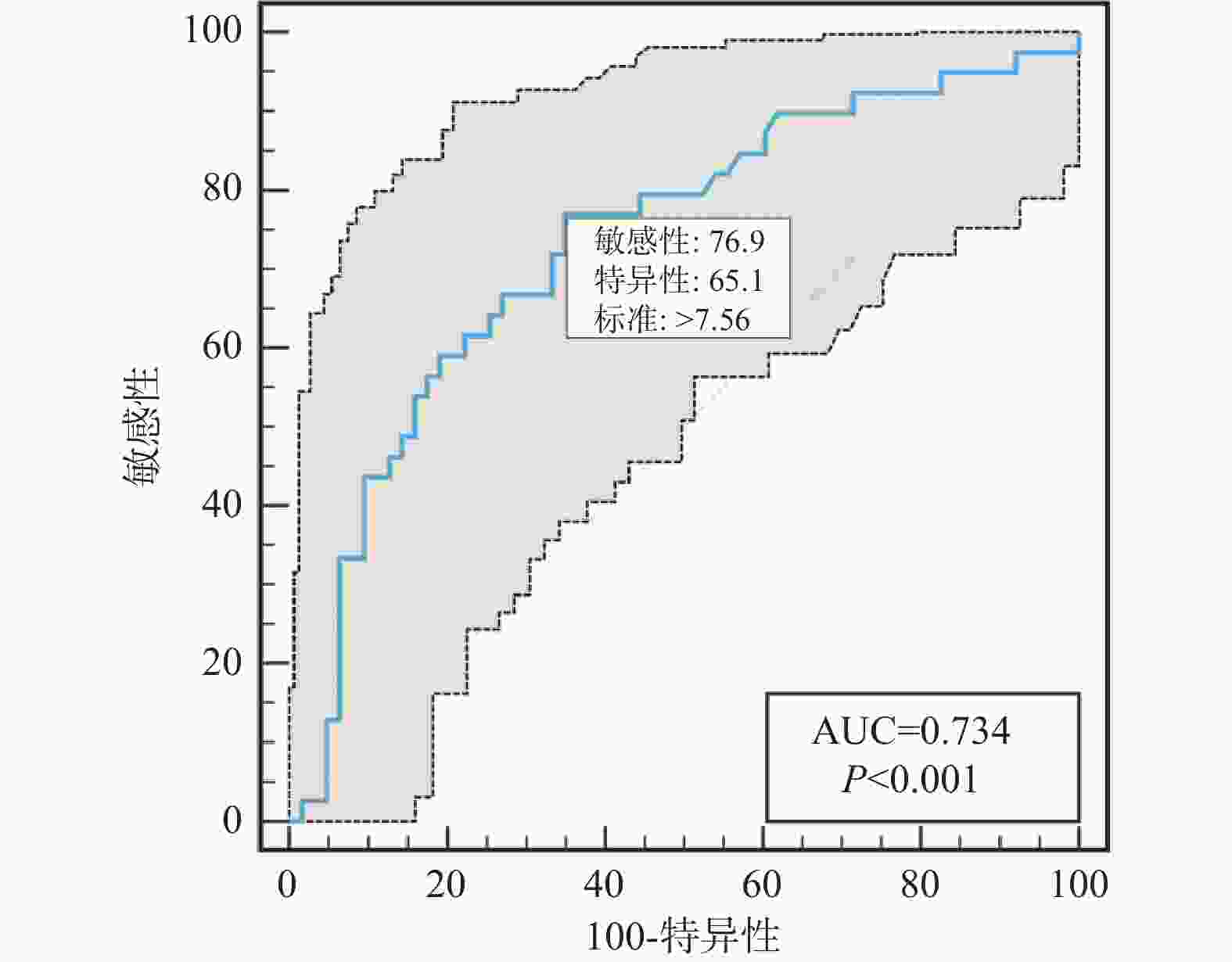
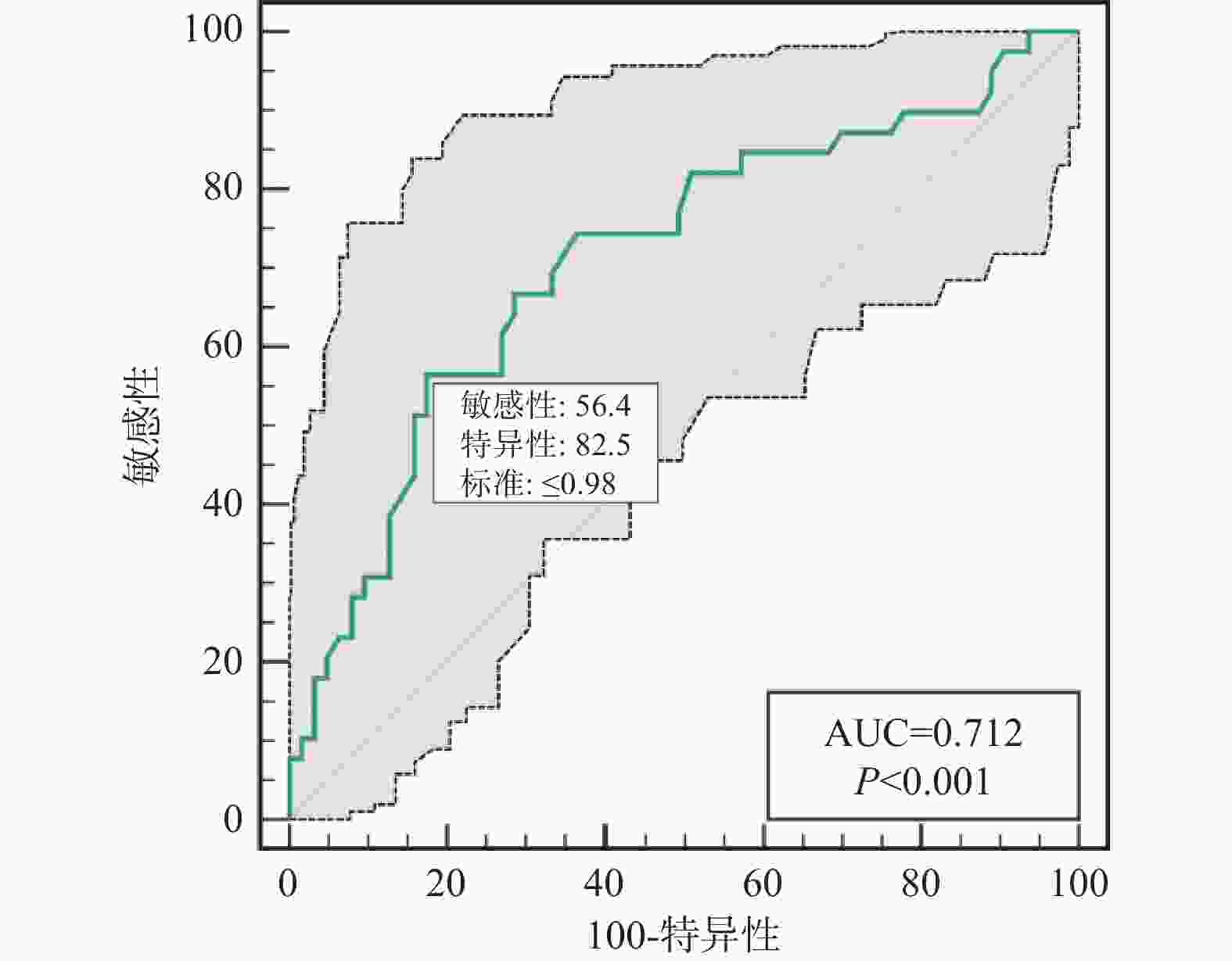
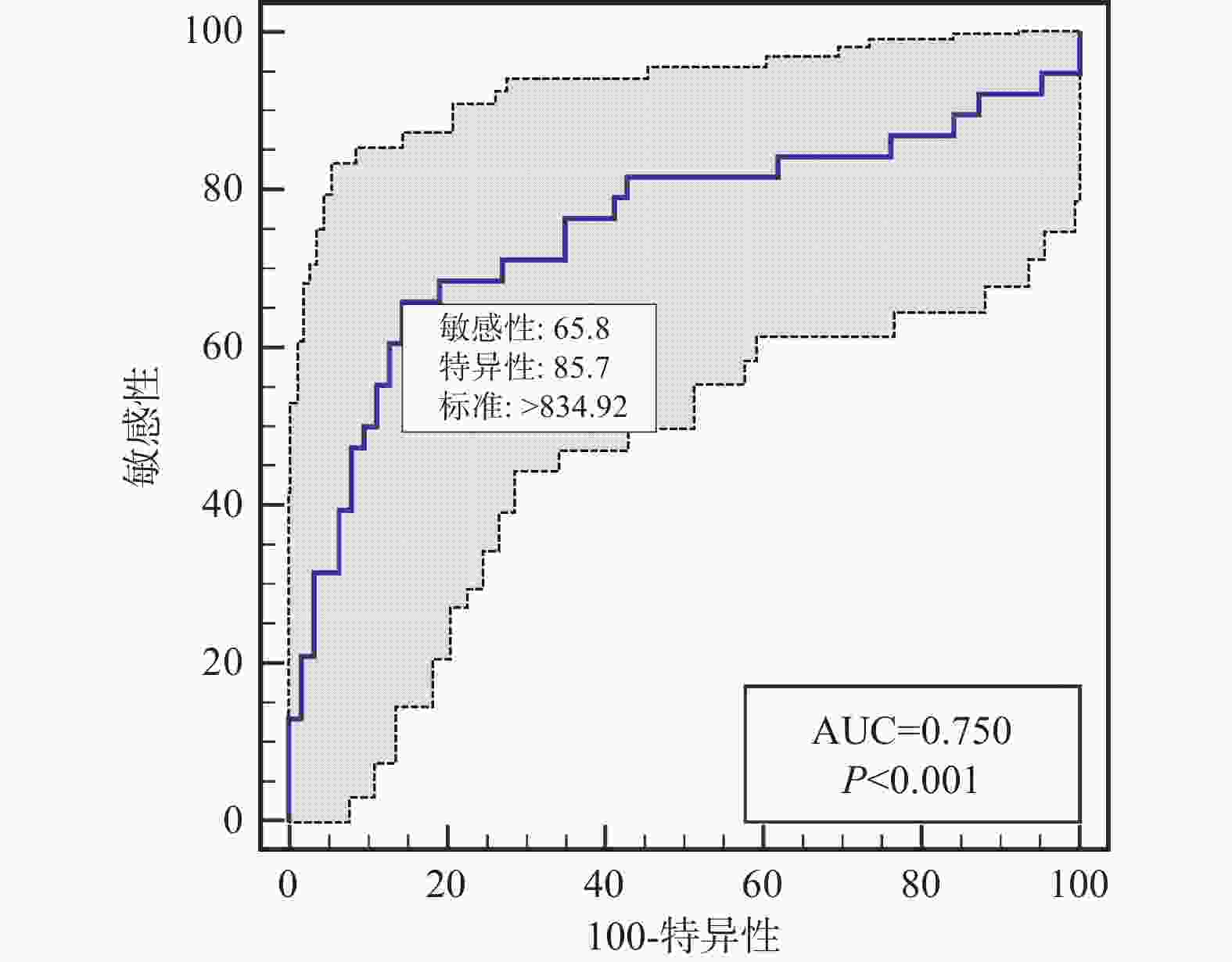
检测指标 AUC 95%CI 截点值 特异度(%) 灵敏度(%) NIHISS 0.791 0.699~0.865 18 84.13 61.54 PIV 0.750 0.654~0.831 834.92 85.71 65.79 淋巴细胞 0.712 0.614~0.798 0.98 82.54 56.41 中性粒细胞 0.734 0.637~0.817 7.56 65.08 76.92 表 5 缺血性卒中患者血管内介入联合替罗非班治疗预后不良的单因素及多因素分析
Table 5. Univariate and multivariate analysis of poor prognosis in patients with ischemic stroke treated with endovascular intervention combined with tirofiban
项目 单因素分析 多因素分析 OR值a 95%CI P OR值b 95%CI P 入院NIHSS < 0.001* 0.001* ≤18 — — — — > 18 8.48 3.432,22.476 5.944 2.011,19.137 PIV < 0.001* 0.012* ≤834.92 — — — — > 834.92 10.192 4.066,27.574 4.863 1.410,18.685 淋巴细胞 < 0.001* 0.1 > 0.98 — — — — ≤0.98 6.118 2.526,15.670 2.666 0.819,8.719 中性粒细胞 < 0.001* 0.2 ≤7.56 — — — — > 7.56 6.212 2.589,16.101 2.202 0.631,7.657 注:a是单因素逻辑回归的OR值,b是多因素逻辑回归的结果;*P < 0.05。 -
[1] Jolugbo P,Ariëns R A. Thrombus composition and efficacy of thrombolysis and thrombectomy in acute ischemic stroke[J]. Stroke,2021,52(3):1131-1142. doi: 10.1161/STROKEAHA.120.032810 [2] Qiu Y M,Zhang C L,Chen A Q,et al. Immune cells in the BBB disruption after acute ischemic stroke: Targets for immune therapy?[J]. Frontiers in Immunology,2021,12(2):67-81. [3] Mendelson S J,Prabhakaran S. Diagnosis and management of transient ischemic attack and acute ischemic stroke: A review[J]. JAMA,2021,325(11):1088-1098. doi: 10.1001/jama.2020.26867 [4] Wang J,Zou D. Tirofiban-induced thrombocytopenia[J]. Annals of Medicine,2023,55(1):223-231. [5] Phipps M S,Cronin C A. Management of acute ischemic stroke[J]. BMJ,2020,12(8):368-375. [6] Zhu H,Hu S,Li Y,et al. Interleukins and ischemic stroke[J]. Frontiers in Immunology,2022,31(8):82-87. [7] Okyar Baş A,Güner M,Ceylan S,et al. Pan-immune inflammation value; A novel biomarker reflecting inflammation associated with frailty[J]. Aging Clinical and Experimental Research,2023,35(8):1641-1649. doi: 10.1007/s40520-023-02457-0 [8] Li J,Qiu Y,Zhang C,et al. The role of protein glycosylation in the occurrence and outcome of acute ischemic stroke[J]. Pharmacological Research,2023,191(2):106-112. [9] Yang X C,Liu H,Liu D C,et al. Prognostic value of pan-immune-inflammation value in colorectal cancer patients: A systematic review and meta-analysis[J]. Frontiers in Oncology,2022,12(6):1036-1041. [10] Hendrix P,Melamed I,Collins M,et al. NIHSS 24 h after mechanical thrombectomy predicts 90-day functional outcome[J]. Clinical Neuroradiology,2022,32(2):401-406. doi: 10.1007/s00062-021-01068-4 [11] Bogdanov L,Shishkova D,Mukhamadiyarov R,et al. Excessive adventitial and perivascular vascularisation correlates with vascular inflammation and intimal hyperplasia[J]. International Journal of Molecular Sciences,2022,23(20):121-128. [12] Liu C,Niu K,Xiao Q. Updated perspectives on vascular cell specification and pluripotent stem cell-derived vascular organoids for studying vasculopathies[J]. Cardiovascular Research,2022,118(1):97-114. doi: 10.1093/cvr/cvaa313 [13] Shuai J,Gong Z,Huang L,et al. Effect of intravenous tirofiban vs placebo before endovascular thrombectomy on functional outcomes in large vessel occlusion stroke: The RESCUE BT randomized clinical trial[J]. JAMA,2022,328(6):543-553. doi: 10.1001/jama.2022.12584 [14] Al-Salihi M M,Ayyad A,Al-Jebur M S,et al. Safety and efficacy of tirofiban in the management of stroke: A systematic review and meta-analysis of randomized controlled trials[J]. Clinical Neurology and Neurosurgery,2023,6(14):107-115. [15] Fan Q,Zhao Y,Zhang J,et al. Factors influencing early diagnosis and poor prognosis of dysphagia after senile ischemic stroke[J]. Journal of Molecular Neuroscience,2024,74(2):31-42. doi: 10.1007/s12031-024-02210-w [16] Murat B,Murat S,Ozgeyik M,et al. Comparison of pan‐immune‐inflammation value with other inflammation markers of long‐term survival after ST‐segment elevation myocardial infarction[J]. European Journal of Clinical Investigation,2023,53(1):138-147 [17] Dolapoglu A,Avci E. Relationship between pan-immune-inflammation value and in major cardiovascular and cerebrovascular events in stable coronary artery disease patients undergoing on-pump coronary artery bypass graft surgery[J]. Journal of Cardiothoracic Surgery,2024,19(1):241-250. doi: 10.1186/s13019-024-02691-1 [18] Lee L E,Ahn S S,Pyo J Y,et al. Pan-immune-inflammation value at diagnosis independently predicts all-cause mortality in patients with antineutrophil cytoplasmic antibody-associated vasculitis[J]. Clinical and Experimental Rheumatology,2021,39(2):88-93. doi: 10.55563/clinexprheumatol/m46d0v [19] Murad H. Short editorial neutrophil-to-lymphocyte ratio and abdominal aortic atherosclerosis among asymptomatic individuals [Z]. SciELO Brasil, 2022,30(17): 735-736 [20] Zhang N,Tse G,Liu T. Neutrophil–lymphocyte ratio in the immune checkpoint inhibitors-related atherosclerosis[J]. European Heart Journal,2021,42(22):2215-2219. doi: 10.1093/eurheartj/ehab158 [21] Lechner K,von Schacky C,McKenzie A L,et al. Lifestyle factors and high-risk atherosclerosis: Pathways and mechanisms beyond traditional risk factors[J]. European Journal of Preventive Cardiology,2020,27(4):394-406. doi: 10.1177/2047487319869400 [22] Bugger H,Zirlik A. Anti-inflammatory strategies in atherosclerosis[J]. Hä mostaseologie,2021,41(6):433-442. [23] Wu X B,Huang L X,Huang Z R,et al. The lymphocyte-to-monocyte ratio predicts intracranial atherosclerotic stenosis plaque instability[J]. Frontiers in Immunology,2022,13(4):915-924. [24] Oggero S,de Gaetano M,Marcone S,et al. Extracellular vesicles from monocyte/platelet aggregates modulate human atherosclerotic plaque reactivity[J]. Journal of Extracellular Vesicles,2021,10(6):1208-1212. -





 下载:
下载: