Effects of miR-125a-3p on Atherosclerotic Plaque, M1/M2 Macrophages, MMP-9 and VEGF
-
摘要:
目的 探讨miR-125a-3p对大耳兔动脉粥样硬化斑块形成、M1/M2巨噬细胞、基质金属蛋白酶9(MMP-9)和血管内皮生长因子(VEGF)的影响。 方法 15只成年雄性健康日本大耳兔,随机分为3组,每组5只,对照组给予普通饲料喂养,动脉粥样硬化模型组给予牛血清白蛋白注射和高胆固醇饲料喂养,miR-125a-3p抑制剂干预组给予动脉粥样硬化兔注射miR-125a-3p干扰慢病毒载体。油红O染色后图像分析法测定斑块面积,免疫组化法测定MMP-9和VEGF,免疫荧光法检测斑块组织中M1标记物CD11c和M2标记物CD206。 结果 与动脉粥样硬化组相比,miR-125a-3p抑制剂组斑块面积百分比显著降低(P < 0.0001)。与对照组相比,动脉粥样硬化组MMP-9(P < 0.001)、VEGF(P < 0.01)和CD11c(P < 0.001)水平显著升高,CD206水平显著降低(P < 0.001);与动脉粥样硬化组相比,miR-125a-3p抑制剂干预组MMP-9(P < 0.01)、VEGF(P < 0.01)和CD11c(P < 0.001)水平有所降低,CD206水平有所升高(P < 0.001)。 结论 抑制miR-125a-3p可减轻动脉粥样硬化斑块的形成,平衡M1/M2巨噬细胞,降低斑块组织中MMP-9和VEGF的表达,miR-125a-3p可能是治疗不稳定动脉粥样硬化斑块的新靶点。 -
关键词:
- miR-125a-3p抑制剂 /
- 动脉粥样硬化 /
- M1/M2巨噬细胞 /
- 基质金属蛋白酶9 /
- 血管内皮生长因子
Abstract:Objective To investigate the effects of miR-125a-3p inhibitors on the atherosclerotic plaque formation, M1/M2 macrophages, MMP-9 and VEGF. Methods Fifteen healthy adult male Japanese big-eared rabbits were randomly divided into 3 groups with 5 rabbits in each group. Those in the control group were fed with the normal diet,, those in the atherosclerosis model group were injected with bovine serum albumin and fed with the high cholesterol diet, and those in the miR-125a-3p inhibitor intervention group were injected with miR-125a-3p to interfere with lentivirus vector. The plaque area was determined by image analysis after oil red O staining, MMP-9 and VEGF were determined by immunohistochemistry, and M1 marker CD11c and M2 marker CD206 in plaque tissues were detected by immunofluorescence. Results Compared with the atherosclerosis group, the percentage of plaque area in miR-125a-3p inhibitor group decreased significantly (P < 0.0001). Compared with the control group, the levels of MMP-9 (P < 0.001), VEGF (P < 0.01) and CD11c (P < 0.001) increased significantly, and the level of cd206 decreased significantly in the atherosclerosis group (P < 0.001); Compared with the atherosclerosis group, the levels of MMP-9 (P < 0.01), VEGF (P < 0.01) and CD11c (P < 0.001) decreased, and the level of cd206 increased in miR-125a-3p inhibitor intervention group (P < 0.001). Conclusion Inhibition of miR-125a-3p can reduce the formation of atherosclerotic plaques, balance M1/M2 macrophages, and reduce the expression of MMP-9 and VEGF in plaque tissues.miR-125a-3p may be a new target for the treatment of unstable plaques. -
Key words:
- miR-125a-3p inhibitors /
- Atherosclerosis /
- M1/M2 macrophages /
- MMP-9 /
- VEGF
-
动脉粥样硬化(atherosclerosis,AS)是一种慢性炎症主导的疾病,其首要驱动因素是巨噬细胞表型失调[1]。激活的巨噬细胞主要被极化成两种表型,经典激活的M1和间接激活的M2巨噬细胞,启动并促进炎症是M1巨噬细胞的主要作用,而M2巨噬细胞的主要作用为抑制炎症[2]。在炎症的早期启动中,由于各种炎症因子的诱导,M1巨噬细胞被大量激活,能够有效清除病原体;随着炎症进展,激活了大量的M2巨噬细胞,炎症反应被抑制[2-3]。Schmitz等[4-5]发现,M2巨噬细胞主要存在于稳定性动脉粥样硬化斑块中,而M1巨噬细胞主要存在于不稳定性动脉粥样硬化斑块中,提示斑块的不稳定可能是由于M1和M2之间失衡。
MicroRNA在单核细胞向巨噬细胞分化过程中起着重要的调控作用。最近研究显示,随着单核细胞分化为M1巨噬细胞,miR-125a-3p和miR-125a-5在此过程中也表达升高。M1巨噬细胞比例的升高,M1/M2巨噬细胞的分化失衡,导致不稳定斑块的形成[6-7]。研究发现MMP-9、VEGF在不稳定斑块中呈高表达[8-9],并且MMP导致巨噬细胞积累,VEGF将巨噬细胞诱导为M1巨噬细胞[10-11],表明MMP-9、VEGF在不稳定斑块中起重要作用。笔者的研究[12]显示miR-125a-3p在动脉粥样硬化斑块的不稳定及破裂中也起着重要的作用。本研究拟进一步在动物体内实验,观察miR-125a-3p抑制剂对动脉粥样硬化斑块形成、M1/M2巨噬细胞以及斑块组织中MMP-9和VEGF表达的影响,以探讨其在动脉粥样硬化斑块的稳定性中的作用,为不稳定斑块的防治提供新的药物靶点。
1. 材料与方法
1.1 实验动物
15只成年雄性健康日本大耳兔,体重2~2.5 kg,由昆明医科大学实验动物学部提供。本研究经医院伦理委员会审批,实验动物的处理符合实验动物相关要求。
1.2 主要试剂和仪器
牛血清白蛋白(Solarbio)、0.5%胆固醇,l0%蛋黄,5%猪油、miR-125a-3p干扰慢病毒载体(广州复能基因有限公司)、生理盐水、甲醛溶液、70%乙醇、4%中性福尔马林、油红O染液、0.01M的PBST、2%BSA、CD11c抗体(Affinity)、CD206抗体(Affinity)、VEGF抗体(Santa Cruz Biotechmology)、MMP-9抗体(Solarbio)。Axio Lab A1显微镜(蔡司)、Axio Observer A1荧光显微镜(蔡司)。
1.3 实验方法
1.3.1 兔动脉粥样硬化模型的建立及miR-125a-3p抑制剂干预
15只成年雄性健康日本大耳兔,给予普通饲料和水适应性喂养7 d,再将其随机分为3组,对照组、动脉粥样硬化模型组(AS模型组)和miR-125a-3p抑制剂干预组(miR-125a-3p抑制剂组)。对照组给以普通饲料喂养,动脉粥样硬化模型组和miR-125a-3p干预组一次性静脉注射牛血清白蛋白(250 mg/kg),即日起给予(0.5%胆固醇,l0%蛋黄,5%猪油)150 g/d喂养2周,给予动脉粥样硬化模型组和miR-125a-3p干预组第2次注射牛血清白蛋白(250 mg/kg),并继续给予高胆固醇饲料喂养。期间,所有组提供充足干净水,定期打扫和清洗兔笼。分别于动脉粥样硬化建立4周和8周后, miR-125a-3p干预组注射以miR-125a-3p干扰慢病毒载体(5 mL/只),对照组和动脉粥样硬化模型组注射以等量生理盐水,12周时耳缘静脉注射空气处死兔子,立即剖开胸、腹腔,游离主动脉全长,剥离外膜脂肪组织,纵行剖开,行以下述处理。
1.3.2 血管内膜油红“O”染色血管粥样斑块大体标本染色步骤
(1)从甲醛溶液中取出标本,用流水洗15 min,剥去外膜,再用蒸馏水浸洗;(2)取储备液60 mL加入蒸溜水至100 mL,混匀放置10 min后染色,染色时间为2~4 min;(3)用70%乙醇浸泡标本至斑块呈红色,底色呈白色为止,最后用蒸馏水浸泡标本,浸入甲醛溶液中保存。油红O染液的配制:储备液:油红O 0.5 g,98%异丙醇 100 mL。临用前取上液6 mL,加蒸馏水4 mL,静置10 min,过滤即可。
1.3.3 免疫组织化学方法检测斑块组织中MMP-9、VEGF
主动脉经4%中性福尔马林固定后,石蜡切片进行MMP-9、VEGF表达测定(SP法,阴性对照一抗用0.01 mol/L PBS代替)。显微镜下拍照后用“Image Pro Plus 4.5”软件进行图像分析,测定阳性物质表达面积和积分光密度。
1.3.4 免疫荧光法检测M1标志物CD11c、M2
标志物CD206 石蜡切片经脱蜡、酒精脱水后,进行抗原修复,用0.01 M的PBST漂洗5 min,重复3次;以2% BSA于37 ℃湿盒内封闭30 min;标本片上滴加适当稀释的荧光标记抗体,放在湿盒中,37 ℃孵育30 min,0.01 mol/L PBS漂洗5 min,重复3次,不时震荡。缓存甘油封片,镜检。
1.4 统计学处理
SPSS 11.0软件进行统计学分析。计量资料以均数±标准差表示,多组间均数比较应用方差分析,P < 0.05为差异有统计学意义。
2. 结果
2.1 血管内膜油红“O”染色结果
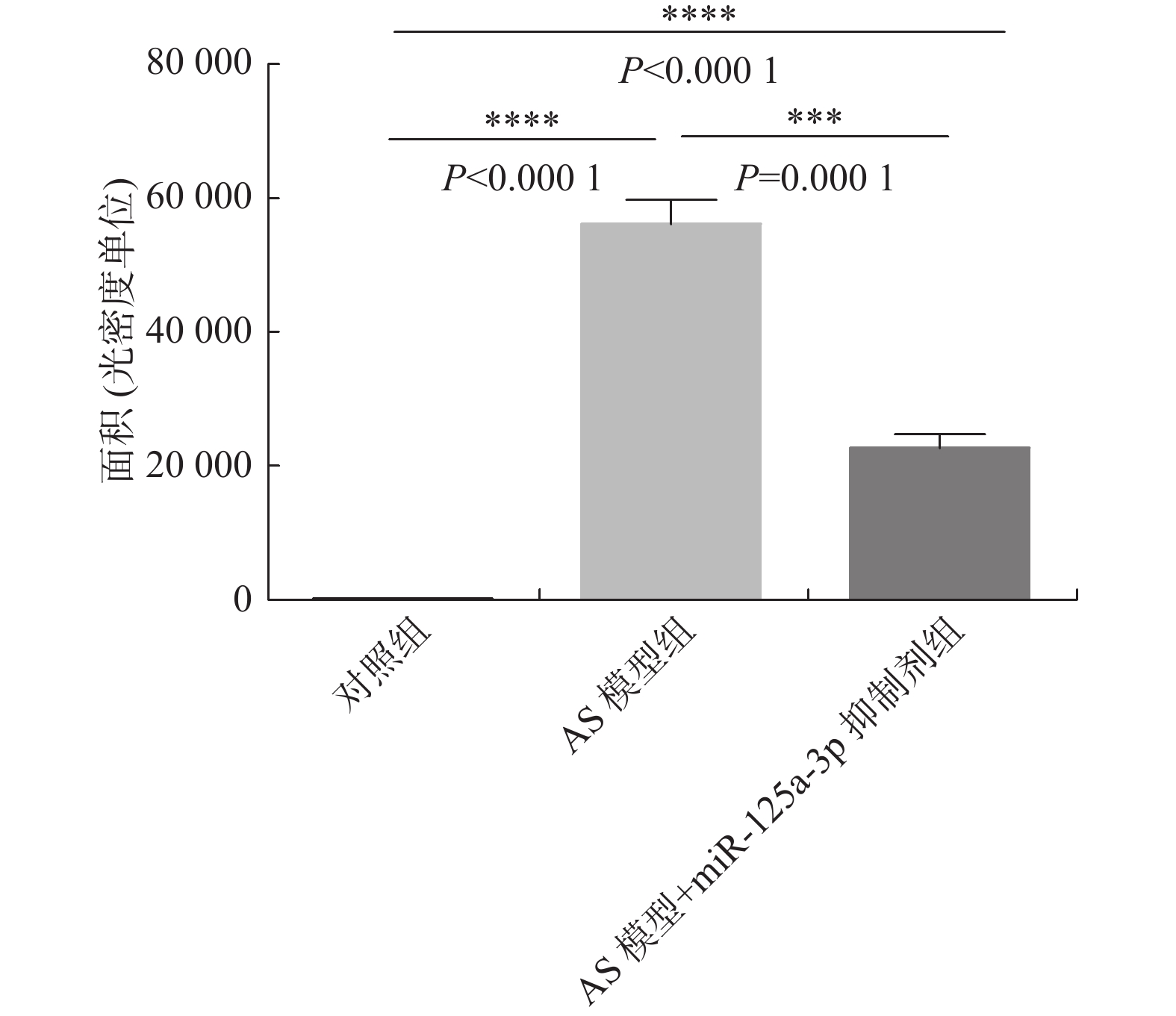
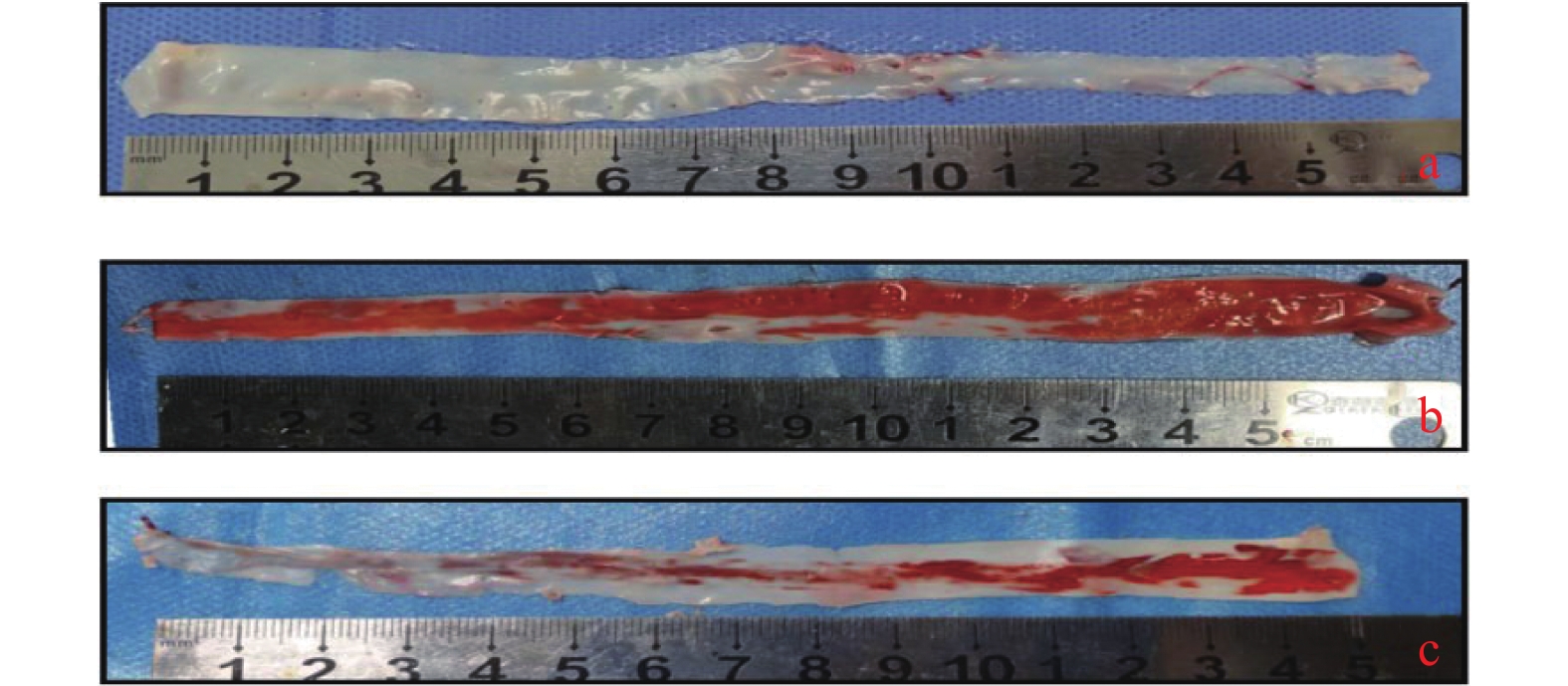
血管内膜油红“O”染色显示,动脉粥样硬化病变处被染成红色。血管内膜油红“O”染色统计结果显示动脉粥样硬化组病变区域远大于miR-125a-3p抑制剂干预组,各组间的差异具有显著性(P < 0.01)(图1、图2)。结果表明:miR-125a-3p抑制剂能减少动脉粥样硬化斑块的形成。
2.2 免疫组织化学方法检测斑块组织中MMP9的结果
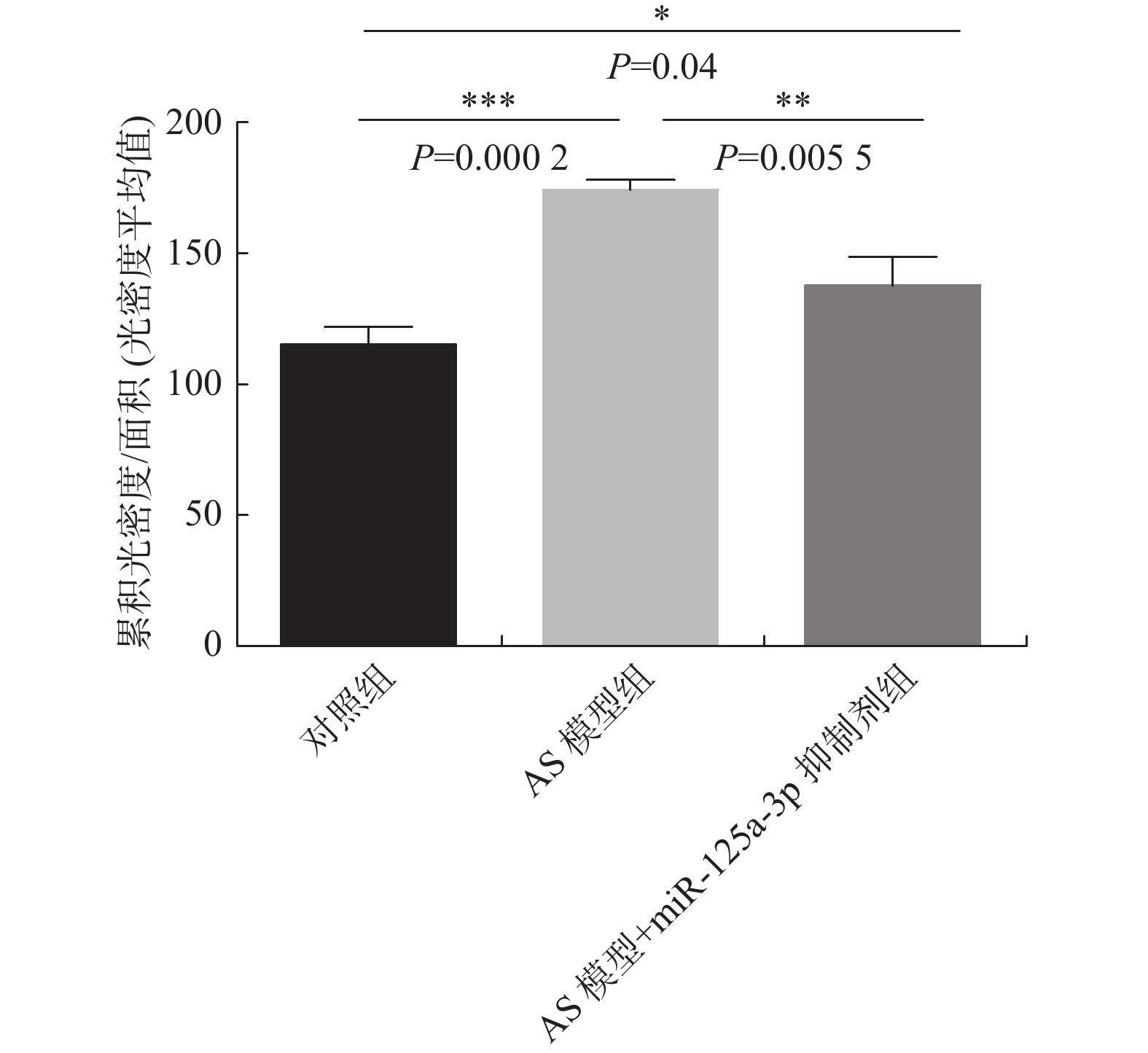
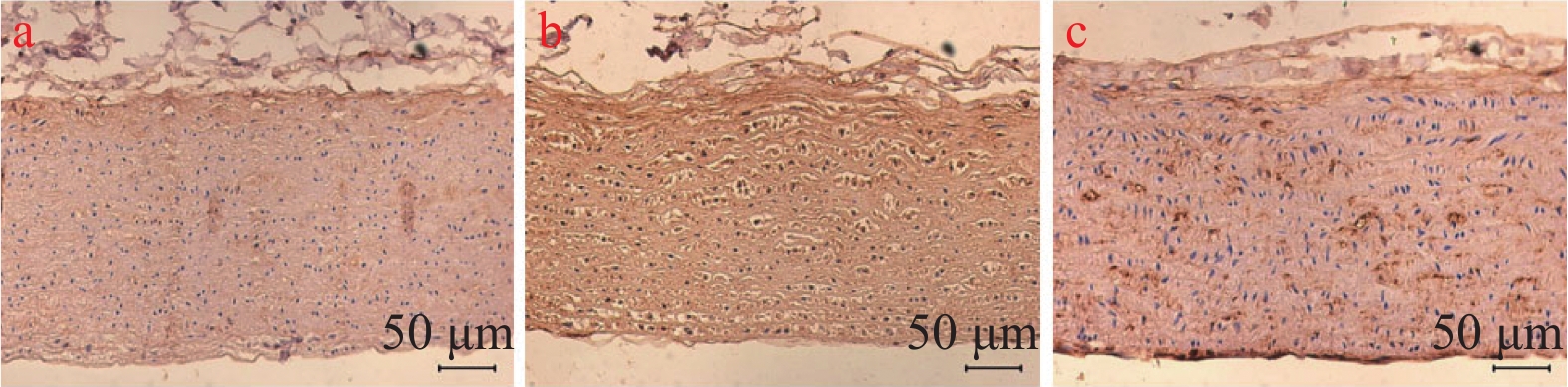
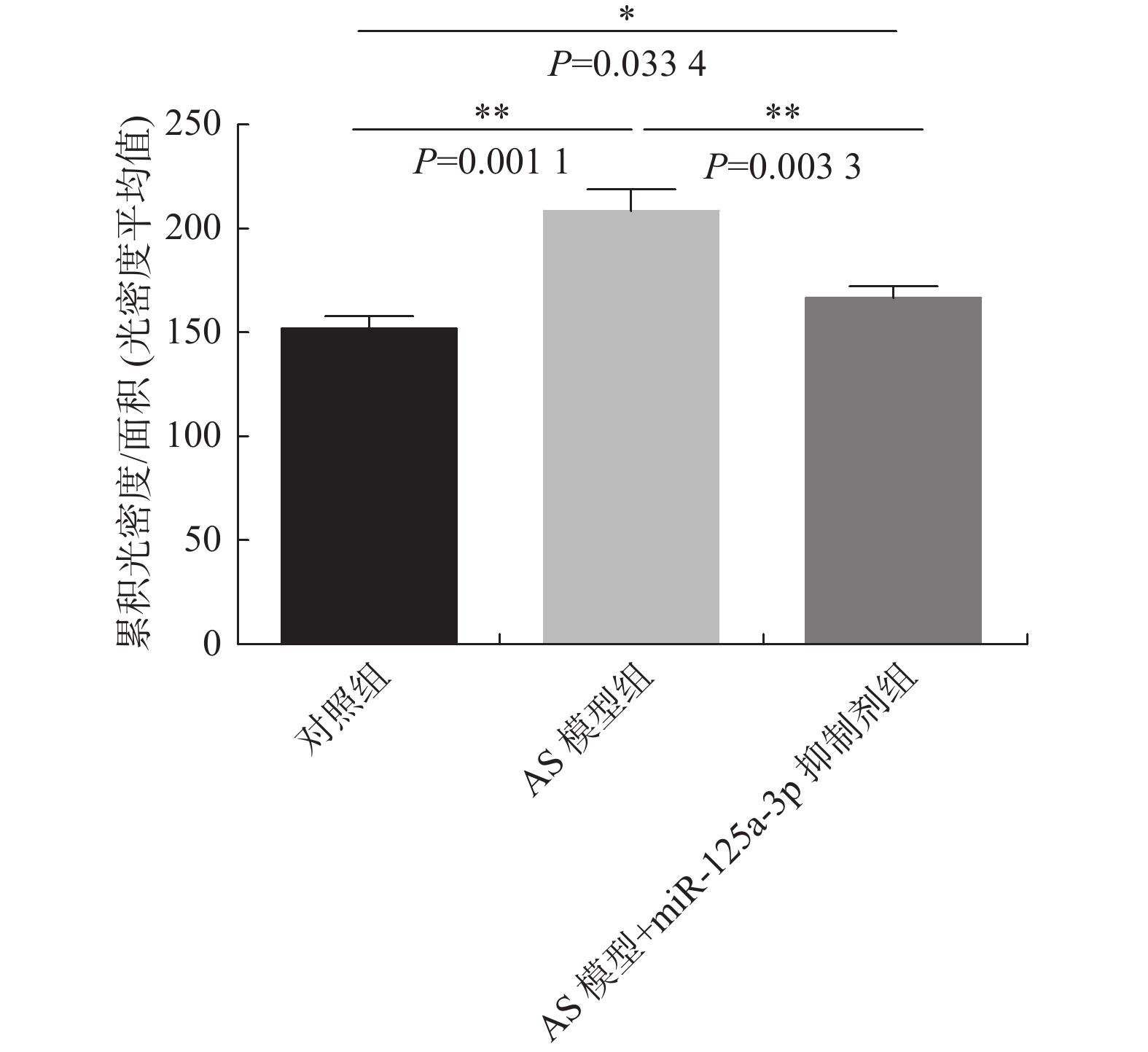
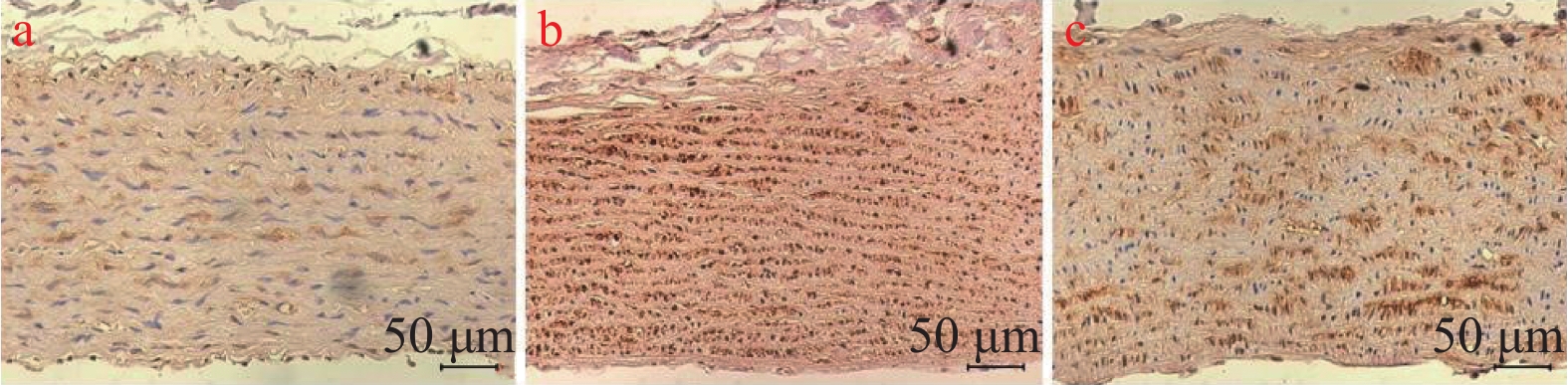
MMP-9免疫组化染色结果显示,与对照组比较,AS模型组的MMP-9水平显著升高(P < 0.001),与AS模型组比较,miR-125a-3p抑制剂干预后MMP-9水平显著下降(P < 0.01)(图3、图4)。结果表明:miR-125a-3p抑制剂干预后,降低了斑块组织中MMP-9的表达。
2.3 免疫组织化学方法检测斑块组织中VEGF的结果
VEGF免疫组化染色结果显示,与对照组对比,AS模型组的VEGF水平显著提高(P < 0.01);与AS模型组对比,miR-125a-3p抑制剂干预后VEGF水平下降,(P < 0.01)(图5、图6)。结果表明:miR-125a-3p抑制剂干预后,降低了斑块组织中VEGF的表达。
2.4 免疫荧光染色检测M1标志物CD11c的结果
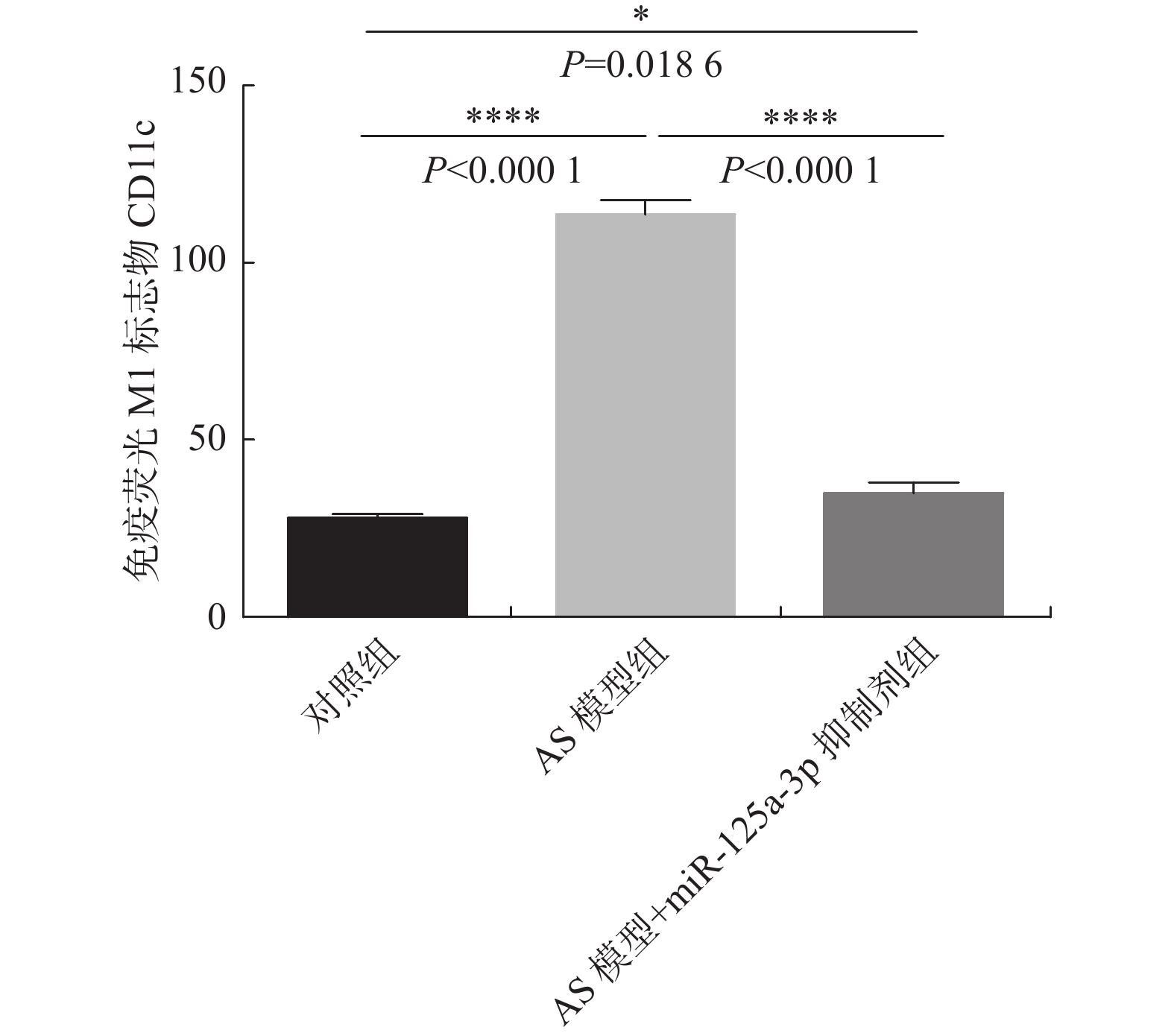
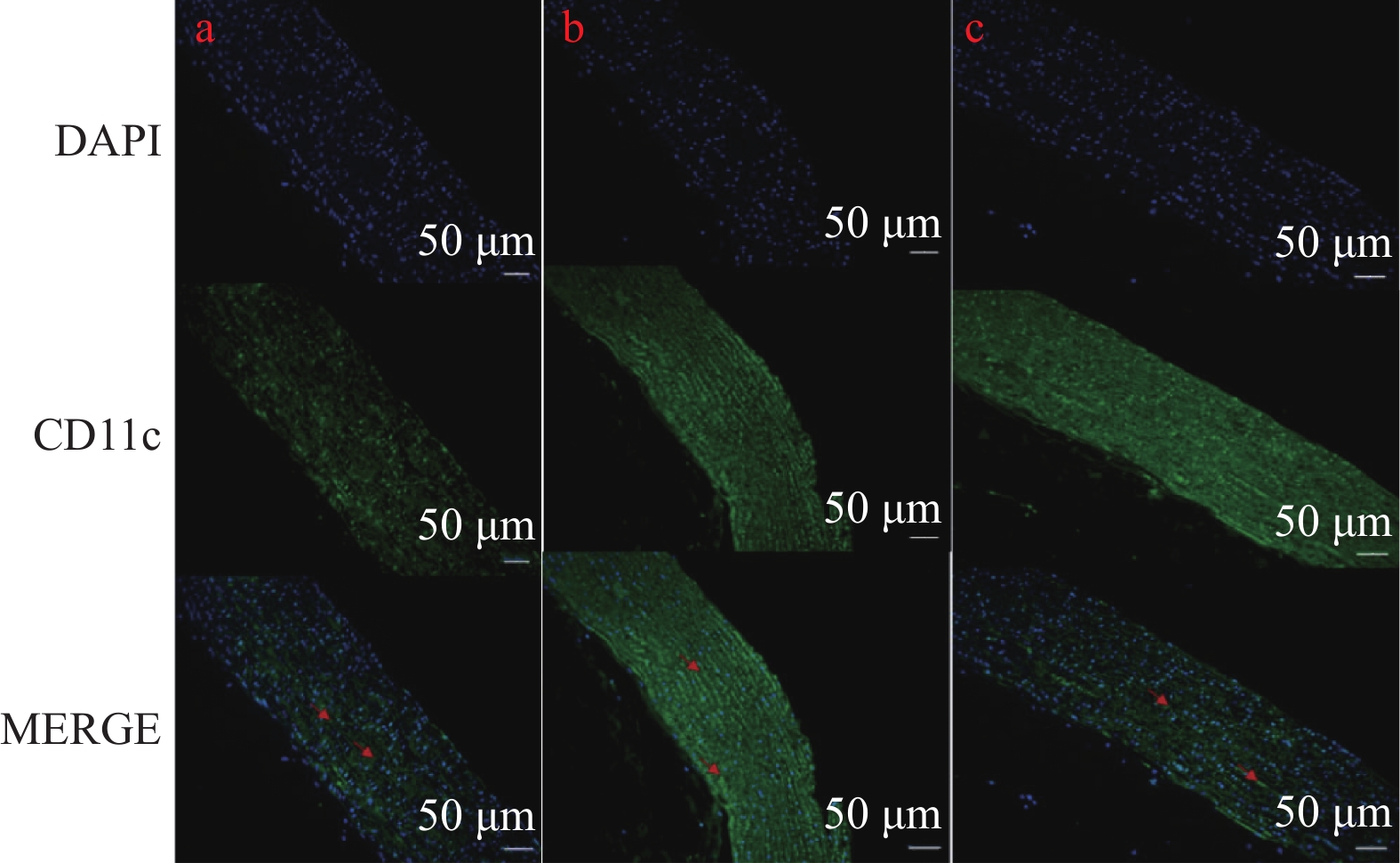
免疫荧光检测M1标志物CD11c染色结果显示:与对照组比较,AS模型组的CD11c水平有明显升高(P < 0.0001);与AS模型组比较,miR-125a-3p抑制剂干预后CD11c水平显著下降(P < 0.0001)(图7、图8)。结果表明:miR-125a-3p抑制剂减少了斑块组织中M1 巨噬细胞。
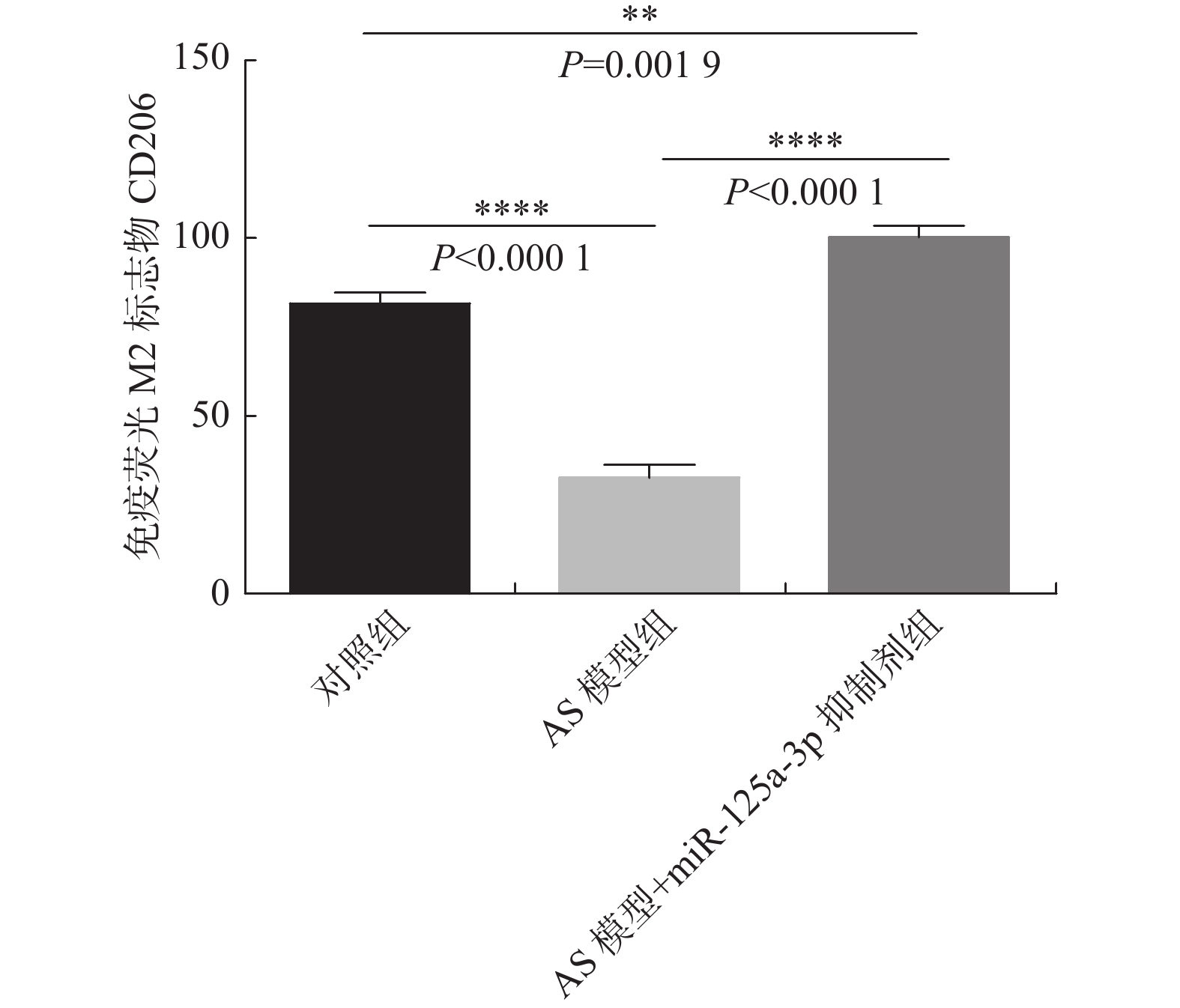
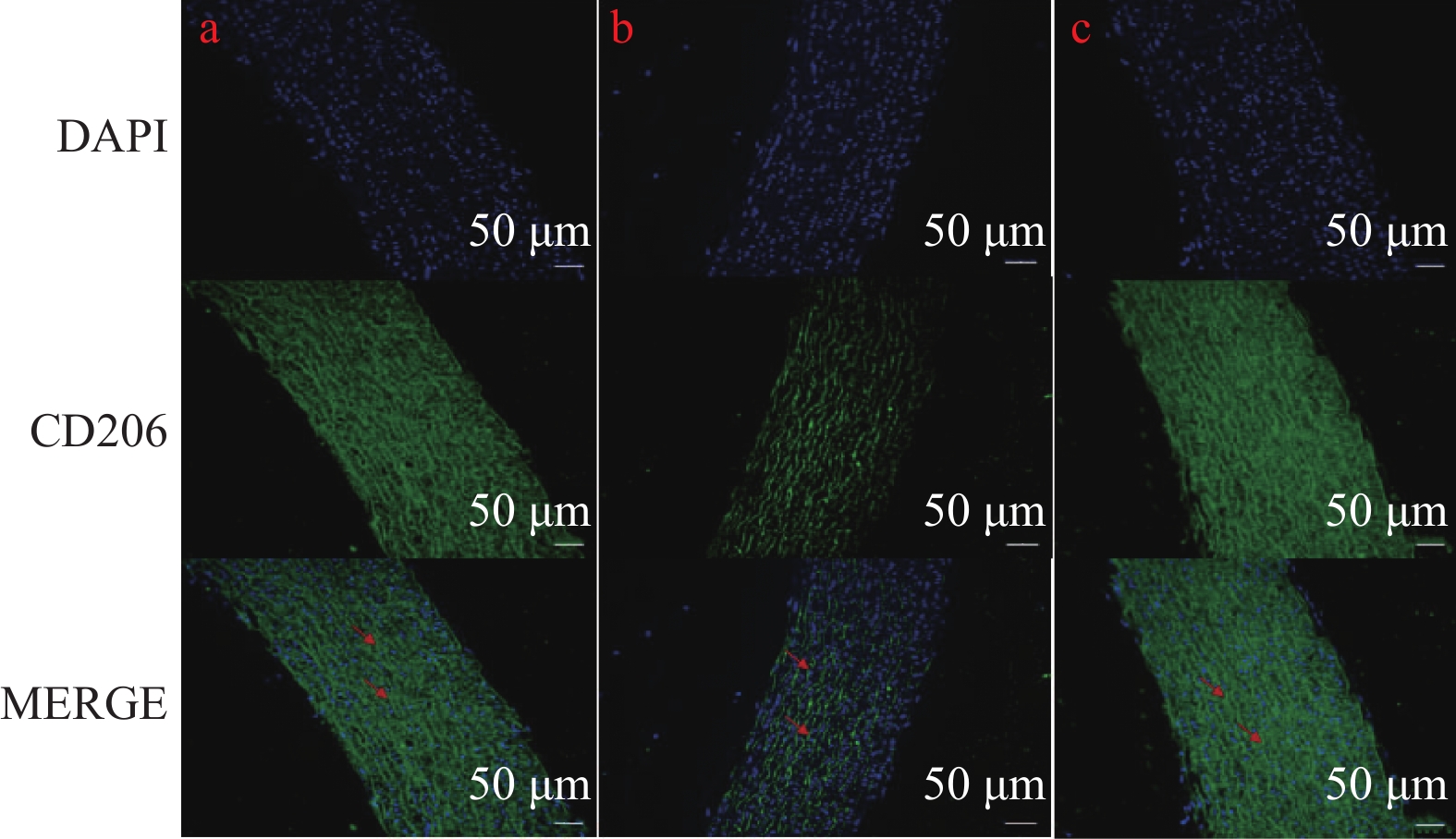
2.5 免疫荧光染色检测M2 标志物CD206的结果
免疫荧光检测M2标志物CD206染色结果显示,与对照组对比,AS模型组的CD206水平显著下降(P < 0.0001),miR-125a-3p抑制剂干预后CD206水平明显升高(P < 0.0001)(图9、图10)。结果表明:miR-125a-3p抑制剂增加了斑块组织中M2 巨噬细胞。
3. 讨论
AS是一种慢性炎症性疾病,严重威胁人体健康。研究表明,不稳定AS斑块容易导致不良心血管事件的发生[13-14]。巨噬细胞是AS病变中主要的免疫细胞,在AS整个病理生理过程中都发挥着重要作用[5]。在动脉粥样硬化中,当循环中的单核细胞进入内膜后,单核细胞会分化为巨噬细胞[15]。巨噬细胞和单细胞暴露在炎症细胞因子、氧化脂质、胆固醇晶体和其他因素中。所有这些刺激不仅诱导特定的转录反应,而且还广泛相互作用,导致动脉粥样硬化斑块中巨噬细胞的转录[7]。基于不同的激活方式,巨噬细胞主要分为两种表型,即经典激活的M1和替代激活的M2巨噬细胞[2-3]。M1巨噬细胞能够开始并维持炎症反应,分泌促炎细胞因子,激活内皮细胞,并诱导其他免疫细胞募集到发炎组织中;另一方面,M2巨噬细胞促进炎症的消退,吞噬糖凋亡细胞,驱动胶原蛋白沉积,协调组织完整性,释放抗炎介质,主要参与组织修复,具有吞噬、促血管生成和促纤维化能力。M1巨噬细胞在促进斑块不稳定方面发挥了重要作用,而M2巨噬细胞则维持斑块的稳定,提示斑块的不稳定可能是M1和M2亚型之间失衡的结果[6, 16]。
miRNA是一种小型、进化保守的非编码RNA,长度为18~25个核苷酸,在基因调控中具有重要作用,转录后调控基因表达[17-18]。miRNA可以抑制数千个目标基因并协调正常过程,包括细胞增殖、分化和凋亡[19]。同时,miRNA对巨噬细胞的激活起到重要调节作用[7],例如Lin-Li Lv等的研究表明[20],外体miR-19b-3p调节的TEC和巨噬细胞之间的通路,导致M1巨噬细胞激活。由于M1巨噬细胞加剧斑块的不稳定,因此,笔者可以推测miRNA对不稳定斑块的发生起到了一定的作用。笔者的研究[12]也提示miR-125a-3p在动脉粥样硬化斑块的不稳定及破裂中起着重要的作用。
VEGF是一种有效的内皮细胞生长因子和血管生成诱导因子,对血管的完整性和血管功能具有重要意义。研究发现,VEGF在不稳定斑块中发挥着重要作用,能在一定程度上加速动脉粥样硬化斑块的进展和不稳定性。其机制可能是VEGF增加血管通透性,引起红细胞外渗,进而导致斑块内出血,加速动脉粥样硬化[21]。基质金属蛋白酶-9(MMP-9)属于MMP家族,并已被广泛研究。随着MMP-9活性的增加,MMP-9可导致纤维帽变薄,从而导致斑块的不稳定[22]。
本研究结果显示,抑制miR-125a-3p可使动脉粥样硬化斑块病变区域面积减少,斑块组织中M1 巨噬细胞、MMP-9,VEGF表达减少,M2 巨噬细胞增加。提示miR-125a-3p抑制可以减轻动脉粥样硬化斑块形成,平衡M1/M2巨噬细胞,减少MMP-9,VEGF表达,促进斑块稳定,miR-125a-3p可能是治疗不稳定动脉粥样硬化斑块的新靶点。
-
-
[1] Moore K J,Sheedy F J,Fisher E A. Macrophages in atherosclerosis:A dynamic balance[J]. Nat Rev Immunol,2013,13(10):709-721. doi: 10.1038/nri3520 [2] Mills C D,Ley K. M1 and M2 macrophages:The chicken and the egg of immunity[J]. J Innate Immun,2014,6(6):716-726. doi: 10.1159/000364945 [3] Murray P J,Allen J E,Biswas S K,et al. Macrophage activation and polarization:Nomenclature and experimental guidelines[J]. Immunity,2014,41(1):14-20. doi: 10.1016/j.immuni.2014.06.008 [4] Schmitz G,Grandl M. Role of redox regulation and lipid rafts in macrophages during Ox-LDL-mediated foam cell formation[J]. Antioxid Redox Signal,2007,9(9):1499-1518. doi: 10.1089/ars.2007.1663 [5] 杨新春,张大鹏. 慢性冠状动脉综合征的概念和要点及意义[J]. 中国心血管病研究,2019,17(10):871-873. doi: 10.3969/j.issn.1672-5301.2019.10.002 [6] Stoger J L,Gijbels M J,Van Der Velden S,et al. Distribution of macrophage polarization markers in human atherosclerosis[J]. Atherosclerosis,2012,225(2):461-468. doi: 10.1016/j.atherosclerosis.2012.09.013 [7] Kuznetsova T,Prange K H M,Glass C K,et al. Transcriptional and epigenetic regulation of macrophages in atherosclerosis[J]. Nature Reviews Cardiology,2020,17(4):216-228. doi: 10.1038/s41569-019-0265-3 [8] Van der Veken B,De Meyer G R,Martinet W. Intraplaque neovascularization as a novel therapeutic target in advanced atherosclerosis[J]. Expert Opin Ther Targets,2016,20(10):1247-1257. doi: 10.1080/14728222.2016.1186650 [9] 徐声波,吴平路,余晖,等. AIS患者CTRP1、MMP-9水平与颈动脉硬化斑块稳定性及神经功能缺损程度的关系[J]. 脑与神经疾病杂志,2021,29(8):492-496. [10] Ganta V C,Choi M,Farber C R,et al. Antiangiogenic VEGF165b regulates macrophage polarization via S100A8/S100A9 in peripheral artery disease[J]. Circulation,2019,139(2):226-242. doi: 10.1161/CIRCULATIONAHA.118.034165 [11] Clemente C,Rius C,Alonso-Herranz L,et al. MT4-MMP deficiency increases patrolling monocyte recruitment to early lesions and accelerates atherosclerosis[J]. Nat Commun,2018,9(1):910. doi: 10.1038/s41467-018-03351-4 [12] 戴海龙,肖娟,潘云. 冠心病患者外周血单核细胞中miR-125a-3p的表达研究[J]. 中国心血管病研究,2020,18(3):203-205. doi: 10.3969/j.issn.1672-5301.2020.03.003 [13] Mushenkova N V,Nikiforov N G,Melnichenko A A,et al. Functional phenotypes of intraplaque macrophages and their distinct roles in atherosclerosis development and atheroinflammation[J]. Biomedicines,2022,10(2):452. doi: 10.3390/biomedicines10020452 [14] Barquera S,Pedroza-Tobias A,Medina C,et al. Global overview of the epidemiology of atherosclerotic cardiovascular disease[J]. Arch Med Res,2015,46(5):328-338. doi: 10.1016/j.arcmed.2015.06.006 [15] Guilliams M,Mildner A,Yona S. Developmental and functional heterogeneity of monocytes[J]. Immunity,2018,49(4):595-613. doi: 10.1016/j.immuni.2018.10.005 [16] Bouhlel M A,Derudas B,Rigamonti E,et al. PPARgamma activation primes human monocytes into alternative M2 macrophages with anti-inflammatory properties[J]. Cell Metab,2007,6(2):137-143. doi: 10.1016/j.cmet.2007.06.010 [17] Rupaimoole R,Slack F J. MicroRNA therapeutics:towards a new era for the management of cancer and other diseases[J]. Nat Rev Drug Discov,2017,16(3):203-222. doi: 10.1038/nrd.2016.246 [18] Bartel D P. MicroRNAs:Genomics,biogenesis,mechanism,and function[J]. Cell,2004,116(2):281-297. doi: 10.1016/S0092-8674(04)00045-5 [19] Lujambio A,Lowe S W. The microcosmos of cancer[J]. Nature,2012,482(7385):347-355. doi: 10.1038/nature10888 [20] Lv L L,Feng Y,Wu M,et al. Exosomal miRNA-19b-3p of tubular epithelial cells promotes M1 macrophage activation in kidney injury[J]. Cell Death Differ,2020,27(1):210-226. doi: 10.1038/s41418-019-0349-y [21] Mao Y,Liu X,Song Y,et al. VEGF-A/VEGFR-2 and FGF-2/FGFR-1 but not PDGF-BB/PDGFR-β play important roles in promoting immature and inflammatory intraplaque angiogenesis[J]. PloS One,2018,13(8):e0201395. doi: 10.1371/journal.pone.0201395 [22] Bot P T,Pasterkamp G,Goumans M J,et al. Hyaluronic acid metabolism is increased in unstable plaques[J]. Eur J Clin Invest,2010,40(9):818-827. doi: 10.1111/j.1365-2362.2010.02326.x 期刊类型引用(6)
1. 郑艳,马振,王南丁,肖艳琪,王金仙,杨艾琳. 基于PI3K/AKT/eNOS通路研究芪丹通脉片对ApoE~(-/-)小鼠动脉粥样硬化易损斑块的影响. 中医学报. 2024(01): 55-62 .  百度学术
百度学术2. 李震,郝恩刚,刘丹青. 微RNA-296、血管内皮生长因子-B的表达与冠心病患者冠脉病变程度的关系. 中国医药导报. 2024(04): 11-15 .  百度学术
百度学术3. 江巍,白盟盟,王海峰. 老年2型糖尿病患者血清微小RNA-125a-3p和基质金属蛋白酶9水平与颈动脉粥样硬化的关系. 中国医药. 2024(04): 545-549 .  百度学术
百度学术4. 秦飞宇,黄朝晖,殷媛. 肿瘤相关巨噬细胞在结直肠癌免疫检查点抑制剂治疗耐受中的研究进展. 中华肿瘤防治杂志. 2024(07): 437-441 .  百度学术
百度学术5. Nguyen Xuan Huynh,梁硕,孟毅,刘志勇. 益气活血清热解毒方治疗动脉粥样硬化临床研究. 陕西中医. 2023(06): 746-750 .  百度学术
百度学术6. 李星,刘京锋,李博. 血清miR-125a-3p、miR-224-3p表达与脑梗死患者颈动脉粥样硬化斑块的关系. 中国医药导报. 2023(26): 91-94 .  百度学术
百度学术其他类型引用(2)
-






 下载:
下载:
 下载:
下载:

