Cost-Effectiveness Analysis of Nilotinib Versus Dasatinib as Second-Line Treatment of Chronic Myeloid Leukemia
-
摘要:
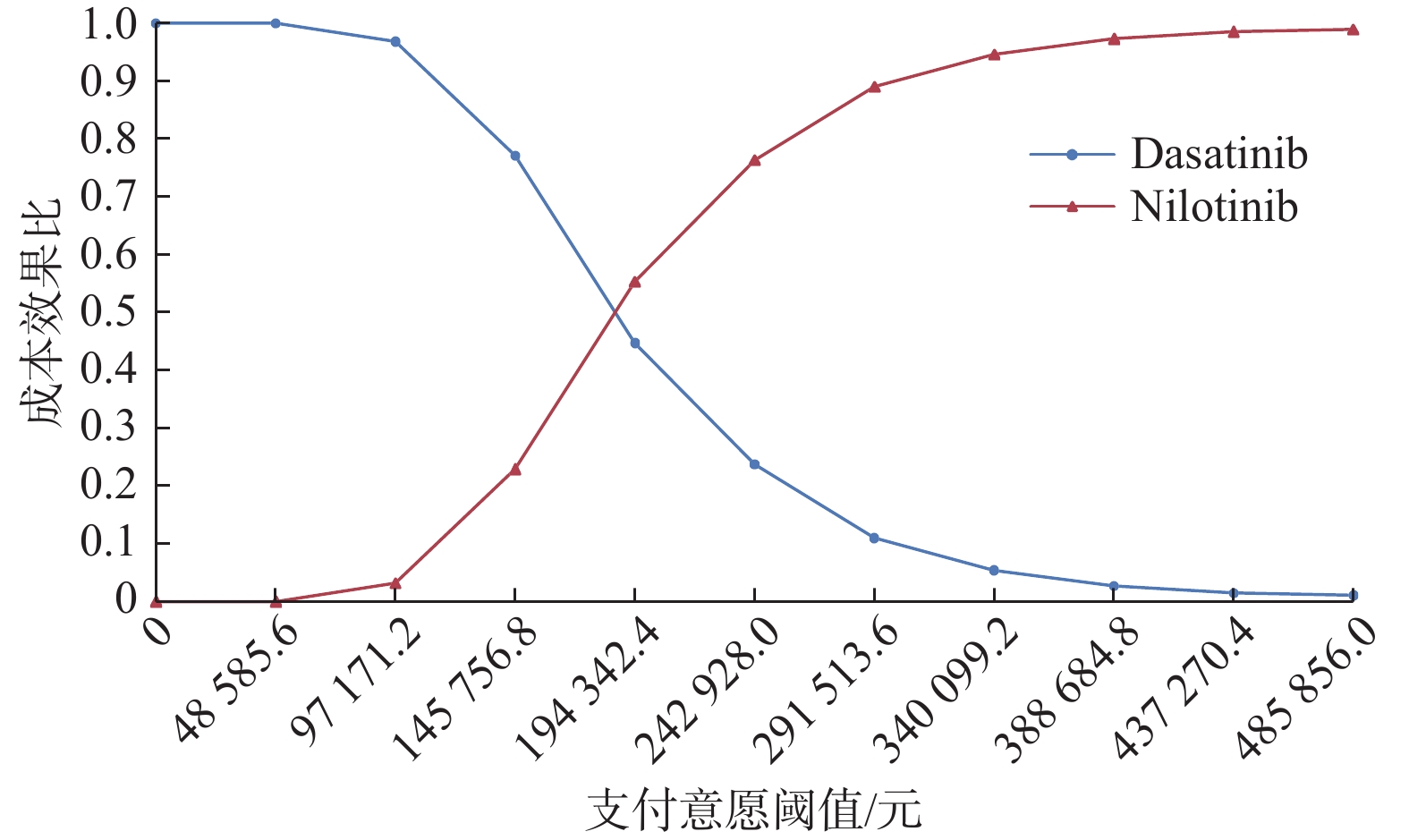
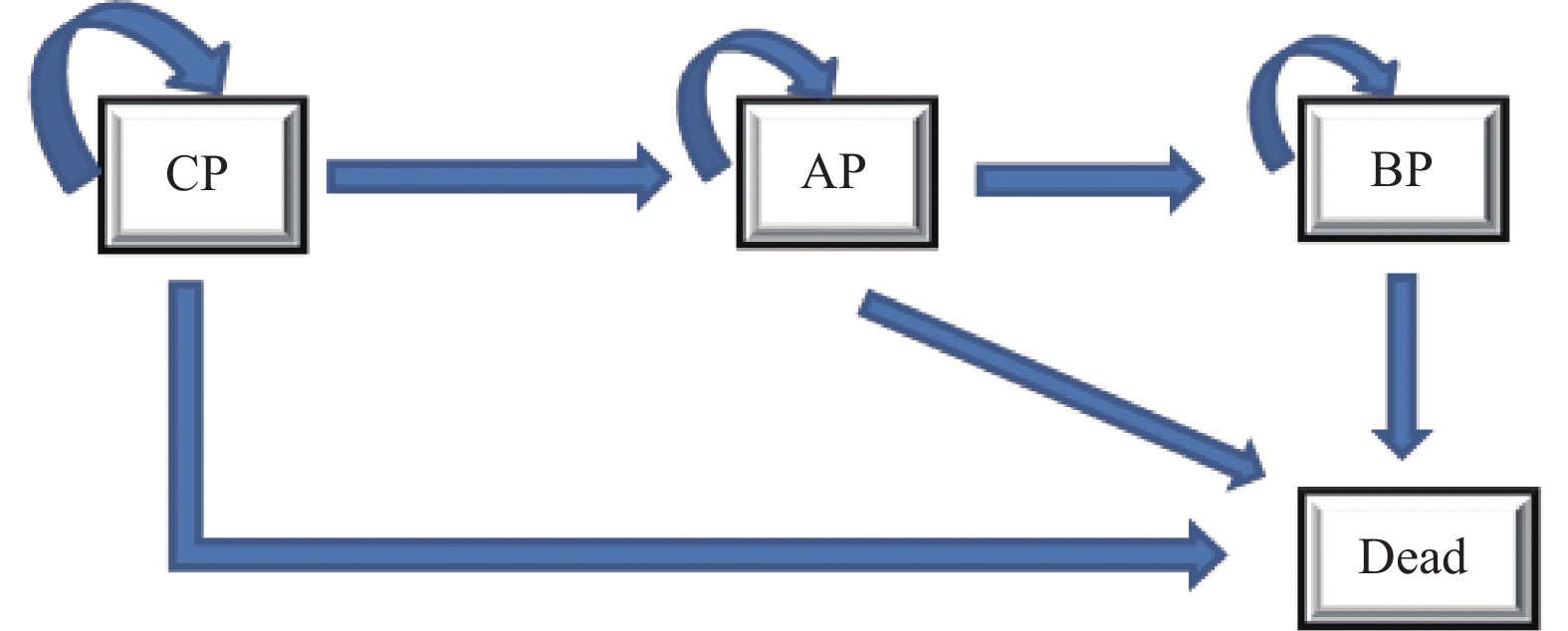
目的 评估费城染色体阳性慢性髓性白血病慢性期(Ph+CML-CP)患者中对伊马替尼耐药或不耐受的二线尼洛替尼与达沙替尼的成本效果。 方法 建立状态转移马尔可夫(Markov)模型进行成本效用分析,模型包括4种健康状态:慢性期(CP),加速期(AP),急变期(BP)和死亡。尼洛替尼与达沙替尼治疗的无进展生存率,疾病进展发生率,总生存率等有关临床参数来源于既往发表的研究和专家意见,健康状态效用值来源于文献。通过Treeage软件以增量成本效果比(ICER)作为评价指标,对尼洛替尼和达沙替尼2个方案的总产出和总成本进行评价,并通过单变量、概率敏感性分析评估模型稳定性。 结果 与选用达沙替尼治疗相比,选用尼洛替尼治疗的ICER 为182487.71元·QALY-1,低于3倍2021年全国人均GDP。敏感性分析显示主要的影响参数有贴现率,达沙替尼价格和尼洛替尼价格,模型结果稳定。 结论 选用尼洛替尼相对达沙替尼用于对伊马替尼耐药或不耐受的Ph+CML-CP患者治疗具有成本效用优势。 Abstract:Objective To evaluate the cost-effectiveness of nilotinib versus dasatinib in the second-line treatment of Philadelphia chromosome-positive chronic myeloid leukemia in chronic phase. Methods Establish a Markov model for cost-effectiveness analysis, including four health states: chronic phase (CP), accelerated phase (AP), blast phase (BP), and death. Clinical parameters related to progression-free survival rates, disease progression rates, overall survival rates, etc. for treatment with nilotinib and dasatinib are derived from previously published studies and expert opinions, while health state utility values are sourced from the literature. Using Treeage software, the incremental cost-effectiveness ratio (ICER) was used as an evaluation metric to assess the total output and total costs of the two schemes of nilotinib and dasatinib, and model stability is evaluated through univariate and probabilistic sensitivity analyses. Results Compared with using dasatinib for treatment, the ICER for using nilotinib treatment is 182487.71 yuan per QALY, which is less than 3 times the national per capita GDP in 2021. Sensitivity analysis showed that the main influencing parameters are the discount rate, dasatinib price, and nilotinib price, and the model results are stable. Conclusion Nilotinib has a cost-utility advantage over dasatinib in the treatment of Ph+CML-CP patients who are resistant or intolerent to imatinib. -
Key words:
- Nilotinib /
- Dasatinib /
- Chronic myeloid leukemia /
- Cost-effectiveness analysis /
- Second-line treatment
-
新生儿高胆红素血症是新生儿时期最常见的疾病之一[1]。当血液中胆红素浓度升高并与其清除之间失去平衡时,在临床上表现为黄疸,即胆红素沉积于皮肤、黏膜和结膜中导致新生儿皮肤、巩膜黄染[2]。研究[3]发现约有60%的足月儿和80%早产儿在出生后的3 d内出现新生儿高胆红素血症,增加了新生儿出生后一周的入院率。若不及时进行干预,易出现胆红素脑病,对新生儿中枢神经系统造成永久性的损害,甚至是死亡[4]。蓝光照射疗法是治疗新生儿高胆红素血症的有效手段,能避免血清胆红素呈现进行性升高。但在临床护理中,新生儿多由于缺乏安全感、哭闹躁动而影响治疗效果,使黄疸消退减慢,甚至影响生长发育[5]。因此,积极采取有效诊疗手段降低患儿胆红素水平,同时寻求安全有效的护理措施以加速黄疸消退、促进新生儿的生长发育就显得尤为重要。一方面,足底反射区按摩作为一种简便、安全、非侵入的护理措施,将压力施加于足底相应的反射点,从而改善与反射点相关身体不同部位的血液、淋巴循环以及神经支持,加速体内代谢产物的排出[6],目前已成熟运用于成人失眠、调理肠胃等方面,并取得了显著的疗效[7−8]。另一方面,既往研究[9−10]表明足底反射疗法对婴儿肠绞痛等急性疼痛有缓解作用,同时对胃肠道功能、促进排便也有一定的作用[11−12]。手部穴位按摩则通过刺激穴位,疏通经络达到提高患儿免疫力、促进排便和降低胆红素水平的目的[13]。因此,足底反射区和手部穴位按摩均可通过加速新生儿首次排便、增加排便频率从而减少胆红素的肝肠循环来促进黄疸消退[14]。本研究旨在探讨足底反射区结合手部穴位按摩对新生儿高胆红素血症的应用效果,以期为临床护理提供价值参考。
1. 资料与方法
1.1 一般资料
选取2024年3月至2024年7月收治于云南省某三甲医院新生儿重症监护室的112例新生儿高胆红素血症患儿为研究对象,根据两样本均数比较的样本含量公式:
$$ {n}_{1} = {n}_{2} = \frac{2{\left({{\rm Z}}_{\alpha }+{{\rm Z}}_{\beta }\right)}^{2}*{\sigma }^{2}}{{\delta }^{2}} $$ 公式中的$ {n}_{1} $和$ {n}_{2} $分别是干预组和对照组的样本量,两组样本数量相等。$ \delta $为两总体均数之差的绝对值,$ \sigma $为样本标准差,其中 $ \alpha $ = 0.05(双侧)、$ \beta $ = 0.1 查表得出 Zα=1.96、Zβ = 1.282。通过查阅文献[15],得出$ \delta $ = 0.36,$ \sigma $ = 0.59,代入公式计算,两组样本量均为56例。纳入标准:(1)符合新生儿高胆红素血症诊断标准[16];(2)日龄≤28 d;(3)5minApgar评分 > 7分;(4)患儿生命体征平稳,评估后符合光疗指征;(5)患儿父母知情同意本次研究并签署知情同意书。排除标准:(1)合并新生儿溶血、严重感染、自身免疫性疾病;(2)先天性疾病、先天畸形;(3)新生儿窒息史、新生儿呼吸窘迫综合征。本研究获家属知情同意,经云南省某三甲医院医学伦理审查委员会批准通过(2024KY034)。
1.2 干预方法
对照组:给予常规护理干预,使用厂家、型号相同的光疗箱进行蓝光照射治疗。(1)将患儿置于光疗箱的“鸟巢”中,给予遮光眼罩遮蔽眼睛、光疗纸尿裤遮蔽会阴,充分暴露患儿其余部位,光疗时间以每日 < 8 h为宜[17];(2)调节光源,使箱内温度合适,避免箱内温度过高,提高患儿的舒适度;(3)密切监测患儿体温、呼吸、血压、心率等生命体征,观察其疗效以及是否出现不良反应;(4)做好患儿皮肤护理,臀部和脐部做好清洁消毒护理,避免发生感染,光疗结束后对患儿进行抚触并检查皮肤情况;(5) 2 h改变一次体位,避免长期处于同一体位而发生压力性损伤,加强巡视避免眼罩滑落使口鼻受压;(6)保证患儿机体营养摄入,同时做好患儿排泄、睡眠以及奶量等基本情况的记录。
试验组:采用常规护理结合足底反射区、手部穴位按摩。保持按摩环境的舒适、安静,维持适宜的温、湿度,按摩时间为09:30am~10:00am,15:30pm~16:00pm。(1)足底反射区按摩选取足底脾、胃、小肠以及结肠反射区进行按摩,具体干预方法如下:①按摩开始前,护理人员洗净、擦干并温暖双手;②置患儿于仰卧位,护理人员掌心倒适量的润肤油,轻轻触摸患儿的双脚以放松和温暖,此阶段共持续1 min;③以拇指分别揉压患儿双足底部脾、胃反射区,再以拇指推揉患儿足底结肠反射区,环形推揉升结肠、横结肠、降结肠最后至乙状结肠,最后再用拇指揉压小肠区域。双足交替按摩2~3 min,2次/d。(2)手部穴位按摩选取补脾经、清大肠、清肝经和清小肠,具体干预方法如下:①取适量润肤油双手搓热后轻轻触摸患儿双手,让患儿适应按摩;②补脾经:护理人员旋推患儿大拇指螺纹面,再使患儿拇指呈弯曲状,由拇指外侧缘指尖向指根方向推揉,共50次;③清大肠:大肠经位于食指桡侧缘,护理人员沿患儿食指桡侧缘从虎口直推至食指指尖,动作迅速且轻柔,共推50次;④清肝经:肝经位于食指螺纹面,辅助并保持患儿食指伸直,用拇指从食指指根沿肝经直推至指尖,共50次;⑤清小肠:小肠经位于小指尺侧缘,由指根直推至指尖,共50次,手部穴位按摩时间控制在10 min以内,2次/d。在按摩的过程中应密切监测患儿生命体征,观察患儿对按摩的反应,注意手法轻柔,若出现哭闹、皮肤红肿等立即停止操作并给予相应处理。
1.3 评价指标
(1)经皮胆红素水平:分别测量并记录患儿入院时、入院第3天、入院第5天的经皮胆红素值,测量时间为早晨沐浴后,固定同一经皮胆红素测量仪以及测量人员;(2)前3 d排便次数:观察并记录患儿前3 d每天排便次数,统计3 d排便总次数;(3)奶量增加水平、体重增长水平、日睡眠时间:记录患儿护理前后的奶量增加水平、体重增长水平以及日睡眠时间。
1.4 统计学分析
采用SPSS27.0软件进行统计分析,计量资料采用均数±标准差($ \bar x \pm s $)表示;组间比较时,符合正态分布且方差齐者,采用两独立样本t检验;偏态分布者则采用中位数±四分位间距[M(P25,P75)]进行描述,使用秩和检验;计数资料用例数和百分率[n(%)]表示,使用卡方检验。P < 0.05为差异有统计学意义。
2. 结果
2.1 一般资料比较
两组住院患儿在性别、胎龄(周)、出生体重(g)、5min Apgar评分(分)、分娩方式、喂养方式等基线资料比较,差异无统计学意义(P > 0.05),具有可比性,见表1。
表 1 两组患儿一般资料比较[n(%)/M(P25,P75)Table 1. Comparison of general data of two groups [n(%)/M(P25,P75)组别 对照组(n = 56) 试验组(n = 56) χ2/Z P 性别 0.146 0.703 男 33(58.9) 31(55.4) 女 23(41.1) 25(44.6) 胎龄(周) 39(38,39.75) 39(38,39) −0.918 0.359 出生体重(g) 3150 (2870 ,3395 )3170 (2950 ,3433.75 )0.463 0.644 5 min Apgar评分(分) 9(9,10) 9(9,10) 0.300 0.764 分娩方式 0.387 0.534 顺产 38(67.9) 41(73.2) 剖宫产 18(32.1) 15(26.8) 喂养方式 0.387 0.534 母乳喂养 15(26.8) 18(32.1) 配方奶喂养 41(73.2) 38(67.9) 2.2 两组患儿各时间点经皮胆红素水平比较
两组患儿入院时经皮胆红素比较,差异无统计学意义(P > 0.05),具有可比性;试验组在护理第3天、第5天时测得的经皮胆红素水平均低于对照组,差异有统计学意义(P < 0.05),见表2。
表 2 两组患儿各时间点经皮胆红素水平比较($ \bar x \pm s $,mg/dL)Table 2. Comparison of transcutaneous bilirubin level at each time point between the two groups($ \bar x \pm s $,mg/dL)组别 n 入院时 护理第3天 护理第5天 对照组 56 15.888 ± 1.406 9.355 ± 2.645 5.599 ± 2.078 试验组 56 15.805 ± 1.431 7.336 ± 2.606 4.366 ± 1.864 t 0.311 4.068 3.304 P 0.757 < 0.001* 0.001* *P < 0.05。 2.3 两组患儿前3 d排便总次数比较
试验组患儿前3 d排便总次数多于对照组,差异有统计学意义(P < 0.05),见表3。
表 3 两组患儿前3 d排便总次数比较($ \bar x \pm s $)Table 3. Comparison of the total bowel movements in the first three days between two groups of children($ \bar x \pm s $)组别 n 前3 d排便总次数(次) 对照组 56 9.68 ± 3.470 试验组 56 11.75 ± 4.265 t −2.819 P 0.006* *P < 0.05。 2.4 两组患儿每日睡眠时间、体重增长水平、奶量增长水平比较
试验组患儿每日睡眠时间较对照组长,体重增长水平、奶量增长水平高于对照组,差异有统计学意义(P < 0.05),见表4。
表 4 两组患儿每日睡眠时间、体重增长水平、奶量增长水平比较($ \bar x \pm s $)Table 4. Comparison of daily sleep duration,weight gain levels,and milk intake levels between the two groups of children($ \bar x \pm s $)组别 n 每日睡眠时间(h) 体重增长(g) 奶量增加(mL) 对照组 56 17.488 ± 0.670 128.48 ± 88.554 24.86 ± 11.271 试验组 56 18.003 ± 0.565 173.93 ± 89.680 32.86 ± 16.191 t −4.294 −2.698 −3.035 P < 0.001* 0.008* 0.003* *P < 0.05。 3. 讨论
3.1 足底反射区结合手部穴位按摩能加速黄疸消退,促进排便
本研究结果显示,试验组患儿在实施干预后的第3天、第5天经皮胆红素水平均低于对照组,与Basiri等[18]研究发现的足底反射区按摩能够在短时间内降低新生儿高胆红素血症患儿血清胆红素水平的研究结果一致,试验组前3 d排便总次数多于对照组。中医学中,新生儿黄疸被归属于“胎黄、胎疸”范畴,《诸病源候论》[19]中:“脏器有热,熏蒸于胎……体皆黄。”阐明了胎黄的病因病机,母亲在怀孕时受湿热之邪入侵,致胎儿脾胃功能失常,影响肝胆疏泄,胆汁溢于肌肤,从而身目黄染[20]。中医治疗以肝胆为主,加以脾、胃、大肠辅之,利湿退黄为基本原则。因此,本研究选择足底脾、胃、大肠、小肠四个反射区,通过按摩刺激相应的反应点来加强脾胃功能,促进肠道排出二便[12],减少胆红素的肝肠循环,使胆红素随二便排出体内,加速新生儿黄疸的消退;在手部选择补脾经、清大肠、清肝经和清小肠,清小肠、清大肠合用以清热利湿,使湿热之邪从二便排走,清肝经可增强肝脏的代谢能力,实现清肝利胆的功效,补脾经则因脾为后天之本,脾虚致脏器不足,补脾以清热利湿,补足肝脏[21]。因此,可选择足底反射疗法结合手部穴位按摩对新生儿高胆红素血症进行护理,但应认识到其只作为辅助疗法,蓝光照射疗法仍是治疗新生儿高胆红素血症的首选[22]。
3.2 足底反射区结合手部穴位按摩能促进患儿生长发育
本研究结果显示,试验组患儿每日睡眠时间、体重增加量、奶量增加水平均高于对照组。在足底反射区按摩时,刺激传出神经将冲动传递至支配骨骼肌的神经纤维,促进下肢血液循环,放松肌肉,促进患儿入睡、延长睡眠时间。按摩的同时刺激了新生儿的皮肤,通过皮肤传导至中枢神经促进神经细胞发育,传导至迷走神经增加胃泌素等消化激素的分泌,增强其消化吸收功能,促进新生儿的生长发育,提高机体免疫力[23]。
综上所述,足底反射区结合手部穴位按摩可有效改善新生儿高胆红素血症患儿的黄疸症状,加速黄疸消退,促进新生儿生长发育,且操作简单、易被父母所接受。但本研究样本量较少,仅在一家医院进行研究,具有一定的局限性。在后续研究中,应扩大样本量,综合多中心的临床试验,为足底反射区结合手部穴位按摩护理提供更坚实的数据支撑,使此护理方法在临床中获得更为广泛的应用,促进新生儿护理发展。
-
表 1 状态转移概率
Table 1. Transition probability
表 2 药品成本
Table 2. Drug cost
药品名称 规格 生产产家 价格(元/盒) 达沙替尼 50 mg/片,60片/盒 AstraZeneca Pharmaceuticals LP 7274.16 20 mg/片,60片/盒 3607.00 50 mg/片,7片/盒 正大天晴药业集团股份有限公司 377.11 20 mg/片,7片/盒 186.99 50 mg/片,7片/盒 石药集团欧意药业股份有限公司 373.25 20 mg/片,7片/盒 185.08 尼洛替尼 200 mg/粒,120粒/盒 Novartis PharmaSte 11030.40 150 mg/粒,120粒/盒 8850.00 药品价格来源于药智网(https://www.yaozh.com/)。 表 3 成本与效用参数
Table 3. Cost and utility parameters
参数模型 均值 下限 上限 概率分布 文献来源 药品成本(元/d) 尼洛替尼CP期#
尼洛替尼AP期#
尼洛替尼BP期#367.68(295)
367.68(295)
367.68(295)275.76(221.25)
275.76(221.25)
275.76(221.25)404.45(324.5)
404.45(324.5)
404.45(324.5)Gamma
Gamma
Gamma药智网
药智网
药智网达沙替尼CP期
达沙替尼AP期
达沙替尼BP期242.47
362.71
362.71106.64
159.52
159.52266.72
398.98
398.98Gamma
Gamma
Gamma药智网
药智网
药智网其他成本 (元) 门诊挂号费 15.00 10.50 19.50 Gamma * 全血细胞计数和外周血分类 24.00 16.80 31.20 Gamma * 骨髓细胞遗传学分析、荧光原位杂交 642.00 449.40 834.60 Gamma * 定量聚合酶链反应检测BCR-ABL 350.00 245.00 455.00 Gamma * 聚合酶链反应扩增BCR-ABL转录本后测序 1292.00 904.40 1679.60 Gamma * 效用值 CP期使用尼洛替尼效用值 0.810 0.648 0.972 Beta [16] CP期使用达沙替尼效用值 0.780 0.624 0.936 Beta [17] AP期效用值 0.650 0.520 0.780 Beta [18] BP期效用值 0.53 0.424 0.636 Beta [12] 死亡 0 Beta 不良反应 1563.32 1094.32 2023.32 Gamma [17] 贴现率(%) 5 0 8 Beta [19] #括号内为数值尼洛替尼用量为300 mg q12 h ;* 2022年云南省三级甲等医院收费标准。 表 4 成本效果分析
Table 4. Cost-effectiveness results
治疗方案 尼洛替尼用法用量 QALYs 总成本/元 ICER/元·QALY−1 达沙替尼 8.77 257929.14 尼洛替尼 400 mg q12 h(100%) 9.11 319830.67 182487.71 300 mg q12 h(45.9%) 9.11 292090.70 100709.42 -
[1] 中华医学会血液学分会. 慢性髓性白血病中国诊断与治疗指南(2020年版)[J]. 中华血液学杂志,2020,(5):353-364. doi: 10.3760/cma.j.issn.0253-2727.2020.05.001 [2] Morel F,Ka C,Le Bris MJ,et al. Deletion of the 5' abl region in Philadelphia chromosome-positive chronic myeloid leukemia[J]. Leukemia,2003,17(2):473-474. doi: 10.1038/sj.leu.2402816 [3] Melo J V. The diversity of BCR-ABL fusion proteins and their relationship to leukemia phenotype[J]. Blood,1996,88(7):2375-2384. doi: 10.1182/blood.V88.7.2375.bloodjournal8872375 [4] Baccarani M,Cortes J,Pane F,et al. Chronic myeloid leukemia: An update of concepts and management recommendations of European Leukemia Net[J]. J Clin Oncol,2009,27(35):6041-6051. doi: 10.1200/JCO.2009.25.0779 [5] Mace M L,Dahl J,Jabbour E J. Which tyrosine-kinase inhibitor to use first in chronic phase chronic myelogenous leukemia?[J]. Expert Opin Pharmacother,2015,16(7):999-1007. [6] Radich J P, Deininger M, Abboud C N, et al. NCCN clinical practice guidelines in oncology: Chronic myelogenous leukemia (2023, Version 1) [M/OL]. [2023-1-23]. https://www.nccn.org//login?ReturnURL=https://www.nccn.org/professionals/physician_gls/pdf/cml.pdf [7] 陈琳,杨敏,程国华. 尼洛替尼与达沙替尼二线治疗慢性髓系白血病的药物经济学评价[J]. 肿瘤,2016,36(6):698-704,710. [8] 徐伟,高楠,马丽,等. 大剂量伊马替尼、达沙替尼和尼洛替尼治疗慢性髓性白血病的成本效用分析[J]. 中国医院药学杂志,2017,37(19):1974-1978. [9] Bonifacio M,Maheshwari V,Tran D,et al. Economic model to evaluate the cost-effectiveness of second-line nilotinib versus dasatinib for the treatment of Philadelphia chromosome-positive chronic myeloid leukemia (CML-CP) in Italy[J]. Pharmacoecon Open,2022,6(1):95-104. doi: 10.1007/s41669-021-00286-3 [10] Li N,Yang X,Fan L,et al. Nilotinib versus dasatinib as second-line therapy in patients with Philadelphia chromosome-positive chronic myeloid leukemia in chronic phase who are resistant or intolerant to imatinib: A cost-effectiveness analysis based on real-world data[J]. J Med Econ,2017,20(4):328-336. doi: 10.1080/13696998.2016.1261032 [11] Yue X,Hincapie A L,Li Y,et al. Safety and cost-effectiveness of ponatinib versus other tyrosine kinase inhibitors as second-line therapy in patients with chronic myeloid leukemia in the United States[J]. Leuk Lymphoma,2022,63(4):946-954. doi: 10.1080/10428194.2021.2002320 [12] Giles F J,Coutre P D L,Pinilla-Ibarz J,et al. Nilotinib in imatinib-resistant or imatinib-intolerant patients with chronic myeloid leukemia in chronic phase: 48-month follow-up results of a phase II study[J]. Leukemia,2013,27(1):107-112. doi: 10.1038/leu.2012.181 [13] Shah N P,Kim D W,Kantarjian H M,et al. Potent transient inhibition of BCR-ABL with dasatinib 100 mg daily achieves rapid and durable cytogenetic responses and high transformation-free survival rates in chronic phase chronic myeloid leukemia patients with resistance,suboptimal response or into[J]. Heamatologica,2010,95(2):232-240. doi: 10.3324/haematol.2009.011452 [14] Griffin J D,Guerin A,Chen L,et al. Comparing nilotinib with dasatinib as second-line therapies in patients with chronic myelogenous leukemia resistant or intolerant to imatinib - a retrospective chart review analysis[J]. Curr Med Res Opin,2013,29(6):623-631. doi: 10.1185/03007995.2013.789012 [15] Shah N P,Guilhot F,Cortes J E,et al. Long-term outcome with dasatinib after imatinib failure in chronic-phase chronic myeloid leukemia: Follow-up of a phase 3 study[J]. Blood,2014,123(15):2317-2324. doi: 10.1182/blood-2013-10-532341 [16] Kulpeng W,Sompitak S,Jootar S,et al. Cost-utility analysis of dasatinib and nilotinib in patients with chronic myeloid leukemia refractory to first-line treatment with imatinib in Thailand[J]. Clin Ther,2014,36(4):534-543. [17] Huang X,Jiang Q,Hu J,et al. Four-year follow-up of patients with imatinib-resistant or intolerant chronic myeloid leukemia receiving dasatinib: Efficacy and safety[J]. Front Med,2018,13(3):344-353. [18] Padula W V,Larson R A,Dusetzina S B,et al. Cost-effectiveness of tyrosine kinase inhibitor treatment strategies for chronic myeloid leukemia in chronic phase after generic entry of imatinib in the United States[J]. J Natl Cancer Inst,2016,108(7):djw003. doi: 10.1093/jnci/djw003 [19] 刘国恩. 中国药物经济学评价指南(2020中英双语版)[M]. 北京: 中国市场出版社, 2020: 27-47. [20] Nguyen J T,Cole A L,Leech A A,et al. Cost-effectiveness of first-line tyrosine kinase inhibitor therapy initiation strategies for chronic myeloid leukemia[J]. Value Health,2020,23(10):1292-1299. doi: 10.1016/j.jval.2020.05.019 [21] Li N,Zheng B,Cai H F. et al. Cost effectiveness of imatinib,dasatinib,and nilotinib as first-line treatment for chronic-phase chronic myeloid leukemia in china[J]. Clin Drug Investig,2018,38(1):79-86. doi: 10.1007/s40261-017-0587-z [22] Cai D,Shi S,Jiang S,et al. Estimation of the cost-effective threshold of a quality-adjusted life year in China based on the value of statistical life[J]. Eur J Health Econ,2022,23(4):607-615. doi: 10.1007/s10198-021-01384-z -






 下载:
下载:
 下载:
下载: