Uncertainty Evaluation of the Determination of the Content of Ambroxol Hydrochloride Injection by Using TOP-DOWN Method and GUM Method
-
摘要:
目的 通过评定盐酸氨溴索注射液含量测定结果的不确定度,提高含量测定结果的可靠性,保证高风险制剂药物的安全性和有效性。 方法 分别采用TOP-DOWN法和GUM法对HPLC外标法含量测定结果进行不确定度评定。TOP-DOWN法为合成偏倚不确定度分量和期间精密度不确定度分量2个分量后进行评价;GUM法根据实验过程分析出6个不确定来源,合成不确定度后进行评价。 结果 当置信概率为95%,TOP-DOWN法和 GUM法评定的扩展不确定度分别为1.84%和2.36%(K = 2)。 结论 2种评定结果均表明盐酸氨溴索注射液含量测定结果可靠,能保证药物的安全性和有效性。 Abstract:Objective By assessing the uncertainty of the determination results for the concentration of ambroxol hydrochloride injection, the reliability of the concentration measurement results is improved, ensuring the safety and efficacy of high-risk dosage form medications. Methods The uncertainty assessment of the content determination results by HPLC external standard method was conducted using both the TOP-DOWN method and the GUM method in the past. The TOP-DOWN method evaluated after synthesizing two components: the combined bias uncertainty component and the intermediate precision uncertainty component. The GUM method analyzed six sources of uncertainty based on the experimental process and evaluated after synthesizing the uncertainty. Results When the confidence level was 95%, the expanded uncertainty assessed by the TOP-DOWN method and the GUM method was 1.84% and 2.36% respectively (K = 2). Conclusion The results from both assessments indicated that the determination of ambroxol hydrochloride injection content was reliable, ensuring the safety and efficacy of the drug. -
目前,在世界范围内脂质代谢紊乱相关疾病的发病率及死亡率呈现逐年升高的趋势,早期诊断并制定早期干预策略非常必要[1]。γ-谷氨酰基转移酶(gamma-glutamyl transferase,GGT)是一种普遍存在的细胞表面酶,可裂解细胞外谷胱甘肽(G-SH)或其他γ-谷氨酰化合物,并在维持G-SH稳态和防御生物体中的氧化应激方面发挥关键作用。但在临床实际工作中,GGT活性检测仅用于肝脏和阻塞性胆道疾病的诊断以及作为饮酒量的指标。随着对GGT生理功能和作用机理研究的深入,多项研究表明GGT活性水平升高与脂质代谢紊乱相关性疾病(如代谢综合征、胰岛素抵抗、心脑血管疾病、脂肪性肝病、氧化应激负担等)以及患者风险状况和预后息息相关[2-3]。Cruz M A等[4]在一项验证肝脂肪变性程度与天冬氨酸转氨酶、谷丙氨酸转移酶和GGT之间关联研究中发现,相比较前两项指标,GGT升高与非酒精性脂肪肝病(non-alcoholic fatty liver disease,NAFLD)分级呈明显正相关且更能反映出脂肪肝的严重程度。多项研究显示GGT具有对脂质代谢紊乱相关性疾病的强大预测能力,是较好的早期预测标志物[5-7]。虽然GGT与脂质代谢紊乱相关性疾病的相关研究多有报道,但在正常体检人群中,GGT升高与血脂代谢相关性如何,尚未见研究报道。本研究旨在探讨正常体检人群GGT与血脂异常的关系,为脂质代谢紊乱相关性疾病的早诊早治提供依据。
1. 资料与方法
1.1 临床资料
选取2020年04月至2021年08月西安交通大学第一附属医院医院体检中心的3137例体检者为研究对象,其中男1918例,年龄范围18~93岁,平均(49.50 ± 12.71)岁;女1219例,年龄范围21~96岁,平均(49.08 ± 13.01)岁。所有体检者均经过影像学、实验诊断学及全身体格检查,并在体检前1 d禁酒、禁油腻、清淡饮食,晨起、静息、空腹状态静脉采血。排除标准:严重心、肝、肾功能不全;酗酒;自身免疫性疾病;胆道疾病;恶性肿瘤患;GGT异常升高(大于400 U/L);酒精性和病毒性肝炎;存在引起血脂异常的相关疾病(如噬血细胞综合征、脂性肾病等)。该项研究通过了西安交通大学第一附属医院医学伦理审查委员会批准。
1.2 试剂和仪器
GGT、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、高密度脂蛋白(high lipoprotein,HDL)和低密度脂蛋白(low density lipoprotein,LDL)检测仪器采用日本日立 LABOSPECT 008 AS 全自动生化分析仪,试剂由富士胶片和光纯药株式会社提供。
1.3 统计学处理
采用R软件(3.6.3版本)进行统计学分析,不服从正态分布的计量资料采用M(P25,P75)表示;性别和年龄进行倾向性匹配得分以消除偏倚;率的比较采用χ2检验;多组间量值的两两比较采用Bonferroni法校正后进行多重Dunn's test假设检验;相关性采用Spearman秩相关;二元Logistic多因素回归分析采用“逐步法”进行;P < 0.05为差异具有统计学意义。
2. 结果
2.1 血脂4项在GGT不同浓度间的结果比较
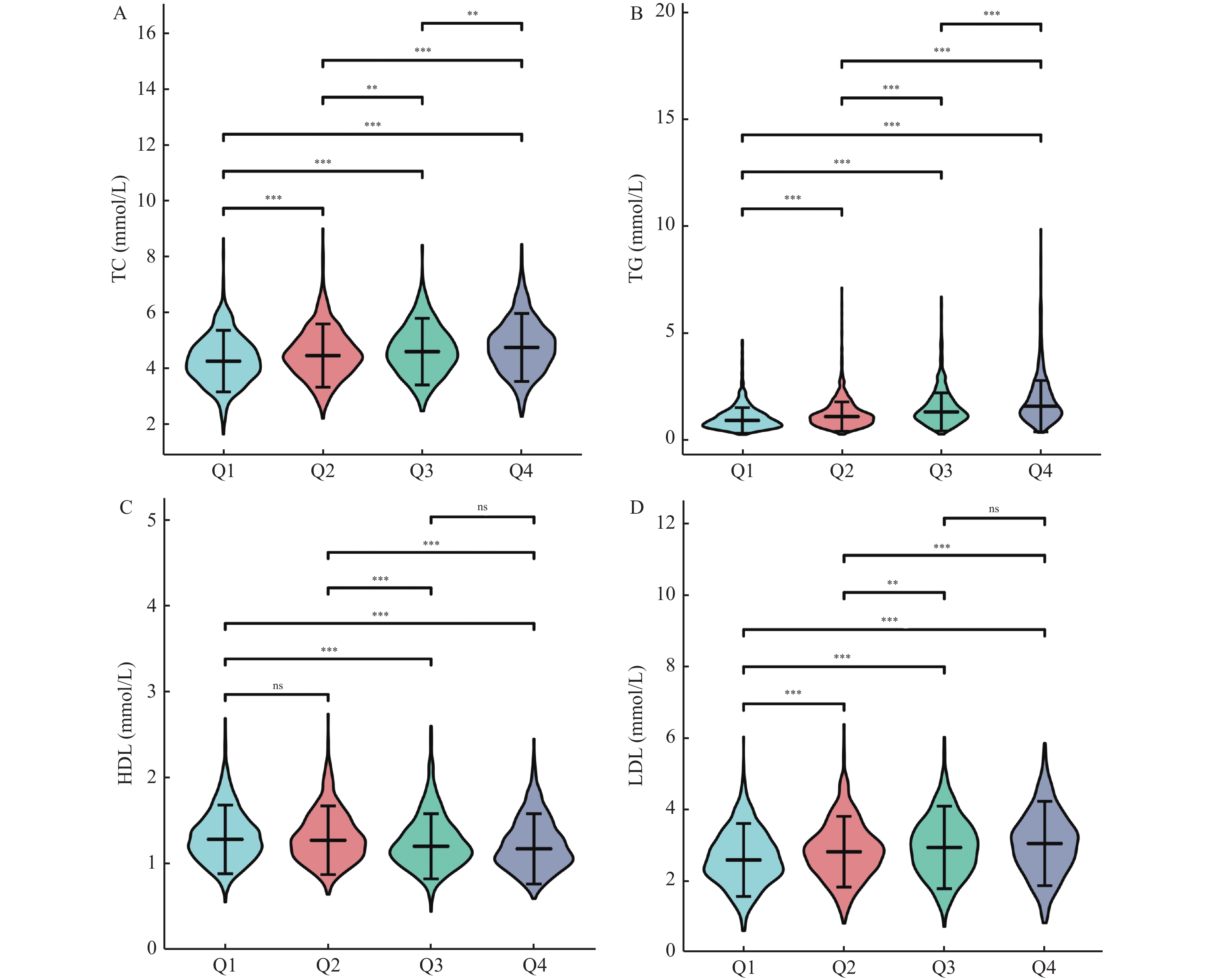
为了明确血脂4项指标在不同GGT浓度间的水平差异,本研究首先将GGT浓度按照四分位数间距(P25 = 16 U/L,P50 = 22 U/L,P75 = 30 U/L)分为4组(Q1组-Q4组),之后对性别和年龄进行倾向性匹配得分以消除基线资料所带来的偏倚。通过对3137例体检者在各组的基线资料和血脂4项水平和异常率的比较发现,血脂4项指标水平在各组间均有统计学差异(P < 0.001),且TC、TG和LDL水平随GGT浓度升高而增加,HDL水平随GGT浓度升高而降低;在异常率比较方面,血脂4项指标均随GGT浓度升高而增加(P < 0.001),见表1、图1。
表 1 3137例体检者在不同GGT浓度中的血脂四项指标水平和异常率[M(P25,P75)/n(%)]Table 1. Levels and abnormal rate of four indexes of blood lipids in 3137 physical examination subjects at different GGT concentrations [M(P25,P75)/n(%)]变量 Q1组 Q2组 Q3组 Q4组 χ2 P 例数(n) 799 790 784 764 性别 0.440 0.932 男 487 (61.0) 485 (61.4) 473 (60.3) 473 (61.9) 女 312 (39.0) 305 (38.6) 311 (39.7) 291 (38.1) 年龄(岁) 51.0 (39.0,62.0) 49.0 (35.0,63.0) 51.0 (40.0,61.0) 51.0 (40.0,58.0) 49.835 0.116 血脂水平 TC (mmol/L) 4.3 (3.7,4.8) 4.5 (3.9,5.0) 4.6 (4.0,5.2) 4.8 (4.2,5.4) 92.286 < 0.001* TG (mmol/L) 0.9 (0.7,1.3) 1.1 (0.8,1.5) 1.3 (1.0,1.9) 1.6 (1.2,2.4) 715.542 < 0.001* HDL (mmol/L) 1.3 (1.1,1.5) 1.3 (1.1,1.5) 1.2 (1.0,1.4) 1.2 (1.0,1.4) 349.156 < 0.001* LDL (mmol/L) 2.6 (2.1,3.2) 2.8 (2.3,3.3) 3.0 (2.4,3.5) 3.1 (2.4,3.6) 122.618 < 0.001* 血脂异常率 TC (mmol/L) 78 (6.8) 119 (9.0) 146 (13.1) 181 (16.5) 58.082 < 0.001* TG (mmol/L) 192 (16.7) 340 (25.9) 463 (41.5) 612 (55.7) 531.980 < 0.001* HDL (mmol/L) 359 (31.2) 455 (34.6) 489 (43.9) 525 (47.8) 98.333 < 0.001* LDL (mmol/L) 309 (26.9) 456 (34.7) 478 (42.9) 529 (48.1) 160.612 < 0.001* *P < 0.05。 2.2 GGT与血脂四项指标的相关性分析
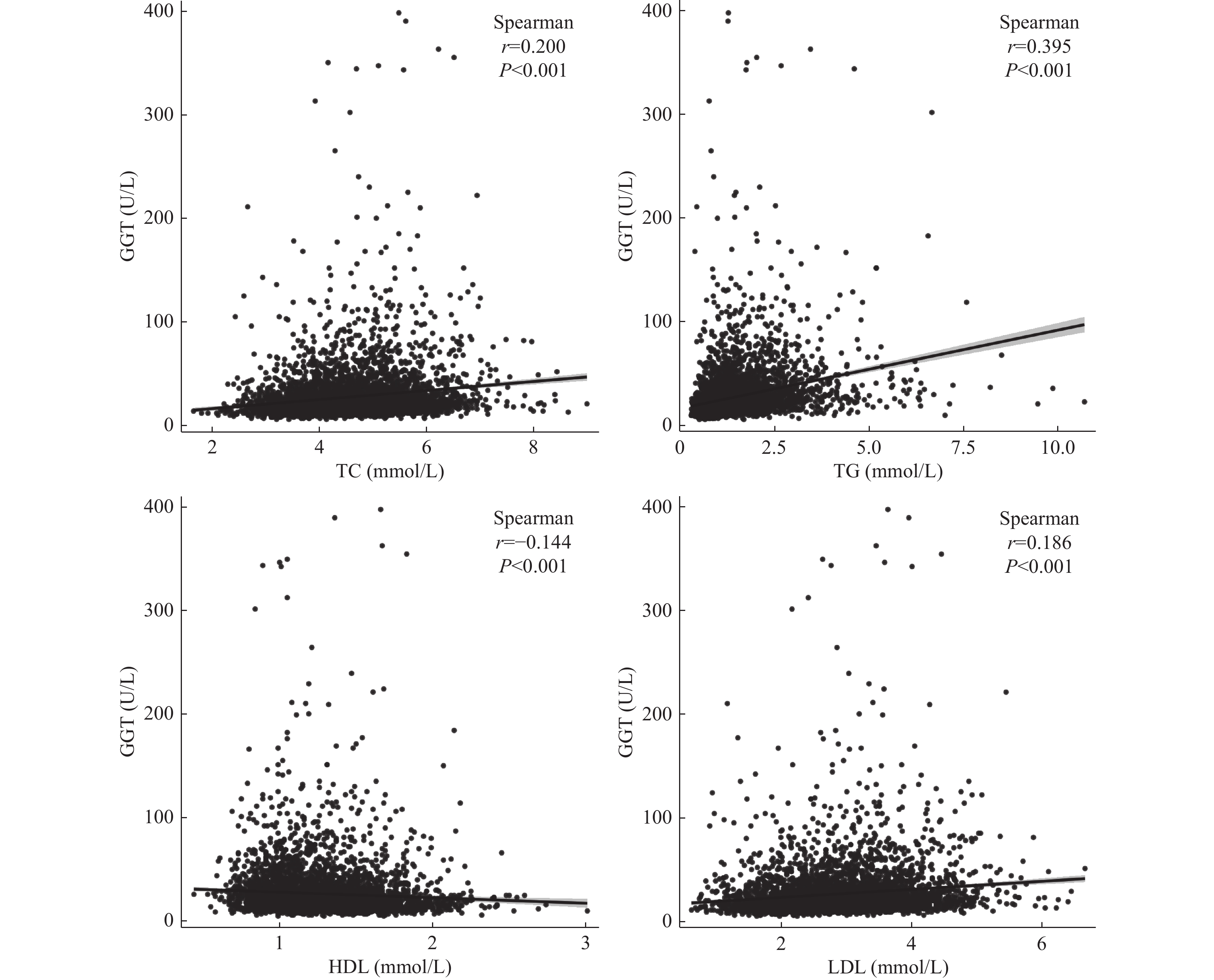
本研究进一步对3137例体检者GGT浓度与血脂4项进行了Spearman相关性分析,结果显示,GGT浓度与血脂四项指标水平均有相关性(P均<0.001),其中,HDL呈负相关,TC、TG和LDL呈正相关,且与TG的相关性最强(rs = 0.395),见表2、图2。
表 2 GGT与TC、TG、HDL和LDL的相关性Table 2. Correlation of GGT with TC,TG,HDL and LDL指标 GGT r P TC 0.200 < 0.001* TG 0.395 < 0.001* HDL −0.144 < 0.001* LDL 0.186 < 0.001* 注:数据均呈偏态分布,采用Spearman相关性分析,*P < 0.05。 2.3 GGT浓度在血脂异常中的比较
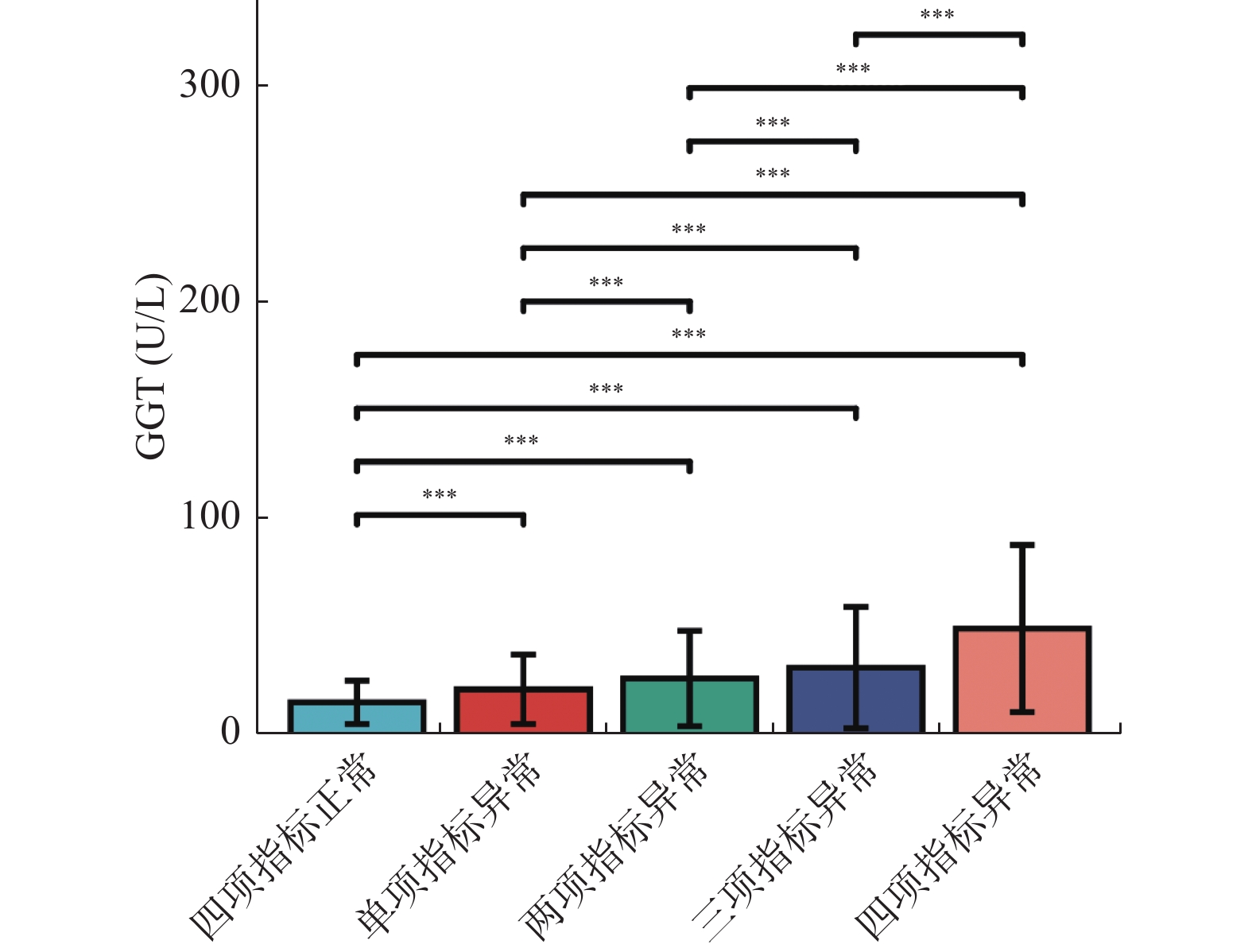
本研究还探讨了TC、TG、HDL和LDL 4项指标不同异常情况下与GGT浓度的关系。各指标参考值范围分别为:TC 3.10~5.69 mmol/L;TG 0.56~1.47 mmol/L;HDL 1.16~1.42 mmol/L;LDL 2.07~3.10 mmol/L。TC、TG和LDL以大于正参考值上限为异常,HDL以小于正常参考值下限为异常。根据各指标的异常情况将研究对象分为4项指标正常组、单项指标异常组、2项指标同时异常组、3项指标同时异常组、4项指标同时异常组。结果显示,GGT浓度在各分组间均有统计学差异(P均<0.001),并随着异常指标的增加出现递增的趋势,且以4项指标同时异常组为最高,见表3、图3。
表 3 GGT在不同血脂异常分组中的构成比和浓度水平[M(P25,P75)/n(%)]Table 3. Composition ratio and concentration level of GGT in different dyslipidemia groups [M(P25,P75)/n(%)]组别 n 构成比 中位数 四项指标正常 3137 905(28.85) 16(12.0,22.0) 单项指标异常 3137 949(30.25) 22(16.0,32.0) 两项指标异常 3137 783(24.96) 27(19.0,41.0) 三项指标异常 3137 445(14.19) 32(23.0,51.0) 四项指标异常 3137 55(1.75) 50(40.0,78.5) 2.4 GGT阳性的二元Logistic回归分析
为筛选GGT升高的危险因素,分别以GGT大于中位数和大于正常参考值上限界定为GGT阳性,将GGT是否阳性为因变量,以TC、TG、HDL和LDL为自变量,采用“逐步法”分别进行二元logistic多因素回归分析。结果显示,GGT阳性无论以GGT大于中位数还是以大于正常参考值上限为界定,TG均是影响GGT浓度升高的独立危险因素,OR值分别为2.360(95% CI:2.068~2.695)和1.635(95% CI:1.481~1.805),见表3。
3. 讨论
Rytz C L等[8]认为脂质代谢紊乱导致脂肪组织中活性氧的增加,增加的氧化应激引起细胞变性、坏死和纤维化。Panchal等[9]在脂质代谢紊乱的小鼠体内发现了肝细胞损伤、脂肪空泡、纤维化、脂质沉积和炎细胞浸润等现象,并观察到随着机体脂肪量增加,糖耐量受损、高胰岛素血症和肝酶活性增加愈加明显。研究认为[10-11],脂肪沉积增加会诱导细胞损伤、炎症和氧化应激,谷胱甘肽是一种细胞内抗氧化剂,也是氧化应激的标志物,GGT活性增加反映谷胱甘肽的消耗增加,即GGT活性增加可能反映脂质代谢紊乱患者的氧化应激状态。基于以上观点,本研究首先对不同GGT浓度间(Q1组~Q4组)的反映脂质代谢的TC、TG、HDL和LDL 4项指标进行两两比较以初步了解GGT浓度升高与血脂4项的关系。结果表明血脂4项指标水平和异常率在各组间均有统计学差异,且除HDL水平随GGT浓度升高出现降低外,反映脂质沉积的TC、TG和LDL 3项指标均随GGT浓度升高而增加。之后,笔者对GGT浓度与血脂4项的Spearman相关性进行了分析,结果提示GGT浓度除与HDL呈负相关外(rs = -0.144),与其它3项指标均呈现正相关,相关系数分别为0.200,0.395和0.186,这与研究报道的结果一致。值得一提的是,HDL具有抗炎、抗氧化和抗血栓的特性,与胰岛素抵抗、血脂异常、动脉粥样硬化指数和肥胖有关[12]。有研究证实,低HDL与心血管事件、胰岛素抵抗指数、能量摄入、碳水化合物摄入和体重增加的风险增加有关,对于低HDL的血脂异常者,应同时考虑能量和碳水化合物限制[13-14]。结合本研究中表1、表2和表4所展现的结果,笔者认为HDL是GGT浓度正常的保护因素。
表 4 血脂4项的二元Logistic多因素分析Table 4. Multivariate analysis of binary Logistic regression for blood lipids指标 β SE Wald P OR 95%CI 以中位数分组 TG 0.859 0.068 161.455 0.000 2.360 2.068~2.695 HDL 1.271 0.162 61.261 0.000 0.281 0.204~0.386 LDL 0.340 0.053 41.744 0.000 1.405 1.268~1.558 常数 0.670 0.254 6.968 0.008 0.512 - 以参考值分组 TC 0.333 0.071 22.157 0.000 1.395 1.215~1.603 TG 0.491 0.051 94.702 0.000 1.635 1.481~1.805 常数 4.725 0.343 189.541 0.000 0.009 - 注:“-”表示无数据。 本研究还探讨了TC、TG、HDL和LDL四项指标不同程度的异常是否影响GGT浓度。结果证实GGT浓度会随着血脂异常指标的增加出现递增的趋势,且以血脂四项指标同时异常为最高。Wu K T等[15]研究证实具有高TC/HDL-C或TG/HDL-C比率或两者兼有的成年人患NAFLD和糖尿病的风险更大,尤其是晚期NAFLD。因此,本研究认为,与4项血脂指标均正常或孤立的单个指标异常相比,多个血脂指标的同时异常会引起更多脂质沉积导致氧化应激更为剧烈,出现的显著GGT升高应该是一种累加效应。在明确了GGT浓度升高和血脂异常的密切关系后,本研究进行了GGT升高的二元Logistic回归危险因素分析,以确证四项血脂指标在影响GGT升高中的权重。笔者分别从GGT大于中位数和大于正常参考值两个方面进行分析。结果显示,GGT阳性无论以GGT大于中位数还是以大于正常参考值上限为界定,TG均是影响GGT浓度升高的独立危险因素。一项前瞻性研究证实,在伴随TG异常升高的情况下,GGT和谷丙氨酸转移酶同时升高与2型糖尿病发病率的增加密切相关[16]。根据“多重打击”学说,肝脏脂质沉积的主要是TG,TG引起的脂毒性通过信号级联放大效应、死亡受体介导、巨噬细胞激活、细胞器氧化应激和线粒体功能改变等多种途径影响肝细胞行为[17-18]。因此,针对GGT升高伴随有TG异常代谢者,选择他汀类降脂药或更有助益。
该研究尚有一些局限性。首先,没有纳入脂联素和瘦素这两项指标,根据“多重打击”学说,分析该两项指标与GGT的相关性更有助于反映氧化应激和脂质蓄积的程度。其次,笔者虽然分析了血清GGT水平与单项和多项血脂指标同时异常的情况,但未对每组进行进一步分层。第三,本研究虽然证实了GGT升高和血脂异常的相关性,但GGT是如何参与疾病发生、发展的确切分子机制和以及能否把GGT作为降脂治疗的评估指标,仍有待进一步研究。
综上所述,在体检人群中,血脂异常者的GGT浓度明显高于血脂正常者。GGT浓度与血脂代谢异常程度密切相关。对血脂异常者进行常规GGT水平监测有助于识别脂质代谢紊乱相关疾病的高危人群,帮助临床医生提前规划和启动适当的健康管理策略,改善疾病转归。
-
表 1 实验室间再现性数据
Table 1. Inter-laboratory reproducibility data
序号 x1(%) x2(%) $ \overline {{x_i}} $(%) bi si h k 样品统计 1 100.82 100.20 100.51 0.51 0.44 0.10 1.88 ARV = 100.4%
X = 100.445%
$ {s_{\overline x }} $ = 1.08
sr = 0.2072 100.23 100.33 100.28 0.28 0.07 −0.11 0.30 3 100.80 100.85 100.83 0.82 0.04 0.39 0.15 4 101.70 101.95 101.83 1.83 0.18 1.32 0.76 5 99.48 99.61 99.55 −0.45 0.09 −0.79 0.39 6 100.30 100.80 100.55 0.55 0.35 0.14 1.52 7 98.40 98.20 98.30 −1.70 0.14 −1.94* 0.61 8 100.30 99.70 100.00 0.00 0.42 −0.37 1.82 9 101.48 101.23 101.36 1.36 0.18 0.88 0.76 10 99.01 99.15 99.08 −0.92 0.10 −1.22 0.42 11 101.32 101.33 101.33 1.32 0.00 0.85 0.03 12 100.28 100.06 100.17 0.17 0.16 −0.21 0.67 13 98.58 98.59 98.59 −1.41 0.01 −1.68 0.03 14 100.71 100.55 100.63 0.63 0.11 0.21 0.49 15 101.42 102.15 101.79 1.79 0.52 1.28 2.22* 16 100.99 100.92 100.96 0.95 0.05 0.51 0.21 17 101.77 101.92 101.85 1.85 0.11 1.33 0.46 注:标*为异常值。 表 2 实验室内重复性数据
Table 2. Repeatability data within the laboratory
n 1 2 3 4 5 6 7 8 9 10 xi 99.9 100.2 100.6 100.7 101.1 100.3 101.9 100.5 102.7 101.4 n 11 12 13 14 15 16 17 18 $ \bar x $ SR’ xi 99.4 99.5 101.5 101.6 101.8 100.3 101.1 100.4 100.9 0.88% 表 3 GUM法各分量相对不确定度结果汇总表
Table 3. Summary of Relative Uncertainty Components Using the GUM Method
分量 来源 影响因素 分布 分类 相对不确定度 urel (p) 对照品纯度 纯度 矩形 B 2.9×10−4 urel(m) 对照品称重 示值、偏载误差 矩形 B 8.5×10−3 urel(va) 容量瓶定容 容量允差MPE、温度效应 三角和矩形 B 1.4×10−3 urel(vb) 移液管量取 容量允差MPE、温度效应 三角和矩形 B 4.0×10−3 urel(r) 仪器性能 整机性能定量重复性 矩形 B 6.5×10−3 urel(x) 样品重复性测量 12份样品 正态 A 2.7×10−3 -
[1] 范玲,于栋伟. 氨溴索的药理作用及临床应用研究进展[J]. 北方药学,2015,12(9):116-117. [2] 张瑞红,陈迪. 盐酸氨溴索注射液在儿科呼吸系统疾病治疗中的应用价值[J]. 中国医药指南,2018,16(2):47-48. [3] 王玉,王思寰,李文莉. 不确定度评定与药品检验[M]. 北京: 中国医药科技出版社,2021: 11-15. [4] 肖亭,王晨,许明哲,等. 测量结果不确定度评定在我国药物分析领域中的应用[J]. 药物分析杂志,2021,41(11):1851-1859. [5] 侯梦妮,谢珍,刘柱,等. 不确定度评定在药品检验中的研究进展[J]. 海峡药学,2018,30(6):54-57. [6] 杨娟,王立云,杨龙华,等. 测量不确定度在化学药物质量控制中的应用及研究进展[J]. 中国药师,2020,23(3):530-534. [7] 吴婷,龙焰君,张慧文,等. HPLC法测定注射用头孢他啶含量的不确定度评定[J]. 广东药科大学学报,2023,39(4):20-24. [8] 中国合格评定国家认可委员会. 材料理化检测测量不确定度评定指南及实例 CNAS GL009: 2018[S]. 北京: 中国计量出版社,2018: 5-12. [9] 王斗文,邓云,王冰,等. 检验检测实验室质量控制技术top-down不确定度评定[M]. 北京: 中国质检出版社,2017: 5-15. [10] 李菁,康帅,王冰,等. MCM法和GUM法在药品内标法含量测定不确定度评定中的比较研究[J]. 中国药学杂志.,2022,57(6):472-477. [11] 国家药典委员会. 《中华人民共和国药典》(2020年版二部)[M]. 北京: 中国医药科技出版社,2020: 1270-1271. [12] 国家认证认可监督管理委员会. RB/T 141–2018 化学检测领域测量不确定度评定 利用质量控制和方法确认数据评定不确定度[S]. 北京: 中国标准出版社,2018: 3-21. [13] 孙煜,何虹,黄慧,等. 高效液相色谱法测定灵芝二维甲硫氨酸胶囊溶出度及测量不确定度评定[J]. 化学分析计量,2021,30(4):79-84. [14] 国家标准化管理委员会. GB/T 27411-2012 检测实验室中常用不确定度评定方法与表示[S]. 北京: 中国标准出版社,2012: 7-16. [15] 国家标准化管理委员会. GB/Z 22553-2010/ISO/TS 21748: 2004 利用重复性、再现性和正确度的估计值评估测量不确定度的指南[S]. 北京: 中国标准出版社,2004: 13-15. [16] 刘翔,王湘波,彭凡,等. 湖南省药检系统进行氨甲环酸含量测定实验室比对的结果分析[J]. 中国药事,2015,29(11):1156-1162. [17] 丁建东,宁攀良. Top-down控制图法评定石墨炉原子吸收光谱法测定血中铅含量的不确定度[J]. 化学分析计量,2024,33(2):117-122. [18] 张鑫, 王硕, 段卫宇, 等. Top-down 法评定X射线荧光光谱法测定车用柴油中总硫含量的测量不确定度[J]. 当代化工,2022,51(12):3017-3020. [19] 蔡凌霄, 贾苒, 白正伟, 等. 利用TOP-DOWN法评定电感耦合等离子体原子发射光谱法测定土壤样品中铅元素含量的不确定度[J]. 化学分析计量,2023,32(7):104-108. 期刊类型引用(0)
其他类型引用(1)
-






 下载:
下载:
 下载:
下载: 
