Adverse Reactions Analysis and Prediction Model of Cefoperazone Sodium Sulbactam Sodium
-
摘要:
目的 通过分析注射用头孢哌酮钠舒巴坦钠在昆明市医疗机构中使用的安全性,探索其发生不良反应(ADR)的影响因素,以及因素之间的相关性,从而构建其发生不良反应的预测模型,为临床合理应用提供参考。 方法 提取2015年01月至2020年06月期间,昆明市药品不良反应报告监测数据库中注射用头孢哌酮钠舒巴坦钠的不良反应报告222份作为观察组,同期使用注射用头孢哌酮钠舒巴坦钠未发生不良反应的250份病例作为对照组,收集2组患者的临床资料,通过相关性分析因素之间的关系;采用多因素Logistic回归分析发生不良反应的相关因素,根据结果拟合构建发生不良反应的预测模型;通过受试者工作特征(ROC)曲线评价预测模型的效能。 结果 相关性分析结果显示,年龄与原患疾病的例次呈正相关关系(Kendall’ s tau-b = 0.764,P < 0.05);用药时间与住院时间呈负相关关系(r = -0.124,P < 0.05);多因素Logistic回归分析结果显示:退休人员、肝肾功能损伤患者、用药时间在(11~15)d是头孢哌酮钠舒巴坦钠发生不良反应的相关因素,其预测模型为Logit(P) = 1.357 + 3.485 × 肝肾功能损伤 + 2.681 × 用药天数(11~15),该模型ROC曲线下面积为0.877,预测模型的灵敏度为91.8%,特异度为77.4%。 结论 肝肾功能损伤患者、用药时间在11~15 d是头孢哌酮钠舒巴坦钠发生不良反应的相关因素,该预测模型具有较高的临床应用价值。 -
关键词:
- 注射用头孢哌酮钠舒巴坦钠 /
- 药品不良反应 /
- 预测模型
Abstract:Objective To analyze the safety of cefoperazone Sodium and Sulbactam Sodiumfor injection in Kunming medical institutions, explore the influencing factors of adverse reactions (ADR) and the correlation between the factors, so as to construct the prediction model of adverse reactions, and provide reference for the rational application ofcefoperazone Sodium and Sulbactam Sodium in clinical practice. Methods From January 2015 to June 2020, 222 adverse reaction reports of cefoperazone sodium and sulbactam sodium for injection in the Kunming City Adverse Drug Reaction Report Monitoring Database were extracted as the observation group. During the same period, no adverse reaction occurred when using cefoperazone sodium and sulbactam sodium for injection, The 250 responding cases were used as the control group. The clinical data of the two groups of patients were collected, and the relationship between the factors was analyzed through correlation; the related factors of adverse reactions were analyzed by multivariate logistic regression, and the prediction of adverse reactions was constructed according to the results Model. Evaluate the effectiveness of predictive models through receiver operating characteristic (ROC) curves. Results Correlation analysis showed that age was positively correlated with the number of primary diseases (Kendall’ s tau-b = 0.764, P < 0.05). There was a negative correlation between medication time and hospital stay (r = -0.124, P < 0.05). Multivariate logistic regression analysis showed that retirees, patients with liver and kidney dysfunction, and medication time (11-15) days were related factors for the adverse reactions of cefoperazone sodium and sulbactam sodium. The prediction model is logit (P)= 1.357 + 1.739 × retirees + 3.485 × liver and kidney damage + 2.681 × days of medication (11-15). The area under the ROC curve of this model is 0.877, and the sensitivity and specificity are 91.8% and 77.4%, respectively. Conclusion Liver and kidney dysfunction patients, medication time (11~15) d are the related factors of adverse reactions of Cefoperazone Sodium and Sulbactam Sodiumand the prediction model has high clinical value. -
注射用头孢哌酮钠舒巴坦钠是三代头孢菌素头孢哌酮和β-内酰胺酶舒巴坦组成的复方制剂,具有广谱抗菌活性,主要用于下呼吸道感染、泌尿生殖系统感染、腹腔和盆腔感染以及重症皮肤和软组织感染等。在国产仿制药一致性评价工作推广的大背景下,该药目前临床应用广泛,但不良反应报告日益增多,说明书中显示最常见的不良反应类型为胃肠道反应。有研究显示,头孢哌酮钠舒巴坦钠的不良反应风险因素主要有年龄、既往史、原患疾病和用药时间等[1]。为探究头孢哌酮钠舒巴坦钠的风险因素之间是否具有相关性,以及为一致性评价工作提供更多的安全性评价数据基础,拟检索昆明市药品不良反应报告监测数据库中的上报案例,通过对相关信息进行整理,寻找其影响因素的发生规律,并对因素进行相关性分析和预测模型的构建,为后期临床合理安全应用提供参考。
1. 资料与方法
1.1 资料来源
检索昆明市药品不良反应报告监测数据库,提取2015年01月至2020年06月份上报的头孢哌酮钠舒巴坦钠不良反应报告222份,作为观察组;抽取同期昆明市第三人民医院使用头孢哌酮钠舒巴坦钠未发生不良反应的住院患者250例,作为对照组,整理两组患者的相关信息。
1.2 方法
采用回顾性分析的方法,利用Excel 2016软件对两组患者的年龄、性别、身体质量指数(BMI)、原患疾病、用药原因、用药时间、住院时间、累及系统-器官及主要临床表现、不良反应结果和分级程度、给药剂量及频次等进行统计分析,结合相关文献报道,分析不良反应发生的影响因素。
1.3 统计学处理
数据通过Excel 2016进行整理,计量资料采用均数±标准差(
$\bar x \pm s $ )表示,使用t检验;计数资料采用例数或百分比表示,使用χ2检验。通过相关性分析方法对单因素进行统计,连续变量使用Pearson相关系数分析,有序变量使用Kendall’ s tau-b相关系数分析,检验水准ɑ值取双侧0.05,取值范围在[-1,+1],相关系数越接近0,表示相关关系越弱;越接近-1或+1,表示相关关系越强。单因素分析采用χ2/t检验,多因素分析采用二分类Logistic回归分析,根据结果拟合构建发生不良反应的预测模型,通过受试者工作特征(ROC)曲线评价预测模型的效能。双侧检验,以P < 0.05为差异有统计学意义。2. 结果
2.1 患者的性别和年龄分布
222份不良反应报告中男性患者87例,占39.19%;女性患者135例,占60.81%。性别比(男/女)为1∶1.55。年龄分布情况显示,最小年龄者为14岁,最大年龄者为87岁,其中65岁以上的老年患者居多(表1),平均年龄(63.22 ± 15.41)岁,平均身体质量指数(BMI)为(21.21 ± 1.56) kg/m2。
表 1 头孢哌酮钠舒巴坦钠不良反应报告患者的性别与年龄分布(n)Table 1. Gender and age distribution of patients with adverse reactions of cefoperazone sodium and sulbactam sodium (n)年龄(岁) 男 女 总例数 构成比(%) 5~14 4 8 12 5.40 15~44 20 25 45 20.27 45~64 23 16 39 17.57 ≥ 65 40 86 126 56.76 合计 87 135 222 100.00 注:《国际疾病分类》(ICD-10)编码分类:婴儿期为不足1岁,幼儿期为1~4岁,少儿期为5~14岁,青壮年期为15~44岁,中年期为45~64岁,老年期为65岁及以上。 2.2 原患疾病与用药原因
222份不良反应报告中原患疾病主要包括慢性阻塞性肺疾病伴急性下呼吸道感染、心功能不全、肝损伤、高血压等(表2)。用药原因包括下呼吸系统感染199例,占比89.63%;腹腔感染23例,占比10.37%。年龄与原患疾病例次的相关性分析显示,两者呈正相关关系(Kendall’ s tau-b = 0.764,P < 0.05),结果提示,患者年龄越大,可能合并原患疾病类型越多。
表 2 头孢哌酮钠舒巴坦钠不良反应报告患者的原患疾病Table 2. Primary diseases of ADR patients caused by cefoperazone sodium and sulbactam sodium序号 原患疾病 n 构成比(%) 1 慢性阻塞性肺疾病伴
急性下呼吸道感染210 28.23 2 心功能不全 111 14.91 3 肝损伤 74 9.95 4 高血压 71 9.54 5 糖尿病 46 6.18 6 腰椎退行性病变 50 6.72 7 肺结核 43 5.78 8 肾损伤 41 5.52 9 脑膜炎 33 4.43 10 前列腺增生 24 3.23 11 腹腔感染 26 3.49 12 胃炎 15 2.02 2.3 不良反应累及系统和临床表现
222份不良反应报告根据《WHO药品不良反应术语集》对不良反应名称和累及系统-器官进行归类,主要累及皮肤和附件、消化系统、呼吸系统等(表3)。原患疾病例次与不良反应临床表现例次的相关性分析显示,两者之间相关性弱(Kendall’ s tau-b = 0.104,P > 0.05),结果提示,原患疾病对不良反应的临床表现类型影响弱;年龄与不良反应临床表现例次的相关性分析显示,两者之间相关性弱(Kendall’ s tau-b = 0.162,P > 0.05),结果提示,年龄对不良反应临床表现类型影响弱。
表 3 头孢哌酮钠舒巴坦钠不良反应报告累及系统-器官分布及临床表现(n)Table 3. The adverse reaction report of cefoperazone sodium and sulbactam sodium involves system-organ distribution and clinical manifestations(n)累及系统-器官 临床表现 例次 合计 构成比(%) 皮肤及附件损害 瘙痒
红斑疹
局部肿胀
皮肤发红
口唇发绀154
3
26
27
29239 50.53 血液系统损害 凝血功能障碍
白细胞减少17
421 4.44 呼吸系统损害 呼吸困难 65 65 13.74 全身性损害 发热
畏寒31
1546 9.73 消化系统损害 恶心
呕吐53
49102 21.56 2.4 不良反应结果及分级程度
222份不良反应报告中的患者经停药或者对症治疗后,有206例好转,占比92.79%,16例痊愈,占比7.21%。分级程度均为一般。
2.5 给药剂量及频次
222份不良反应报告中,头孢哌酮钠舒巴坦钠给药剂量及频次3 g,Tid有155例,占比69.82%;3 g,Bid有34例,占比15.31%;1.5 g,Tid有19例,占比8.56%;1.5 g,Qd有14例,占比6.31%,均未超说明书规定剂量用药。
2.6 患者的用药时间和住院时间
222份不良反应报告中有184例患者用药时间(用药疗程)在5 d以内,占比76.03%;住院时间在16天以上的有121例,占比50.00%(表4)。222例患者的平均用药天数为(3.17 ± 2.16)d,平均住院天数为(18.33 ± 12.17)d。用药时间与住院时间呈负相关关系(r = -0.124,P < 0.05),结果提示,患者用药时间较短时发生的药物不良反应,往往会造成患者的住院时间延长。
表 4 头孢哌酮钠舒巴坦钠不良反应报告患者的用药时间和住院时间Table 4. Adverse reactions of cefoperazone sodium and sulbactam sodium are reported on the duration of medication and hospital stay in patients天数
(d)用药时间
(n)构成比
(%)住院时间/
例数(n)构成比
(%)1~5 163 73.42 8 3.60 6~10 39 17.57 24 10.81 11~15 20 9.01 77 34.68 ≥ 16 − − 113 50.91 合计 222 100.00 222 100.00 2.7 头孢哌酮钠舒巴坦钠不良反应的单因素分析
观察组的女性患者人数高于对照组,2组患者的年龄分层、原患疾病分层和用药时间分层差异均有统计学意义(P < 0.05)。2组患者的婚姻状况、BMI、给药日剂量分层、住院天数分层差异均无统计学意义(P > 0.05),见表5。
表 5 头孢哌酮钠舒巴坦钠不良反应的单因素分析Table 5. Single factor analysis of adverse reactions of cefoperazone sodium and sulbactam sodium研究因素 观察组(n = 222) 对照组(n = 250) χ2/t P 性别 男 87 131 女 135 119 8.256 0.004* 婚姻 已婚 199 230 未婚 23 20 0.791 0.373 BMI(kg/m2) 21.21 ± 1.56 22.51 ± 3.78 2.314 0.251 年龄(岁) 5~14 12 1 15~44 45 66 45~64 39 62 ≥ 65 126 121 17.018 0.001* 原患疾病(例次) 感染性疾病 236 250 心脑血管疾病 228 203 肝肾功能损伤 115 93 其他 165 199 7.355 0.003* 给药日剂量 1.5 g/Qd 14 7 1.5 g/Tid 19 13 3 g/Bid 34 46 3 g/Tid 155 184 6.099 0.106 用药时间(d) 1~5 163 84 6~10 39 86 11~15 20 68 ≥ 16 − 12 79.741 0.000* 住院时间(d) 1~5 8 12 6~10 24 31 11~15 77 105 ≥ 16 113 102 4.917 0.177 *P < 0.05。 2.8 头孢哌酮钠舒巴坦钠不良反应的多因素分析
将表5中差异有统计学意义的变量纳入多因素二分类Logistic回归模型分析,结果显示:肝肾功能损伤患者、用药时间11~15 d为头孢哌酮钠舒巴坦钠发生不良反应的相关因素,OR(95%CI)分别为:2.271(1.004~5.567)、0.236(0.059~0.623),见表6。
表 6 头孢哌酮钠舒巴坦钠不良反应的多因素分析Table 6. Multivariate analysis of adverse reactions of cefoperazone Sodium and Sulbactam Sodium变量 B S.E OR 95% CI Wald χ2 P 常数 1.357 0.664 3.215 − 3.654 0.021* 原患疾病(例次) 感染性疾病 − − 1.000 − 3.392 − 心脑血管疾病 1.549 1.369 6.226 1.141~9.875 3.331 0.157 肝肾功能损伤 3.485 0.535 2.271 1.004~5.567 3.689 0.012* 其他 1.511 1.255 5.412 0.587~10.246 2.021 0.997 用药时间(d) 1~5 − − 1.000 − 5.224 − 6~10 3.698 2.587 1.358 0.487~5.574 2.541 1.568 11~15 2.681 3.523 0.236 0.059~0.623 6.667 0.010* ≥ 16 1.411 1.524 1.968 0.473~2.369 3.569 0.578 *P < 0.05。 2.9 头孢哌酮钠舒巴坦钠不良反应的预测模型和效能评估
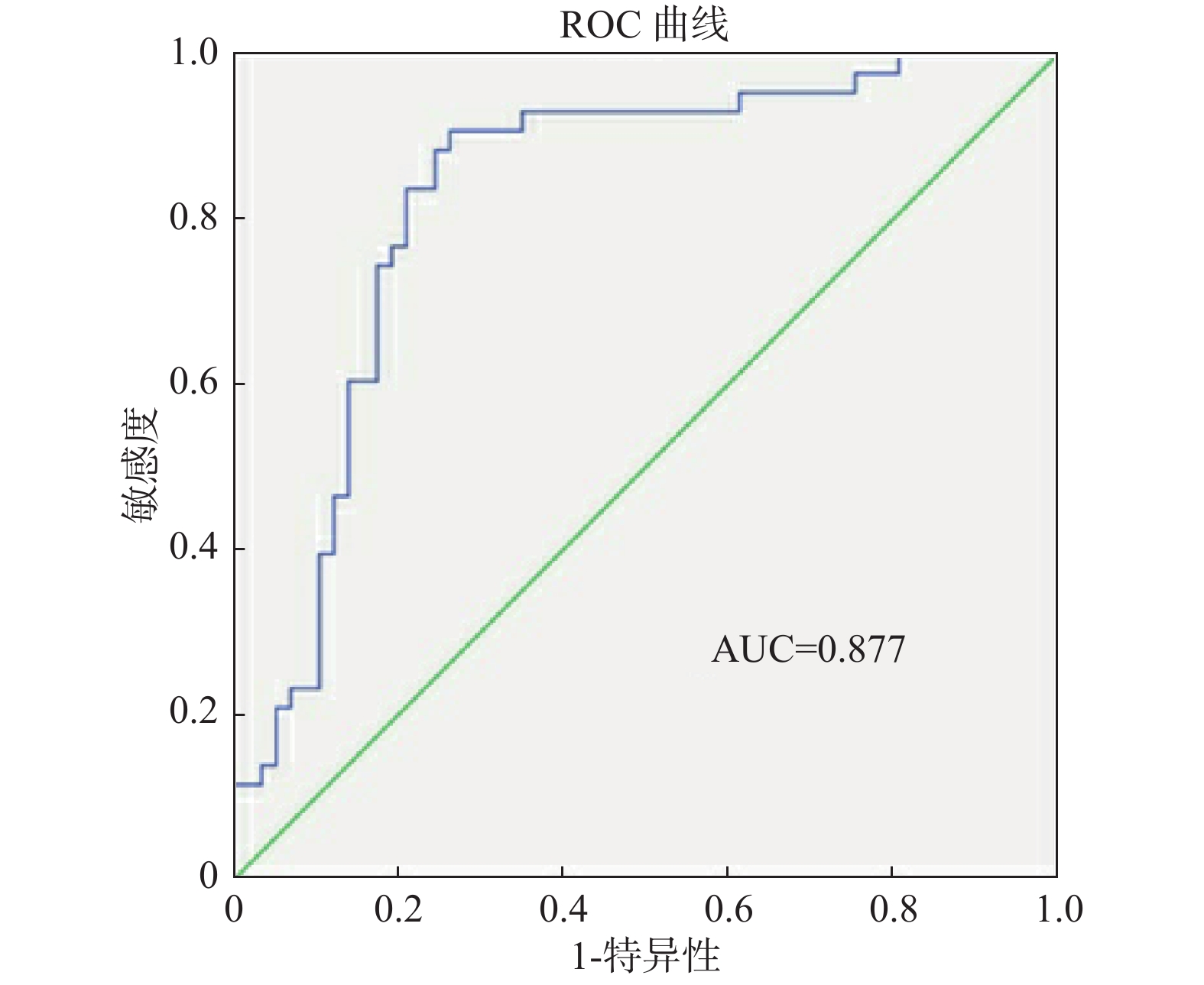
根据多因素二分类Logistic回归模型分析结果,患者使用头孢哌酮钠舒巴坦钠发生不良反应的预测模型为:Logit(P) = 1.357+ 3.485 × 肝肾功能损伤 + 2.681 × 用药天数(11~15),其中P为发生不良反应的概率。ROC曲线分析显示:AUC为0.877(95%CI0.812~0.957,P < 0.001),截断点设置为P = 0.694时,预测模型的灵敏度和特异度分别为91.8%和77.4%,见图1。
3. 讨论
3.1 不良反应与年龄、性别的关系
从222例不良反应的报告中显示,女性患者的比例高于男性患者,且老年患者居多。其原因可能是慢性阻塞性肺疾病和心功能不全患者居多,分别占比28.23%和14.91%,这两类疾病在老年患者中常见,可能与用药机会有关。头孢哌酮的药物动力学变化与肝功能损害程度有关,舒巴坦的药物动力学变化与肾功能减退程度有关。老年患者的肝、肾功能减退,对药品的代谢、排泄功能降低,故药品在体内容易引起蓄积,从而易引发不良反应的发生[2]。222例患者的平均BMI值在成年人的正常范围内18.5~23.99 kg/m2,体重过低或过高而调整给药剂量的情况可排外。
3.2 不良反应与原患疾病和用药原因的关系
头孢哌酮钠舒巴坦钠临床主要应用于治疗下呼吸道感染、腹腔和盆腔感染、泌尿生殖系统感染等。222例患者中主要以下呼吸系统感染为主,占比89.63%,符合头孢哌酮钠舒巴坦钠的适应症。某呼吸内科抗菌药物应用的统计中,头孢哌酮钠舒巴坦钠的用药频度(DDDs)显示最高,原因可能与呼吸内科以老年患者居多,这类患者通常有免疫功能低下,有抗生素暴露史,同时受多种疾病侵袭等因素,可增加致病菌的耐药性,有使用β-内酰胺酶抑制剂复合制剂的条件[3]。但下呼吸系统感染常见的致病菌是肺炎克雷伯菌,肺炎克雷伯菌的耐药率与抗菌药物的使用强度有关[4],因此过度使用β-内酰胺酶抑制剂复合制剂不仅会增加致病菌的耐药率,同时可能增加其不良反应的发生率。在原患疾病中,慢性阻塞性肺疾病伴下呼吸道感染例次占比最高(28.23%),心脑血管疾病包括心功能不全、高血压、糖尿病均占比较高,共占比30.63%,这些可能与老年患者居多有关。有研究显示,老年患者在使用头孢哌酮钠舒巴坦钠时,应尽可能减少与呼吸系统、消化系统药物的联合使用,避免药物之间的配伍禁忌[5]。相关性分析结果也显示,年龄与原患疾病的例次呈正相关关系,即表示年龄越大,原患疾病合并的例次就越多。这与老年患者的基础疾病较多相吻合。多因素分析结果显示,肝肾功能损伤患者为头孢哌酮钠舒巴坦钠发生不良反应的独立危险因素,这与老年患者的特征相符。
3.3 不良反应的临床表现及原因分析
头孢哌酮钠舒巴坦钠所致不良反应可累及多个系统-器官,其说明书中显示最常见的不良反应类型为胃肠道反应。而从表3可见,累及系统-器官以皮肤及附件损害为主,其次为消化系统损害。其中皮肤及附件损害中,以皮肤瘙痒多见,未发生严重过敏反应,可能与所有病例的分级程度均为“一般”有关。相关性分析结果显示,不良反应的临床表现例次与原患疾病例次以及年龄均呈弱相关,说明临床表现的例次不因原患疾病例次的增加和年龄的增长而增多,即不良反应的临床表现具有个体特异性。有两项分别包括1348例和350例头孢菌素类抗菌药物的研究显示,头孢哌酮发生不良反应的占比最高,其累及的系统-器官同样是皮肤及附件损害最多[6-7]。头孢哌酮在生产过程中可能混入杂质、蛋白质和降解产物等,产生抗原性,从而引起过敏反应[8]。β-内酰胺类抗菌药物多数为半合成类抗生素,除青霉素中含有少量青霉噻唑蛋白和多肽外,其他药物多数是因含高聚物而发生过敏反应,而头孢哌酮的聚合速度与药品的含水量和贮存温度有关[9]。因此药品发生不良反应,与贮存条件有一定的关系,头孢哌酮钠舒巴坦钠性状为白色结晶性粉末,具有引湿性,应当在凉暗干燥处贮存。舒巴坦同样会引起皮疹、腹泻、过敏性休克等不良反应[10],他唑巴坦具有青霉烷酸结构,对于青霉素过敏者需禁用。消化系统损害以恶心、呕吐等临床表现为主,长期使用可能引起肠道菌群失调,导致继发感染。血液系统损害中,有22例发生凝血功能障碍,与相关报道一致[11]。其原因可能是头孢哌酮的结构中含有N-甲基硫化四氮唑侧链,可与维生素K竞争性结合,从而干扰维生素K的合成[12]。因此,医护人员用药前应当充分了解患者的家族史、既往史、过敏史、用药史等信息,避免引起青霉素类和头孢菌素类的交叉过敏[13],根据药品说明书进行规范的皮试液配置,并在用药前15 min内减慢滴速,加强用药观察[14]。有个案报道,皮试阴性患者仍然会发生过敏性休克,需在首次使用头孢类抗菌药物0.5~1 h内严密观察,做好急救准备[15]。
3.4 不良反应与用法用量的关系
药物应用时应当遵循药物毒理学、药效动力学和药代动力学规律[16]。注射用头孢哌酮钠舒巴坦钠限定日剂量 ≤ 9 g,因该药为时间依赖型药物,给药频次为Q12 h/Q8 h。222份不良反应报告均未出现超剂量或超频次用药的情况。说明因药物体内蓄积引发不良反应的可能性小。该药的配制要求是先用氯化钠注射液或灭菌注射用水适量5~10 mL溶解后,再加入5%葡萄糖注射液或者0.9%氯化钠注射液150~250 mL静脉滴注使用。有研究显示,注射用头孢哌酮钠舒巴坦钠与5%葡萄糖注射液或者0.9%氯化钠注射液配伍后,在室温条件下放置1 h质量均是稳定的[17]。对于严重肾功能损伤的患者,肌酐清除率 < 30 ml/min时,舒巴坦的剂量不应超过0.5 g/12 h[3]。药品的使用应当正确参照说明书中的规定剂量,避免因剂量过大引起不良反应的发生。
3.5 不良反应与用药时间和住院时间的关系
从表4结果中显示,用药时间在5 d以内占比73.42%,住院时间超过16 d占比50.91%,两者之间呈负相关关系,说明用药短期内发生的不良反应,可能导致住院时间延长。山西省的头孢哌酮钠舒巴坦钠不良反应发生时间在7 d以内占比89%[18],结果与本研究相似,但该研究未纳入住院时间的统计。用药时间与住院时间负相关的原因可能与个体的耐受程度和敏感性有关,耐受程度低、敏感性高的个体早期更容易出现不良反应,同时病情转归的时间长;耐受程度高、敏感性低的个体发生不良反应的时间延迟,病情转归的时间短。用药时间11~15 d作为头孢哌酮钠舒巴坦钠发生不良反应的独立危险因素,也说明了该药物在使用的过程中,仍需长期观察不良反应发生的可能性。
注射用头孢哌酮钠舒巴坦钠是三代头孢菌素头孢哌酮和β-内酰胺酶舒巴坦组成的复方制剂,具有广谱抗菌活性,目前临床应用广泛。舒巴坦对大多数β-内酰胺酶均有较强的抑制作用,抑酶作用优于克拉维酸,能够与头孢哌酮联合发挥较好的协同作用[19]。有研究显示,头孢哌酮钠舒巴坦钠的不良反应发生以女性居多;年龄多在59岁以上;原患疾病以呼吸系统疾病为主;不良反应表现以皮疹为主[20-21],其结果与本研究相似,具有一定代表性。药物警戒是药品上市后及时完善药品信息,提高患者用药安全的重要手段。寻找出药品发生不良反应的相关性因素,才能有效防范不良反应发生,保障患者用药安全。目前关于避免药物不良反应发生的方法学研究较少,有学者认为,根据单体西药的四气、五味、归经属性,利用中医辨证思维可提高疗效,减少药物不良反应的发生,对抗菌药物进行寒、热药性的初步评价,可提高个体化治疗的疗效和安全性[22]。可见,目前不良反应的防范工作已从依赖医疗机构的主动上报,采取回顾性分析评价,转换到了避免不良反应发生的主动预测。这就需要更多的样本数据支持因素分析,寻找因素之间的相关性,为预防药物不良反应发生的模型搭建提供数据基础。
-
表 1 头孢哌酮钠舒巴坦钠不良反应报告患者的性别与年龄分布(n)
Table 1. Gender and age distribution of patients with adverse reactions of cefoperazone sodium and sulbactam sodium (n)
年龄(岁) 男 女 总例数 构成比(%) 5~14 4 8 12 5.40 15~44 20 25 45 20.27 45~64 23 16 39 17.57 ≥ 65 40 86 126 56.76 合计 87 135 222 100.00 注:《国际疾病分类》(ICD-10)编码分类:婴儿期为不足1岁,幼儿期为1~4岁,少儿期为5~14岁,青壮年期为15~44岁,中年期为45~64岁,老年期为65岁及以上。 表 2 头孢哌酮钠舒巴坦钠不良反应报告患者的原患疾病
Table 2. Primary diseases of ADR patients caused by cefoperazone sodium and sulbactam sodium
序号 原患疾病 n 构成比(%) 1 慢性阻塞性肺疾病伴
急性下呼吸道感染210 28.23 2 心功能不全 111 14.91 3 肝损伤 74 9.95 4 高血压 71 9.54 5 糖尿病 46 6.18 6 腰椎退行性病变 50 6.72 7 肺结核 43 5.78 8 肾损伤 41 5.52 9 脑膜炎 33 4.43 10 前列腺增生 24 3.23 11 腹腔感染 26 3.49 12 胃炎 15 2.02 表 3 头孢哌酮钠舒巴坦钠不良反应报告累及系统-器官分布及临床表现(n)
Table 3. The adverse reaction report of cefoperazone sodium and sulbactam sodium involves system-organ distribution and clinical manifestations(n)
累及系统-器官 临床表现 例次 合计 构成比(%) 皮肤及附件损害 瘙痒
红斑疹
局部肿胀
皮肤发红
口唇发绀154
3
26
27
29239 50.53 血液系统损害 凝血功能障碍
白细胞减少17
421 4.44 呼吸系统损害 呼吸困难 65 65 13.74 全身性损害 发热
畏寒31
1546 9.73 消化系统损害 恶心
呕吐53
49102 21.56 表 4 头孢哌酮钠舒巴坦钠不良反应报告患者的用药时间和住院时间
Table 4. Adverse reactions of cefoperazone sodium and sulbactam sodium are reported on the duration of medication and hospital stay in patients
天数
(d)用药时间
(n)构成比
(%)住院时间/
例数(n)构成比
(%)1~5 163 73.42 8 3.60 6~10 39 17.57 24 10.81 11~15 20 9.01 77 34.68 ≥ 16 − − 113 50.91 合计 222 100.00 222 100.00 表 5 头孢哌酮钠舒巴坦钠不良反应的单因素分析
Table 5. Single factor analysis of adverse reactions of cefoperazone sodium and sulbactam sodium
研究因素 观察组(n = 222) 对照组(n = 250) χ2/t P 性别 男 87 131 女 135 119 8.256 0.004* 婚姻 已婚 199 230 未婚 23 20 0.791 0.373 BMI(kg/m2) 21.21 ± 1.56 22.51 ± 3.78 2.314 0.251 年龄(岁) 5~14 12 1 15~44 45 66 45~64 39 62 ≥ 65 126 121 17.018 0.001* 原患疾病(例次) 感染性疾病 236 250 心脑血管疾病 228 203 肝肾功能损伤 115 93 其他 165 199 7.355 0.003* 给药日剂量 1.5 g/Qd 14 7 1.5 g/Tid 19 13 3 g/Bid 34 46 3 g/Tid 155 184 6.099 0.106 用药时间(d) 1~5 163 84 6~10 39 86 11~15 20 68 ≥ 16 − 12 79.741 0.000* 住院时间(d) 1~5 8 12 6~10 24 31 11~15 77 105 ≥ 16 113 102 4.917 0.177 *P < 0.05。 表 6 头孢哌酮钠舒巴坦钠不良反应的多因素分析
Table 6. Multivariate analysis of adverse reactions of cefoperazone Sodium and Sulbactam Sodium
变量 B S.E OR 95% CI Wald χ2 P 常数 1.357 0.664 3.215 − 3.654 0.021* 原患疾病(例次) 感染性疾病 − − 1.000 − 3.392 − 心脑血管疾病 1.549 1.369 6.226 1.141~9.875 3.331 0.157 肝肾功能损伤 3.485 0.535 2.271 1.004~5.567 3.689 0.012* 其他 1.511 1.255 5.412 0.587~10.246 2.021 0.997 用药时间(d) 1~5 − − 1.000 − 5.224 − 6~10 3.698 2.587 1.358 0.487~5.574 2.541 1.568 11~15 2.681 3.523 0.236 0.059~0.623 6.667 0.010* ≥ 16 1.411 1.524 1.968 0.473~2.369 3.569 0.578 *P < 0.05。 -
[1] 金晶,李青,冷光. 头孢哌酮/他唑巴坦不良反应风险因素分析[J]. 药物流行病学杂志,2016,25(6):346-349. [2] 刘宪军,付娜. 109例头孢哌酮钠舒巴坦钠不良反应报告分析[J]. 中国药物警戒,2014,11(6):355-357. [3] 胡新春,邓超英. 呼吸内科抗菌药物的临床应用与分析研究[J]. 国际呼吸杂志,2015,35(21):1617-1619. doi: 10.3760/cma.j.issn.1673-436X.2015.21.004 [4] 陈菲,王璐,王静. 肺炎克雷伯菌耐药与抗菌药物使用强度现况及其关联分析[J]. 蚌埠医学院学报,2019,44(8):1091-1096. [5] 程英,段菲,权晨. 注射用头孢哌酮钠他唑巴坦钠配伍禁忌临床分析[J]. 中国药业,2019,28(3):73-75. doi: 10.3969/j.issn.1006-4931.2019.03.024 [6] 栗啸阳,郭代红,刘思源,等. 13458例头孢菌素类药品不良反应报告分析[J]. 药物流行病学杂志,2020,29(3):166-169. [7] 张士洋,程军,陈志武. 350例头孢菌素类抗生素不良反应报告分析[J]. 安徽医药,2011,15(4):516-518. doi: 10.3969/j.issn.1009-6469.2011.04.053 [8] 何云开,刘产明,曾晓辉. 头孢哌酮钠/舒巴坦钠致喉头水肿及过敏性休克各1例[J]. 江苏药学与临床研究,2004,12(S1):76-76. [9] 王全一,李彦博,傅蓉. 高效凝胶色谱法测定注射用头孢哌酮钠他唑巴坦钠中的高聚物[J]. 中国药业,2013,22(12):83-84. doi: 10.3969/j.issn.1006-4931.2013.12.053 [10] 钟雪,刘田,冯婉玉. 他唑巴坦致过敏反应案例报道及文献复习[J]. 中国新药杂志,2019,28(14):1784-1788. doi: 10.3969/j.issn.1003-3734.2019.14.020 [11] 石姗平,吴雪,农杰昌,等. 头孢哌酮/舒巴坦致凝血功能异常的影响因素分析[J]. 药物流行病学杂志,2019,28(9):578-580. [12] 庞立峰. 注射用头孢哌酮钠舒巴坦钠致凝血功能异常1例[J]. 中国药物警戒,2018,15(5):62-63. [13] 田艳平,朱燕,尹红,等. 46例注射用头孢哌酮/舒巴坦致过敏性休克分析[J]. 中国药物警戒,2010,7(4):246-248. doi: 10.3969/j.issn.1672-8629.2010.04.019 [14] 代蓉,邹玲,赵丽,李晓华,等. 1例头孢哌酮钠他唑巴坦钠过敏性休克病人的急救护理[J]. 护理研究,2015,29(23):2939-2939. doi: 10.3969/j.issn.1009-6493.2015.23.057 [15] 宋明辉,张建伟,张荣厚. 注射用头孢哌酮钠他唑巴坦钠静脉滴注致过敏性休克1例[J]. 海峡药学,2020,32(1):210-211. doi: 10.3969/j.issn.1006-3765.2020.01.090 [16] 施毅,李培. 根据药代动力学/药效动力学理论合理使用氨基糖苷类抗生素[J]. 中华结核和呼吸杂志,2012,35(10):726-728. doi: 10.3760/cma.j.issn.1001-0939.2012.10.004 [17] 马亚松,李敏,贾玉捷,孙燕,杨宏硕. 注射用头孢哌酮钠他唑巴坦钠与输液配伍稳定性研究[J]. 化工管理,2020,10(4):95-96. doi: 10.3969/j.issn.1008-4800.2020.04.061 [18] 金晶,李青,冷光. 山西省头孢哌酮钠他唑巴坦钠不良反应报告分析[J]. 山西医药杂志,2016,45(10):1159-1161. [19] 张扣兴,唐英春,毕筱刚,等. 头孢哌酮钠/他唑巴坦钠体外抗菌活性和影响因素[J]. 中国临床药理学杂志,2001,17(3):195-198. doi: 10.3969/j.issn.1001-6821.2001.03.010 [20] 朱芸. 浅析静脉滴注头孢哌酮/他唑巴坦所致不良反应的特点[J]. 健康必读,2019(23):16-17. [21] 范晓. 浅析静脉滴注头孢哌酮/他唑巴坦所致不良反应的特点[J]. 当代医药论丛,2017,15(3):8-9. doi: 10.3969/j.issn.2095-7629.2017.03.006 [22] 张楠,郭晓昕,贾海忠. 避免药物不良反应发生的方法学研究进展[J]. 中国药物警戒,2020,17(1):56-62. -






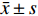
 下载:
下载:
 下载:
下载:

