Signal Analysis of Niraparib-Related Adverse Events Based on US FAERS Database
-
摘要:
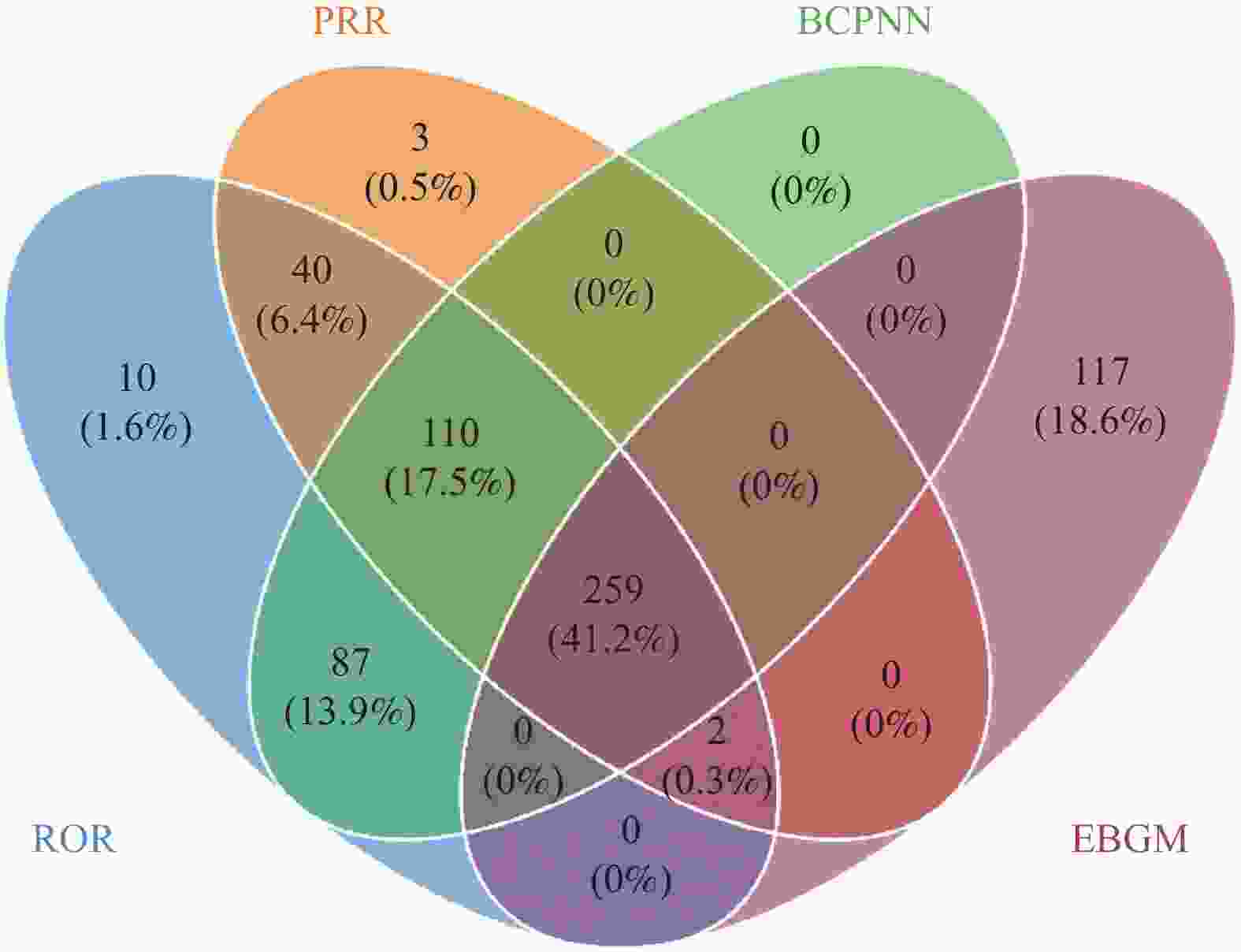
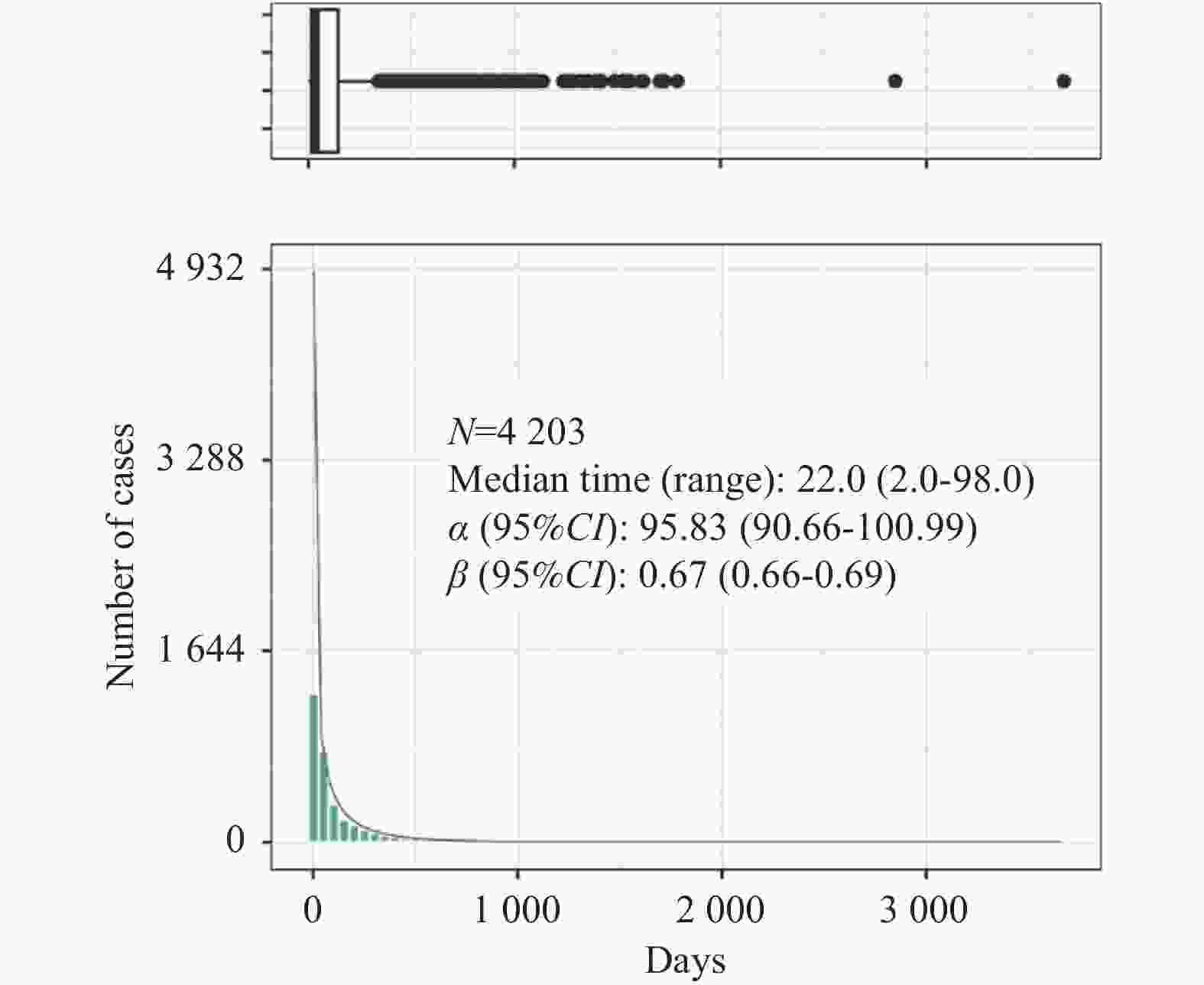
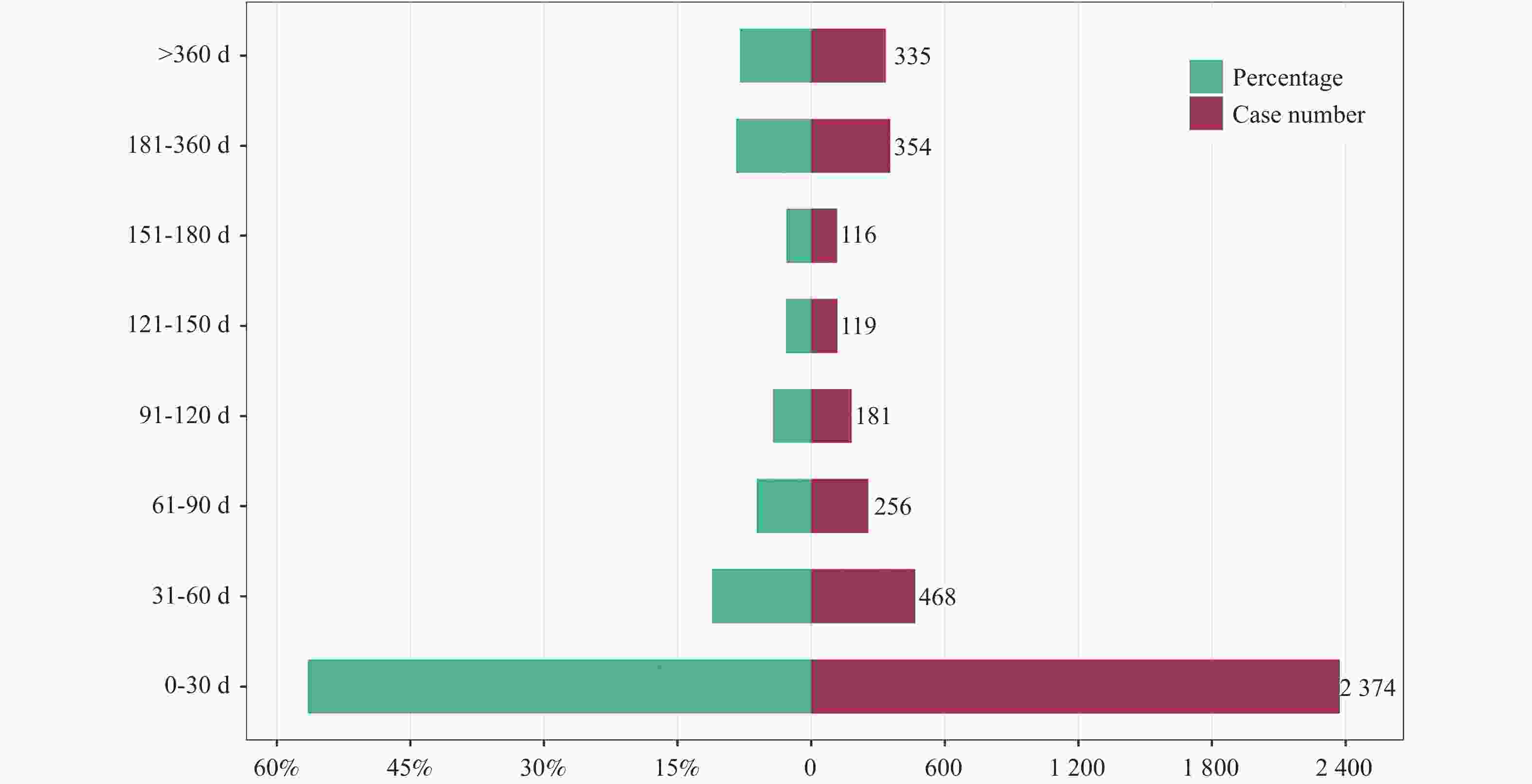
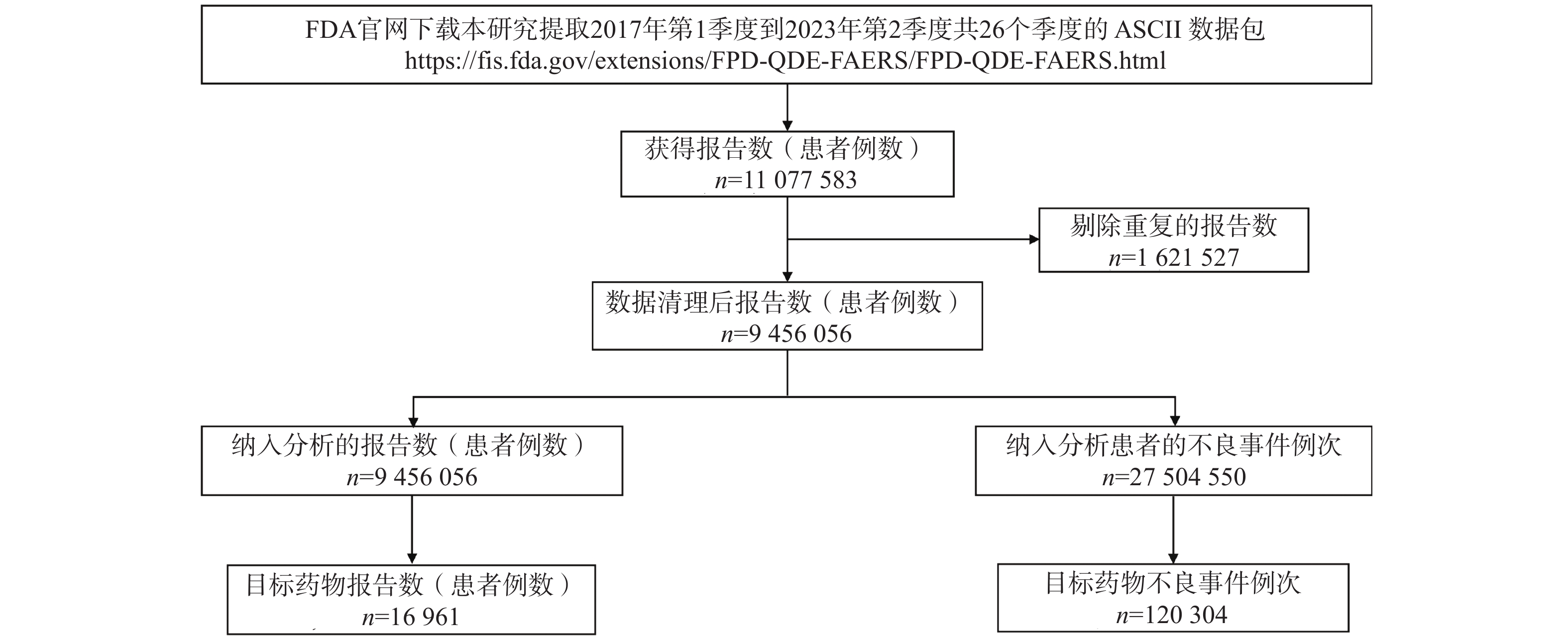
目的 挖掘尼拉帕利的风险信号,为临床安全合理用药提供参考。 方法 提取美国FDA 不良事件报告系统( FAERS)数据库中2017年第 1季度至 2023 年第 2季度的尼拉帕利相关不良事件(ADE)报告。采用报告比值比法(ROR)、比例报告比值法(PRR)、贝叶斯可信区间递进神经网络法(BCPNN)和多项式伽马泊松分布缩减法(MGPS)对风险信号进行挖掘,利用监管活动医学词典(MedDRA)26.1中的首选系统器官分类(SOC)和首选术语(PT)对风险信号进行描述和分类,并对尼拉帕利ADE的发生时间进行分析。 结果 提取以尼拉帕利为首要怀疑药物的 ADE报告16 961例。通过筛选分析,共得到 32 个PTs,涉及 11个 SOCs,与药品说明书记载基本一致。说明书未提及的周围神经病、红细胞计数下降、红细胞压积降低、脱水、潮热等可疑信号需给予关注。中位发生时间为22 d (IQR 2~98 d),韦伯分布检验提示早期失败型曲线。 结论 在使用尼拉帕利时,尤其是在治疗初期,除关注血小板计数下降、恶心、疲劳等药品说明书提及的ADE 外,还应密切关注周围神经病、红细胞计数下降等说明书中未收录但信号值较强的ADE,以保障患者的用药安全。 Abstract:Objective To explore the risk signals of niraparib and provide references for rational and safe clinical medication. Methods Niraparib-related adverse drug events (ADEs) reports from Q1 2017 to Q2 2023 were extracted from the US FDA Adverse Event Reporting System (FAERS) database. Risk signals were identified using the reporting odds ratio (ROR), proportional reporting ratio (PRR), Bayesian confidence propagation neural network (BCPNN), and multi-item gamma Poisson shrinker (MGPS) methods. The Risk signals were described and classified by preferred system organ classes (SOCs) and preferred terms (PTs) from the Medical Dictionary for Regulatory Activities (MedDRA) version 26.1, and the occurrence of niraparib-related ADEs was also analyzed. Results A total of 16,961 ADE reports with niraparib as the primary suspected drug were extracted. Through screening and analysis, 32 PTs were identified involving 11 SOCs, which were largely consistent with the information in the drug label. However, suspicious signals not mentioned in the label, including neuropathy peripheral, decreased red blood cell count, reduced hematocrit, dehydration, and hot flashes, require further attention.The median occurrence time was 22 days (IQR 2-98 days), and the Weibull distribution test indicated an early failure-type curve. Conclusion When using niraparib, particularly in early stages of treatment, it is essential to monitor not only the ADEs mentioned in the drug instructions, such as decreased platelet count, nausea and fatigue, but also to pay close attention to the ADEs not included in the instructions, such as peripheral neuropathy and decreased red blood cell count, which exhibit strong signal values, to ensure patient medication safety. -
表 1 尼拉帕利不良事件报告的基本情况
Table 1. Basic information on adverse event reports for niraparib
项目 分类 报告数(n) 占比(%) 性别 男性 224 1.32 女性 11119 65.56 数据缺失 5618 33.12 年龄(岁) <18 6 0.04 18~44 193 1.14 45~64 2334 13.76 64~74 1717 10.12 ≥75 1040 6.13 数据缺失 11671 68.81 上报国家 美国 13963 82.32 日本 966 5.70 加拿大 502 2.96 其他国家 1530 9.02 上报者 消费者 11643 68.65 医师 3194 18.83 药师 1421 8.38 其他健康专业人员 444 2.62 未知 259 1.52 上报年份(年) 2017 931 5.49 2018 3168 18.68 2019 1376 8.11 2020 2321 13.68 2021 2973 17.53 2022 3831 22.59 2023 2361 13.92 适应症 卵巢癌 12296 72.50 输卵管癌 810 4.78 腹膜癌 737 4.34 其他癌或未知 3118 18.38 严重 ADE 住院或延长住院 3945 23.26 死亡 1089 6.42 危及生命 762 4.49 残疾 42 0.25 表 2 尼拉帕利相关报告在SOC层级的信号值
Table 2. Signal values of reports related to niraparib at the SOC level
SOC 例次 ROR(95%CI) PRR(χ2) IC(IC025) EBGM
(EBGM05)各类检查 21531 3.56 (3.51-3.61)* 3.10 ( 32134.13 )*1.62 (1.60)* 3.07 (3.03)* 胃肠系统疾病 19614 2.21 (2.17-2.24)* 2.01 ( 10724.16 )*1.00 (0.98)* 2.00 (1.97) 全身性疾病及给药部位各种反应 17539 0.80 (0.78-0.81) 0.83 (768.56) −0.27 (−0.30) 0.83 (0.81) 各类损伤、中毒及操作并发症 8995 0.61 (0.60-0.62) 0.64 ( 2061.92 )−0.64 (−0.67) 0.64 (0.63) 各类神经系统疾病 8603 0.92 (0.90-0.94) 0.93 (50.83) −0.11 (−0.14) 0.93 (0.91) 精神病类疾病 6406 0.99 (0.96-1.01) 0.99 (0.67) −0.01 (−0.05) 0.99 (0.97) 各种肌肉骨骼及结缔组织疾病 5321 0.87 (0.85-0.89) 0.88 (97.66) −0.19 (−0.23) 0.88 (0.85) 呼吸系统、胸及纵隔疾病 4716 0.86 (0.83-0.88) 0.86 (108.76) −0.21 (−0.26) 0.86 (0.84) 皮肤及皮下组织类疾病 3926 0.54 (0.52-0.56) 0.55 ( 1504.81 )−0.85 (−0.90) 0.55 (0.54) 良性、恶性及性质不明的肿瘤 3916 0.94 (0.91-0.97) 0.94 (15.36) −0.09 (−0.14) 0.94 (0.91) 感染及侵染类疾病 3238 0.48 (0.47-0.50) 0.50 ( 1743.50 )−1.01 (−1.06) 0.50 (0.48) 血液及淋巴系统疾病 3053 1.56 (1.51-1.62)* 1.55 (601.82) 0.63 (0.58)* 1.55 (1.49) 代谢及营养类疾病 2871 1.19 (1.15-1.24)* 1.19 (88.51) 0.25 (0.20)* 1.19 (1.15) 血管与淋巴管类疾病 2544 1.11 (1.07-1.15)* 1.11 (26.84) 0.15 (0.09)* 1.11 (1.06) 各种手术及医疗操作 2113 1.29 (1.23-1.35)* 1.28 (133.80) 0.36 (0.30)* 1.28 (1.23) 肾脏及泌尿系统疾病 1627 0.65 (0.62-0.68) 0.65 (308.46) −0.62 (−0.69) 0.65 (0.62) 心脏器官疾病 1290 0.51 (0.49-0.54) 0.52 (590.12) −0.95 (−1.03) 0.52 (0.49) 眼器官疾病 981 0.42 (0.39-0.45) 0.42 (779.89) −1.23 (−1.32) 0.43 (0.40) 社会环境 403 0.73 (0.66-0.81) 0.73 (38.86) −0.44 (−0.59) 0.73 (0.67) 免疫系统疾病 362 0.24 (0.22-0.27) 0.25 (847.53) −2.02 (−2.17) 0.25 (0.22) 肝胆系统疾病 330 0.33 (0.30-0.37) 0.33 (438.81) −1.57 (−1.73) 0.34 (0.30) 耳及迷路类疾病 328 0.63 (0.56-0.70) 0.63 (72.13) −0.67 (−0.83) 0.63 (0.56) 生殖系统及乳腺疾病 301 0.33 (0.30-0.37) 0.34 (398.23) −1.57 (−1.73) 0.34 (0.30) 内分泌系统疾病 141 0.45 (0.38-0.53) 0.45 (94.75) −1.14 (−1.38) 0.45 (0.38) 产品问题 117 0.05 (0.05-0.07) 0.06 ( 1908.94 )−4.15 (−4.42) 0.06 (0.05) 各种先天性家族性遗传性疾病 33 0.10 (0.07-0.14) 0.10 (261.10) −3.25 (−3.74) 0.10 (0.07) 妊娠期、产褥期及围产期状况 5 0.01 (0.00-0.03) 0.01 (462.55) −6.29 (−7.47) 0.01 (0.00) 注:*表示算法中具有统计学显著信号。 -
[1] Maiorano M F P,Maiorano B A,Biancofiore A,et al. Niraparib and advanced ovarian cancer: A beacon in the non-BRCA mutated setting[J]. Pharmaceuticals (Basel),2023,16(9):1261. doi: 10.3390/ph16091261 [2] Scott L J. Niraparib: First global approval[J]. Drugs,2017,77(9):1029-1034. doi: 10.1007/s40265-017-0752-y [3] Del Campo J M,Matulonis U A,Malander S,et al. Niraparib maintenance therapy in patients with recurrent ovarian cancer after a partial response to the last platinum-based chemotherapy in the ENGOT-OV16/NOVA trial[J]. J Clin Oncol,2019,37(32):2968-2973. doi: 10.1200/JCO.18.02238 [4] González-Martín A,Pothuri B,Vergote I,et al. Niraparib in patients with newly diagnosed advanced ovarian cancer[J]. N Engl J Med.,2019,381(25):2391-2402. doi: 10.1056/NEJMoa1910962 [5] 英国警示尼拉帕利的严重高血压及可逆性后部脑病综合征风险[J]. 中国药物价,2021,38(2): 152. [6] Smith M R,Scher H I,Sandhu S,et al. Niraparib in patients with metastatic castration-resistant prostate cancer and DNA repair gene defects (GALAHAD): A multicentre,open-label,phase 2 trial[J]. Lancet Oncol,2022,23(3):362-373. doi: 10.1016/S1470-2045(21)00757-9 [7] Jiang Y,Zhou L,Shen Y,et al. Safety assessment of brexpiprazole: Real-world adverse event analysis from the FAERS database[J]. J Affect Disord,2024,346:223-229. doi: 10.1016/j.jad.2023.11.025 [8] Mao X,Zhang R,Liang X,et al. A pharmacovigilance study of FDA adverse events for sugammadex[J]. J Clin Anesth,2024,97:111509. doi: 10.1016/j.jclinane.2024.111509 [9] 苏小涵,曾姣,李雪,等. 基于美国FAERS数据库的乳腺癌患者使用阿贝西利不良事件分析[J]. 中国药物警戒,2024,21(5):580-586. [10] 孔北华,刘继红,黄鹤,等. 卵巢癌 PARP 抑制剂临床应用指南(2022版)[J]. 现代妇产科进展,2022,31(8):561-572. [11] Hirschl N,Leveque W,Granitto J,et al. PARP inhibitors: Strategic use and optimal management in ovarian cancer[J]. Cancers (Basel),2024,16(5):932. doi: 10.3390/cancers16050932 [12] Wu X H,Zhu J Q,Yin R T,et al. Niraparib maintenance therapy in patients with platinum-sensitive recurrent ovarian cancer using an individualized starting dose (NORA): A randomized,double-blind,placebo-controlled phase III trial[J]. Ann Oncol,2021,32(4):512-521. doi: 10.1016/j.annonc.2020.12.018 [13] Li N,Zhu J,Yin R,et al. Efficacy and safety of niraparib as maintenance treatment in patients with newly diagnosed advanced ovarian cancer using an individualized starting dose (PRIME Study): A randomized,double-blind,placebo-controlled,phase 3 trial (LBA 5)[J]. Gynecologic Oncology,2022,166:S50-S51. [14] Liu J F,Gaillard S,Wahner Hendrickson A E,et al. Niraparib,dostarlimab,and bevacizumab as combination therapy in pretreated,advanced platinum-resistant ovarian cancer: Findings from cohort A of the OPAL phase II trial[J]. JCO Precis Oncol,2024,8:e2300693. [15] Reiss K A,Mick R,Teitelbaum U,et al. Niraparib plus nivolumab or niraparib plus ipilimumab in patients with platinum-sensitive advanced pancreatic cancer: A randomised,phase 1b/2 trial[J]. Lancet Oncol,2022,23(10):e446. [16] 国家卫生健康委员会办公厅.卵巢癌诊疗指南(2022年版)[EB/OL]. (2022-04-11)[2024-09-02]. http://www.nhc.gov.cn/yzygj/s7659/202204/a0e67177df1f439898683e1333957c74.shtml [17] Zhao M,Qiu S,Wu X,et al. Efficacy and safety of niraparib as first-line maintenance treatment for patients with advanced ovarian cancer: Real-world data from a multicenter study in China[J]. Target Oncol,2023,18(6):869-883. doi: 10.1007/s11523-023-00999-x [18] 刘畅浩,林少丹,林仲秋. 《PARP抑制剂在卵巢癌中的应用: ASCO指南》解读[J]. 中国实用妇科与产科杂志,2020,36(9):835-839. [19] Berek J S,Matulonis U A,Peen U,et al. Safety and dose modification for patients receiving niraparib[J]. Ann Oncol,2019,30(5):859. doi: 10.1093/annonc/mdy255 [20] Jesus M,Cabral A,Monteiro C,et al. Peripheral neuropathy potentially associated to poly (ADP-ribose) polymerase inhibitors: An analysis of the Eudravigilance database[J]. Curr Oncol,2023,30(7):6533-6545. doi: 10.3390/curroncol30070479 [21] Tian X,Chen L,Gai D,et al. Adverse event profiles of PARP inhibitors: Analysis of spontaneous reports submitted to FAERS[J]. Front Pharmacol,2022,13:851246. doi: 10.3389/fphar.2022.851246 [22] Balko R A,Hendrickson A W,Grudem M E,et al. Can poly (ADP-ribose) polymerase inhibitors palliate paclitaxel-induced peripheral neuropathy in patients with cancer?[J]. Am J Hosp Palliat Care,2019,36(1):72-75. doi: 10.1177/1049909118786958 [23] Farr é s J,Llacuna L,Martin-Caballero J,et al. PARP-2 sustains erythropoiesis in mice by limiting replicative stress in erythroid progenitors[J]. Cell Death Differ,2015,22(7):1144-1157. doi: 10.1038/cdd.2014.202 -






 下载:
下载: