Exploring the Efficacy of Different Mathematical Models with Multi-b Value DWI in Predicting Lymphatic Vascular Invasion of Endometrial Cancer
-
摘要:
目的 评估不同数学模型多b值扩散加权成像(diffusion-weighted imaging,DWI)在预测子宫内膜癌(endometrial cancer,EC)淋巴血管侵犯(lymphovascular space invasion,LVSI)中的能力。 方法 收集2019年9月至2021年5月期间接受多b值DWI盆腔磁共振成像(magnetic resonance imaging,MRI)检查的患者61例。测量并比较表观扩散系数(apparent-diffusion-coefficient,ADC)、双指数模型参数(D、D*和f)和拉伸指数模型参数(DDC和α),分析经病理证实的预后相关危险因素:组织学分级和淋巴血管侵犯(lymphovascular space invasion,LVSI)。进行受试者工作特征曲线评估不同模型参数在预测EC肿瘤分级和LVSI中的诊断性能。通过多元Logistic回归模型确定EC肿瘤分级和LVSI相关DWI模型参数。使用组内相关系数(ICC)评估观察者间一致性。 结果 高级别组的ADC、D、f和DDC显著低于低级别组(AUC:0.699~0.882,P < 0.05)。与没有LVSI的肿瘤相比,有LVSI肿瘤的ADC、D*、f和DDC值显著降低(AUC:0.671~0.759,P < 0.05)。联合f和DDC在区分高级别和LVSI肿瘤方面具有最大AUC(0.895、0.797)。多元Logistic回归分析显示,f和DDC均可作为肿瘤分级和LVSI独立相关的预测因子。ICC分析显示,D(ICC = 0.973;95%CI = 0.956~0.985)、D*(ICC = 0.911;95%CI = 0.851~0.946)、ADC(ICC = 0.968;95%CI = 0.947~0.980)、f(ICC = 0.957;95%CI = 0.922~0.974)、DDC(ICC = 0.947;95 %CI = 0.912~0.968)和α值(ICC = 0.931;95%CI = 0.884~0.958)的观察者间一致性非常好。 结论 不同数学模型多b值DWI是一种有用且无创的方法,可用于预测EC预后相关的高组织学分级和LVSI,具有更全面的生物学信息。 Abstract:Objective To evaluate the efficacy of different mathematical models of multi-b-value DWI in predicting lymphatic vascular invasion (LVSI) of endometrial cancer (EC). Methods The study population comprised 61 women who underwent multi-b-value DWI pelvic MRI between September 2019 and May 2021. The apparent-diffusion-coefficient (ADC), bi-exponential model parameters (D, D* and f) and stretched-exponential model parameters (DDC and α) were measured and compared to analyze the following prognosis-related risk factors confirmed by pathology: histological grade and LVSI. The receiver operating characteristic (ROC) curve was performed to evaluate the diagnostic performance of these parameters in predicting EC histological grade and LVSI. The EC histological grade and LVSI related DWI model parameters were determined by multiple logistic regression model. The intra-group correlation coefficient (ICC) was used to assess the inter-observer agreement. Results The ADC, D, f, and DDC of the high histological grade group were significantly lower than those of the low histological grade group (P < 0.05, AUC: 0.699-0.882). Compared with tumors without LVSI, tumors with LVSI had significantly lower ADC, D*, f and DDC values ( P < 0.05, AUC: 0.671-0.759). The combination of f and DDC showed higher AUC (0.895, 0.797) than a single parameter in distinguishing high histological grade and LVSI tumors. Multivariate logistic regression analysis showed that both f and DDC can be used as independent predictors of histological grade and LVSI. ICC analysis showed that the inter-observer agreement for the D (ICC = 0.973; 95%CI = 0.956-0.985), D* (ICC = 0.911; 95%CI = 0.851-0.946), ADC (ICC = 0.968; 95%CI = 0.947-0.980), f (ICC = 0.957; 95%CI = 0.922-0.974), DDC (ICC = 0.947; 95%CI = 0.912−0.968) and α value (ICC = 0.931; 95%CI = 0.884-0.958) were very good. Conclusions Multi-b value DWI with different mathematical models is a useful and noninvasive approach for prediction of prognosis-related risk factors in EC with more comprehensive biological information. -
高血压是目前临床上最常见的慢性心脑血管疾病之一,进展性心室重塑是其发生心力衰竭,是心脏猝死的核心病理生理过程。交感神经兴奋与高血压间相互促进,近年来经导管去肾动脉交感神经技术作为治疗顽固性高血压的重要手段的应用价值受到挑战[1-3],考虑经导管消融无法从血管内膜彻底毁损肾动脉壁层交感神经纤维,从而难于达到阻断过度激活的交感神经传入和传出从而影响肾交感神经持续兴奋[4-5]。那是否彻底毁损肾动脉神经后可达到改善血压并阻止组织重塑发展呢?本动物实验通过外科方法建立去肾动脉交感神经大鼠模型,观察术后高血压大鼠心脏重塑相关指标及影响因子的变化,旨在评价去肾动脉交感神经术对SHR急性期心室重塑的影响。
1. 资料与方法
1.1 研究对象
本实验研究对象采用的是北京维通利华公司提供雄性12周龄自发性高血压大鼠(SHR)50只,平均体重(265±12) g,随机分为左侧肾动脉神经干预组(L组10只),右侧肾动脉神经干预组(R组10只),双侧肾动脉神经干预组(D组10只),假手术组(S组10只),空白对照组(B组10只)。采用昆明医科大学实验动物学部提供的雄性12周龄普通WKY大鼠5只,平均体重(245±28) g,作为阴性对照组(F组)。所有大鼠饲养于SPF级动物实验室。
1.2 方法
1.2.1 大鼠无创血压及血浆RAAS因子测量
采用北京软隆生物技术有限公司提供BP-2010无创鼠尾血压计于术前,术后1周、2周、3周、4周、5周、6周测量每只大鼠血压,心率。同期抽血采用Elisa法测血浆血浆PRA、Ang II、ALD 等RAAS相关因子水平等。
1.2.2 大鼠肾动脉去神经模型构建[6]
各组大鼠于手术前完善术前准备。术前用10%水合氯醛0.03~0.05 mL/kg进行腹腔注射麻醉。仰卧位固定大鼠后,腹部备皮,碘伏消毒,行腹正中切口,暴露双侧肾的肾动脉,游离肾动脉并剥除其周围组织及留取标本,再以无菌棉球蘸取10%苯酚酒精溶液分别按分组准确擦拭左侧或右侧或双侧肾动脉游离端。复位内脏,青霉素冲洗腹腔后关闭腹腔。假手术组大鼠同样方法麻醉、开腹,暴露双侧肾的肾动脉后,将内脏复位。置于温箱中麻醉复苏,清醒后置笼喂养。术后1周内每天注射80万 U青霉素预防感染。
1.2.3 大鼠HW/BW(心脏体重质量比)值测算及大鼠心肌厚度测量
饲养6周后用10%水合氯醛麻醉所有大鼠,仰卧位固定,开胸、腹,取大鼠心脏组织,生理盐水冲洗心脏各腔室残留血液,用滤纸吸干表面,剥除多余的结缔组织后置于分析天平上称重,计算心脏重量与大鼠体重比值HW/BW。将取下的大鼠心脏沿冠状面剖开暴露心房、心室最大面,取游标卡尺量取各样本心尖部心肌组织厚度,并记录。
1.2.4 心脏、肾脏组织RAAS相关因子检测
取心室肌组织用于行western blot法检测ACE、AngⅠ、AngⅡ、ALD含量相对值进行比较分析,同时与心肌厚度行相关性分析。取处理侧肾脏实质组织以免疫组化方法定性检测AngⅠ、AngⅡ及NA(去甲肾上腺素)表达水平。
1.2.5 肾动脉周围剥离组织及肾动脉干病理检测
将处理组实验大鼠肾动脉周围剥离组织及肾动脉干进行染色并光镜下观察肾动脉周围神经留存情况。
1.2.6 大鼠心肌HE及Masson染色
将大鼠心脏标本按组织病检切片及染色要求处理。HE染色后光学显微镜观察心肌形态学及组织学改变,心肌细胞排列顺序及间质纤维组织增生情况,并拍照。
1.3 统计学处理
采用SPSS软件进行统计分析,计量资料以
${{\bar x}} \pm {{s}}$ 表示,各组间差异用方差分析比较,相关分析采用PEARSON线性相关分析,P < 0.05为差异有统计学意义。2. 结果
2.1 实验动物基础状态及围术期血压变化情况
手术处理组实验大鼠均成功完成模型构建23只,术中肾动脉撕裂急性失血死亡围手术期因5只,围手术期死亡2只,模型构建成功率77%,其余各组实验动物均成活至6周观察期,见表1。SHR不同分组围术期收缩压及舒张压等血压值的变化呈现术后明显降低,又逐渐恢复,至第六周时又恢复到基线水平的趋势变化,见图1。
表 1 基础各实验组大鼠体重、心率比较(${{\bar x}} \pm {{s}}$ )Table 1. Baseline parameters of differential rat groups($\bar x\pm s $ )组别 n 体重(g) 心率(次/min) 阴性对照组 5 282.40 ± 9.84 422.40 ± 39.70 空白对照组组 10 284.90 ± 15.91 424.30 ± 56.98 假手术组组 10 282.90 ± 15.57 421.60 ± 79.95 手术处理组 30 281.20 ± 15.40 423.43 ± 36.15 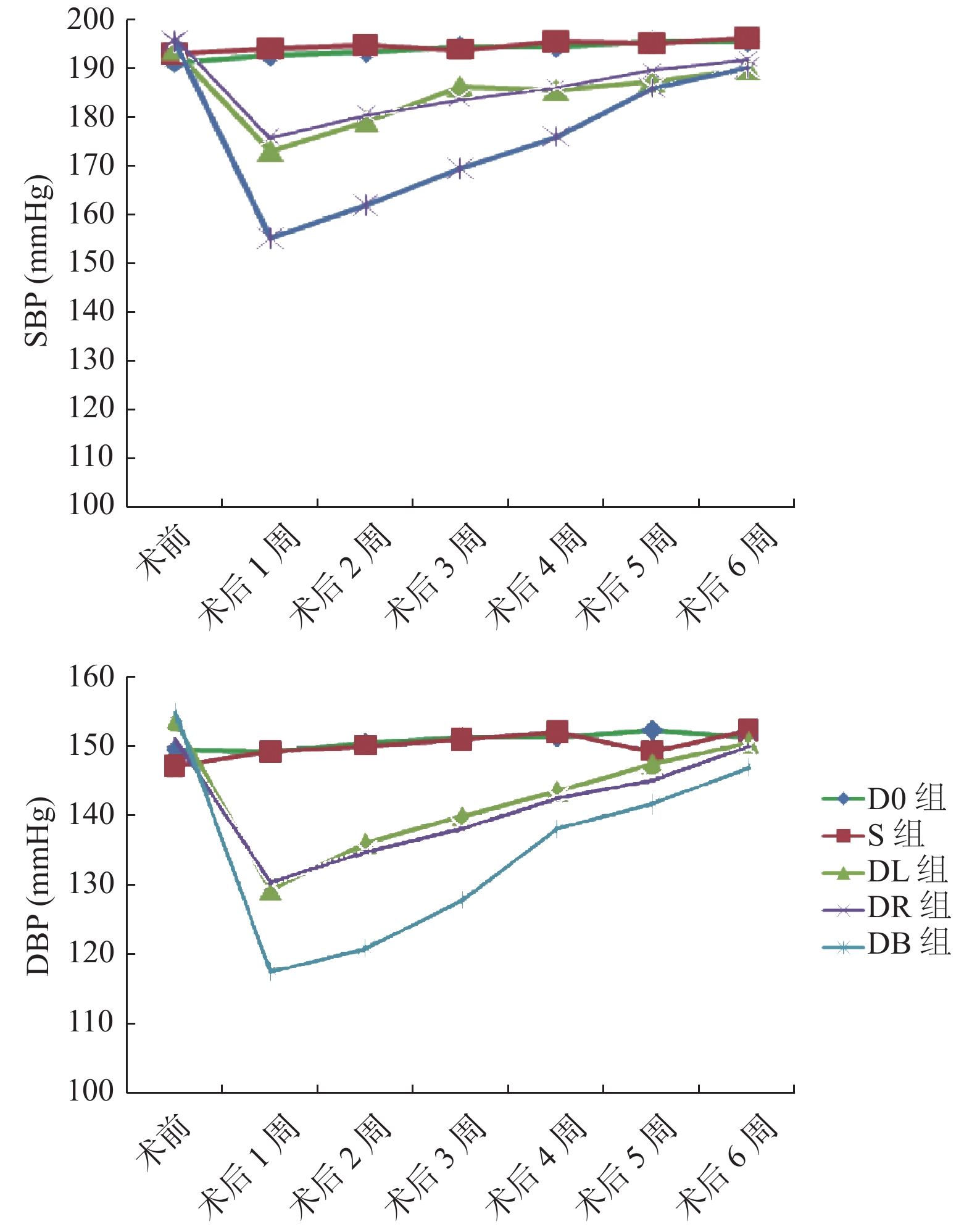 图 1 图1.SHR大鼠围术期收缩压(SBP)及舒张压(DBP)的变化趋势D0组:空白对照组,S组:假手术组,DL左侧处理组,DR组:右侧处理组,DB组:双侧处理组。Figure 1. Variation trend of systolic blood pressure and diastolic pressure in peri-operative period
图 1 图1.SHR大鼠围术期收缩压(SBP)及舒张压(DBP)的变化趋势D0组:空白对照组,S组:假手术组,DL左侧处理组,DR组:右侧处理组,DB组:双侧处理组。Figure 1. Variation trend of systolic blood pressure and diastolic pressure in peri-operative period2.2 去肾动脉神经处理对血浆RAAS相关因子水平影响
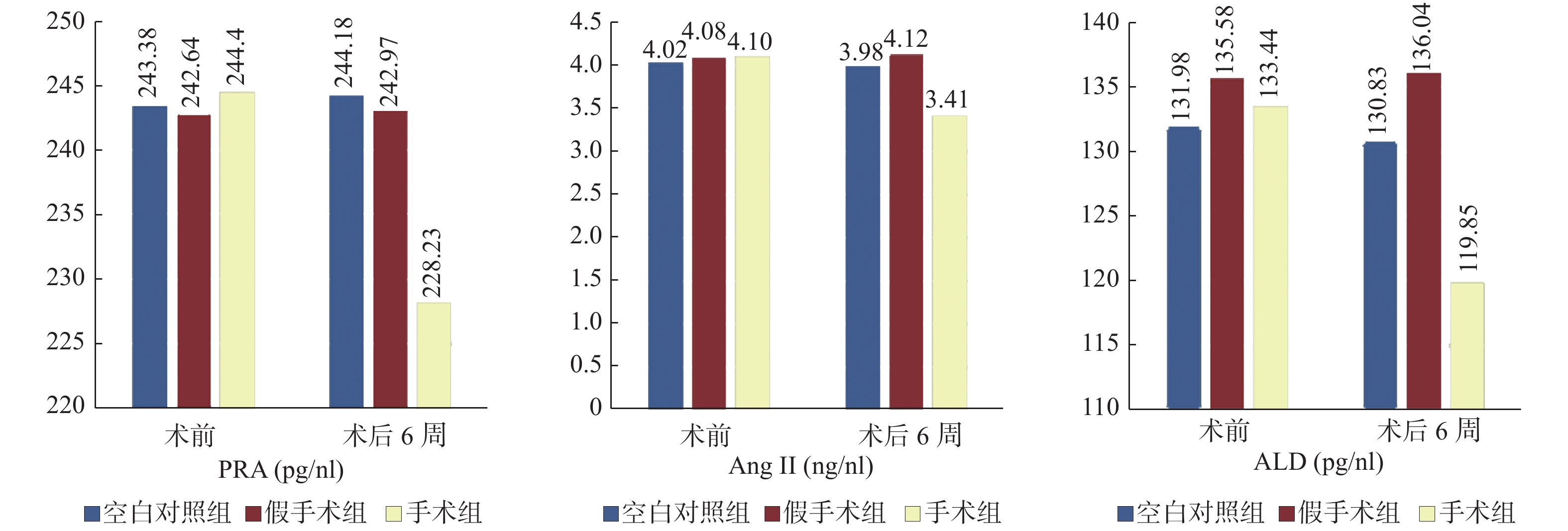
不同处理组围术期血浆PRA,AngⅡ,ALD浓度水平变化见图2。图中显示手术组3个RAAS相关因子经去肾动脉神经处理后均出现下降趋势,相关因子循环浓度水平处理前后比较均显示显著差异PRA[(244.40±11.5)vs (228.23±7.5),P < 0.05];AngⅡ[(4.10±0.35)vs (3.41±0.28),P < 0.05];ALD[(133.44±6.98) vs (119.85±4.12),P < 0.05]。空白对照组及假手术组相关因子围术期变化未见显著差异。
2.3 各组间大鼠心肌厚度及HW/BW值的比较
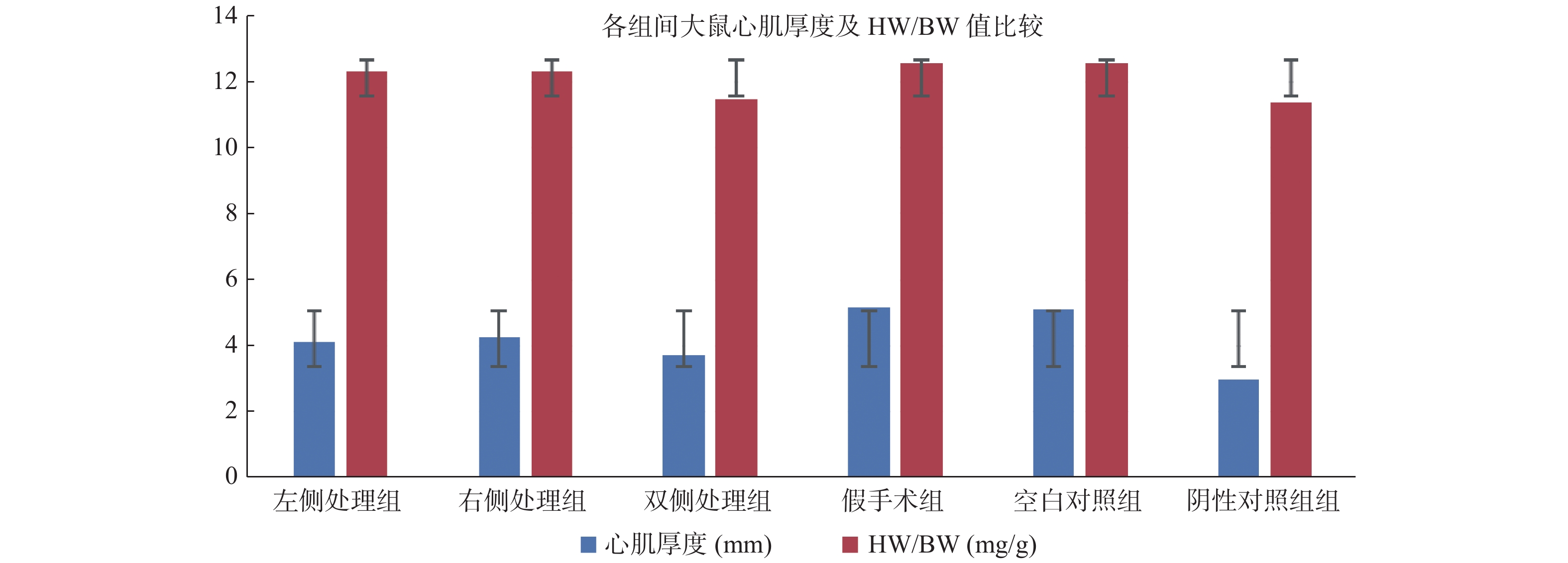
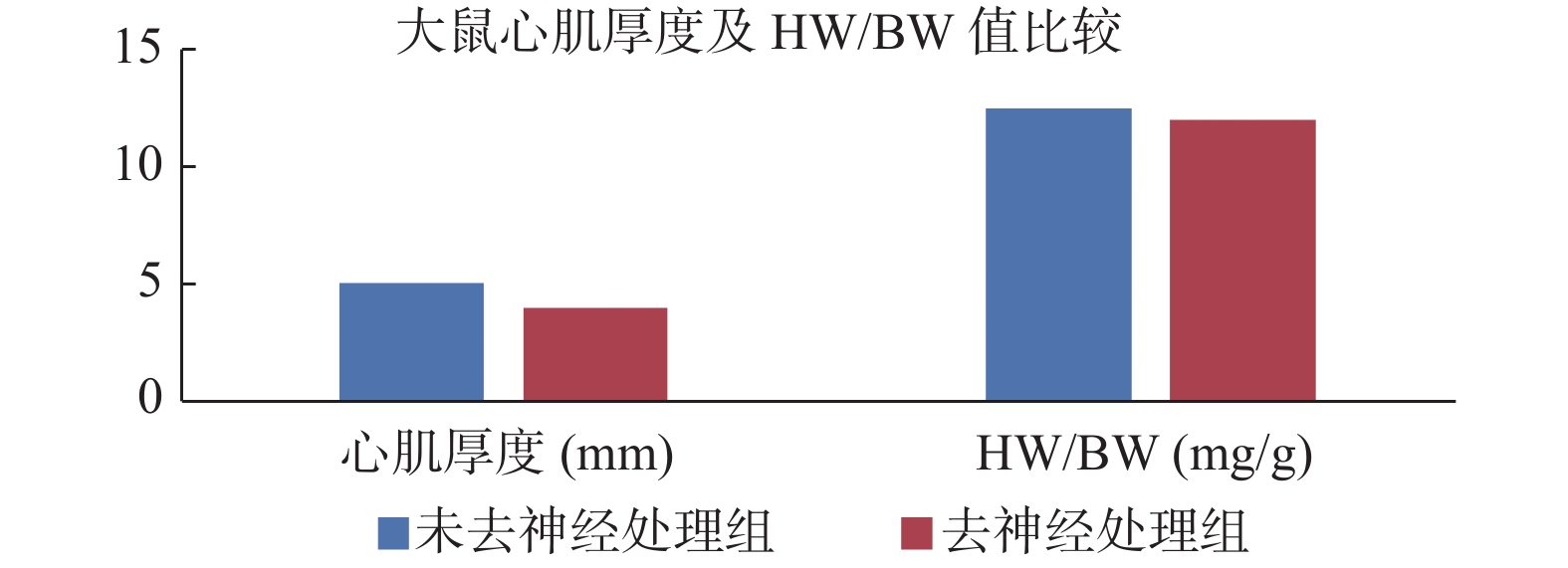
统计学组间对比分析后显示空白对照组和假手术组大鼠的心肌厚度及HW/BW比值与手术干预组相比有显著差异;表3及图3显示左侧处理组及右侧处理组大鼠的心肌厚度及HW/BW值显著高于双侧手术组。左侧手术组与右侧手术组大鼠的心肌厚度及HW/BW值差异无统计学意义,假手术组大鼠与空白对照组相关指标,差异无统计学意义(P > 0.05),见表2~表3、图3~图4。
表 3 各组间大鼠心肌厚度及HW/BW值比较(${{\bar x}} \pm {{s}}$ )Table 3. Comparison of ventricular muscle thickness and HW/BW among different groups ($\bar x \pm s $ )组别 n 心肌厚度(mm) HW/BW(mg/g) 未去神经处理组 20 5.12 ± 0.35 12.58 ± 0.37 去神经处理组 23 4.03 ± 0.37 12.06 ± 0.52 表 2 各组间大鼠心肌厚度及HW/BW值比较(${{\bar x}} \pm {{s}}$ )Table 2. Comparison of ventricular muscle thickness and HW/BW among different groups ($\bar x \pm s $ )组别 n 心肌厚度(mm) HW/BW(mg/g) 左侧处理组 8 4.11 ± 0.34 12.34 ± 0.29 右侧处理组 8 4.24 ± 0.39 12.31 ± 0.28 双侧处理组 7 3.70 ± 0.13 11.46 ± 0.46 假手术组 10 5.15 ± 0.26 12.57 ± 0.25 空白对照组 10 5.10 ± 0.21 12.59 ± 0.49 阴性对照组组 5 2.98 ± 0.16 11.38 ± 0.37 2.4 去肾动脉神经处理对组织RAAS相关因子影响
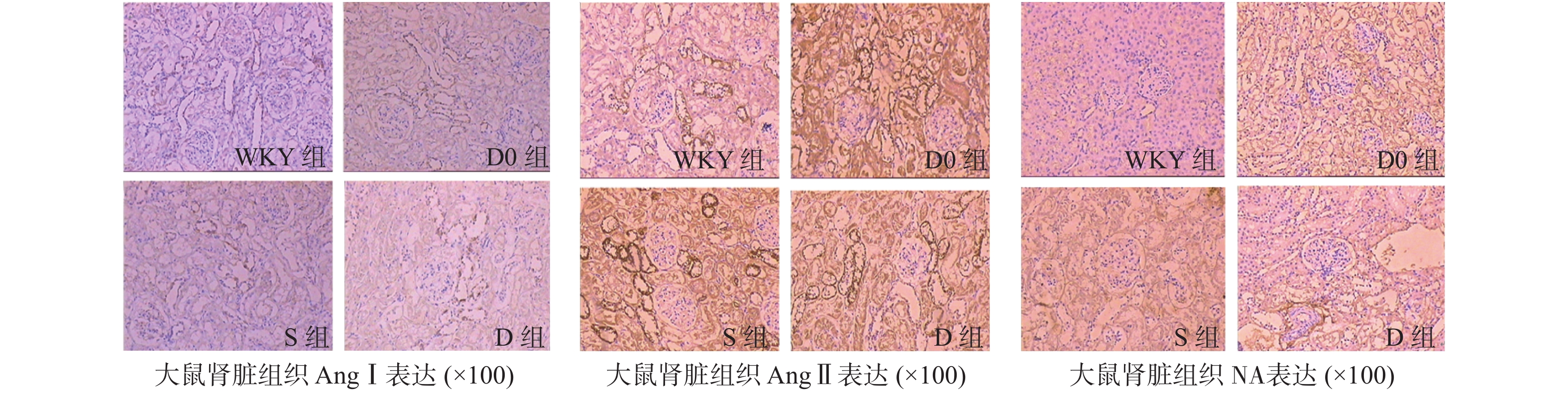
心室肌组织用于行western blot法检测ACE、AngI、AngII、ALD含量相对值进行比较分析结果(表4),结果分析显示不管是左侧组还是右侧组ACE、AngI、AngII、ALD含量相对值均较双侧处理组水平增高,且有显著差异,总手术处理组相关因子水平较假手术组明显降低。多因素相关性分析显示,大鼠心肌组织RAAS相关因子含量与血压、HW/BW及心肌厚度之间相关性有显著意义,且呈正相关性趋势,尤其是与心肌厚度呈明显正相关(表5)。不同处理组间大鼠肾脏组织免疫组化定性分析检测结果见图5。定量显色水平对比(表6)。肾脏AngI、AngII阳性物定位于远曲小管胞浆内,去甲肾上腺素(NA)定位于肾集合管胞浆内,定性分析结果显示手术处理组(D组)AngI、AngII,NA阳性物显色水平低于假手术组(S组),阴性对照组最低。免疫组化定量组间对比分析提示手术处理组AngⅠ,AngⅡ及NA IOD值显著低于空白对照及假手术组,差异有统计学意义(P < 0.05),结果也显示阴性对照组相关指标阳性表达最低。
表 4 各组间大鼠心肌组织ACE、AngI、AngII、ALD的比较($\bar x\pm s $ )Table 4. Comparison of AngII,AngI,ALD,ACE among different group ($ \bar x\pm s$ )组别 n AngII AngI ALD ACE 左侧处理组 8 1.42 ± 0.05 1.42 ± 0.08 1.41 ± 0.09 1.41 ± 0.08 右侧处理组 8 1.49 ± 0.11 1.40 ± 0.77 1.41 ± 0.76b 1.39 ± 0.89 双侧处理组 7 1.18 ± 0.04 1.17 ± 0.04 1.13 ± 0.05 1.13 ± 0.05 假手术组 10 1.96 ± 0.15 1.95 ± 0.15 1.92 ± 0.14f 1.90 ± 0.11 空白对照组 10 2.00 ± 0.18 1.96 ± 0.17 1.95 ± 0.17 1.93 ± 0.15 阴性对照组 5 0.65 ± 0.08 0.56 ± 0.11 0.58 ± 0.11g 0.49 ± 0.08 总处理组 23 1.37 ± 0.15 1.34 ± 0.13 1.32 ± 0.15 1.31 ± 0.15 表 5 大鼠心肌RAAS相关因子含量与血压、HW/BW及心肌厚度之间相关性分析Table 5. Correlation analysis among AngII,AngI,ALD,ACE with blood pressure,HW/BW and ventricular muscle thickness项目 AngI AngII ALD ACE r P r P r P r P 收缩压 0.674 0.001 0.667 0.001 0.707 0.001 0.722 0.001 舒张压 0.744 0.001 0.722 0.002 0.747 0.001 0.780 0.001 HW/BW 0.701 0.002 0.752 0.001 0.708 0.001 0.741 0.001 心肌厚度 0.914 0.001 0.908 0.001 0.912 0.001 0.906 0.001 表 6 不同处理组大鼠肾脏组织因子免疫组化IOD值对比分析(${{\bar x}} \pm {{s}}$ )Table 6. Comparison analysis IOD of tissue factor in kidney by immunohistochemistry (${{\bar x}} \pm {{s}}$ )组别 AngⅠ AngⅡ NA 阴性对照组WKY(n = 5) 0.11 ± 0.01 0.12 ± 0.00 0.06 ± 0.01 空白对照组D0(n = 10) 0.29 ± 0.02 0.36 ± 0.02 0.16 ± 0.01 假手术组S(n = 10) 0.28 ± 0.01 0.35 ± 0.01 0.17 ± 0.14 手术处理组D(n = 23) 0.18 ± 0.01 0.30 ± 0.01 0.13 ± 0.01 2.5 肾动脉周围剥离组织及肾动脉干病理检测
将处理组实验大鼠肾动脉周围剥离组织及肾动脉干进行染色并光镜下观察肾动脉周围神经留存情况,见图6。
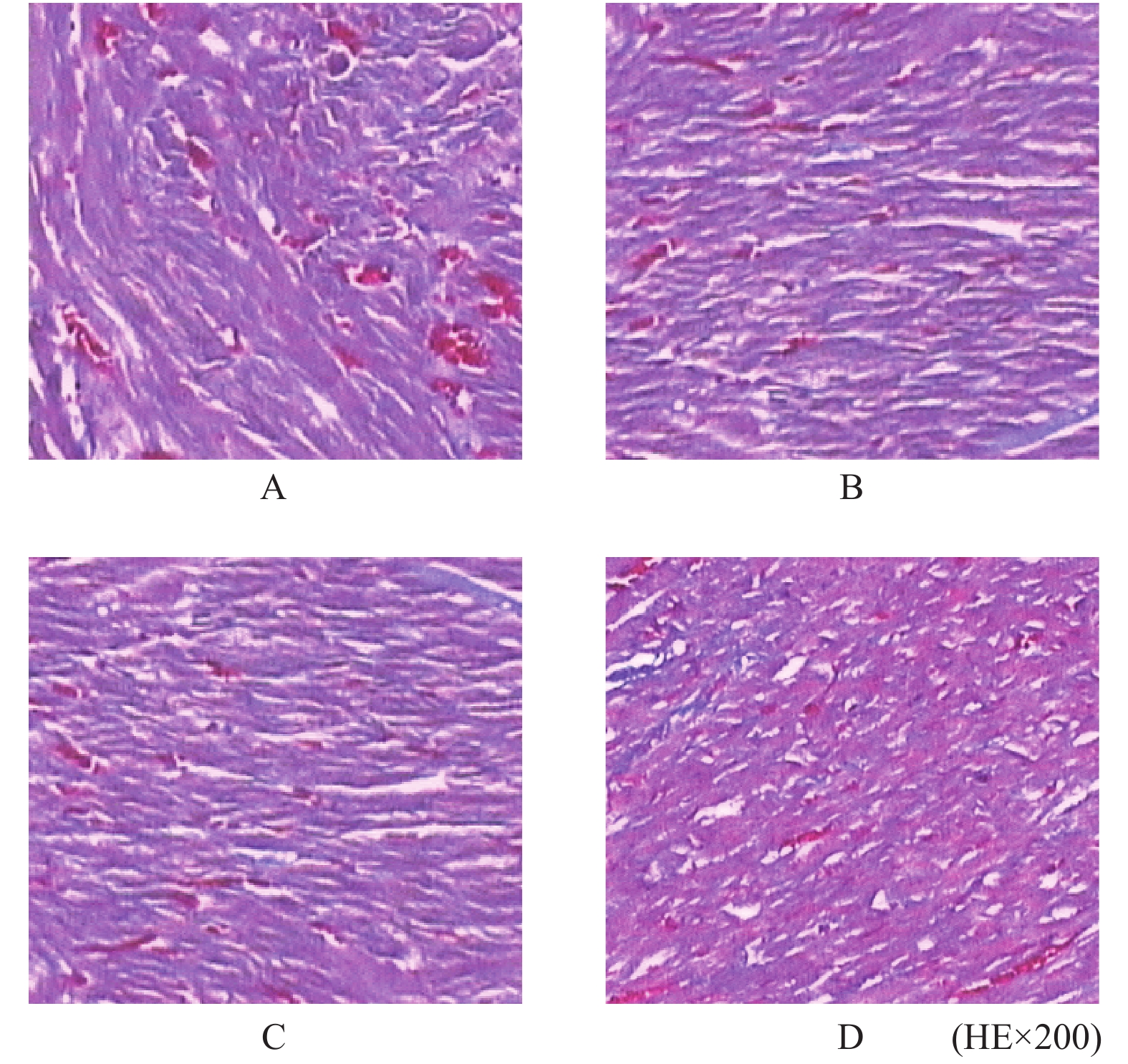
2.6 大鼠心肌HE染色形态学分析
将各组大鼠心脏石蜡切片HE染色在×100显微镜下观察其形态(图7)。图7D可以看出,假手术组大鼠心肌细胞肥大,排列紊乱,间质水肿;而图7A及图7B可见,左侧处理组及右侧处理组大鼠心肌细胞部分肥大,排列较紊乱,但较假手术组及空白对照组程度稍有缓解;从图7C观察示双侧处理组大鼠心肌局部细胞肥大程度较单纯左侧组及右侧组缓解。
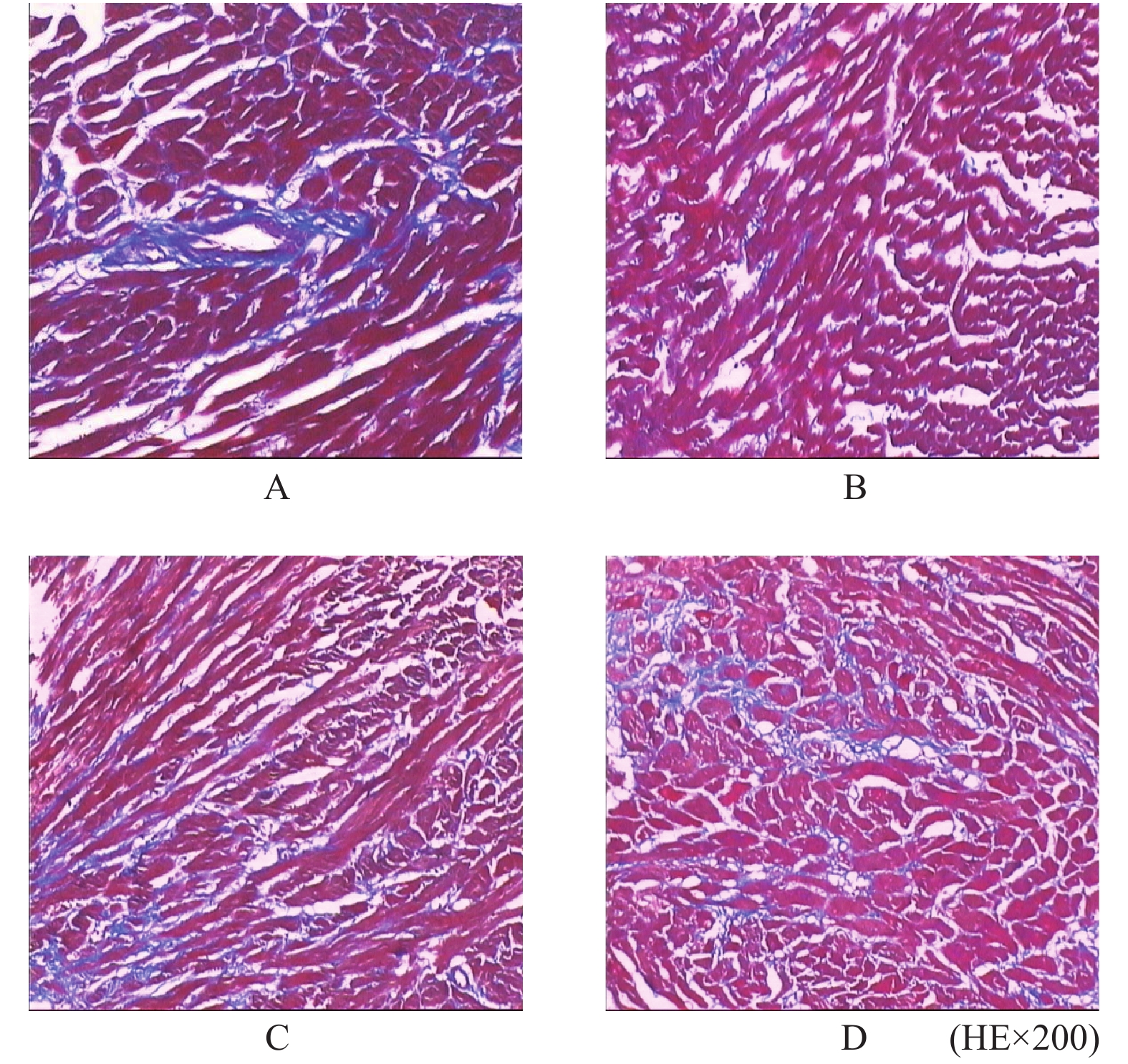
2.7 大鼠心肌masson 染色形态学分析
将各组大鼠心脏石蜡切片行masson染色后于显微镜下观察结果见图8。从图8A可见处理组大鼠心肌细胞肥大,纤维组织增生;图8D假手术组大鼠的心肌细胞肥大,其间纤维组织增生,走行紊乱;
3. 讨论
高血压引起的心力衰竭及心脏猝死及其它危害越来越受到人们重视,其核心环节是交感兴奋状态下进展性的心室重塑。因此,具备降血压和降低交感兴奋双重作用的降压药物较单纯具降压作用的药物更具临床应用价值。RAAS交感神经支配、负责多个系统的动态平衡机制,RAAS神经系统平衡失调可激发诸多不利的病理生理影响[7-8]。全身交感神经的持续激活在高血压促发的心脏重塑进展中起着重要的作用[9-10]。
肾脏交感神经作为全身交感神经重要组成部分,脊髓发出传出与传入神经纤维包绕着肾动脉壁层外膜,中枢交感神经系统发出刺激通过传出神经作用于肾脏,传出与传入交感神经的相互反馈致使肾脏在分泌RAAS相关因子紊乱从而影响血压及靶器官功能及结构的改变[8-9]。本实验采用文献报道的去肾动脉神经法[6]构建SHR去肾动脉交感神经模型,利用物理及化学手段彻底消除肾交感神经的传出与传入,尽力阻断中枢神经与肾脏靶分泌器官的相互反馈及高交感神经作用位点。在实验中,我们通过病检观察发现肾动脉周围无残余的神经组织,证实通过该方法去肾动脉交感神经较为彻底有效,旨在为了彻底毁损肾交感传出传入神经传递神经递质后,观察影响心脏重塑相关指标变化。消除了传统经导管消融法从肾动脉内膜消融去神经化程度不全的嫌疑及混杂干扰因素[3]。
本实验从宏观及微观角度观察心室的结构及重量,心肌细胞的形态,以及细胞间纤维组织的增生程度来了解各组大鼠心室重塑的程度,并进行组间比较。虽然,围术期观察6周的血压变化未显示去除肾动脉神经能产生持续有效降低血压的效应,甚至观察期内就恢复到基础状态,但组织病理学观察发现不同处理组间大鼠心肌重塑程度相关指标有显著差别,经过去肾动脉交感神经术处理的高血压大鼠对比未经处理的高血压大鼠的心脏重塑指标改善,包括HW/BW值及心肌厚度显著降低,镜下心肌肥大,排列紊乱及间质纤维增生紊乱情况较为减轻;并且完全处理组较部分处理组心室重塑相关指标缓解的情况更为明显;说明去肾动脉交感神经术对自发性高血压大鼠的心室重塑进展有着明显的延缓及下调促进因子水平作用,并且去神经化的完全程度与心室重塑的缓解情况可能相关。该结果与近期研究提示的去肾动脉交感神经术后对心脏重塑缓解效应可能独立于血压下降的变化而存在 [2-3],甚至患者心脏舒张功能及心力衰竭临床症状得到明显改善[11-13]。本实验结果与上述临床研究结果相符合,且从组织病理学改善指标独立于血压变化得到明确证实。
相关的临床研究数据亦指出,RAAS相关因子活性减低程度与相关通路参与并引起心肌结构产生变化影响相关[14],本实验中通过去神经化处理后同步检测循环水平及组织水平的RAAS相关因子活性表达,结果显示去神经处理大鼠心肌组织中RAAS相关因子(ACE、AngI、AngII、ALD)表达水平降低,且含量变化与心肌厚度,心肌细胞肥大及排列紊乱程度,间质增生等重塑指标明显呈正相关关系。肾脏组织RAAS相关因子的定性与定量分析也显示去肾动脉神经能显著下调肾脏组织RAAS相关因子活性表达水平。持续更新的临床研究结果[15-16]证实该项技术在对顽固性高血压患者心力衰竭及相关并发症的防治提供了新的思路及研究热点方向。
本研究缺陷在于,本研究仅为观察对比研究,去肾动脉神经对心室重塑缓解作用维持的持久性及临床应用指导价值尚需更长久实验观察证实,具体缓解心脏重塑的信号通路调控机制尚需进一步深入探讨。
-
表 1 EC预后相关的高组织学分级和LVSI的不同DWI模型参数差异
Table 1. High histological grades related to EC prognosis and differences in parameters of different DWI models of LVSI
指标 ADC(×10−3 mm2/s) D(×10−3 mm2/s) D*(×10−3 mm2/s) f DDC(×10−3 mm2/s) α 肿瘤分级 低级 1.05 ± 0.12 0.66 ± 0.09 7.76(4.00~87.85) 0.26 ± 0.07 0.93 ± 0.16 0.73 ± 0.04 高级 0.87 ± 0.12 0.55 ± 0.06 7.10(4.64~29.20) 0.22 ± 0.06 0.69 ± 0.15 0.71 ± 0.07 t/U 6.472 5.417 1.062 2.523 9.471 1.245 P < 0.001* < 0.001* 0.635 0.041* < 0.001* 0.219 LVSI 阴性 1.03 ± 0.14 0.64 ± 0.01 7.32(4.00~87.85) 0.26 ± 0.07 0.91 ± 0.18 0.73 ± 0.05 阳性 0.93 ± 0.13 0.59 ± 0.08 10.2(4.96~56.95) 0.21 ± 0.08 0.75 ± 0.16 0.71 ± 0.05 t/U 4.233 1.938 2.755 3.981 4.520 1.742 P 0.018* 0.065 0.039* 0.017* 0.002* 0.051 *P < 0.05。 表 2 DWI模型得出的单个和组合参数在预测EC肿瘤分级和LVSI中的诊断性能
Table 2. Diagnostic performance of individual and combined parameters derived from DWI models in predicting EC tumor grade and LVSI
参数 截止值 AUC P 敏感度(%) 特异度(%) 肿瘤分级 ADC ≤ 0.945 0.862 < 0.001* 83.3 83.7 D ≤ 0.619 0.848 < 0.001* 94.4 58.1 f ≤ 0.233 0.699 0.005* 83.3 65.1 DDC ≤ 0.821 0.882 < 0.001* 88.9 79.1 联合f和DDC 0.895 < 0.001* 88.9 79.1 LVSI ADC(×10−3 mm2/s) ≤ 0.922 0.686 0.019* 58.8 81.8 D*(×10−3 mm2/s) > 5.805 0.671 0.017* 94.1 40.9 f ≤ 0.203 0.711 0.007* 58.8 77.3 DDC ≤ 0.931 0.759 < 0.001* 88.2 54.6 联合f和DDC 0.797 < 0.001* 76.5 70.5 *P < 0.05。 表 3 多元Logistic回归模型确定EC肿瘤分级和LVSI相关DWI模型参数
Table 3. Multivariate Logistic regression model to determine EC tumor grade and LVSI related DWI model parameters
参数 OR 95 %CI P 方差膨胀因子a 模型拟合 肿瘤分级 常量 0.904 0.325~1.842 0.129 f 0.001 0~0.720 0.044 1.029 DDC 0.001 0~0.007 < 0.001* 1.029 LVSI 常量 0.823 0.394~1.438 0.321 f 0.001 0~0.336 0.030* 1.029 DDC 0.004 0~0.214 0.006* 1.029 a方差膨胀因子小于5,表明回归模型不存在多重共线性。*P < 0.05。 -
[1] 王成艳. 子宫内膜癌组织学分型和淋巴脉管间隙浸润的多模态MR成像研究进展[J]. 临床放射学杂志,2020,39(9):1885-1889. [2] 蓝喜,何文雯,郑成军,等. Ⅱ型子宫内膜癌预后因素的COX回归分析[J]. 昆明医科大学学报,2020,41(7):160-164. doi: 10.3969/j.issn.1003-4706.2020.07.032 [3] Daix M,Angeles M A,Migliorelli F,et al. Concordance between preoperative ESMO-ESGO-ESTRO risk classification and final histology in early-stage endometrial cancer[J]. J Gynecol Oncol,2021,32(4):48. doi: 10.3802/jgo.2021.32.e48 [4] 郝建成,孙丽娟,郝金钢. 乳腺结节状病变的MRI诊断[J]. 昆明医科大学学报,2021,42(10):127-131. doi: 10.12259/j.issn.2095-610X.S20211007 [5] Lin M,Yu X,Chen Y,et al. Contribution of mono-exponential,bi-exponential and stretched exponential model-based diffusion-weighted MR imaging in the diagnosis and differentiation of uterine cervical carcinoma[J]. Eur Radiol,2017,27(6):2400-2410. doi: 10.1007/s00330-016-4596-8 [6] Wang Y,Hu D,Yu H,et al. Comparison of the diagnostic value of monoexponential,biexponential,and stretched exponential diffusion-weighted MRI in differentiating tumor stage and histological grade of bladder cancer[J]. Acad Radiol,2019,26(2):239-246. doi: 10.1016/j.acra.2018.04.016 [7] Lin L,Xue Y,Duan Q,et al. Grading meningiomas using mono-exponential,bi-exponential and stretched exponential model-based diffusion-weighted MR imaging[J]. Clin Radiol,2019,74(8):15-23. [8] 张箭,薛旭涛,刘燕,等. 肿瘤全域ADC直方图在鉴别子宫内膜癌组织级别中的应用[J]. 临床放射学杂志,2019,38(4):678-683. [9] 范婵媛,闵祥德,方俊华,等. 基于ADC图的纹理分析在低,高级别前列腺癌诊断中的价值[J]. 中华放射学杂志,2019,53(10):859-863. doi: 10.3760/cma.j.issn.1005-1201.2019.10.013 [10] Yue W,Meng N,Wang J,et al. Comparative analysis of the value of diffusion kurtosis imaging and diffusion-weighted imaging in evaluating the histological features of endometrial cancer[J]. Cancer Imaging,2019,19(1):9. doi: 10.1186/s40644-019-0196-6 [11] Thieme S F,Collettini F,Sehouli J,et al. Preoperative evaluation of myometrial invasion in endometrial carcinoma:Prospective intra-individual comparison of magnetic resonance volumetry,diffusion-weighted and dynamic contrast-enhanced magnetic resonance imaging[J]. Anticancer Res,2018,38(8):4813-4817. doi: 10.21873/anticanres.12791 [12] Lavaud P,Fedida B,Canlorbe G,et al. Preoperative MR imaging for ESMO-ESGO-ESTRO classification of endometrial cancer[J]. Diagn Interv Imaging,2018,99(6):387-396. doi: 10.1016/j.diii.2018.01.010 [13] Wang F,Wang Y,Zhou Y,et al. Comparison between types I and II epithelial ovarian cancer using histogram analysis of monoexponential,biexponential,and stretched-exponential diffusion models[J]. J Magn Reson Imaging,2017,46(6):1797-1809. doi: 10.1002/jmri.25722 [14] Yabuuchi H,Kamitani T,Sagiyama K,et al. Characterization of parotid gland tumors:Added value of permeability MR imaging to DWI and DCE-MRI[J]. Eur Radiol,2020,30(12):6402-6412. doi: 10.1007/s00330-020-07004-3 [15] Gurney Champion O J,Klaassen R,Froeling M,et al. Comparison of six fit algorithms for the intra-voxel incoherent motion model of diffusion-weighted magnetic resonance imaging data of pancreatic cancer patients[J]. PloS One,2018,13(4):0194590. [16] Liang C Y,Chen M D,Zhao X X,et al. Multiple mathematical models of diffusion-weighted magnetic resonance imaging combined with prognostic factors for assessing the response to neoadjuvant chemotherapy and radiation therapy in locally advanced rectal cancer[J]. Eur J Radiol,2019,110(5):249-255. -






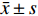
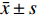
 下载:
下载:

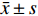
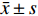

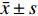
 下载:
下载: