Efficacy and Safety of Jingangteng Capsules Combined with Antimicrobial Drugs in the Treatment of Chronic Pelvic Inflammatory Disease: A Meta-analysis
-
摘要:
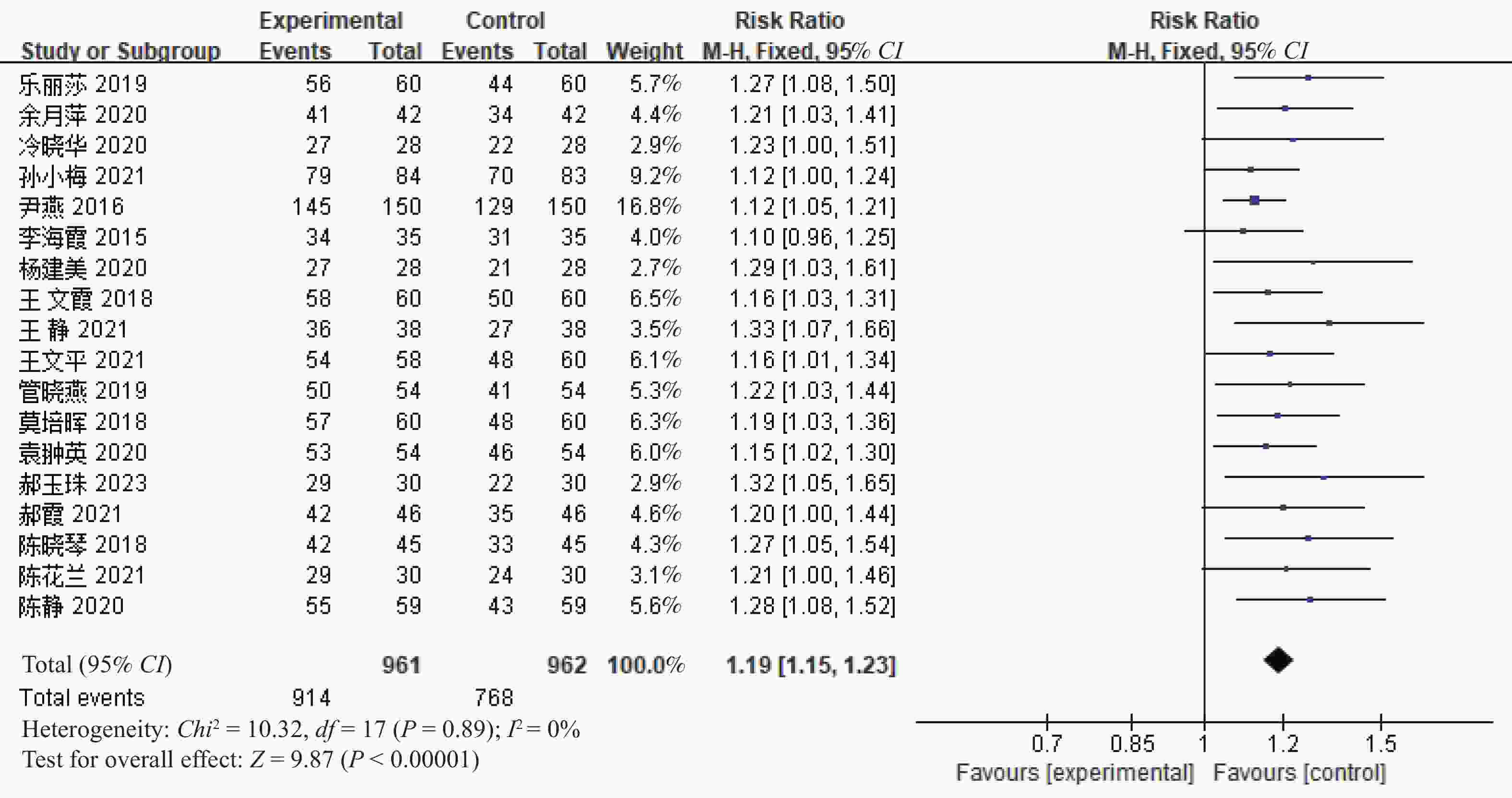
目的 系统评价金刚藤胶囊联合抗菌药物治疗慢性盆腔炎的有效性和安全性。 方法 检索国内外数据库中金刚藤胶囊联合抗菌药物治疗慢性盆腔炎的随机对照试验(RCTs)研究,使用RevMan 5.4 软件进行Meta分析。 结果 最终纳入24篇RCTs研究,样本量共计2 441例。Meta分析结果显示,金刚藤胶囊联用抗菌药物可显著提高慢性盆腔炎患者的临床总有效率[RR=1.19,95%CI (1.15,1.23),P < 0.001];与单纯使用抗菌药物治疗相比还能降低不良事件的发生率[RR=0.70,95%CI (0.51,0.95),P < 0.05]。此外,金刚藤胶囊联合抗菌药物治疗慢性盆腔炎与单纯抗菌药物治疗相比在促进炎性因子、淋巴细胞恢复上均有明显改善(P < 0.05),可缩短症状缓解时间和改善血液流变学指标(P < 0.05)。 结论 金刚藤胶囊联合抗菌药物治疗慢性盆腔炎有较好的疗效和安全性,但鉴于研究证据质量情况,需结合临床实践综合应用。 Abstract:Objective To systematically evaluate the efficacy and safety of Jingangteng capsule combined with antibiotics in the treatment of chronic pelvic inflammatory disease. Methods Randomized controlled trials (RCTs) of Jingangteng capsule combined with antibiotics in the treatment of chronic pelvic inflammatory disease were searched from domestic and foreign databases. RevMan 5.4 software was used for Meta-analysis. Results Twenty-four studies of RCTs were finally included, with a total sample size of 2, 441 cases. Meta-analysis showed that the combination of antimicrobial drugs with Jingangteng capsule significantly increased the overall clinical effectiveness rate of patients with chronic pelvic inflammatory disease [RR=1.19, 95%CI (1.15, 1.23), P < 0.001]. It also reduced the incidence of adverse events compared with treatment with antimicrobial drugs alone [RR=0.70, 95%CI (0.51, 0.95), P < 0.05]. In addition, the treatment of chronic pelvic inflammatory disease with Jingangteng capsule combined with antimicrobial drugs improved in promoting the recovery of inflammatory factor, and lymphocytes compared with antimicrobial drug therapy alone (P < 0.05), and also effectively shortened the symptomatic remission time and improved the hemorheological indexes (P < 0.05). Conclusion Jingangteng capsule combined with antibacterial agents has good efficacy and safety in the treatment of chronic pelvic inflammatory disease, but in view of the quality of research evidence, it should be applied according to the actual clinical situation. -
Key words:
- Jingangteng capsule /
- Chronic pelvic inflammatory /
- Systematic evaluation /
- Meta-analysis
-
表 1 纳入文献的基本特征
Table 1. Basic characteristics of included studies
纳入文献
(年)样本(n) 年龄(岁) 病程(a) 干预措施 疗程 结局
指标T C T C T C T C 陈花兰[9] 2021 30 30 38.86±5.28 38.79±5.32 1.22±0.13 1.14±0.21 抗+金刚藤胶囊
4粒/次 3次/d左氧氟沙星 2周 (1)(2)(6) 陈静[10] 2020 59 59 40.12±6.13 39.87±6.05 3.83±0.86 3.94±0.95 抗+金刚藤胶囊
4粒/次 3次/d替硝唑 12周 (1)(2)(6) 陈晓琴[11] 2018 45 45 38.83±3.72 37.62±3.62 3.21±1.17 3.29±1.25 抗+金刚藤胶囊
4粒/次 3次/d司帕沙星 2周 (1)(6) 管晓燕[12] 2019 54 54 34.01±3.46 33.56±2.89 2.26±0.55 2.29±0.59 抗+金刚藤胶囊
4粒/次 3次/d头孢硫脒+
替硝唑12周 (1)(2) 郝霞[13] 2021 46 46 34.59±2.01 34.70±1.96 2.61±1.05 2.70±1.01 抗+金刚藤胶囊
4粒/次 3次/d头孢曲松钠+
甲硝唑2周 (1)(2)(4) 郝玉珠[14] 2023 30 30 35.31±3.26 35.28±3.27 2.63±0.66 2.61±0.71 抗+金刚藤胶囊
4粒/次 3次/d左氧氟沙星 2周 (1)(2)(3)(4)(5)(6) 胡开泰[15] 2019 30 30 36.1±1.4 35.5±1.5 − − 抗+金刚藤胶囊
2粒/次 3次/d甲硝唑 2周 (1)(2) 乐丽莎[16] 2019 60 60 35.37±5.41 35.45±5.26 2.23±0.49 2.17±0.58 抗+金刚藤胶囊
4粒/次 3次/d克林霉素
磷酸2周 (1)(2)(3) 雷敏[17] 2022 60 60 32.15±4.45 32.20±4.50 12.32±1.45 12.35±1.50 抗+金刚藤胶囊
4粒/次 3次/d司帕沙星 10d (1)(4) 冷晓华[18] 2020 28 28 38.0±3.0 38.3±3.2 13.0±2.4 13.3±2.6 抗+金刚藤胶囊
4粒/次 3次/d司帕沙星 10d (1) 李春红[19] 2021 44 44 38.66±4.18 38.67±4.17 2.01±0.43 2.03±0.45 抗+金刚藤胶囊
4粒/次 3次/d左氧氟沙星+
甲硝唑2周 (2)(4)(6) 李海霞[20] 2015 35 35 37.5±10.6 39.5±11.3 − − 抗+金刚藤胶囊
4粒/次 3次/d头孢曲松钠+
奥硝唑10d (1) 莫培晖[21] 2018 60 60 54.8±7.2 54.3±7.4 5.2±1.4 5.1±1.8 抗+金刚藤胶囊
4粒/次 3次/d司帕沙星 2周 (1)(2) 欧阳静[22] 2018 41 41 29.89±4.03 30.18±3.97 3.41±0.98 3.23±1.05 抗+金刚藤胶囊
4粒/次 3次/d头孢唑肟钠+
奥硝唑2周 (4)(5)(6) 潘春芳[23] 2021 45 45 45.32±2.15 45.23+2.23 3.2±1.2 3.3+1.3 抗+金刚藤胶囊
4粒/次 3次/d阿奇霉素 2周 (2)(4)(5)(6) 孙小梅[24] 2021 84 83 46.92±9.51 47.51±9.64 2.93±1.02 3.04±0.96 抗+金刚藤胶囊
6粒/次 3次/d头孢曲松钠+
替硝唑3周 (1)(4)(5)(6) 王静[25] 2021 38 38 31.29±3.19 31.73±3.56 3.58±0.35 3.55±0.21 抗+金刚藤胶囊
4粒/次 3次/d克林霉素
磷酸酯2周 (1)(2)(3) 王文平[26] 2021 58 60 45.3±6.7 46.2±5.9 3.8±2.1 3.8±1.9 抗+金刚藤胶囊
4粒/次 3次/d甲硝唑 2周 (1)(2) 王文霞[27] 2018 60 60 38.46±5.53 38.52±5.81 2.40±0.72 2.52±0.79 抗+金刚藤胶囊
4粒/次 3次/d阿奇霉素 2周 (1)(2)(4) 杨建美[28] 2020 28 28 38.03±1.26 5.02±0.14 4.92±0.47 抗+金刚藤胶囊
4粒/次 3次/d头孢曲松钠+
阿奇霉素2周 (1)(2) 尹燕[29] 2016 150 150 36.67±10.1 37.74±11.01 14.11±9.35 14.57±10.16 抗+金刚藤胶囊
3粒/次 3次/d左氧氟沙星 6周 (1)(6) 余月萍[30] 2020 42 42 31.26±4.34 31.29±4.42 2.67±0.16 2.69±0.18 抗+金刚藤胶囊
4粒/次3次/d罗红霉素+
甲硝唑2周 (1)(6) 袁翀英[31] 2020 54 54 31.39±1.57 31.04±1.25 14.74±1.53 14.12±1.06 抗+金刚藤胶囊4粒/次3次/d 头孢美唑钠 2周 (1) 朱文婷[32] 2020 39 39 52.91±487 52.87±4.90 3.86±0.71 3.89±0.67 抗+金刚藤胶囊4粒/次 3次/d 司帕沙星 2周 (2)(5)(6) T:实验组;C:对照组;−:未提及;结局指标:(1)临床总有效率;(2)炎性因子(CRP、PCT 、IL-1、IL-4、IL-6、IL-8、IL-10、TNF-α、GM-CSF);(3)血液流变学指标(WBC、ESR、全血粘度、血浆粘度、HO-1);(4)临床症状缓解时间(体温、下腹痛、白带异常、下腹坠痛、腰骶酸痛、盆腔肿块消失);(5)T淋巴细胞(CD3+、CD4+、CD8+、CD4+/CD8+);(6)不良反应事件。 表 2 Meta分析结果汇总表
Table 2. Summary of meta-analysis results
结局指标 纳入文献(篇) 样本量(n) 效应模型 异质性检验结果 Meta分析结果 P I2(%) MD 95%CI P 炎性因子 CRP 11篇[9,10,12-14,19,20,27-29,31] 1180 随机 <0.0001** 94 2.35 1.60~3.09 <0.0001** PCT 4篇[23,26,28,31] 372 随机 <0.0001** 85 0.15 0.12~0.19 <0.0001** IL-1 5篇[14,16,23,25,26] 464 随机 0.03* 64 6.48 5.23~7.73 <0.0001** IL-4 3篇[23,26,27] 328 固定 <0.0001** 0 10.87 9.56~12.18 <0.0001** IL-6 5篇[9,13,15,19,21] 420 随机 <0.0001** 94 14.43 7.29~21.57 <0.0001** IL-8 7篇[14-16,19,23,26,32] 614 随机 <0.0001** 96 16.32 10.55~22.08 <0.0001** IL-10 3篇[13,14,16] 271 随机 <0.0001** 65 6.79 4.93~8.64 <0.0001** TNF-α 6篇[19,21,23,26,27,32] 614 随机 0.0002** 100 21.17 10.11~32.22 <0.0001** GM-CSF 2篇[28,31] 164 随机 <0.0001** 54 4.28 3.03~5.52 <0.0001** 血液流变学 WBC 2篇[10,12] 226 固定 0.60 0 0.97 0.60~1.33 <0.0001** ESR 2篇[12,16] 228 固定 0.83 0 3.57 2.78~4.36 <0.0001** 全血粘度 2篇[16,25] 196 固定 0.82 0 1.52 1.27~1.77 <0.0001** 血浆粘度 2篇[16,25] 196 固定 0.17 46 0.32 0.27~0.38 <0.0001** HO-1 2篇[28,31] 164 固定 0.91 0 41.95 34.27~49.63 <0.0001** 症状恢复时间 体温 2篇[14,27] 180 固定 0.91 0 −1.94 −2.11~−1.78 <0.0001** 下腹痛 6篇[14,17,22-24,27] 639 固定 0.82 0 −2.20 −2.36~−2.03 <0.0001** 腰骶酸痛 2篇[13,19] 180 固定 0.31 1 −1.71 −2.20~−1.21 <0.0001** 白带异常 8篇[13,14,17,19,22-24,27] 819 随机 <0.0001** 91 −2.55 −3.06~−2.03 <0.0001** 下腹坠痛 6篇[13,17,19,22-24] 639 随机 0.01* 66 −2.57 −3.06~−2.08 <0.0001** 盆腔肿块消失 5篇[13,17,22-24] 551 随机 0.001** 78 −4.56 −5.79~−3.32 <0.0001** T淋巴细胞 CD3+ 3篇[14,22,24] 299 随机 <0.0001** 96 11.67 5.69~17.65 0.0001** CD4+ 5篇[14,22-24,32] 455 随机 <0.0001** 91 5.16 2.97~7.35 <0.0001** CD8+ 4篇[14,22,23,32] 310 固定 0.46 0 5.00 4.33~5.68 <0.0001** CD4+/CD8+ 4篇[14,22,23,32] 196 固定 0.91 0 0.52 0.48~0.56 <0.0001** *P < 0.05;**P < 0.01。 表 3 不同疗程的亚组分析结果
Table 3. Results of subgroup analysis for different courses of treatment
亚组(疗程) 纳入文献(篇) 样本量(例) 效应模型 异质性检验结果 Meta分析结果 P I2(%) MD 95%CI P CRP 10 d 1篇[20] 70 − − − 2.97 −1.30~−7.24 0.17 2周 7篇[9,13-14,19,27,28,31] 584 随机 <0.0001** 97 0.15 0.12~0.19 <0.0001** 6周 1篇[29] 150 − − − 2.72 1.07~4.37 0.001** 12周 2篇[10,12] 226 随机 0.09 65 0.98 0.73~1.22 <0.0001** 白带异常 10 d 1篇[17] 120 − − − −2.00 −2.51~−1.49 <0.0001** 2周 6篇[14,15,19,22,23,27] 532 随机 <0.0001** 92 −2.62 −3.21~−2.03 <0.0001** 3周 1篇[24] − − − −2.74 −3.59~−1.89 <0.0001** 下腹坠痛 10 d 1篇[17] 120 − − − −3.00 −3.52~−2.48 <0.0001** 2周 4篇[13,19,22,23] 352 随机 0.02* 70 −2.49 −3.19~−1.79 <0.0001** 3周 1篇[24] 167 − − − −2.44 −3.10~−1.78 <0.0001** 盆腔肿块消失 10 d 1篇 120 − − − −3.00 −4.19~−1.81 <0.0001** 2周 3篇 264 随机 0.08 60 −4.61 −5.94~−3.28 <0.0001** 3周 1篇 167 − − − −5.91 −6.97~−4.85 <0.0001** CD3+ 299 随机 <0.0001** 96 11.67 5.69~17.65 0.0001** 2周 2篇[14,17] 141 随机 <0.0001** 94 11.67 7.48~20.51 <0.0001** 3周 1篇[19] 157 − − − 7.16 5.72~8.60 <0.0001** CD4+ 2周 4篇[14,22,23,32] 288 随机 <0.0001** 87 5.78 3.40~8.17 <0.0001** 3周 1篇[24] 167 − − − 2.88 1.94~3.82 <0.0001** −:不涉及;*P < 0.05;**P < 0.01。 表 4 不良事件发生情况统计表
Table 4. Statistics on the occurrence of adverse events
纳入文献 不良事件发生情况 对照组 实验组 陈花兰[9] 恶心3例、腹痛腹胀1例、头痛头晕3例、肝功能异常1例 恶心1例、头痛头晕1例 陈静[10] 恶心呕吐3例、腹痛腹胀1例、皮肤瘙痒2例 恶心呕吐4例、腹痛腹胀2例、皮肤瘙痒2例 陈晓琴[11] 胃痛4例、恶心4例、胃肠道反应5例、过敏3例 恶心2例、胃痛1例、胃肠道反应1例、过敏1例 郝玉珠[14] 恶心2例;皮疹3例 恶心2例;腹痛3例;皮疹1例 李春红[19] 呕吐3例;皮疹1例; 呕吐1例;头痛2例; 欧阳静[22] 呕吐1例;恶心2例;腹泻1例 呕吐2例;恶心3例;腹泻1例 潘春芳[23] 胃痛3例;过敏4例;胃肠道4例 胃痛1例;过敏1例;胃肠道1例 孙小梅[24] 呕吐2例;腹泻2例 乏力2例;头痛2例;呕吐1例;腹泻1例 王文平[26] 腹痛1例;恶心2例 恶心1例;皮疹1例 王文霞[27] 恶心1例;腹痛1例;皮疹1例 恶心2例;腹痛1例; 尹燕[29] 头晕、恶心和肠胃不适等不良反应事件共有17例 头晕、恶心和肠胃不适等不良反应事件共有16例 朱文婷[32] 过敏2例;胃肠道反应5例;胃痛1例 过敏1例;胃肠道反应1例 -
[1] 曹俊岩,刘小古,曾莉,等. 支原体及衣原体感染对慢性盆腔炎病情及阴道菌群的影响[J]. 中华医院感染学杂志,2023,33(13):2037-2041. [2] 吴威,朱文丽,柴淑慧,等. 女性盆腔炎外周血补体C3、C4及MCP-1因子的表达[J]. 中华医院感染学杂志,2022,32(14):2183-2186. [3] 张艳红,尹宁,王彩虹,等. 盆炎清方治疗慢性盆腔炎疗效及对MCP-1、T细胞亚群的变化研究[J]. 中华中医药学刊,2023,41(6):169-172. [4] 谷风,严英,陶红星. 利湿化瘀中药对慢性盆腔炎血液流变学及血清C-反应蛋白的影响[J]. 中华中医药杂志,2011,26(5):1102-1105. [5] 沈凡琪,韩延华,刘丽. 中医药治疗盆腔炎性疾病相关信号通路的研究进展[J]. 中国实验方剂学杂志,2023,29(18):251-258. [6] 《中成药治疗优势病种临床应用指南》标准化项目组. 中成药治疗盆腔炎性疾病后遗症临床应用指南(2020年)[J]. 中国中西医结合杂志,2021,41(3):286-299. [7] 禹立芳. 金刚藤胶囊配伍康妇消炎栓治疗盆腔炎性包块100例临床观察[J]. 中国妇幼保健,2011,26(33):5249-5250. [8] 中华医学会妇产科学分会感染性疾病协作组. 盆腔炎症性疾病诊治规范(2019修订版)[J]. 中华妇产科杂志,2019,54(7):433-437. [9] 陈花兰. 金刚藤胶囊联合左氧氟沙星治疗盆腔炎性疾病的临床疗效研究[J]. 临床合理用药杂志,2021,14(36):42-44. [10] 陈静. 金刚藤胶囊联合替硝唑注射液及注射用头孢硫脒治疗慢性盆腔炎的临床效果[J]. 河南医学研究,2020,29(11):2046-2047. [11] 陈晓琴,李云秀. 金刚藤胶囊配合乳酸司帕沙星片对慢性盆腔炎的临床疗效[J]. 检验医学与临床,2018,15(3):356-358. [12] 管晓燕. 金刚藤胶囊联合注射用头孢硫脒及替硝唑注射液治疗54例慢性盆腔炎的临床研究[J]. 北方药学,2019,16(5):100-101. [13] 郝霞,李蔚. 金刚藤胶囊结合头孢曲松钠和甲硝唑对慢性盆腔炎血清CRP、IL-6、IL-10和MMP-2水平的影响[J]. 中华中医药学刊,2021,39(11):182-185. [14] 郝玉珠,张洁洁. 金刚藤胶囊联合左氧氟沙星治疗慢性盆腔炎患者的效果[J]. 实用中西医结合临床,2023,23(4):29-32. [15] 胡开泰. 金刚藤胶囊联合甲硝唑对慢性盆腔炎患者炎症因子的影响[J]. 医药界,2019,4(8):49-49. [16] 乐丽莎. 金刚藤胶囊联合克林霉素磷酸酯治疗慢性盆腔炎的疗效及对血清炎症因子水平和血液流变学的影响[J]. 广西医科大学学报,2019,36(1):71-74. [17] 雷敏. 金刚藤胶囊治疗慢性盆腔炎的临床疗效观察[J]. 中文科技期刊数据库(全文版)医药卫生,2022,1(6):21-24. [18] 冷晓华. 司帕沙星与金刚藤胶囊对慢性盆腔炎患者的疗效分析[J]. 中国保健营养,2020,30(26):263-264. [19] 李春红,揭慧颖,揭长芳. 金刚藤胶囊联合左氧氟沙星及甲硝唑对慢性盆腔炎患者血清炎症介质的影响[J]. 医疗装备,2021,34(13):107-108. [20] 李海霞. 金刚藤软胶囊联合常规抗菌药物治疗慢性盆腔炎35例[J]. 中国药业,2015,24(12):88-89. [21] 莫培晖,兰代群,闫志强. 慢性盆腔炎患者辅助使用金刚藤治疗过程中体内微环境的变化及临床意义分析[J]. 中国性科学,2018,27(9):82-84. [22] 欧阳静. 金刚藤胶囊联合西药对慢性盆腔炎患者症状改善及血清CD4+/CD8+水平的影响[J]. 慢性病学杂志,2018,19(12):1753-1754. [23] 潘春芳,李小燕. 金刚藤胶囊联合阿奇霉素对慢性盆腔炎的治疗有效率及临床证候改善情况分析[J]. 中外女性健康研究,2021,11(22):62-63. doi: 10.3969/j.issn.2096-0417.2021.22.zwnxjkyj202122029 [24] 孙小梅. 金刚藤胶囊联合头孢菌素类抗菌药物及替硝唑治疗慢性盆腔炎患者的临床疗效[J]. 医学理论与实践,2021,34(3):466-467. [25] 王静. 金刚藤胶囊联合克林霉素磷酸酯治疗慢性盆腔炎患者的效果[J]. 中国民康医学,2021,33(7):77-79. doi: 10.3969/j.issn.1672-0369.2021.07.032 [26] 王文平,黄锦,敬巧,等. 金刚藤胶囊联合甲硝唑治疗对慢性盆腔炎患者效果、生活质量及炎性因子水平的影响[J]. 中外医学研究,2021,19(11):12-15. [27] 王文霞,白文佩. 金刚藤胶囊联合阿奇霉素治疗慢性盆腔炎的临床研究[J]. 现代药物与临床,2018,33(5):1164-1167. [28] 杨建美. 金刚藤胶囊联合头孢曲松钠、阿奇霉素治疗盆腔炎性疾病的临床效果分析[J]. 临床医药文献电子杂志,2020,7(87):140-140. [29] 尹燕,高彩云,席丽. 盐酸左氧氟沙星与金刚藤联合治疗盆腔炎的效果观察[J]. 齐齐哈尔医学院学报,2016,37(32):4053-4054. [30] 余月萍,白君. 金刚藤胶囊治疗慢性盆腔炎临床研究[J]. 新中医,2020,52(12):101-103. [31] 袁翀英,王雅丽. 金刚藤胶囊联合头孢美唑钠治疗慢性盆腔炎的临床研究[J]. 现代药物与临床,2020,35(8):1605-1608. [32] 朱文婷,梅玉英,李海琴. 金刚藤胶囊联合司帕沙星对慢性盆腔炎患者血清炎症因子水平及免疫功能的影响[J]. 临床医药实践,2020,29(11):817-820. [33] 王华斌. 桂枝茯苓丸辅治慢性盆腔炎疗效及对血液流变学、氧化应激和血清hs-CRP、TGF-β1、GM-CSF、补体C3水平的影响[J]. 中华中医药学刊,2020,38(2):214-217. [34] 贾利平,刘玉珠,周小飞. 中西医结合治疗慢性盆腔炎疗效观察及安全性分析[J]. 中华中医药学刊,2018,36(4):939-941. [35] 林华,刘永逸. 金刚藤化学成分及其质量控制分析方法研究概述[J]. 中国药物评价,2022,39(6):456-460. [36] 李筠,陈刚. 金刚藤胶囊对慢性盆腔炎大鼠盆腔粘连的作用及其药理机制[J]. 中药药理与临床,2020,36(1):144-149. [37] 梅明,谢岱,林世和,等. 金刚藤多糖的水提工艺及影响大鼠慢性盆腔炎血液流变研究[J]. 中国药师,2021,24(8):436-439. [38] 覃红珍,黄臻,刘晓琰,等. 金刚藤多糖对慢性盆腔炎大鼠的作用及机制[J]. 中国临床药理学杂志,2020,36(24):4039-4041,4053. [39] 邓高丕. 金刚藤胶囊治疗湿热瘀结型盆腔炎、附件炎的临床疗效观察[J]. 中药材,2007,(5):623-625. [40] 郭艳. 金刚藤胶囊治疗慢性盆腔炎疗效观察[J]. 中外妇儿健康,2011,19(7):37-39. [41] 任妮,翟凤霞,郭淼,等. 中成药辅助治疗湿热瘀结型盆腔炎性疾病后遗症有效性及安全性的网状Meta分析[J]. 现代中西医结合杂志,2022,31(4):532-539. -






 下载:
下载: