A Meta-analysis of the Efficacy and Safety of Camrelizumab Combined with Chemotherapy in the Treatment of Non-small Cell Lung Cancer
-
摘要:
目的 讨论免疫检查点抑制剂卡瑞利珠单独用药与联合化疗治疗非小细胞肺癌的疗效差异以及安全性,综合多个临床试验数据进行聚合分析,得到更准确的疗效及安全性评价。 方法 通过检索PubMed、Embase、Cochrane Library、CBM数据库、中国知网、维普中文数据库和万方数据库,收集建库至2023年11月30日发表的符合要求的随机化对照试验或非随机对照实验,提取数据后应用Revman5.4软件进行数据分析。按照治疗方案的不同,将研究对象分为卡瑞利珠联合化疗组和单独化疗组进行研究讨论。 结果 共纳入19篇文献,共计1545名患者。Meta分析结果显示:与单纯化疗相比,卡瑞利珠联合化疗治疗非小细胞肺癌能更有效的提高治疗总体有效率(OR = 2.50,95%CI:2.02~3.08,P < 0.00001),提高CD4+/CD8+比值(MD = 0.26,95%CI:0.19~0.33,P < 0.00001)以及有效降低血清肿瘤标志物CA125(MD =-10.65,95%CI:-14.34~-6.96,P < 0.00001)、CEA(MD = -5.56,95%CI:-7.64~-3.47,P < 0.00001)、CY211(MD = -2.17,95%CI:-3.22~-1.13,P < 0.00001)。不同不良反应表现不同聚类分析结果,其中卡瑞利珠联合化疗组相较于单独化疗组会增加贫血(OR = 1.95,95%CI:1.09~3.51,P = 0.03)、甲减(OR = 5.61,95%CI:1.82~17.25,P = 0.003)、毛细血管增多症(OR = 2.86,95%CI:1.19~6.88,P = 0.02)等症状的发生比例,差异有统计学意义(P < 0.05);但是皮疹(OR = 1.34,95%CI:0.82~2.16,P=0.24)、骨髓抑制(OR = 1.06,95%CI:0.56~2.02,P=0.86)、白细胞减少(OR = 0.78,95%CI:0.40~1.52,P = 0.47)、脱发(OR = 1.29,95%CI:0.57~2.92,P = 0.54)、神经异常(OR = 1.17,95%CI:0.39~3.56,P = 0.78)、消化道异常(OR = 1.10,95%CI:0.79~1.53,P = 0.57)、肝功异常(OR = 1.54,95%CI:0.92~2.59,P = 0.10)、恶心呕吐(OR = 1.16,95%CI:0.58~2.31,P = 0.67)、咳血(OR = 0.87,95%CI:0.30~2.49,P = 0.79)、发热(OR = 1.22,95%CI:0.65~2.30,P = 0.54)及其他症状(OR = 1.32,95%CI:0.76~2.31,P = 0.32)的发生率没有明显变化,差异无统计学意义(P > 0.05)。综合上述各类不良反应发生率,从总体上看,卡瑞利珠联合化疗相较于单独化疗并不会提高不良反应发生率(OR = 1.32,95%CI:1.13~1.55,P = 0.23),差异无统计学意义(P > 0.05)。 结论 卡瑞利珠联合化疗方案相较于单独化疗方案而言,能更有效的提高非小细胞肺癌患者总体缓解率和CD4+/CD8+比值,降低血清肿瘤标志物绝对值,不会升高不良反应发生率,安全性较好。 Abstract:Objective To discuss the difference in efficacy and safety of immune checkpoint inhibitor camrelizumab alone and combined chemotherapy in the treatment of non-small cell lung cancer. Aggregate analysis of multiple clinical trial data was conducted to obtain more accurate efficacy and safety evaluation, and bring effective information and medication guidance to clinical patients. Methods By searching PubMed, Embase, Cochrane Library, CBM database, CNKI, VIP Chinese database and Wanfang database, we collected the required randomized controlled trials or non-randomized controlled trials published until November 30, 2023. After data extraction, Revman5.4 software was applied for data analysis. According to the different treatment plan, the study subjects were divided into camrelizumab combined chemotherapy group and chemotherapy group alone for research discussion. Results A total of 19 articles were included, with a total of 1545 patients. Meta results showed: compared with chemotherapy alone, camrelizumab combined with chemotherapy in the treatment of non-small lung cancer was more effective in improving the overall response rate (OR = 2.50, 95%CI:2.02~3.08, P < 0.00001), increased the CD4+/CD8+ ratio (MD = 0.26, 95%CI:0.19~0.33, P < 0.00001) and effectively reduced the serum tumor marker CA125 (MD = -10.65, 95%CI:-14.34~-6.96, P < 0.00001) and CEA (MD = 5.56, 95%CI:-7.64~-3.47, P < 0.00001), CY211 (MD = -2.17, 95%CI:-3.22~1.13, P = 0.00001). Different adverse reactions showed different cluster analysis results. Among them, camrelizumab combined chemotherapy increased anemia (OR = 1.95, 95%CI:1.09~3.51, P = 0.03), hypothyroidism (OR = 5.61, 95%CI:1.82~17.25, P = 0.003) and capillary hyperplasia (OR = 2.86, 95%CI:1.19~6.88, P = 0.02) compared with chemotherapy alone, P values were all < 0.05, and the difference was statistically significant. However, rash (OR = 1.34, 95%CI:0.82~2.16, P = 0.24), myelosuppression (OR = 1.06, 95%CI:0.56~2.02, P = 0.86), leukopenia (OR = 0.78, 95%CI:0.40~1.52, P = 0.47), alopecia (OR = 1.29, 95%CI:0.57~2.92, P = 0.54), neurological abnormalities (OR = 1.17, 95%CI:0.39~3.56, P = 0.78), digestive tract abnormalities (OR = 1.10, 95%CI:0.79~1.53, P = 0.57), liver function abnormalities (OR = 1.54, 95%CI:0.92~2.59, P = 0.10), nausea and vomiting (OR = 1.16, 95%CI:0.58~2.31, P = 0.67), coughing up blood (OR = 0.87, 95%CI:0.30~2.49, P = 0.79), fever(OR = 1.22, 95%CI:0.65~2.30, P = 0.54) and others (OR = 1.32, 95%CI:0.76~2.31, P = 0.32) had no significant change in the incidence of symptoms, and all P values were greater than 0.05, the difference was not statistically significant. Taking into account the incidence of all kinds of adverse reactions mentioned above, in general, camrelizumab combined chemotherapy did not increase the incidence of adverse reactions compared with chemotherapy alone (OR = 1.32, 95%CI:1.13~1.55, P = 0.23), with a P value greater than 0.05, and the difference was not statistically significant. Conclusion Compared with chemotherapy alone, camrelizumab combined chemotherapy can more effectively improve the overall response rate and CD4+/CD8+ ratio in patients with non-small cell lung cancer, reduce the absolute value of serum tumor markers, and does not increase the incidence of adverse reactions, with good safety. -
Key words:
- Camrelizumab /
- Non-small cell lung cancer /
- Combination therapy /
- Chemotherapy /
- Meta-analysis /
- PD-1 inhibitors
-
肺癌至今仍是全球癌症死亡的主要原因,其死亡人数占癌症死亡总数的18.0%[1]。非小细胞肺癌患者人数占肺癌总人数的80%~85%,早期症状不明显,大多数在确诊时已到中晚期。在过去手术、放疗、化疗及靶向治疗是主要治疗方案,随着对非小细胞肺癌免疫机制研究的深入,免疫治疗逐渐进入人们视野[2]。免疫检查点抑制剂为非小细胞肺癌患者带来了新的治疗方案,其中程序性细胞死亡配体1(programmed cell death ligand 1,PD-L1)检查点抑制剂在经大量预处理的非小细胞肺癌患者中表现出明显效果[3]。卡瑞利珠是近期获批的程序性细胞死亡受体1(programmed cell death protein 1,PD-1)抑制剂,它在霍奇金淋巴瘤、肝细胞癌、肺癌和食管鳞状细胞癌中表现出了良好的临床获益和可接受的安全性[4]。目前,免疫检查点抑制剂联合化疗治疗非小细胞肺癌的重要性逐步提升,而卡瑞利珠获批时间较短,相关研究较少,并且在不同研究中,安全性出现不同研究结果,所以本文采用Meta分析方法,就纳入文献讨论卡瑞利珠联合化疗对比单独化疗是否能更有效的提高总体有效率、CD4+/CD8+比值,降低血清肿瘤标志物数值和不良反应发生比例进行讨论,通过聚类分析,达到扩大样本量的目的,从而更加客观的为临床患者获益提供更多理论依据。
1. 资料与方法
1.1 资料来源
检索PubMed、EmBase、Cochrane Library、CBM数据库、中国知网、维普中文数据库和万方数据库,文献语种限制为中文和英文,检索年限为建库至2023年11月,末次检索时间为2023年11月30日。中文检索式为“(卡瑞利珠or卡瑞丽珠) and 非小细胞肺癌”;英文检索式为(Carcinoma,Non-Small-Cell Lung or Carcinoma,Non Small Cell Lung or Carcinomas,Non-Small-Cell Lung or Lung Carcinoma,Non-Small-Cell or Lung Carcinomas,Non-Small-Cell or Non-Small-Cell Lung Carcinomas or Non-Small-Cell Lung Carcinoma or Non Small Cell Lung Carcinoma or Carcinoma,Non-Small Cell Lung or Non-Small Cell Lung Carcinoma or Non-Small Cell Lung Cancer or Nonsmall Cell Lung Cancer) AND (carrelizumabor SHR-1210or SHR 1210 or camrelizumab[Supplementary Concept])。使用Endnote X9软件进行文献管理。
1.2 纳入及排除标准
文献纳入标准[5]:(1)研究对象:病理学或多项影像学检查确诊为NSCLC的患者,年龄、种族、国籍、性别不限;(2)干预措施:涉及卡瑞利珠联合化疗治疗非小细胞肺癌;(3)研究观察指标涉及总体有效率、CD4+/CD8+比值、血清肿瘤标志物数值、不良反应发生比例;(4)研究类型:各数据库建库至2023年11月30日所发表的随机对照实验或非随机对照实验。
排除标准[5]:(1)重复文献、研究对象不符合,文献质量较差无法提取有效数据的文献;(2)综述、病案个例、评论类文献;(3)单臂实验;(4)实验中仅有单独用药,未涉及卡瑞利珠联合化疗治疗方案;(5)实验对象仅涉及某一种类型、某一年龄段。
1.3 质量评价
使用Revman 5.4自带的Cochorane风险评价工具对文献进行评价。为判断是否存在偏倚及其影响程度,从以下几方面对纳入文献进行质量评估:(1)样本序列产生是否使用随机序列;(2)是否有分配隐藏;(3)实验过程中是否有盲法;(4)实验结果中是否有不完整数据;(5)是否有选择性结局报道;(6)其他方面:包括样本数量、实验设计等。评价过程由2位评议员独立完成,不一致时通过讨论解决,仍有争议时请专家评议。
1.4 数据提取
2位研究者分别提取文献相关资料,资料提取内容包括作者、报道时间、治疗方案及药物、分组人数及基线情况、总体有效率、血清肿瘤标记物治疗前后数值、T淋巴细胞(CD4+/CD8+)治疗前后比值以及不良情况发生率。
1.5 统计学处理
采用RevMan5.4软件进行统计学分析。异质性检验显示同质性较好的研究(P > 0.1或I 2<50%),采用固定效应模型分析,反之采用随机效应模型分析。计数资料计算比值比(odds ratio,OR)及95%CI,当P < 0.05且95%CI不包含1时,认为差异有统计学意义。计量资料计算加权均数差值及95%CI,当P < 0.05且95%CI不包含0时,认为差异有统计学意义。绘制漏斗图分析发表偏倚,如果漏斗图的完整度和对称度较好则说明发表偏倚较小。
2. 结果
2.1 检索结果
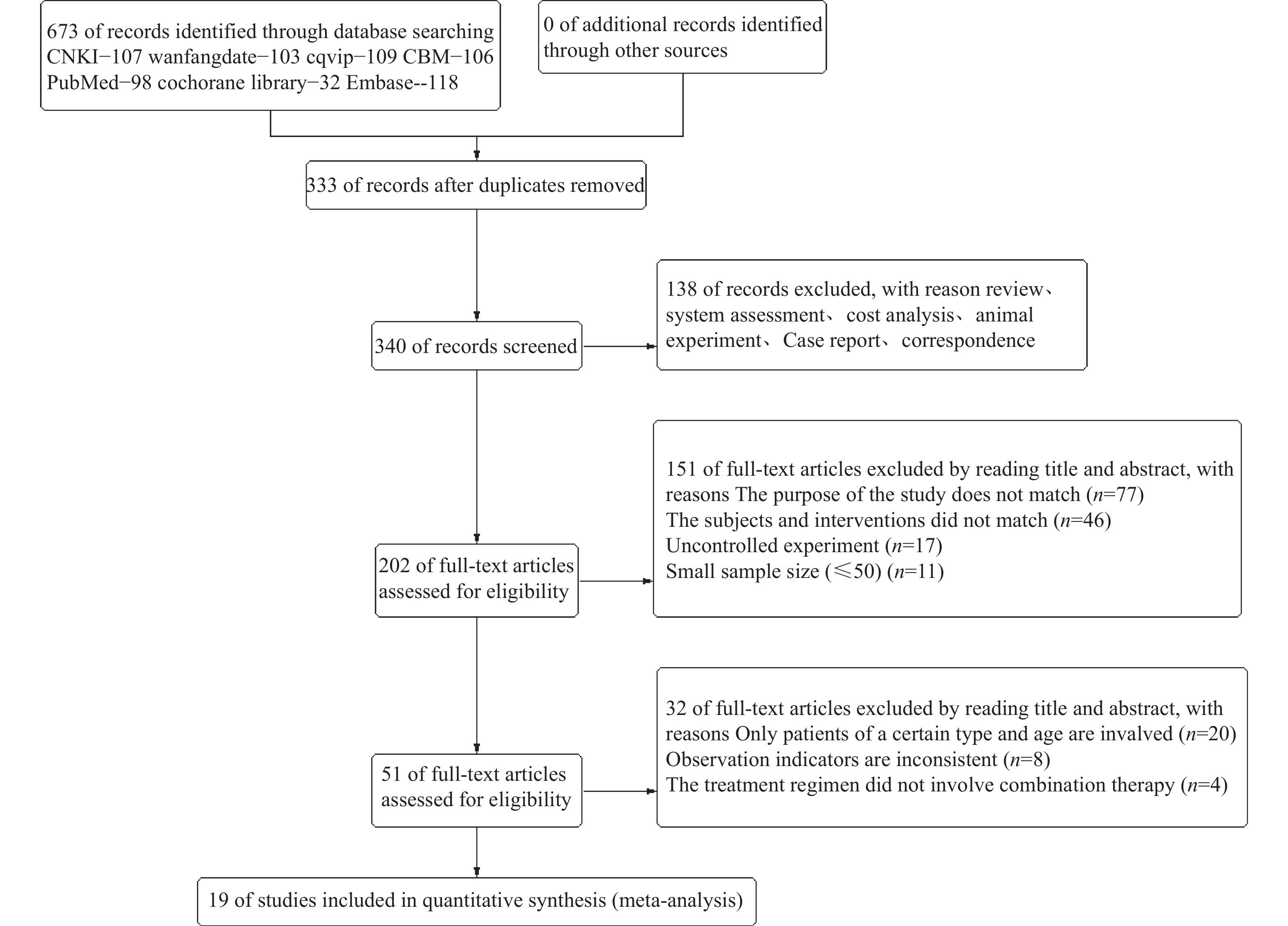
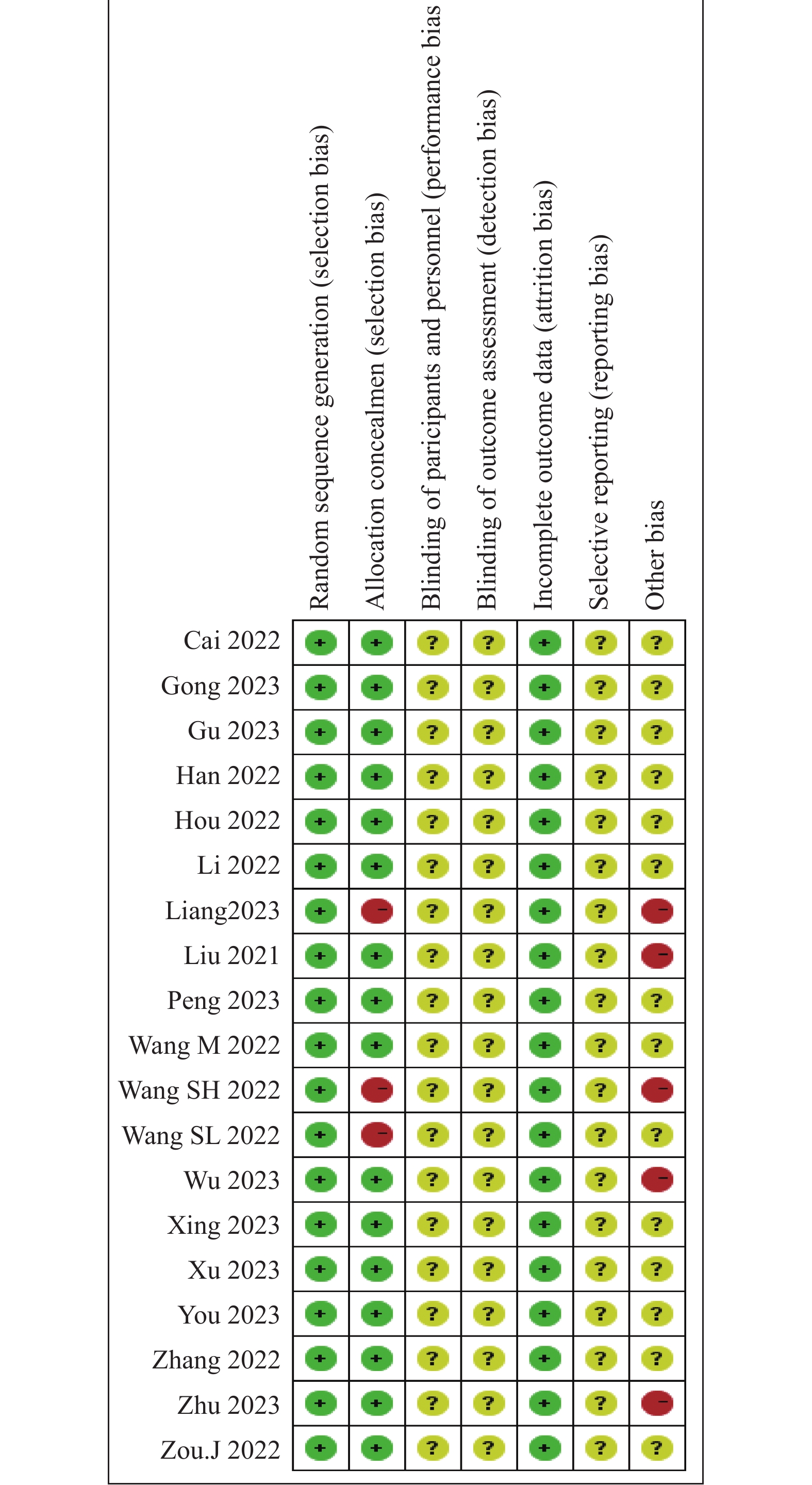
根据检索关键词检索到相关文献673篇,其中相关中文文献425篇,英文文献248篇。使用Endnote X9软件查重以及手工查重后,排除333篇重复文献。按照参考文献纳入和排除标准,排除综述、系统评价、信件往来、Meta分析等138篇文献,通过阅读标题和摘要后,排除研究目的不符、研究对象或干预措施不符合、无对照实验及样本数量较小(≤50)的文献151篇,后通过阅读全文,排除实验对象仅涉及某一类型或某一年龄段、观察指标不一及实验治疗方案未涉及联合治疗的文献32篇,共筛出19篇文献进行Meta分析,包括中文文献18篇,英文文献1篇,见图1,累计1545名研究对象,纳入研究的文献中患者年龄、性别、分期等基线信息的差异均无统计学意义(P > 0.05),各研究特点和情况见表1。使用Revman5.4自带的Cochorane风险评价工具对纳入文献进行评价,根据样本序列产生是否使用随机序列、是否有分配隐藏、实验过程中是否有盲法、实验结果中是否有不完整数据、是否有选择性结局报道以及样本数量、实验设计等其他方面等进行评价,纳入文献中有6篇文献存在高风险,其余文献风险较低,文献质量较好,见图2。
表 1 纳入研究的一般情况($\bar x \pm s $)Table 1. Characteristics of included studies ($\bar x \pm s $)文献 n 年龄(岁) 性别 干预措施 观察指标 实验组 对照组 实验组 对照组 实验组 对照组 实验组 对照组 Cai 2022[6] 55 55 59.61±3.48 59.49±3.54 男:36
女:19男:33
女:22培美曲塞二钠+
顺铂+卡瑞利珠培美曲塞二钠+
顺铂总体有效率、CA125、CEA Gong 2023[7] 34 34 59.96±9.81 58.74±9.12 男:21
女:13男:20
女:14紫杉醇+卡铂+
卡瑞利珠紫杉醇+
卡铂总体有效率、CA125、CY211 Gu 2023[8] 42 43 60.62±4.42 60.58±4.36 男:24
女:18男:26
女:17培美曲塞+顺铂+
卡瑞利珠培美曲塞+
顺铂总体有效率、CA125、CY211、CEA、CD4+/CD8+ Han 2022[9] 40 40 63.52±8.60 64.18±6.42 男:23
女:17男:25
女:15培美曲塞+顺铂+
卡瑞利珠培美曲塞+
顺铂总体有效率、CD4+/CD8+ Hou 2022[10] 42 42 64.87±3.80 65.10±3.19 男:23
女:19男:22
女:20顺铂+多西他赛+
卡瑞利珠顺铂+
多西他赛总体有效率、CA125、CEA Li 2022[11] 35 35 63.72±5.51 63.64±5.39 男:20
女:15男:19
女:16紫杉醇、长春瑞滨、吉西他滨+顺铂化疗+卡瑞利珠 紫杉醇、长春
瑞滨、吉西
他滨+顺铂
化疗总体有效率、CA125、CEA、CY211、CD4+/CD8+ Liang
2023[12]29 30 65.78±6.25 65.62±6.12 男:19
女:10男:18
女:12培美曲塞+顺铂治疗+卡瑞利珠 培美曲塞+顺铂 总体有效率、CA125、CEA、CD4+/CD8+ Liu 2021[13] 31 29 64.57±10.41 65.02±10.68 男:19
女:12男:20
女:9紫杉醇、长春瑞滨、吉西他滨+顺铂化疗+卡瑞利珠 紫杉醇、长春
瑞滨、吉西
他滨+顺铂
化疗总体有效率、CD4+/CD8+ Peng 2023[14] 100 100 60.31±5.31 60.22±5.29 男:58
女:42男:56
女:44多西他赛 + 顺铂+卡瑞利珠 多西他赛 + 顺铂 总体有效率、CD4+/CD8+ Wang M 2022[15] 32 32 61.74±6.21 61.38±6.05 男:18
女:14男:17
女:15紫杉醇、长春瑞滨、吉西他滨+顺铂+
卡瑞利珠紫杉醇、长春瑞
滨、吉西他滨+
顺铂总体有效率、CD4+/CD8+ Wang SH 2022[16] 50 50 63.52±6.83 63.86±6.93 男:31
女:19男:30
女:20紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率、CA125、CY211 Wang SL[17] 40 40 65.85±5.35 65.14±5.61 男:29
女:11男:27
女:13吉西他滨+铂类+
卡瑞利珠吉西他滨+铂类 总体有效率、CA125、CEA、CY211 Wu 2023[18] 30 30 / / / / 培美曲塞+铂类+
卡瑞利珠培美曲塞+铂类 总体有效率 Xing 2023[19] 35 35 68.56±8.96 67.49±8.11 男:20
女:15男:18
女:17培美曲塞+铂类+
卡瑞利珠培美曲塞+铂类 总体有效率、CA125、CY211、CD4+/CD8+ Xu 2023[20] 51 51 55.12±3.88 56.58±4.21 男:25
女:26男:24
女:27紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率、 You 2023[21] 51 51 65.39±9.00 62.06±9.82 男:34
女:17男:33
女:18紫杉醇+顺铂+
卡瑞利珠紫杉醇+顺铂 总体有效率CA125、CEA、CD4+/CD8+ Zhang 2022[22] 40 40 55.84±5.27 56.27±5.43 男:27
女:13男:25
女:15紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率、CA125、CY211、CEA、CD4+/CD8+ Zhu 2023[23] 25 26 60.38±9.41 59.55±4.62 男:13
女:12男:15
女:11多西他赛+
卡瑞利珠多西他赛 总体有效率 Zou.J 2022[24] 50 50 65.82±14.02 67.12±12.41 男:37
女:13男:32
女:18紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率 2.2 总体有效率
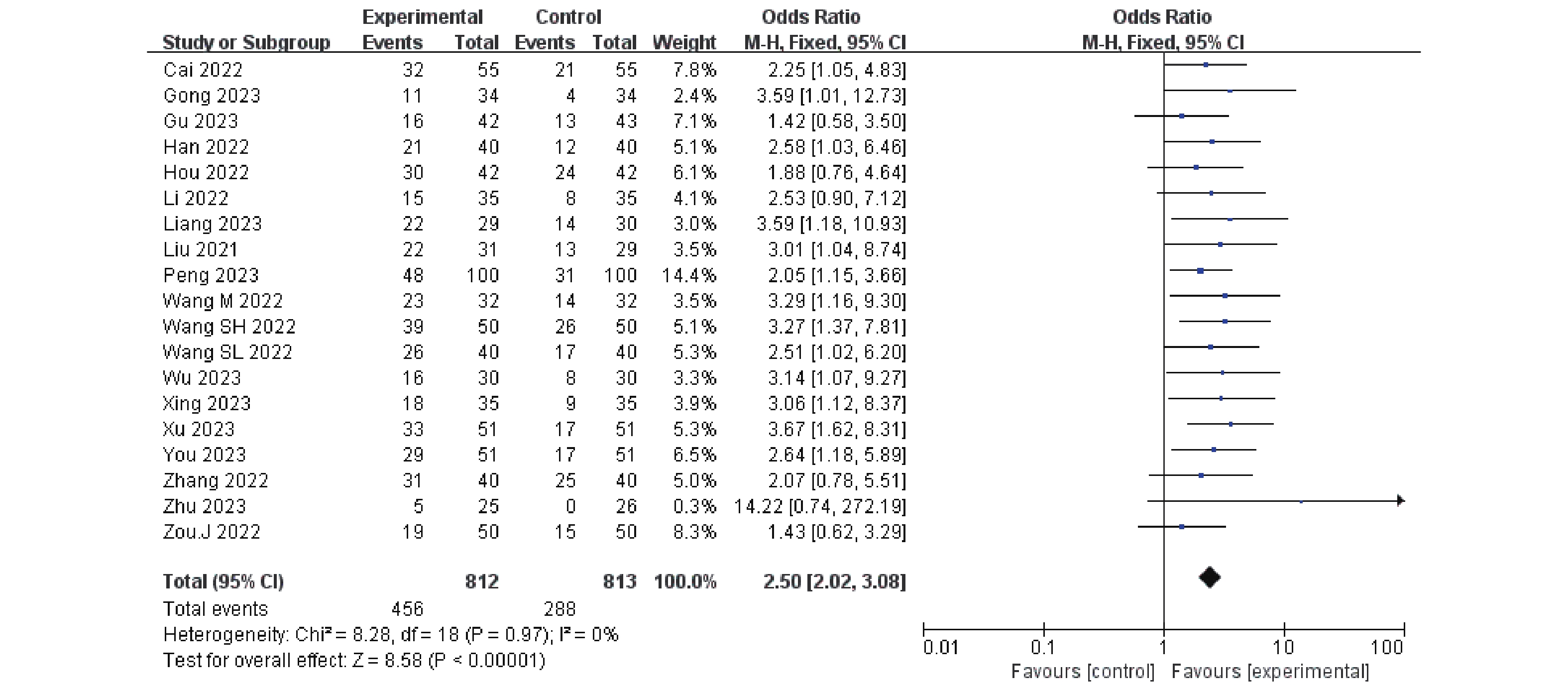
纳入文献中19项研究[6−24]均提及总体有效率指标,由于I 2<50%,同质性较好,采用固定效应模型。结果显示,卡瑞利珠联合化疗组总体有效率高于单独治疗组,OR = 2.50(95%CI:2.02~3.08,P < 0.00001),P < 0.05,差异具有统计学意义,见图3。
2.3 CD4+/CD8+比值
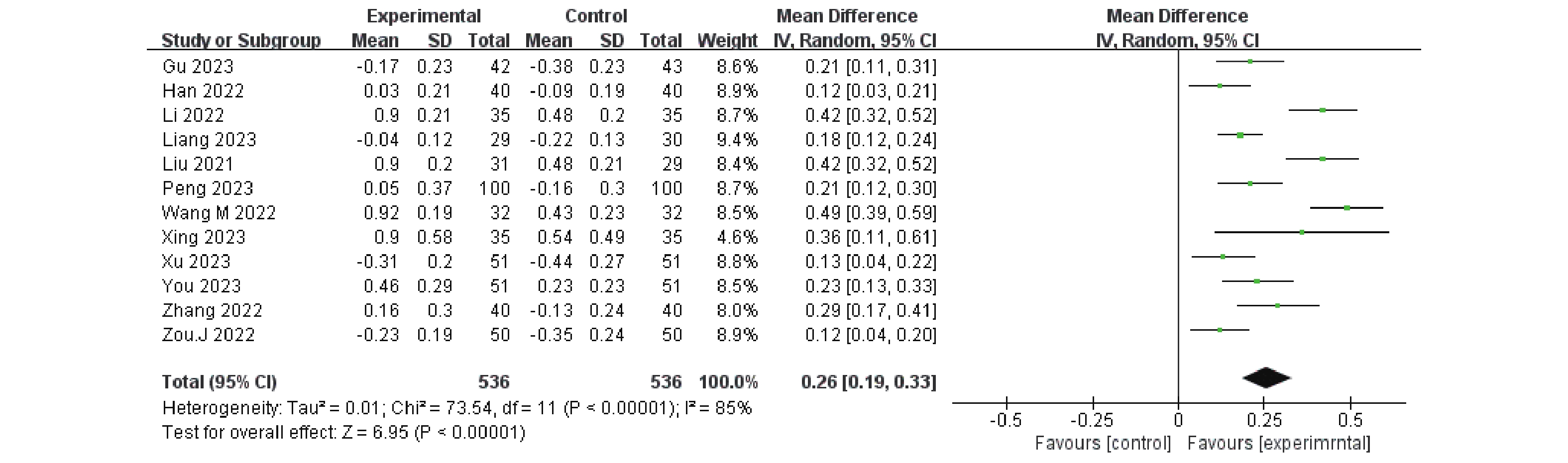
12项研究[8−9,11−13,15,19−24]报道了CD4+/CD8+比值,治疗前后差值由循证医学数据提取换算公式计算而得。I 2>50%,异质性较大,采用随机效应模型。结果显示,卡瑞利珠联合化疗相较于单独化疗能更有效的提高CD4+/CD8+比值,MD = 0.26(95%CI:0.19~0.33,P < 0.00001),P < 0.05,差异具有统计学意义,见图4。
2.4 血清肿瘤标志物
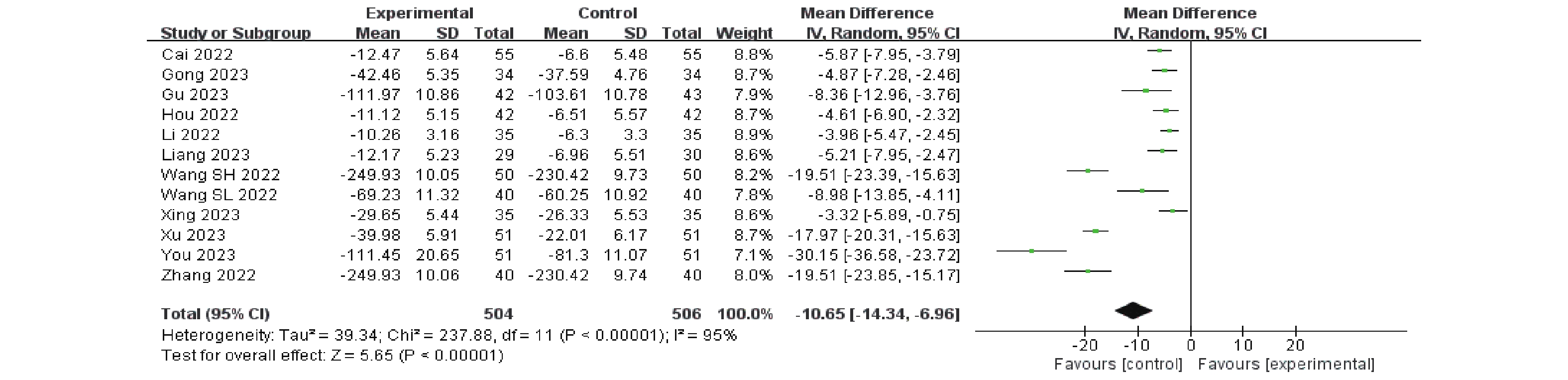
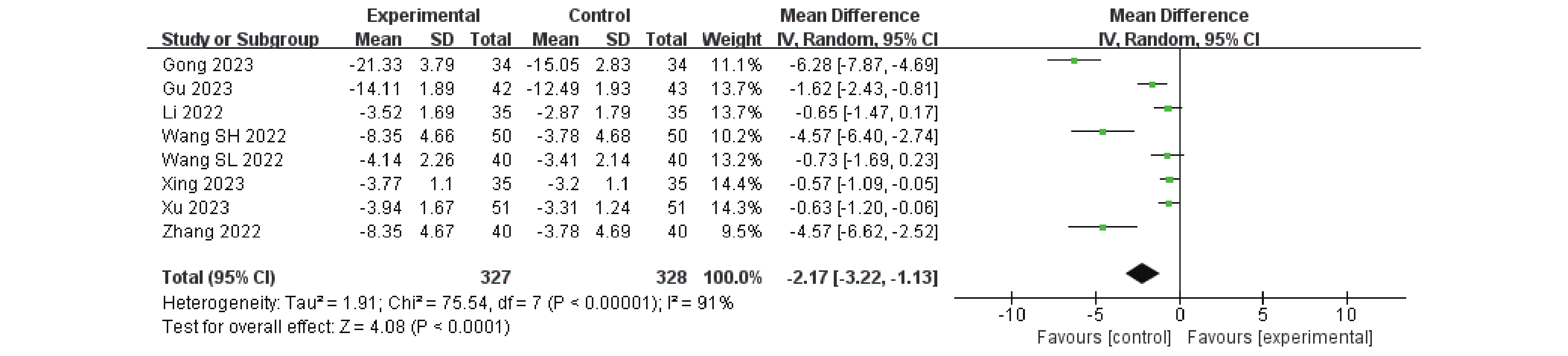
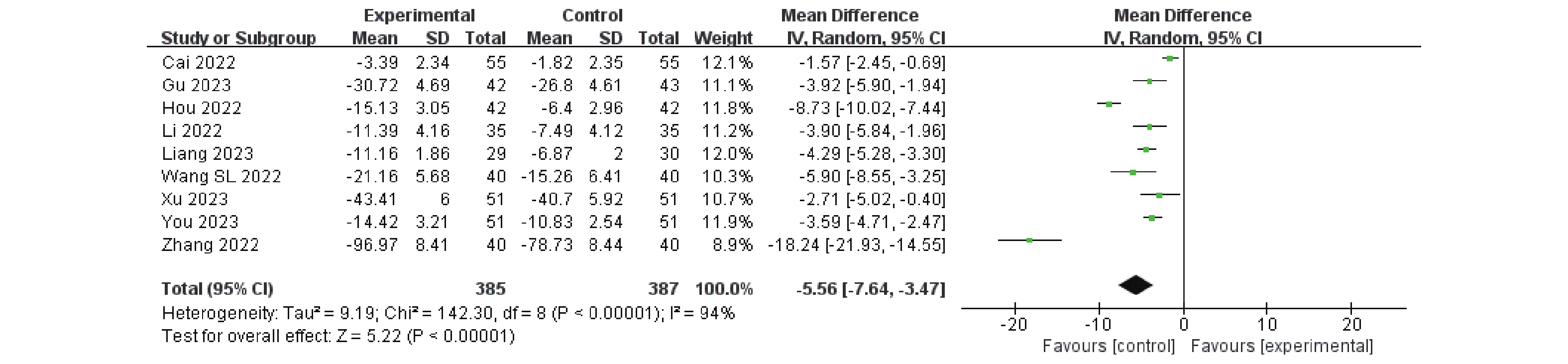
纳入的研究中有12项研究[6−8,10−12,16−17,19−22]报道了CA125数值,9项研究[6,8,10−12,17,20−22]报道了CEA数值,8项研究[7−8,11,16−17,19−21]报道了CY211数值,治疗前后差值由循证医学数据提取换算公式计算而得。I2均>50%,异质性较大,均采用随机效应模型。结果显示,卡瑞利珠联合化疗相较于单独化疗能更有效的降低血清肿瘤标志物CA125(MD = -10.65,95%CI:-14.34~-6.96,P < 0.00001)、CEA(MD = -5.56,95%CI:-7.64~-3.47,P < 0.00001)、CY211(MD = -2,95%CI:-3.22~-1.13,P < 0.00001)数值,P < 0.05,差异具有统计学意义,见图5~7。
2.5 不良反应
纳入研究中报道的不良反应主要包括皮疹、贫血、消化道反应、骨髓抑制、恶心呕吐、白细胞减少及发热等,根据不良反应的类型进行亚组讨论。由于总体I 2<50%,采用固定效应模型。结果显示,卡瑞利珠联合化疗组相较于单独化疗组会引起贫血(OR = 1.95,95%CI:1.09~3.51,P = 0.03)、甲减(OR = 5.61,95%CI:1.82~17.25,P = 0.003)、毛细血管增多症(OR = 2.86,95%CI:1.19~6.88,P = 0.02)等症状的发生比例,P均<0.05,差异具有统计学意义;但是皮疹(OR = 1.34,95%CI:0.82~2.16,P = 0.24)、骨髓抑制(OR = 1.06,95%CI:0.56~2.02,P = 0.86)、白细胞减少(OR = 0.78,95%CI:0.40~1.52,P = 0.47)、脱发(OR = 1.29,95%CI:0.57~2.92,P = 0.54)、神经异常(OR = 1.17,95%CI:0.39~3.56,P = 0.78)、消化道异常(OR = 1.10,95%CI:0.79~1.53,P = 0.57)、肝功异常(OR = 1.54,95%CI:0.92~2.59,P = 0.10)、恶心呕吐(OR = 1.16,95%CI:0.58~2.31,P = 0.67)、咳血(OR = 0.87,95%CI:0.30~2.49,P = 0.79)、发热(OR = 1.22,95%CI:0.65~2.30,P = 0.54)、其他(OR = 1.32,95%CI:0.76~2.31,P = 0.32)症状的发生率没有明显变化,P均大于0.05,差异不具有统计学意义。综合上述各类不良反应发生率,从总体上看,卡瑞利珠联合化疗相较于单独化疗并不会提高不良反应发生率(OR = 1.32,95%CI:1.13~1.55,P = 0.23),P > 0.05,差异不具有统计学意义,见图8。
2.6 发表偏倚分析
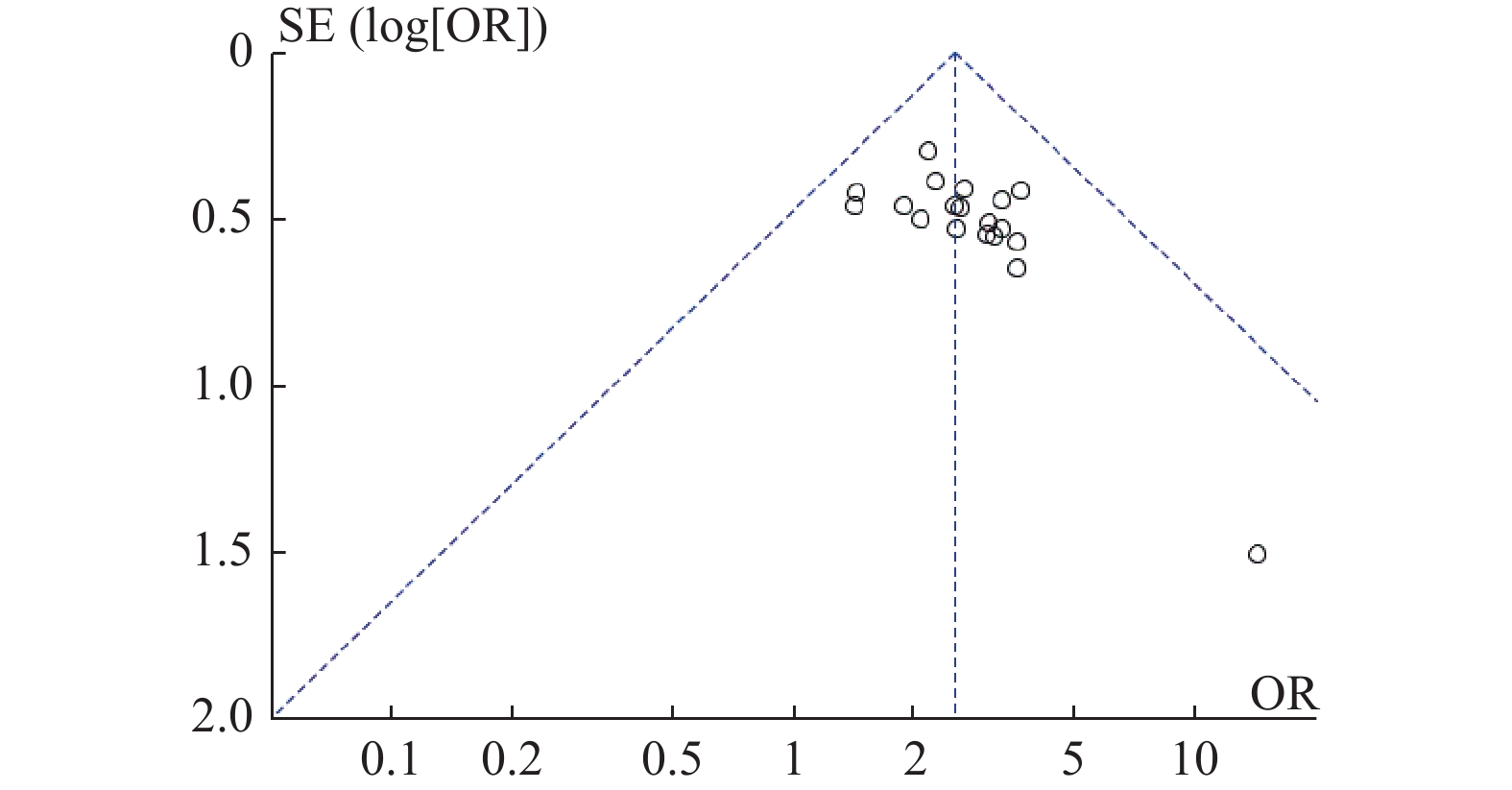
使用RevMan5.4软件绘制漏斗图,非小细胞肺癌患者总体有效率的漏斗图显示,图形并不完全对称;去除朱宇宏等[23]的研究后,漏斗图基本对称,提示此文献与其他文献相比可能存在较大的异质性,见图9。
3. 讨论
3.1 卡瑞利珠现状分析
随着对非小细胞肺癌免疫机制的研究逐渐深入,免疫治疗及其联合治疗方案逐步成为研究热点,但是因为免疫单药治疗效果并不明显,所以研究更多关注联合治疗[25]。卡瑞利珠单抗是中国自主研发的人源化单克隆程序性细胞死亡蛋白-1抗体,可以阻断PD-1与PD-L1之间的结合,达到治疗非小细胞肺癌的效果[26]。但是由于卡瑞利珠用于临床时间较短,还需要大量研究探讨其疗效及安全性。本文采用Meta分析的方法,纳入19项研究,共计1545名研究对象,一定程度上填补了卡瑞利珠研究的空白点,不仅对之后卡瑞利珠的研究提供理论依据,更为临床患者更好获益提供了数据支撑。
3.2 卡瑞利珠联合化疗影响患者治疗的有效性及安全性
本研究对患者疗效的观察从总体有效率、CD4+/CD8+比值、血清肿瘤标志物和不良反应发生率等多个不同角度进行全面分析。总体有效率能直观的反应患者临床疗效,结果显示,卡瑞利珠联合组的总体有效率较单独化疗组升高了19.51%(OR = 2.50,95%CI:2.02~3.08,P < 0.00001),P < 0.05,差异具有统计学意义,直观说明卡瑞利珠联合化疗可以提高非小细胞肺癌患者临床总体有效率。T淋巴细胞在非小细胞肺癌患者中异常表达,CD4+/CD8+比值低于正常人,免疫系统受损,在治疗过程中,CD4+/CD8+比值升高变化可以预测患者疗效及预后[27],本研究通过循证医学数据提取换算公式计算出治疗前后CD4+/CD8+比值差值,经统计分析得卡瑞利珠联合化疗组相较于单独化疗组能更加有效的升高CD4+/CD8+比值(MD = 0.26,95%CI:0.19~0.33,P < 0.00001),P < 0.05,差异具有统计学意义,说明卡瑞利珠联合组能更有效的恢复患者免疫功能,为患者带来更好预后。有研究[28]表明,血清肿瘤标志物CA125、CEA、CY211等能够有效提示非小细胞肺癌患者预后情况,其数值减小与良好预后相关联。本研究通过循证医学数据提取换算公式计算出治疗前后肿瘤标志物CA125、CEA、CY211的差值,经统计分析后可见,卡瑞利珠联合组能更加有效的降低血清肿瘤标志物CA125(MD = -10.65,95%CI:-14.34~-6.96,P < 0.00001)、CEA(MD = -5.56,95%CI:-7.64~-3.47,P < 0.00001)、CY211(MD = -2.17,95%CI:-3.22~-1.13,P < 0.00001)数值,P均<0.05,差异具有统计学意义。这也就说明卡瑞利珠联合组可以为非小细胞肺癌患者带来更好预后效果。纳入文献中,邢磊等[19]的研究中提到不同种类不良反应呈现的P值并不相同,其文章中提到组间贫血、皮疹、肝功异常等均无统计学差异(P > 0.05),而甲减、毛细血管增多症的发生率差异具有统计学意义(P < 0.05),所以本研究就纳入文献所提及的不良反应进行亚组分析,以寻求对卡瑞利珠联合化疗的安全性更客观的评价。结果显示,卡瑞利珠联合化疗会增加贫血、甲减和毛细血管增多症的发生率,但不会增加骨髓抑制、脱发、消化道反应等不良反应的发生率,综合纳入文献所提及的各类不良反应,从总体而言,卡瑞利珠联合化疗不会增加不良反应发生率(OR = 1.32,95%CI:1.13~1.55,P = 0.23),有较好的安全性。
3.3 研究创新性与不足
以上研究结果与丁振兴[29]等的研究结果一致,卡瑞利珠联合化疗能有效的提高总体有效率和免疫功能,降低血清肿瘤标志物,为患者获得更好预后。丁振兴等[29]的研究更偏向于有效性的研究,而本研究更注重对安全性的评价,将纳入文献涉及的各类不良反应进行亚组分析,2项Meta分析互相补充。且丁振兴等[29]的研究中纳入文献有两篇的研究对象仅为非鳞非小细胞肺癌,未排除肺癌类型对治疗效果是否有影响的可能性,本文纳入文献时,排除了仅涉及某一年龄段及某一类型的文献,消除了年龄及肺癌类型对研究的影响,使结果更准确客观。但丁振兴等[29]的研究及本研究所纳入的研究中,仅有1项研究[24]涉及到非中国人种,人种因素和地域因素的影响还需要更多临床研究讨论验证,此外卡瑞利珠联合化疗方案实施时的化疗方案、用药方式、剂量多少等方面对疗效的影响还需进一步的讨论,从而更好地为非小细胞肺癌患者找到更有效更安全的治疗方案。
综上所述,卡瑞利珠联合化疗可以为临床非小细胞肺癌患者带来更好临床获益,总体上并不会升高不良反应发生率,具有相对较好的安全性。由此可见,卡瑞利珠联合化疗不失为一种有效的联合治疗方案。
-
表 1 纳入研究的一般情况($\bar x \pm s $)
Table 1. Characteristics of included studies ($\bar x \pm s $)
文献 n 年龄(岁) 性别 干预措施 观察指标 实验组 对照组 实验组 对照组 实验组 对照组 实验组 对照组 Cai 2022[6] 55 55 59.61±3.48 59.49±3.54 男:36
女:19男:33
女:22培美曲塞二钠+
顺铂+卡瑞利珠培美曲塞二钠+
顺铂总体有效率、CA125、CEA Gong 2023[7] 34 34 59.96±9.81 58.74±9.12 男:21
女:13男:20
女:14紫杉醇+卡铂+
卡瑞利珠紫杉醇+
卡铂总体有效率、CA125、CY211 Gu 2023[8] 42 43 60.62±4.42 60.58±4.36 男:24
女:18男:26
女:17培美曲塞+顺铂+
卡瑞利珠培美曲塞+
顺铂总体有效率、CA125、CY211、CEA、CD4+/CD8+ Han 2022[9] 40 40 63.52±8.60 64.18±6.42 男:23
女:17男:25
女:15培美曲塞+顺铂+
卡瑞利珠培美曲塞+
顺铂总体有效率、CD4+/CD8+ Hou 2022[10] 42 42 64.87±3.80 65.10±3.19 男:23
女:19男:22
女:20顺铂+多西他赛+
卡瑞利珠顺铂+
多西他赛总体有效率、CA125、CEA Li 2022[11] 35 35 63.72±5.51 63.64±5.39 男:20
女:15男:19
女:16紫杉醇、长春瑞滨、吉西他滨+顺铂化疗+卡瑞利珠 紫杉醇、长春
瑞滨、吉西
他滨+顺铂
化疗总体有效率、CA125、CEA、CY211、CD4+/CD8+ Liang
2023[12]29 30 65.78±6.25 65.62±6.12 男:19
女:10男:18
女:12培美曲塞+顺铂治疗+卡瑞利珠 培美曲塞+顺铂 总体有效率、CA125、CEA、CD4+/CD8+ Liu 2021[13] 31 29 64.57±10.41 65.02±10.68 男:19
女:12男:20
女:9紫杉醇、长春瑞滨、吉西他滨+顺铂化疗+卡瑞利珠 紫杉醇、长春
瑞滨、吉西
他滨+顺铂
化疗总体有效率、CD4+/CD8+ Peng 2023[14] 100 100 60.31±5.31 60.22±5.29 男:58
女:42男:56
女:44多西他赛 + 顺铂+卡瑞利珠 多西他赛 + 顺铂 总体有效率、CD4+/CD8+ Wang M 2022[15] 32 32 61.74±6.21 61.38±6.05 男:18
女:14男:17
女:15紫杉醇、长春瑞滨、吉西他滨+顺铂+
卡瑞利珠紫杉醇、长春瑞
滨、吉西他滨+
顺铂总体有效率、CD4+/CD8+ Wang SH 2022[16] 50 50 63.52±6.83 63.86±6.93 男:31
女:19男:30
女:20紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率、CA125、CY211 Wang SL[17] 40 40 65.85±5.35 65.14±5.61 男:29
女:11男:27
女:13吉西他滨+铂类+
卡瑞利珠吉西他滨+铂类 总体有效率、CA125、CEA、CY211 Wu 2023[18] 30 30 / / / / 培美曲塞+铂类+
卡瑞利珠培美曲塞+铂类 总体有效率 Xing 2023[19] 35 35 68.56±8.96 67.49±8.11 男:20
女:15男:18
女:17培美曲塞+铂类+
卡瑞利珠培美曲塞+铂类 总体有效率、CA125、CY211、CD4+/CD8+ Xu 2023[20] 51 51 55.12±3.88 56.58±4.21 男:25
女:26男:24
女:27紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率、 You 2023[21] 51 51 65.39±9.00 62.06±9.82 男:34
女:17男:33
女:18紫杉醇+顺铂+
卡瑞利珠紫杉醇+顺铂 总体有效率CA125、CEA、CD4+/CD8+ Zhang 2022[22] 40 40 55.84±5.27 56.27±5.43 男:27
女:13男:25
女:15紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率、CA125、CY211、CEA、CD4+/CD8+ Zhu 2023[23] 25 26 60.38±9.41 59.55±4.62 男:13
女:12男:15
女:11多西他赛+
卡瑞利珠多西他赛 总体有效率 Zou.J 2022[24] 50 50 65.82±14.02 67.12±12.41 男:37
女:13男:32
女:18紫杉醇+卡铂+
卡瑞利珠紫杉醇+卡铂 总体有效率 -
[1] Sung H,Ferlay J,Siegel R L,et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2021,71(3):209-249. [2] Chen P,Liu Y,Wen Y,et al. Non-small cell lung cancer in China[J]. Cancer Commun (Lond),2022,42(10):937-970. [3] Brahmer J R,Pardoll D M. Immune checkpoint inhibitors: Making immunotherapy a reality for the treatment of lung cancer[J]. Cancer Immunol Res,2013,1(2):85-91. [4] Markham A,Keam S J. Camrelizumab: First Global Approval[J]. Drugs,2019,79(12):1355-1361. [5] 殷秋芳, 罗雯斌, 李春儿. 不同病理和生理特征非小细胞肺癌患者组织和血液中miR-21表达量的Meta分析[J]. 中国卫生检验杂志,2023,33(19):2382-2384,2388. [6] 蔡思敏,胡巍,袁云. 卡瑞利珠单抗联合PC化疗方案对晚期非小细胞肺癌患者血清肿瘤标志物的影响[J]. 药品评价,2022,19(16):993-996. [7] 龚关,林祝贤,林锦琛. 卡瑞利珠单抗联合紫杉醇、卡铂化疗对晚期非小细胞肺癌的疗效[J]. 中外医学研究,2023,21(19):149-152. [8] 谷雨,许斌. 卡瑞利珠单抗联合培美曲塞及顺铂化疗治疗晚期非小细胞肺癌患者的临床疗效研究[J]. 反射疗法与康复医学,2023,4(2):113-116. [9] 韩璐,厉锋. 卡瑞利珠单抗联合化疗治疗晚期NSCLC患者的治疗效果[J]. 分子诊断与治疗杂志,2022,14(10):1692-1695,1700. [10] 侯晓杰. 免疫治疗药物对非小细胞肺癌的有效性和安全性研究[J]. 医学信息,2022,35(18):118-120. [11] 李林. 卡瑞利珠单抗联合化疗治疗晚期非小细胞肺癌的临床疗效及安全性观察[J]. 中文科技期刊数据库(全文版)医药卫生,2022,(7):8-11. [12] 梁平红,周建军. 卡瑞利珠单抗联合化疗治疗晚期非小细胞肺癌效果观察[J]. 现代养生,2023,23(4):257-259. doi: 10.3969/j.issn.1671-0223(s).2023.04.005 [13] 刘艳,段爱雄,高艳,等. 卡瑞利珠单抗联合化疗治疗晚期非小细胞肺癌的临床疗效及安全性观察[J]. 中国医院用药评价与分析,2021,21(10):1169-1172. [14] 彭赖水,黎平康. 免疫治疗应用于晚期非小细胞肺癌的效果与安全性分析[J]. 现代医学与健康研究电子杂志,2023,7(12):1-3. [15] 汪淼,马桂香,丁雷,等. 卡瑞利珠单抗联合化疗治疗中晚期非小细胞肺癌的临床研究[J]. 中文科技期刊数据库(全文版)医药卫生,2022,(3):85-87. [16] 王守华,蒋从飞,刘平. TP方案联合卡瑞利珠单抗治疗驱动基因阴性晚期非小细胞肺癌临床观察[J]. 中国药业,2022,31(S02):72-74. [17] 王素玲,常智. 卡瑞利珠单抗联合化疗对晚期非小细胞肺癌患者近期疗效、肺功能和血清肿瘤标志物的影响[J]. 现代医学与健康研究电子杂志,2022,6(24):42-45. [18] 吴畅,胡小云,杨东晓,等. 卡瑞利珠单抗联合卡铂和培美曲塞治疗晚期非小细胞肺癌疗效分析[J]. 中文科技期刊数据库(全文版)医药卫生,2023,(6):98-100. [19] 邢磊,叶惠兰,时海峰,等. 卡瑞利珠单抗联合化疗治疗晚期非小细胞肺癌的效果[J]. 吉林医学,2023,44(9):2528-2531. doi: 10.3969/j.issn.1004-0412.2023.09.044 [20] 徐菊娣,黄骞,杨志勇,等. 卡瑞利珠单抗辅助化疗对中晚期NSCLC患者的近期疗效及对细胞免疫、血清肿瘤标志物的影响[J]. 现代肿瘤医学,2023,31(6):1047-1051. [21] 尤冬山,夏晓阳,陈爱民,等. 卡瑞利珠单抗联合TP方案对中晚期NSCLC患者疗效免疫功能及外周血VEGF bFGF CA125和CEA的影响[J]. 河北医学,2023,29(10):1743-1748. doi: 10.3969/j.issn.1006-6233.2023.10.031 [22] 张靖悦,郑光辉,聂改红. 卡瑞利珠单抗联合紫杉醇、卡铂化疗对晚期非小细胞肺癌的疗效[J]. 河南医学研究,2022,31(7):1310-1313. doi: 10.3969/j.issn.1004-437X.2022.07.042 [23] 朱宇宏. 卡瑞利珠单抗联合化疗对驱动基因阴性晚期非小细胞肺癌的效果分析[J]. 中文科技期刊数据库(文摘版)医药卫生,2023,(8):49-51. [24] Zou J,Li C,Han Y,et al. Efficacy of Camrelizumab in Advanced Non-Small-Cell Lung Cancer and Prognostic Analysis of Different PET/CT Features[J]. J Oncol,2022,2022:9942918. [25] Gao J,Zhang C,Wei Z,et al. Immunotherapy for early-stage non-small cell lung cancer: A system review[J]. J Cancer Res Ther,2023,19(4):849-865. [26] Cao H,Wei W,Lu Y. Camrelizumab plus chemotherapy in advanced non-squamous non-small cell lung cancer: Treatment response,survival pattern,and safety[J]. J Clin Pharm Ther,2022,47(11):1775-1782. [27] 董惠霞,王茜. 非小细胞肺癌患者外周血T淋巴细胞亚群表达及其临床意义[J]. 医学信息,2023,36(18):136-139. doi: 10.3969/j.issn.1006-1959.2023.18.026 [28] Trulson I,Holdenrieder S. Prognostic value of blood-based protein biomarkers in non-small cell lung cancer: A critical review and 2008-2022 update[J]. Tumour Biol,2024,46(s1):S111-S161. doi: 10.3233/TUB-230009 [29] 丁振兴,侯永乐,李百玮,等. 卡瑞利珠单抗联合化疗治疗晚期NSCLC的疗效及安全性Meta分析[J]. 齐齐哈尔医学院学报,2022,43(21):2058-2063. doi: 10.3969/j.issn.1002-1256.2022.21.013 -






 下载:
下载:

 下载:
下载:

