Effect of Pristimerin on Proliferation of Oral Squamous Cell Carcinoma CAL-27 by Regulating Autophagy
-
摘要:
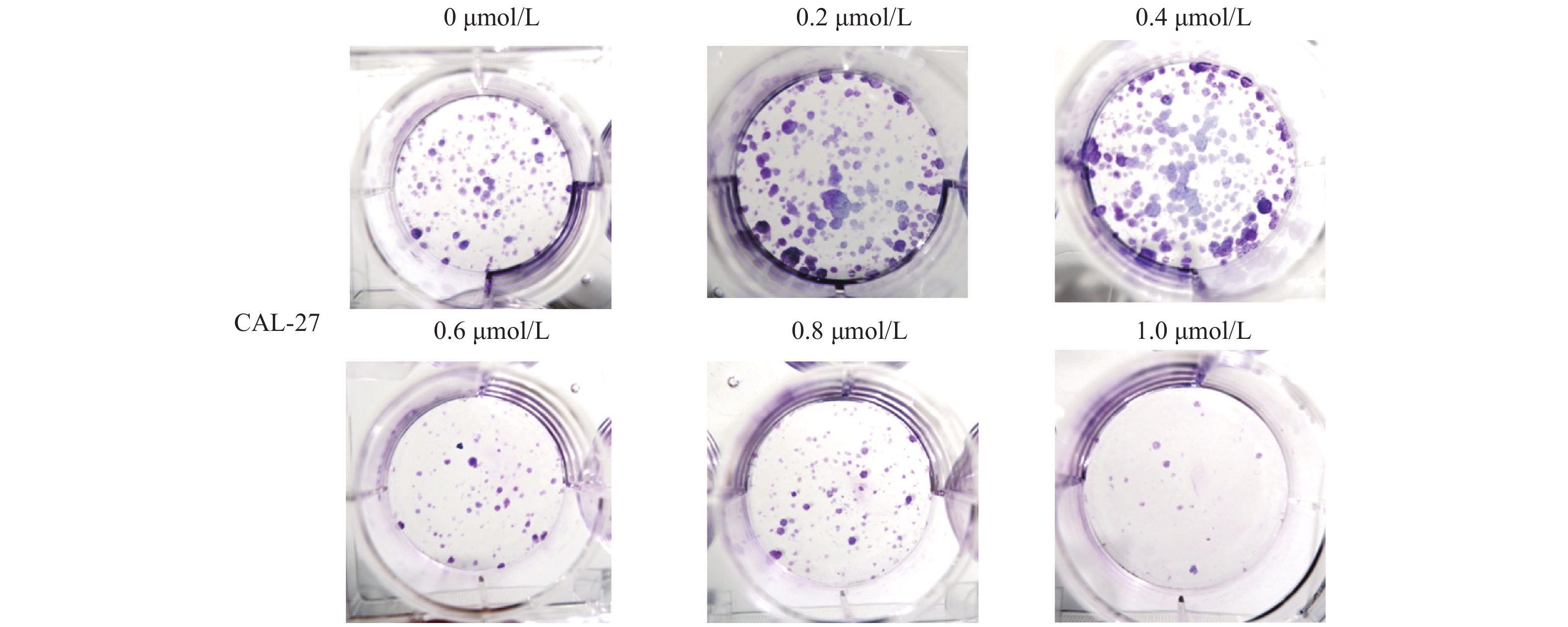
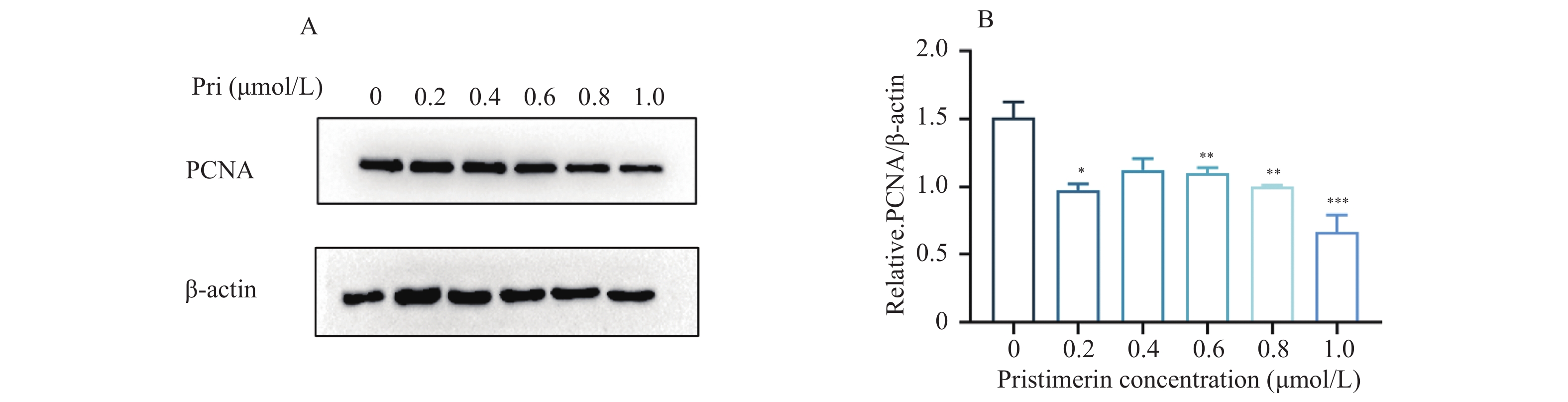
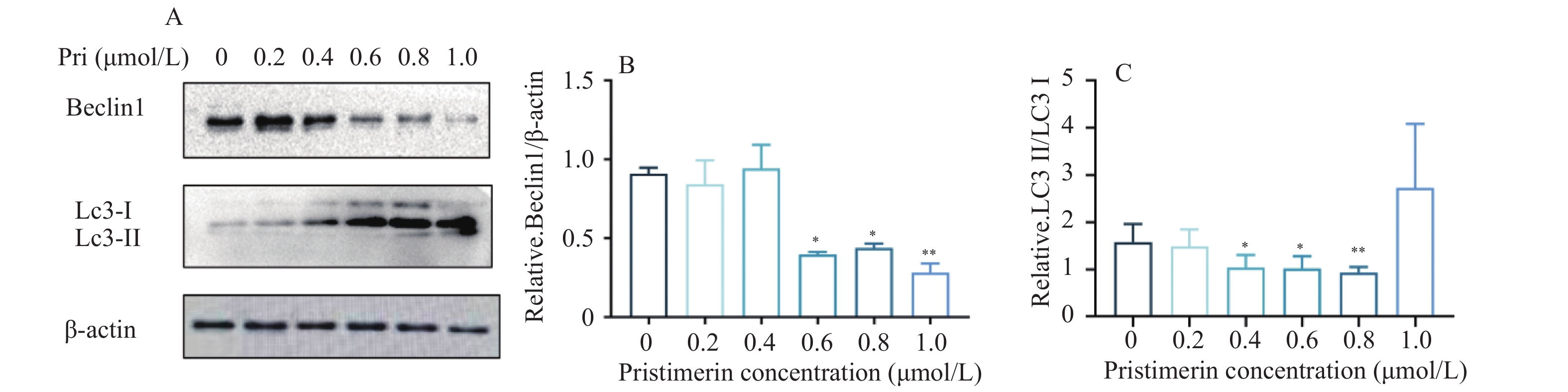
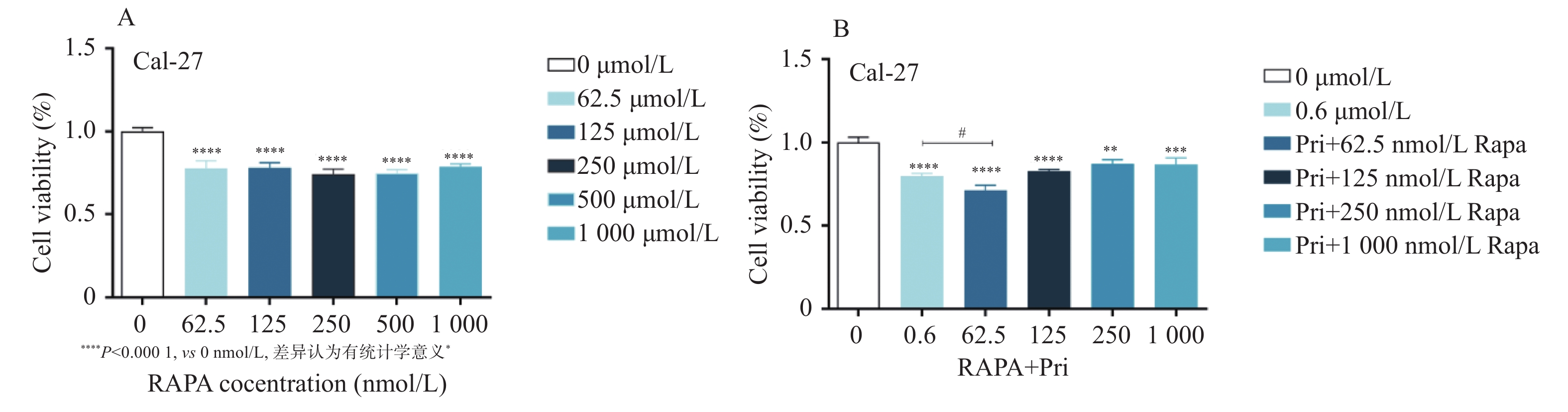
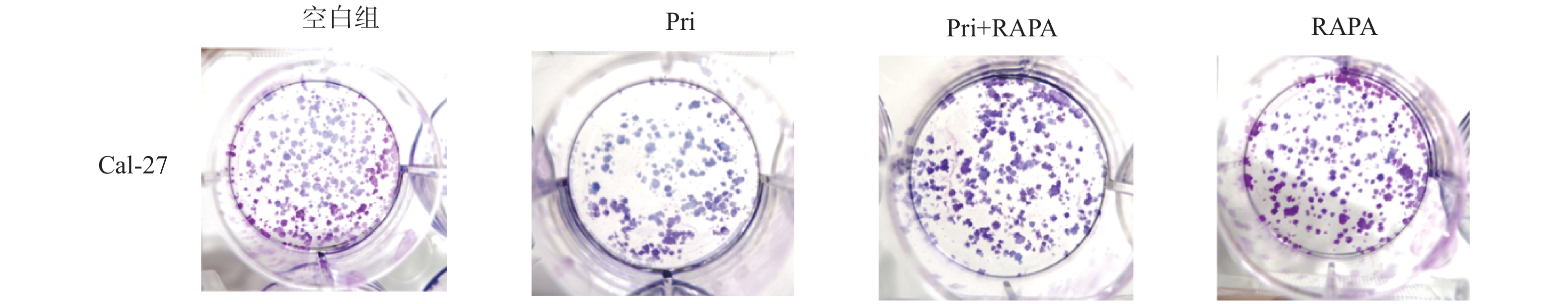
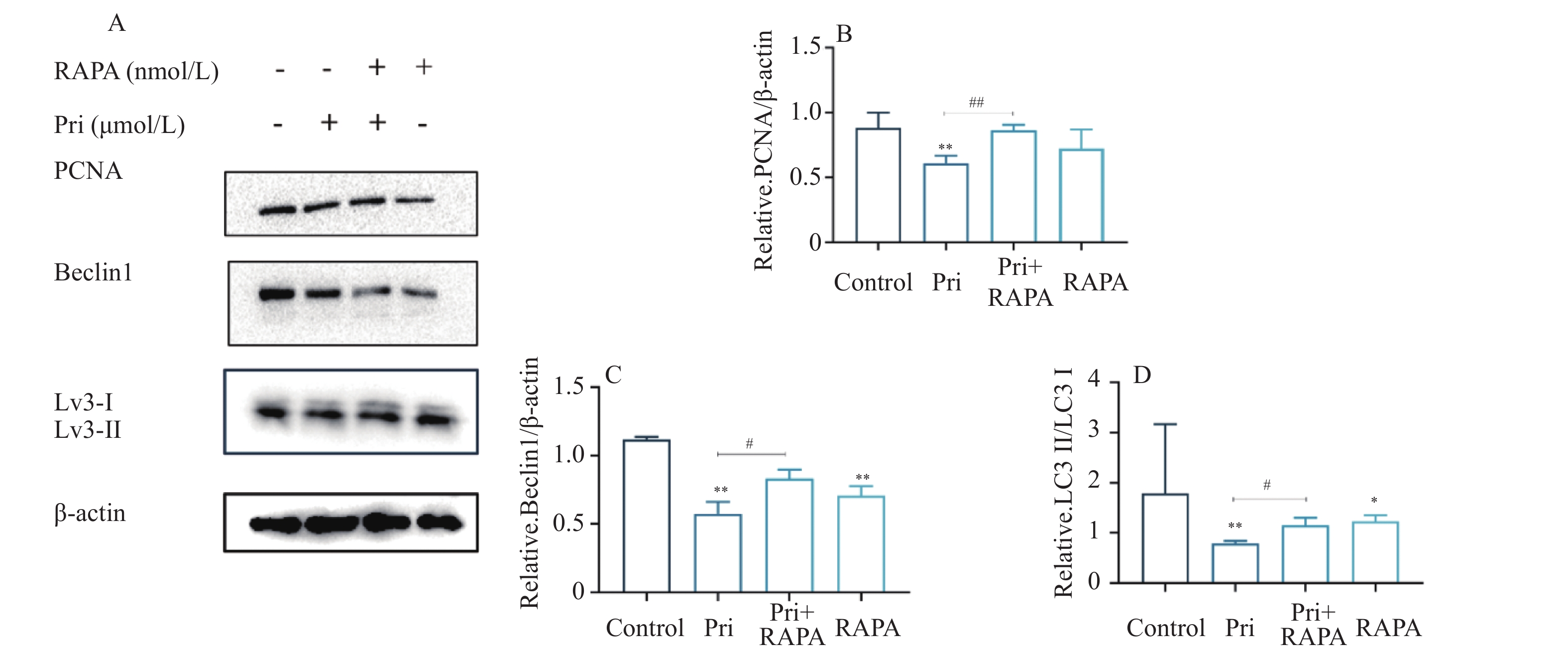
目的 探讨扁塑藤素对人口腔鳞状细胞癌细胞CAL-27增殖能力的影响及其相关作用机制。 方法 CCK8检测不同浓度的扁塑藤素处理CAL-27细胞后的增殖生物活性,计算不同作用时间段所对应的药物浓度水平(IC50);细胞集落形成实验检测CAL-27细胞克隆形成能力;蛋白质印迹法检测细胞增殖指标PCNA以及相关自噬通量BECLIN1、LC3B-II、LC3B-I蛋白表达水平;扁塑藤素联合自噬激动剂雷帕霉素(RAPA)处理CAL-27细胞,蛋白质印迹法检测PCNA以及相关自噬通量BECLIN1、LC3B-II、LC3B-I蛋白表达水平。 结果 较于空白组,各浓度梯度的扁塑藤素可抑制CAL-27细胞活力(P < 0.05),具有浓度-时间依耐性;相较于空白组,经扁塑藤素处理后细胞中PCNA、BECLIN1、LC3B-II/LC3B-I蛋白表达水平都出现明显上调(P < 0.05);扁塑藤素联合自噬激活剂雷帕霉素(RAPA)处理CAL-27细胞相较于仅使用扁塑藤素组细胞活性有所增强(P < 0.05),PCNA、BECLIN1、LC3B-II/LC3B-I蛋白的表达水平均出现明显上调(P < 0.05)。 结论 扁塑藤素在体外能够比较显著抑制口腔鳞状癌系CAL-27细胞的增殖,这可能与其下调自噬相关基因BECLIN1、LC3B-II、LC3B-I的表达相关。 Abstract:Objective To investigate the effect of pristimerin on the proliferation ability of human oral squamous cell carcinoma cells CAL-27 and its related mechanisms. Methods CCK-8 assay was performed to determine the proliferative bioactivity of CAL-27 cells treated with different concentrations of pristimerin, and the IC50 was calculated for different time periods. Colony formation assay was used to detect the cloning ability of CAL-27 cells. Western blotting was used to detect the protein expression levels of the proliferation marker PCNA and the autophagy flux markers BECLIN1, LC3B-II, and LC3B-I. CAL-27 cells were treated with pristimerin in combination with the autophagy inducer rapamycin (RAPA), and Western blotting was used to detect the protein expression levels of PCNA and the autophagy flux markers BECLIN1, LC3B-II, and LC3B-I. Results Compared with the blank group, the pristimerin at various concentration gradients can inhibit the viability of CAL-27 cells (P < 0.05), and it exhibits concentration-time dependence. Compared with the blank group, the expression levels of PCNA, BECLIN1 and LC3B-II/LC3B-I proteins in cells were significantly upregulated after treatment with the pristimerin (P < 0.05). Compared with the group treated with only the pristimerin, the combined treatment of the pristimerin with the autophagy activator rapamycin (RAPA) enhanced the cell activity of CAL-27 cells (P < 0.05), and the expression levels of PCNA, BECLIN1, and LC3B-II/LC3B-I proteins were significantly upregulated (P < 0.05). Conclusion Pristimerin significantly inhibits the proliferation of CAL-27 oral squamous carcinoma cells in vitro, which may be associated with downregulation of autophagy-related genes BECLIN1, LC3B-II, and LC3B-I. -
Key words:
- Pristimerin /
- Oral squamous cell carcinoma /
- Proliferation /
- Autophagy
-
小儿疱疹性口腔炎是由单纯疱疹病毒Ⅰ型(herpes simplex virus 1,HSV-1)所致的一种急性感染性疾病,好发于6岁以下儿童,发病季节无明显差异,具有自限性,病程一般7~10 d,传染性较强且易复发,可能出现严重的并发症[1]。通常发生于小儿口腔黏膜处,常见于齿龈、舌、唇与上颚处,黏膜水肿充血,伴有单个散在或成簇的圆形小水泡。患儿主要表现出疼痛、发热、拒食、淋巴结肿大、流涎甚至惊厥[2]。目前的治疗手段主要为对症支持治疗(包括补液和疼痛管理)及经验性抗病毒治疗方案,大多数在短期内难以达到预期效果,故临床中较多选择联合用药。
单磷酸阿糖腺苷是抗脱氧核糖核酸病毒药,已有研究发现其在小儿疱疹性口腔炎中具有良好治疗作用[3]。康复新液能够促进口腔黏膜上皮细胞的生长和肉芽组织的新生,加速伤口愈合。同时具有抗炎作用,减轻创面等引起的红肿和疼痛症状。还能调节口腔微环境,减少细菌滋生,从而达到治疗小儿疱疹性口腔炎的目的[4]。目前有较多研究开展了康复新液联合单磷酸阿糖腺苷治疗小儿疱疹性口腔炎的随机对照实验,但缺乏相关的系统性评价报告,本文系统收集了康复新液联合单磷酸阿糖腺苷治疗小儿疱疹性口腔炎的随机对照试验(randomized controlled trials,RCTs),旨在评估康复新液辅助治疗小儿疱疹性口腔炎的疗效和安全性,以期为康复新液的临床应用提供循证参考。
1. 资料与方法
1.1 资料来源与检索策略
检索CNKI、Wan fang、VIP、SinoMed、PubMed、Cochrane Library、Web of Science、EMbase数据库中康复新液联合单磷酸阿糖腺苷治疗小儿疱疹性口腔炎的RCT,检索时限截止为2024年10月。中文检索词:“康复新液”“单磷酸阿糖腺苷”“疱疹性口腔炎”等;英文检索词:“Kangfuxin Liquid”“Vidarabine Monophosphate for Injection”“Herpetic Stomatitis”等,检索采用主题词联合自由词的方式。同时利用人工搜索康复新液联合单磷酸阿糖腺苷治疗小儿疱疹性口腔炎的相关文献,减少偏倚。
1.2 文献纳入与排除标准
1.2.1 纳入标准
(1)明确诊断为疱疹性口腔炎的患儿,诊断标准符合《诸福棠实用儿科学(第8版)》[2],性别、地区、种族、病程不限,语种限定为中文和英文。
(2)干预措施:对照组采用单磷酸阿糖腺苷常规抗病毒治疗方案(含或不含溶菌酶肠溶片),试验组在对照组的基础上加上康复新液。
(3)结局指标:主要结局指标为临床疗效比较(即总有效率,总有效率 = 治愈率+显效率+有效率)、不良事件发生率。次要结局指标为:症状改善时间(退热时间、口腔疼痛和口腔疱疹消退时间、流涎消退时间、恢复饮食时间);T淋巴细胞亚群水平(CD3+、CD4+、CD8+、CD4+/CD8+);血清学水平:白细胞(white blood cell,WBC)、血管内皮生长因子(vascular endothelial growth factor,VEGF)、表皮生长因子(epidermal growth factor、EGF)、IL-10、IL-6、C-反应蛋白(c-reactive protein,CRP)、肿瘤坏死因子(tumor necrosis factor ,TNF-α)。
1.2.2 排除标准
(1)动物实验;(2)病例报告、综述、会议摘要、学位论文、重复文献、无法获取全文或数据缺失的文献;(3)干预措施不符(试验组在对照组的基础上联用除康复新液以外的其他中成药或中药处方的文献)。
1.3 数据提取与质量评估
将检索到的文献导入Note Express 3.9.0软件,排除重复文献后由两名研究者阅读题目和摘要进行初筛,对余下的文献进行全文阅读,严格按照制定的纳排标准进行筛选,确定最终纳入定量分析的文献,过程中出现分歧先进行讨论,无法统一者由所有作者一起决定。数据提取包括第一作者及发表年份、样本量、患儿年龄、体质量、病程、干预措施、结局指标等。由两位研究者按照Cochrane风险偏倚评估工具独立对纳入文献进行评价,根据偏倚风险程度评估为高风险、不确定和低风险。若评估过程出现分歧则先进行讨论,无法统一者由所有作者一起决定。
1.4 统计学分析
采用RevMan5.4软件进行Meta分析。二分类变量使用相对危险度(risk ratio,RR)评价,连续型变量使用标准化均数差(standard mean difference,SMD)或均数差(mean difference,MD)评价。以I 2值、P值评估异质性大小,当P > 0.1,I 2 < 50%,认为无明显异质性,采用固定效应模型,当P ≤ 0.1,I 2 ≥ 50%时,认为存在异质性,采用随机效应模型,并进行亚组分析查找异质性来源。以P < 0.05为差异具有统计学意义。
2. 结果
2.1 文献检索
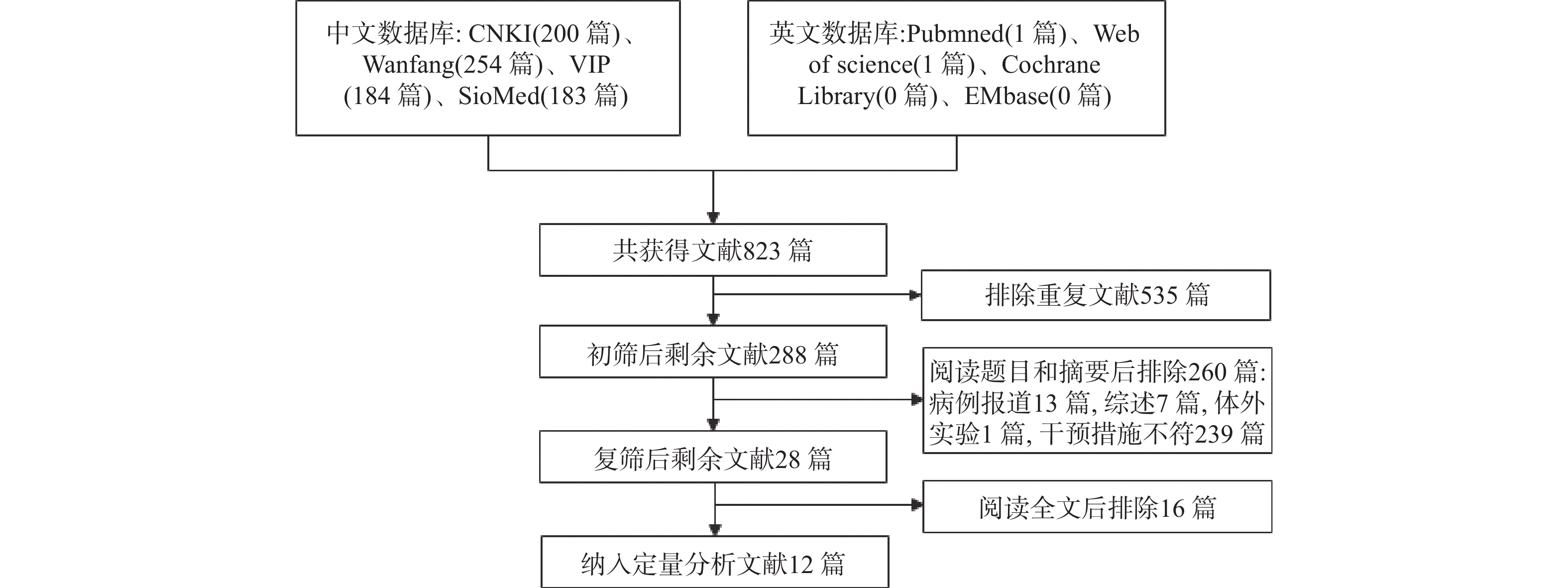
初步检索到文献823篇,排除重复文献后剩余288篇,根据文献纳排标准对文献题目及摘要进行阅读后剩余28篇,阅读全文后最终纳入定量分析12篇,见图1。
2.2 文献特征
共纳入12篇RCTs,发表时间为2015~2024年。样本量1 094例,其中实验组547例,对照组547例,对照组采用单磷酸阿糖腺苷常规抗病毒治疗方案(含或不含溶菌酶肠溶片);试验组在对照组的基础上加上康复新液。
表 1 纳入文献的基本特征(`x±s)Table 1. Basic characteristics of included studies(`x±s)纳入文献 样本(n) 年龄(岁) 体质量(kg) 病程(h) 干预措施 疗程 结局指标 试验组 对照组 试验组 对照组 试验组 对照组 试验组 对照组 试验组 对照组 谢丹丹[5]2024 50 50 2.83 ± 0.58 2.85 ± 0.57 13.60 ± 2.20 13.50 ± 2.10 —— —— KFX(5 mL,tid)+Ara-AMP(5 mg/kg/d,qd)+RJM(20 mg,qd) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,qd) 7 d (1)(2)(3)
(4)(5)王虹[6]2023 46 46 3.39 ± 0.12 3.54 ± 0.14 —— —— 106.56 ± 5.28 108.72 ± 5.04 KFX(5 mL,tid)+Ara-AMP(5 mg/kg,qd)+RJM(20 mg,qd) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,qd) 6 d (1)(2
)(3)(4)宋娜[7]2022 40 40 4.14 ± 1.41 3.65 ± 1.37 12.08 ± 2.69 11.77 ± 2.51 —— —— KFX(5 mL,tid)+Ara-AMP(5 mg/kg,qd) Ara-AMP(5 mg/kg,qd) 7 d (1)(2)
(4)(5)潘俊文[8]2021 25 25 4.52 ± 1.23 4.53 ± 1.25 —— —— —— —— KFX(5 mL,tid)+Ara-AMP(0.1 g,qd) Ara-AMP(0.1 g,qd) 5 d (1)(2) 赵越[9] 2021 60 60 4.43 ± 1.07 4.21 ± 1.03 —— —— 24.48 ± 3.36 24.73 ± 3.51 KFX(5 mL,tid)+Ara-AMP(5 mg/kg,qd)+RJM(20 mg,qd) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,qd) 5 d (1)(2)
(3)(4)丁丽萍[10] 2021 30 30 4.10 ± 0.45 3.76 ± 0.41 —— —— 95.76 ± 9.84 88.8 ± 9.84 KFX(5 mL,tid)+Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) 5 d (1)(2)(4) 崔小会[11] 2020 37 37 3.11 ± 0.96 2.96 ± 0.84 —— —— 52.8 ± 12.24 57.84 ± 10.56 KFX(5 mL,tid)+Ara-AMP(0.1 g,qd) Ara-AMP(0.1 g,qd) 3~5 d (1)(4) 李香君[12] 2019 46 46 3.28 ± 1.44 3.31 ± 1.48 —— —— 23.13 ± 4.32 23.11 ± 4.29 KFX(5 mL,tid)+Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) 5 d (1)(2)
(4)(5)全翠芬[13] 2018 43 43 3.37 ± 1.25 2.16 ± 1.66 12.68 ± 2.09 11.82 ± 2.46 —— —— KFX(5-10 mL,tid)+Ara-AMP(5-10 mg/kg,qd) Ara-AMP(5-10 mg/kg,qd) — (1)(2)(5) 周波[14] 2018 50 50 3.32 ± 0.53 3.42 ± 0.61 —— —— —— —— KFX(5 mL,tid)+Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) — (1)(4) 肖雷[15] 2017 70 70 3.32 ± 0.53 3.42 ± 0.61 —— —— 21.32 ± 10.21 22.64 ± 9.82 KFX(5 mL,tid)+Ara-AM(5 mg/kg,qd)P+RJM(20 mg,tid) Ara-AMP(5 mg/kg,qd)+RJM(20 mg,tid) 5 d (1)(2)(4) 陈学锋[16] 2015 50 50 —— —— —— —— —— —— KFX(5 mL,tid)+Ara-AMP(5-10 mg/kg,qd) Ara-AMP(5-10 mg/kg,qd) 3~5 d (1)(2) 注:T:实验组;C:对照组;——:未提及;KFX:康复新液;Ara-AMP:单磷酸阿糖腺苷;RJM:溶菌酶肠溶片;结局指标:(1)症状改善时间(退热时间、口腔疼痛和口腔疱疹消退时间、流涎消退时间、恢复饮食时间);(2)临床疗效比较(总有效率);(3)两组T淋巴细胞亚群水平(CD3+、CD4+、CD8+、CD4+/CD8+);(4)两组血清学水平(WBC、VEGF、EGF、IL-10、IL-6、CRP、TNF-α);(5)不良反应事件。 2.3 文献质量评价
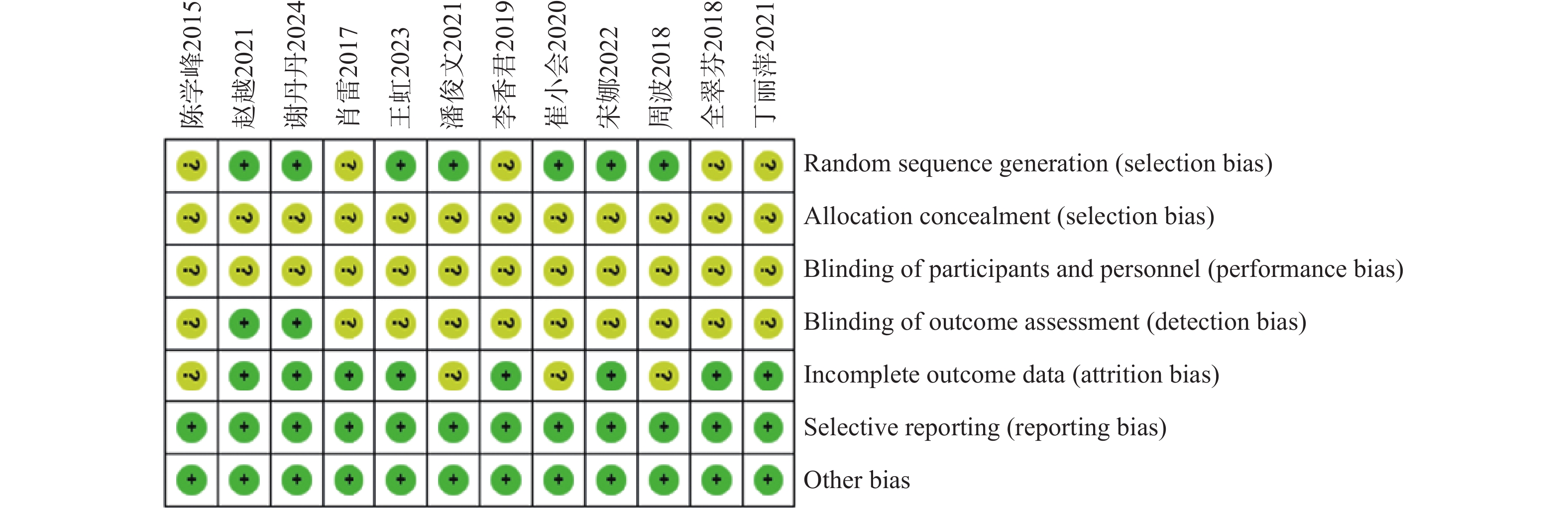
纳入的12篇RCTs中7篇文献报告了具体的随机方法,5篇[5−9]使用随机数字表法,2篇[11-14]使用抽签法,均未提及盲法,文献数据均完整且不存在其他偏倚。
2.4 Meta分析
2.4.1 临床总有效率
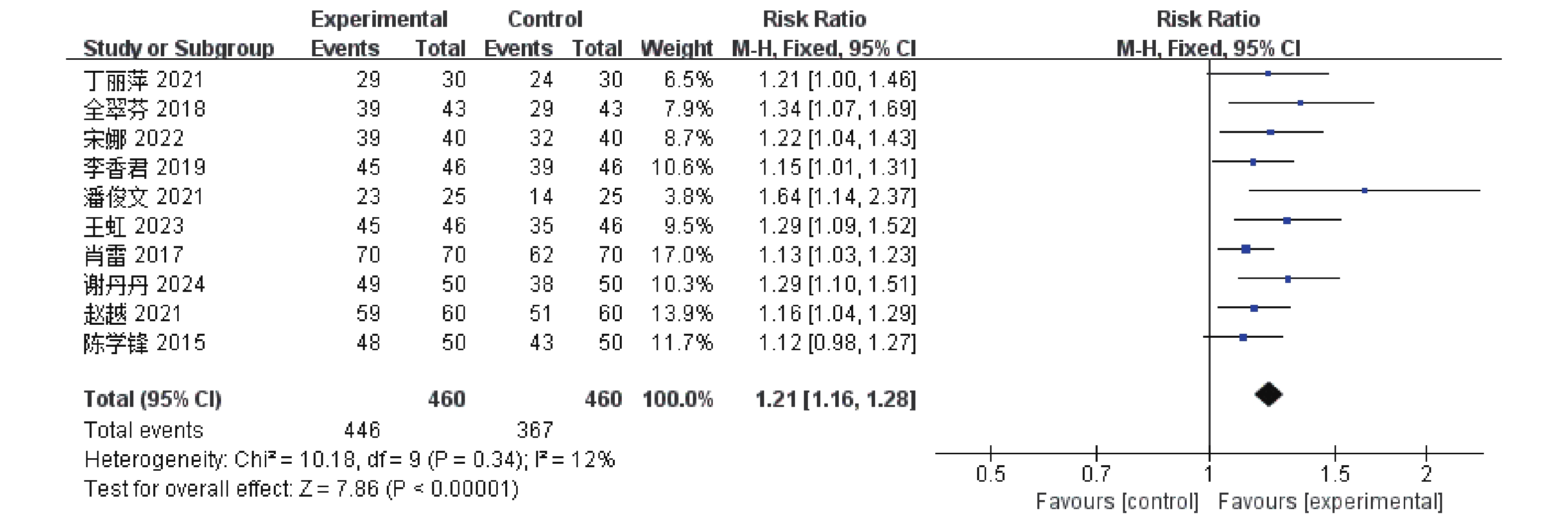
10篇[5−10,12-13,15-16]RCTs报告了临床总有效率,共涉及920例患者,经异质性检验,I 2 = 12%,P = 0.34,各研究间无异质性,故采用固定效应模型。结果显示,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组提高了临床总有效率,差异具有统计学意义[RR = 1.21,95%CI(1.16,1.28),P <
0.00001 ],见图3。2.4.2 症状改善时间
(1)疱疹消失(皮损愈合)时间
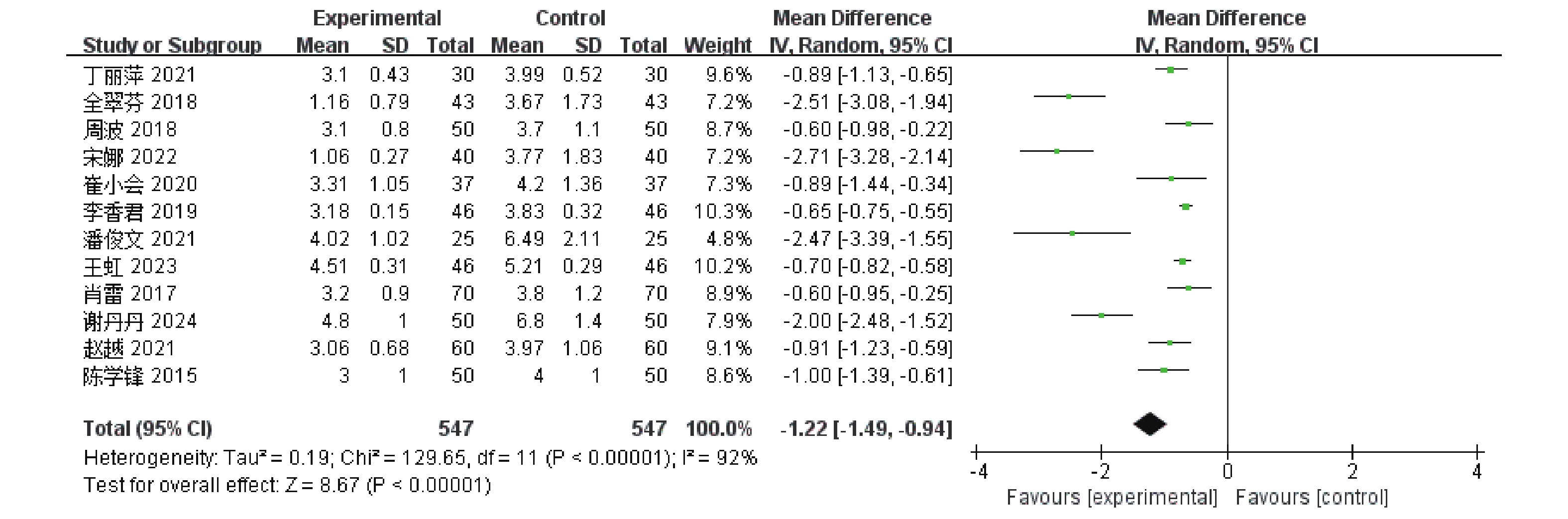
12篇[5−16]RCTs报告了疱疹消失(皮损愈合)时间,共涉及1 094例患者,经异质性检验,I 2 = 92%,P <
0.00001 ,各研究间异质性较大,采用随机效应模型。结果显示,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组更能有利于缩短疱疹消失(皮损愈合)时间,差异具有统计学意义[MD = -1.22,95%CI(-1.49,-0.94),P <0.00001 ],见图4。(2)疼痛消失时间
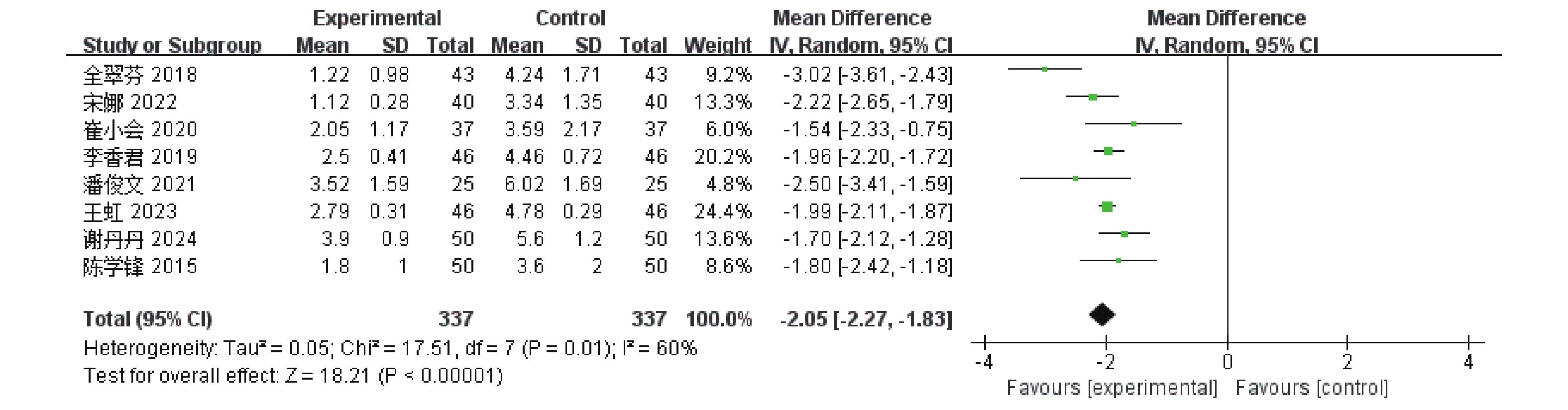
8篇[5−8,11−13,16]RCTs报告了疼痛消失时间,共涉及674例患者,经异质性检验,I 2 = 60%,P = 0.01,各研究间异质性大,采用随机效应模型。结果显示,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组更能有利于缩短疼痛消失时间,差异具有统计学意义[MD = -1.80,95%CI(-2.27,-1.83),P <
0.00001 ],见图5。(3)退热时间
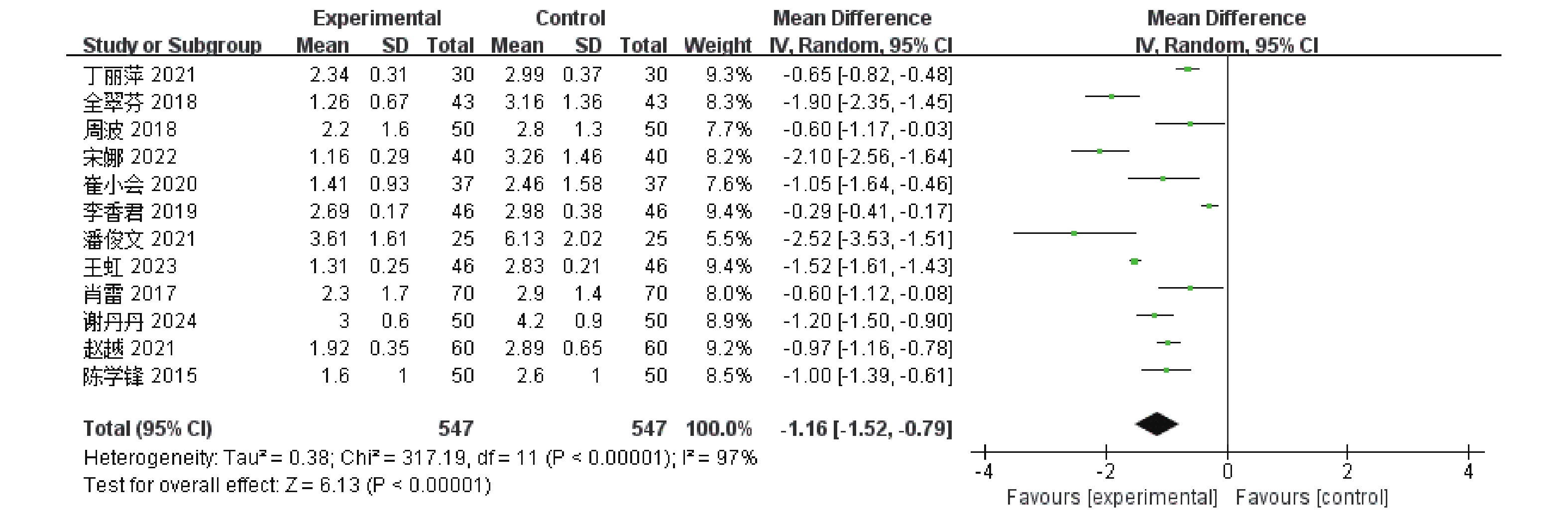
12篇[5−16]RCTs报告了退热时间,共涉及1 094例患者,经异质性检验,I 2 = 97%,P <
0.00001 ,各研究间异质性较大,采用随机效应模型。结果显示,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组更能有利于缩短退热时间,差异具有统计学意义[MD = -1.16,95%CI(-1.52,-0.79),P <0.00001 ],见图6。(4)流涎消失时间
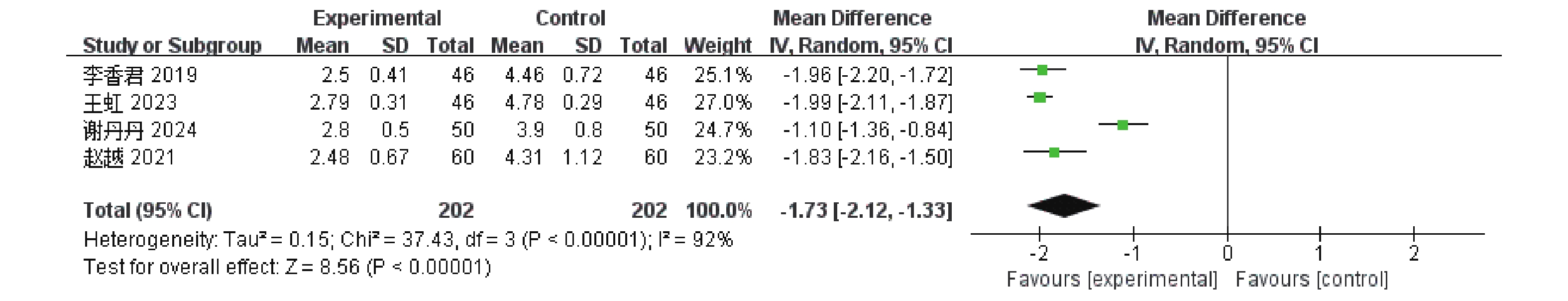
4篇[5-6,9,12]RCTs报告了流涎消失时间,共涉及404例患者,经异质性检验,I 2 = 92%,P <
0.00001 ,各研究间异质性大,采用随机效应模型。结果显示,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组更能有利于缩短流涎消失时间,差异具有统计学意义[MD = -1.73,95%CI(-2.12,-1.33),P <0.00001 ],见图7。(5)恢复饮食时间
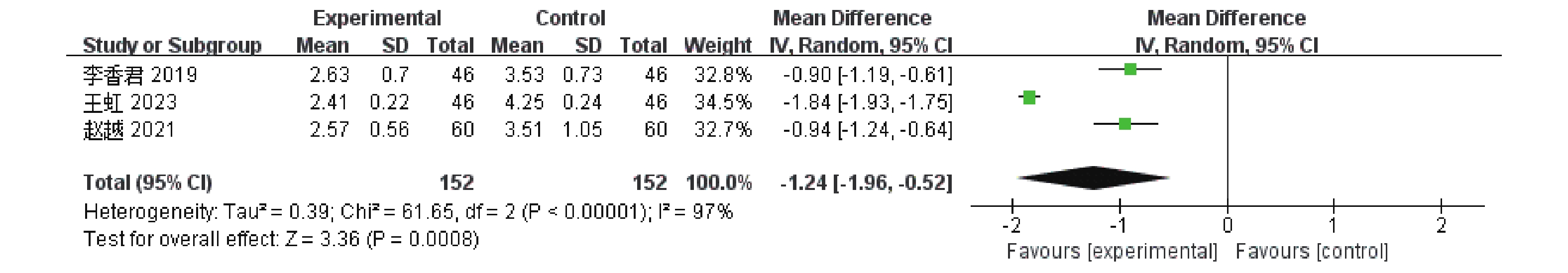
3篇[6,9,12]RCTs报告了流涎消失时间,共涉及304例患者,经异质性检验,I 2 = 97%,P <
0.00001 ,各研究间异质性大,采用随机效应模型。结果显示,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组更有利于缩短恢复饮食时间,差异具有统计学意义[MD = -1.24,95%CI(-1.96,-0.52),P =0.0008 ],见图8。2.4.3 T淋巴细胞亚群水平
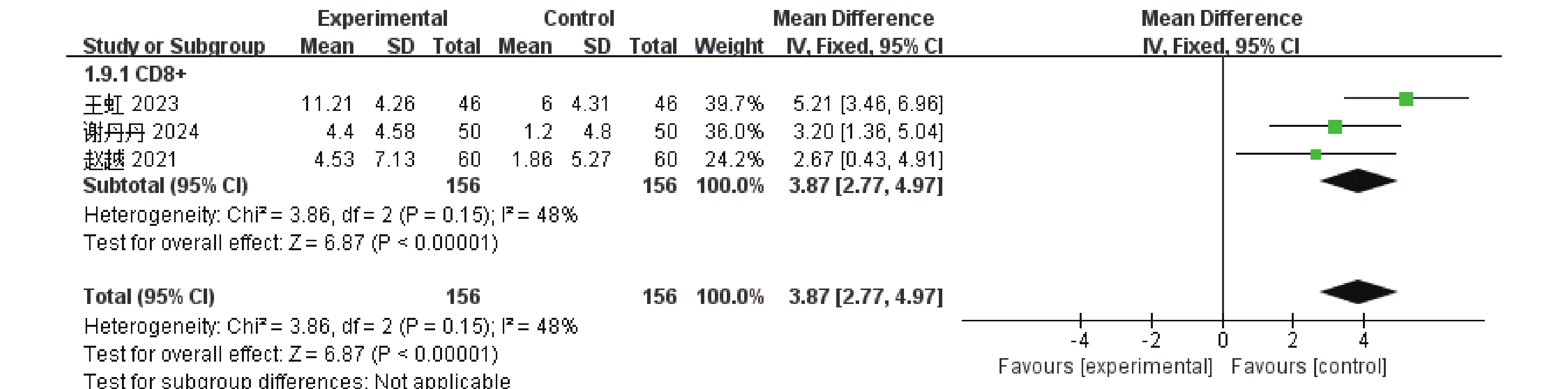
(1)CD8+水平
3篇[5-6,9]RCTs报告了CD8+的值,涉及312例患者。Meta分析显示,研究间无异质性(P = 0.15,I 2 = 48%),采用固定效应模型分析,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组更有利于CD8+值的恢复,差异具有统计学意义[MD = 3.87,95%CI(2.77,4.97),P <
0.00001 ],见图9。(2)CD3+、CD4+和CD4+/CD8+水平
CD3+、CD4+和CD4+/CD8+各研究间异质性较高,按入组时基线值亚组分析后各研究间异质性仍存在,采用随机效应模型。Meta分析显示,康复新液组CD3+[MD = 6.01,95%CI(3.54,8.47),P <
0.00001 ]、CD4+[MD = 3.09,95%CI(0.50,5.68),P = 0.02]、CD4+/CD8+[MD = 0.30,95%CI(0.09,0.51),P = 0.005]恢复效果均优于单磷酸阿糖腺苷抗病毒治疗组,差异具有统计学意义。见表2。2.4.4 血清学水平
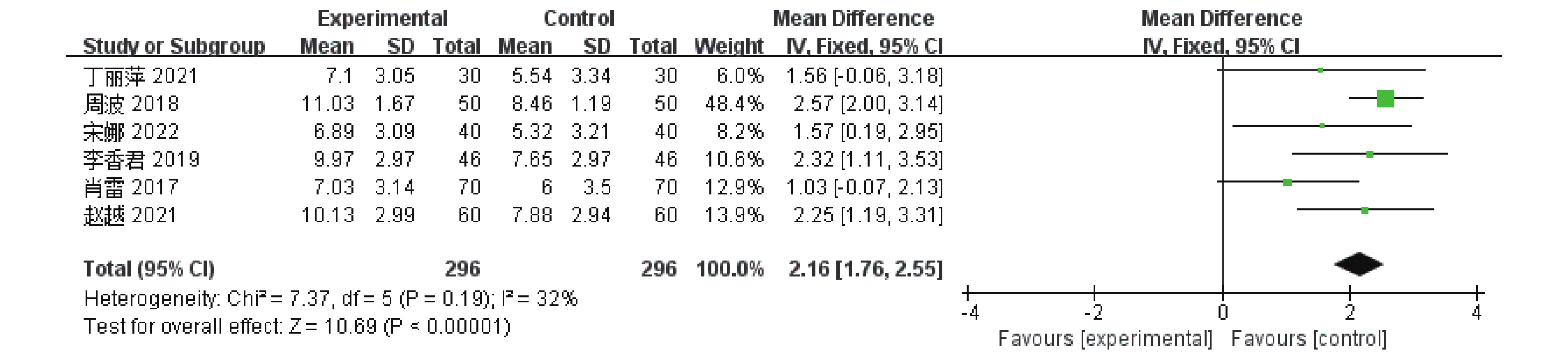
(1)CRP水平
6篇[7,9−12,14-15]报告了CRP的值,涉及592例患者。Meta分析显示,研究间无异质性(P = 0.19,I 2 = 32%),采用固定效应模型分析,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组能有效降低CRP的值,差异具有统计学意义[MD = 2.16,95%CI(1.76,2.55),P <
0.00001 ],见图10。(2)TNF-α水平
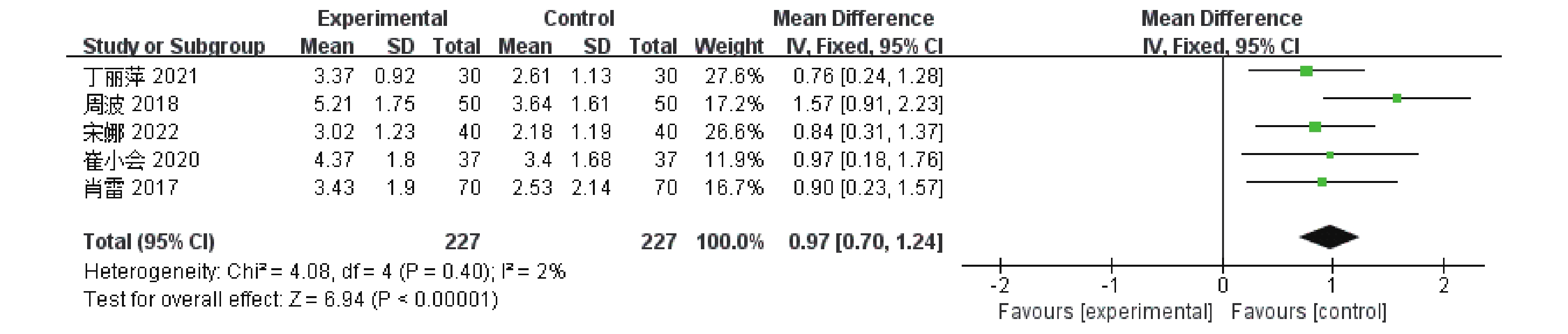
5篇[7,10-11,14-15]报告了TNF-α的值,涉及454例患者。Meta分析显示,研究间无异质性(P = 0.40,I 2 = 2%),采用固定效应模型分析,与单磷酸阿糖腺苷常规抗病毒治疗相比,康复新液组能有效降低TNF-α的值,差异具有统计学意义[MD = 0.97,95%CI(0.70,1.24),P <
0.00001 ],见图11。(3)WBC、IL-10、VEGF、EGF及IL-6水平
WBC、IL-10、VEGF、EGF及IL-6各研究间异质性较高,按入组时基线值亚组分析后各研究间异质性仍存在,采用随机效应模型。Meta分析显示,康复新液组WBC[MD = 2.26,95%CI(1.54,2.98),P <
0.00001 ]、IL-10[MD = 16.10,95%CI(8.07,24.12),P <0.00001 ]、VEGF[MD = 41.83,95%CI(13.31,70.36),P = 0.004]、IL-6[MD = 11.98,95%CI(5.11,18.85),P =0.0006 ]恢复效果均优于单磷酸阿糖腺苷常规抗病毒治疗组,差异具有统计学意义,而EGF[MD = 7.89,95%CI(-5.32,21.11),P = 0.24]在两组中差异无统计学意义(P > 0.05),见表3。表 3 血清学指标的Meta分析Table 3. Tab.3Meta-analysis of serologic indicators结局指标 纳入文献(篇) 样本量(n) 异质性检验 Meta分析 P I 2 MD 95%CI P WBC 7篇[5-6,9-10,12,14-15] 704 < 0.00001 **85% 2.26 1.54~2.98 < 0.00001 **IL-10 8篇[5−7,9−12,15] 758 < 0.00001 **93% 16.10 8.07~24.12 < 0.00001 **VEGF 2篇[5-6] 192 0.00008 **91% 41.83 13.31~70.36 0.004** EGF 2篇[5-6] 192 < 0.00001 **98% 7.89 −5.32~21.11 0.24 IL-6 2篇[5-6] 192 < 0.00001 **96% 11.98 5.11~18.85 0.0006 ****P < 0.01 2.4.5 不良反应
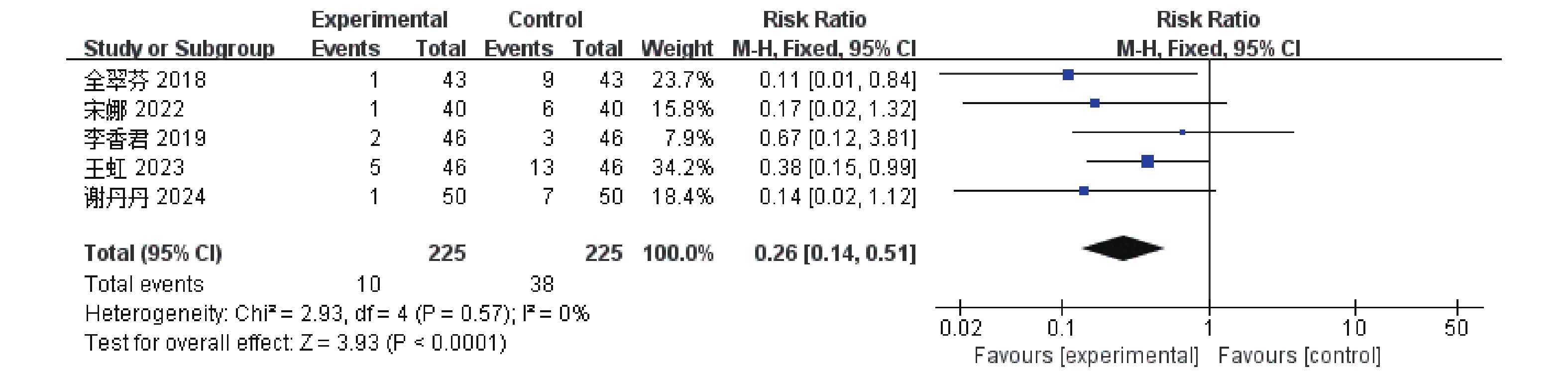
5篇[5−7,12-13]RCTs报告了不良反应事件发生率,涉及450例患者,Meta分析结果分析显示,各研究间异质性较小(P = 0.57,I 2 = 0),采用固定效应模型,结果显示与单磷酸阿糖腺苷常规抗病毒治疗组相比,康复新液组不良事件发生率更低[RR = 0.26,95%CI(0.14,0.51),P <
0.00001 ],见图12。2.5 发表偏倚
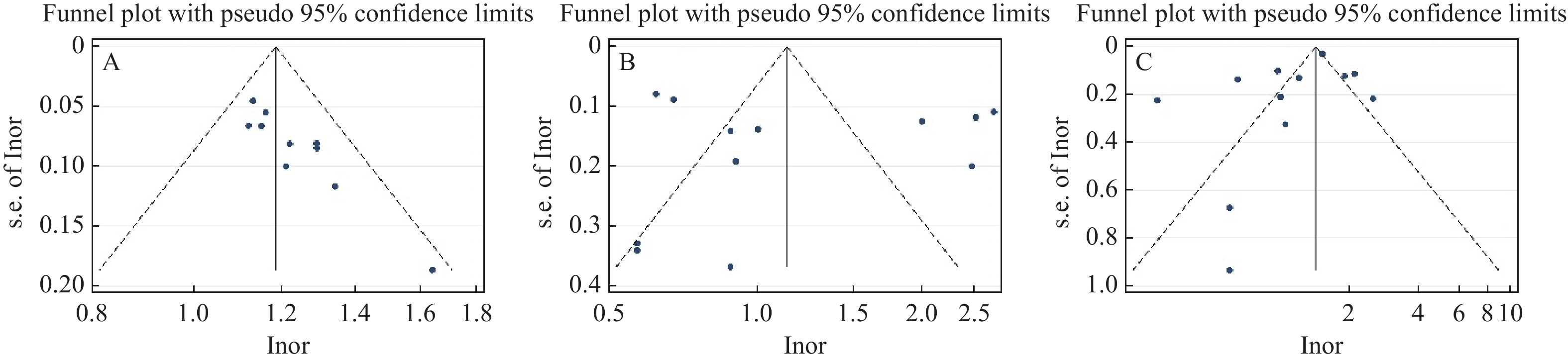
通过漏斗图对单磷酸阿糖腺苷常规抗病毒治疗组 VS 康复新液组的总有效率、疱疹消失(皮损愈合)时间、退热时间进行偏倚评价。结果显示,总有效率(图13A)散点基本对称,而疱疹消失(皮损愈合)时间(图13B)、退热时间(图13C)的散点不对称,存在发表偏倚的可能性,可能与不同文献研究者评判标准有较大差异、患者及研究者判断疗效好转时间的主观性较强、患者疾病程度不一致、文献质量较低等因素相关。进行Egger’ s检验,结果显示总有效率(P = 1.00)、疱疹消失(皮损愈合)时间(P = 0.784)、退热时间(P = 0.411),差异均无统计学意义(P > 0.05),提示各研究间均无明显发表偏倚,见图13。
3. 讨论
小儿疱疹性口腔炎由HSV-1感染引起,通常为自限性感染,可在10~14 d内消退。疱疹性口腔炎常见于6个月至3岁儿童,可能与该年龄段胎盘内获得的抗体消失、自身免疫系统不成熟(sIgA、溶菌酶不足)、口腔黏膜结构的年龄形态特征(由于上皮层薄,糖原和核酸含量低)以及牙齿萌出和微创伤导致的黏膜完整性经常受到自然破坏等因素有关[17]。临床上,HSV-1感染初期患儿会出现发热、食欲不振、乏力和肌痛等前驱症状。随后在硬腭、附着牙龈和舌背、颊黏膜和唇黏膜的非角化黏膜、舌腹面和软腭上会出现红斑和成群的小泡或溃疡,患儿口腔极度疼痛,导致进食困难[18]。所以小儿疱疹性口腔炎的早期诊断很重要,其治疗包括服用抗病毒药物,以及镇痛、维持体内液体和电解质水平等对症支持治疗。然而,治疗过程中可能出现多形性红斑、无菌性脑膜炎和脑炎等并发症[13]。因此,解决以口腔黏膜为表现的急性和复发型小儿疱疹性口腔炎的诊断和治疗问题是目前临床实践中面临的最重要任务之一。
由于疱疹性口腔炎患儿对口服药物依从性差,临床中通常采用外用药治疗。加上常规的抗病毒药物起效时间慢,近年来临床中运用中医药治疗,发现效果较为显著。康复新是从美洲大蠊中提取的中成药,包含许多活性成分,如多元醇、抗菌肽和黏蛋白等,具有利血生肌、清热泻火的作用。康复新液辅助治疗小儿疱疹性口腔炎,有助于抑制炎症、刺激皮肤成纤维细胞中胶原蛋白生成、促进表皮细胞生长和肉芽组织增殖以修复损伤从而加速伤口愈合,并且能够有效改善受损黏膜创面血液循环,提高患儿的免疫功能,有效改善其临床症状[19]。单磷酸阿糖腺苷进入细胞后可竞争性抑制病毒核苷酸还原酶的酶活性而抑制病毒DNA的合成,能有效地抑制单纯疱疹病毒的增殖,减轻疱疹性口腔炎的症状,促进病情的恢复。此外,它还具有免疫调节作用,能够刺激机体产生干扰素,增强机体的抗病毒能力。近年来在治疗小儿疱疹性口腔炎中也取得一些进展。故临床中探讨了治疗小儿疱疹性口腔炎的联合用药方式,发现单磷酸阿糖腺苷联合康复新液能够取得更好的疗效,以及减少不良反应的发生[20]。
本研究结果显示,在临床总有效率方面,康复新液联合单磷酸阿糖腺苷治疗小儿疱疹性口腔炎显著优于单磷酸阿糖腺苷治疗,在疱疹消失(皮损愈合)时间、疼痛消失时间、退热时间、流涎消失时间、恢复饮食时间方面,联合用药也均短于单磷酸阿糖腺苷治疗。结果表明,相比于单磷酸阿糖腺苷常规抗病毒治疗,康复新液联合单磷酸阿糖腺苷可更有效地促使淋巴细胞(CD3+、CD4+、CD8+和CD4+/CD8+)、血清学水平(CRP、TNF-α、WBC、IL-10、VEGF、EGF及IL-6)恢复至正常值。安全性方面,5篇RCTs发生了不良事件,主要包括恶心、呕吐、胃痛、头痛头晕、皮疹、腹泻等症状,且康复新液组不良反应事件发生率低于单磷酸阿糖腺苷常规抗病毒治疗组。
本文也存在一些局限性:纳入的大部分研究未能实现双盲、分配隐藏等,导致出现较高异质性和偏倚风险;症状恢复时间以及不良事件的判定等具有主观性;各研究的结局指标比较分散且样本量少,影响研究的可信度;部分结局指标的基线值有较大差异,导致异质性较高;纳入的文献均为中文文献,可能会限制研究结果的应用及推广。
综上所述,本研究使用多个结局指标评估康复新液联合单磷酸阿糖腺苷治疗小儿疱疹性口腔炎的安全性和有效性。本Meta分析结果证实康复新液在小儿疱疹性口腔炎治疗中发挥重要作用,康复新液联合单磷酸阿糖腺苷治疗可显著缩短症状恢复时间、改善淋巴细胞和血清学水平指标,且不良反应发生率较低。因此,在单磷酸阿糖腺苷的基础上加入康复新液治疗小儿疱疹性口腔炎具有一定的潜力,但还需开展更多的大样本、多中心、高质量的RCTs增加结果的可靠性。
-
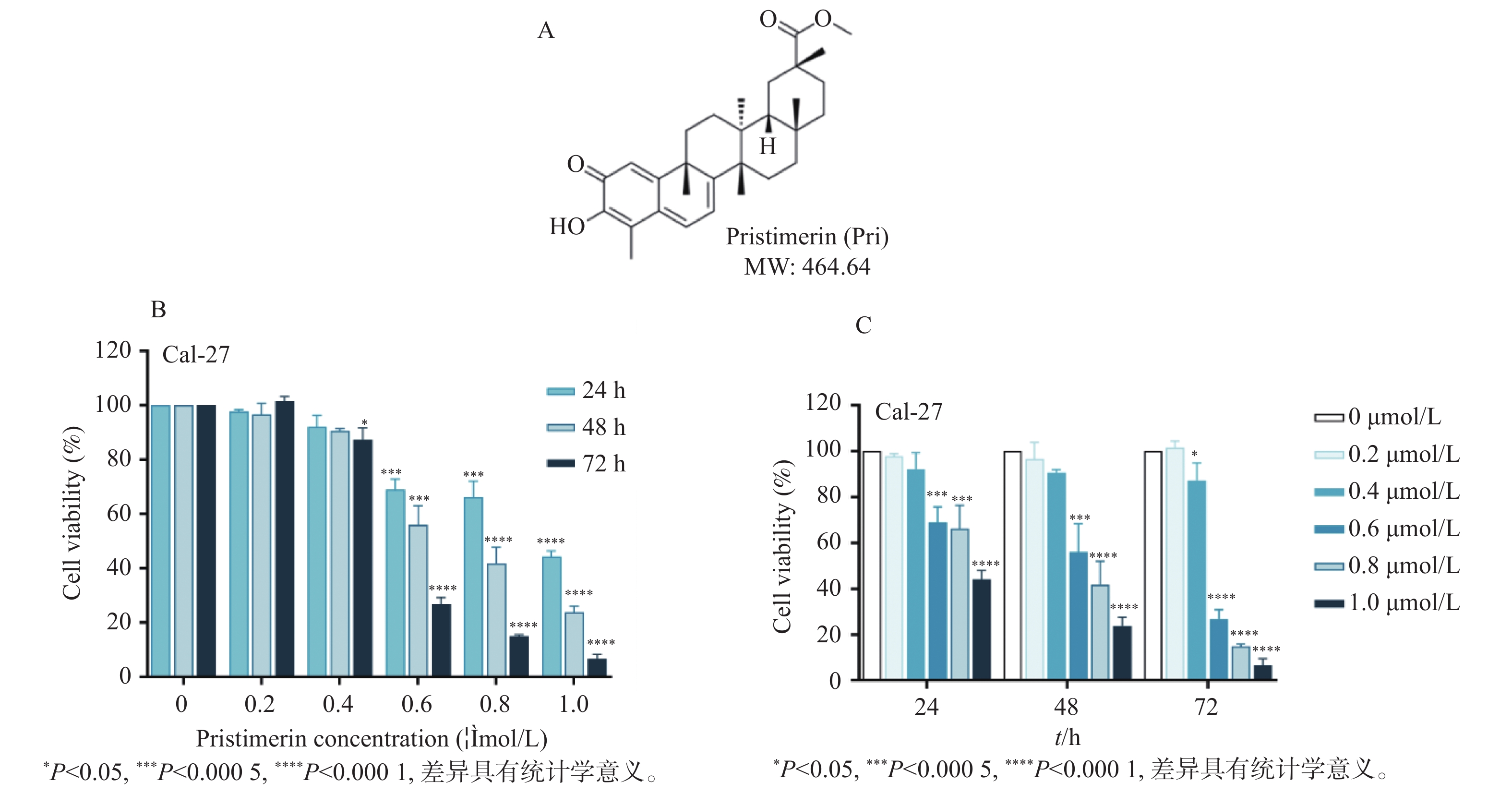
图 1 扁塑藤素抑制口腔鳞状癌Cal-27细胞增殖
A:扁塑藤素化学式和分子结构[17];B:CCK-8测定不同浓度扁塑藤素处理Cal-27细胞对细胞增殖的影响;C:CCK-8定扁塑藤素处理Cal-27细胞24 h、48 h、72 h对细胞增殖的影响。与0 μmol/L组相比,*P < 0.05,***P < 0.0005,****P < 0.0001。
Figure 1. Pristimerin suppresses proliferation of oral squamous cell carcinoma cell
-
[1] Liu J,Jiang X,Zou A,et al. CircIGHG-induced epithelial-to-mesenchymal transition promotes oral squamous cell carcinoma progression via miR-142-5p/igf2bp3 signaling[J]. Cancer Res,2021,81(2):344-355. doi: 10.1158/0008-5472.CAN-20-0554 [2] Sung H,Ferlay J,Siegel R L,et al. Global cancer statistics 2020: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2021,71(3):209-249. doi: 10.3322/caac.21660 [3] Yang Z,Yan G,Zheng L,et al. YKT6,as a potential predictor of prognosis and immunotherapy response for oral squamous cell carcinoma,is related to cell invasion,metastasis,and CD8+ T cell infiltration[J]. Oncoimmunology,2021,10(1):1938890. doi: 10.1080/2162402X.2021.1938890 [4] Ling Z,Cheng B,Tao X. Epithelial-to-mesenchymal transition in oral squamous cell carcinoma: Challenges and opportunities[J]. Int J Cancer,2021,148(7):1548-1561. doi: 10.1002/ijc.33352 [5] Khadela A,Shah Y,Mistry P,et al. Immunomodulatory therapy in head and neck squamous cell carcinoma: Recent advances and clinical prospects[J]. Technol Cancer Res Treat,2023,22:2081074849. [6] Debnath J,Gammoh N,Ryan K M. Autophagy and autophagy-related pathways in cancer[J]. Nat Rev Mol Cell Biol,2023,24(8):560-575. doi: 10.1038/s41580-023-00585-z [7] Cheon S Y,Kim H,Rubinsztein D C,et al. Autophagy,cellular aging and age-related human diseases[J]. Exp Neurobiol,2019,28(6):643-657. doi: 10.5607/en.2019.28.6.643 [8] Lock R,Kenific C M,Leidal A M,et al. Autophagy-dependent production of secreted factors facilitates oncogenic ras-driven invasion[J]. Cancer Discov,2014,4(4):466-479. doi: 10.1158/2159-8290.CD-13-0841 [9] Tompkins K D,Thorburn A. Regulation of apoptosis by autophagy to enhance cancer therapy[J]. Yale J Biol Med,2019,92(4):707-718. [10] Bahrami A,Khazaei M,Hassanian S M,et al. Targeting the tumor microenvironment as a potential therapeutic approach in colorectal cancer: rational and progress[J]. J Cell Physiol,2018,233(4):2928-2936. doi: 10.1002/jcp.26041 [11] Wang Y,Feng W,Wang X,et al. The multifaceted mechanisms of pristimerin in the treatment of tumors state-of-the-art[J]. Biomed Pharmacother,2022,154:113575. doi: 10.1016/j.biopha.2022.113575 [12] Shaaban A A,El-Kashef D H,Hamed M F,et al. Protective effect of pristimerin against lps-induced acute lung injury in mice[J]. Int Immunopharmacol,2018,59:31-39. doi: 10.1016/j.intimp.2018.03.033 [13] Cheng S,Zhang Z,Hu C,et al. Pristimerin suppressed breast cancer progression via mir-542-5p/dub3 axis[J]. Onco Targets Ther,2020,13(1171):6651-6660. [14] Li J,Guo Q,Lei X,et al. Pristimerin induces apoptosis and inhibits proliferation,migration in h1299 lung cancer cells[J]. J Cancer,2020,11(21):6348-6355. doi: 10.7150/jca.44431 [15] Zhao Q,Bi Y,Guo J,et al. Effect of pristimerin on apoptosis through activation of ros/ endoplasmic reticulum (ER) stress-mediated noxa in colorectal cancer[J]. Phytomedicine,2021,80:153399. doi: 10.1016/j.phymed.2020.153399 [16] Zhang Y,Wang J,Hui B,et al. Pristimerin enhances the effect of cisplatin by inhibiting the miR-23a/Akt/GSK3β signaling pathway and suppressing autophagy in lung cancer cells[J]. Int J Mol Med,2019,43(3):1382-1394. [17] Zhao Q,Cheng X,Yu W,et al. Pristimerin induces apoptosis and tumor inhibition of oral squamous cell carcinoma through activating ros-dependent er stress/noxa pathway[J]. Phytomedicine,2021,92(11):153723. [18] Zhao Q,Liu Y,Zhong J,et al. Pristimerin induces apoptosis and autophagy via activation of ros/ask1/jnk pathway in human breast cancer in vitro and in vivo[J]. Cell Death Discov,2019,5(87):125. [19] 石艺,钟燕,刘小虎,等. 扁塑藤素增强顺铂对条件性重编程原代肺癌细胞敏感性的机制[J]. 实用医学杂志,2022,38(7):841-847. doi: 10.3969/j.issn.1006-5725.2022.07.012 [20] 周鑫,杨进,陈林,等. 扁塑藤素对膀胱癌细胞增殖和凋亡的影响及其作用机制[J]. 中国癌症防治杂志,2023,15(1):18-24. [21] Condello M,Pellegrini E,Caraglia M,et al. Targeting autophagy to overcome human diseases[J]. Int J Mol Sci,2019,20(3):725. doi: 10.3390/ijms20030725 [22] Yun C W,Lee S H. The roles of autophagy in cancer[J]. Int J Mol Sci,2018,19(11):725. [23] Rakesh R,PriyaDharshini L C,Sakthivel K M,et al. Role and regulation of autophagy in cancer[J]. Biochim Biophys Acta Mol Basis Dis,2022,1868(7):166400. doi: 10.1016/j.bbadis.2022.166400 [24] Milkovic L,Cipak G A,Cindric M,et al. Short overview of ros as cell function regulators and their implications in therapy concepts[J]. Cells,2019,8(8):793. doi: 10.3390/cells8080793 [25] Nascimbeni A C,Codogno P,Morel E. Local detection of ptdIns3p at autophagosome biogenesis membrane platforms[J]. Autophagy,2017,13(9):1602-1612. doi: 10.1080/15548627.2017.1341465 [26] Ko J H,Yoon S O,Lee H J,et al. Rapamycin regulates macrophage activation by inhibiting nlrp3 inflammasome-p38 mapk-nfκb pathways in autophagy- and p62-dependent manners[J]. Oncotarget,2017,8(25):40817-40831. doi: 10.18632/oncotarget.17256 期刊类型引用(5)
1. 梁锦玲. 经腹部与经阴道彩超联合检查对剖宫产子宫瘢痕妊娠的诊断价值. 影像研究与医学应用. 2024(05): 169-171 .  百度学术
百度学术2. 丁洁. 经阴道三维超声在早期剖宫产瘢痕妊娠中的应用价值研究. 影像研究与医学应用. 2023(10): 141-143 .  百度学术
百度学术3. 吕显玉,朱武银,姚奇. 经阴道超声在剖宫产术后子宫瘢痕妊娠诊断中的效果分析. 世界复合医学. 2023(06): 46-49 .  百度学术
百度学术4. 林晓艺,吴延华,陈艺珠. 经腹部超声联合经阴道超声诊断瘢痕妊娠的临床价值分析. 临床医学工程. 2023(08): 1045-1046 .  百度学术
百度学术5. 安雅楠,王珺,饶克宇,陈素文. 瘢痕部位血管微循环参数联合子宫内膜容受性标志物诊断早孕期瘢痕妊娠价值. 中国计划生育学杂志. 2023(09): 2157-2159+2165 .  百度学术
百度学术其他类型引用(0)
-






 下载:
下载:
 下载:
下载: